Hydnellum
Hydnellum
| |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Classificação científica | |||||||||||||||
| |||||||||||||||
| Espécie-tipo | |||||||||||||||
| Hydnellum suaveolens Scop. : Fr. (1772) | |||||||||||||||
| Sinónimos[1] | |||||||||||||||
| |||||||||||||||
Hydnellum é um gênero de fungos hidnoides da família Bankeraceae (ordem Thelephorales). Amplamente distribuído no Hemisfério Norte, o gênero abrange cerca de 120 espécies. Os basidiomas de suas espécies crescem lentamente, envolvendo pequenos pedaços de grama e vegetação ao redor. A forma dos basidiomas de Hydnellum apresenta grande variabilidade, influenciada por condições ambientais como chuva, umidade, ventos secos e temperatura. Esses fungos são muito duros e lenhosos para serem consumidos confortavelmente. Algumas espécies têm despertado crescente preocupação com a conservação devido à redução generalizada de sua abundância.
As espécies de Hydnellum produzem pigmentos que têm sido utilizados para tingir tecidos. Diversos compostos químicos, alguns com atividade biológica única, foram isolados e identificados a partir do gênero.
Uma das espécies mais conhecidas é a incomum Hydnellum peckii, de coloração branco-rosada e gotas vermelhas. Outra espécie, H. suaveolens, possui um forte odor de anis ou hortelã.
Taxonomia
O gênero Hydnellum foi circunscrito pelo micologista finlandês Petter Adolf Karsten em 1879, tendo como espécie-tipo o que na época era conhecido como Hydnum suaveolens.[2] Anteriormente, fungos hidnoides haviam sido agrupados no gênero Hydnum por Elias Fries em sua obra de 1821, Systema mycologicum.[3] Karsten definiu Hydnellum como possuindo basidiomas com píleo coriáceo e resistente, e um estipe centralmente fixado.[2] Sinônimos de Hydnellum incluem Calodon (Karsten, 1881[4]), e Phaeodon (Joseph Schröter, 1888[5]).[1]
Hydnellum é classificado na família Bankeraceae, descrita por Marinus Anton Donk em 1961. O gênero não estava incluído no conceito original de Donk para a família, que abrangia apenas Bankera e Phellodon, gêneros cujas espécies produzem esporos hialinos (translúcidos) e ornamentados. Donk deixou Hydnellum na tribo Hydnelleae da família Thelephoraceae, junto com Sarcodon e Hydnodon.[6] Em 1981, no entanto, Walter Jülich revisou o conceito de Donk para a Bankeraceae, incluindo gêneros hidnoides que produzem esporos castanhos e lobados, como Hydnellum e Sarcodon.[7]
Filogenia
Estudos filogenéticos mostram que, em sua circunscrição atual, o gênero Hydnellum é polifilético e apenas distantemente relacionado aos gêneros de esporos brancos Bankera e Phellodon, atualmente agrupados na família Bankeraceae.[8][9][10] Análises da região do espaçador interno transcrito por Parfitt e colegas[11] e Ainsworth e colegas[12] revelaram múltiplas linhagens crípticas dentro do gênero. A maioria das espécies crípticas pertence ao complexo de espécies H. concrescens/H. scrobiculatum, resultando em frequentes interpretações errôneas desses nomes antigos e amplamente utilizados.[12][13] Atualmente, o número de linhagens filogeneticamente distintas confirmadas por sequenciamento molecular excede o número de táxons descritos no gênero, tornando inevitáveis futuras revisões taxonômicas.
Morfologia
Os basidiomas de Hydnellum possuem píleos e estipes, frequentemente com formas de crescimento indeterminadas, que podem crescer de súbito e se deteriorar ao longo de várias semanas.[14][10] Basidiomas vizinhos podem se fundir, formando píleos intricadamente entrelaçados e estipes parcialmente fundidos.[15] A carne apresenta uma aparência zonada e é fibrosa quando fresca, mas torna-se dura e lenhosa quando seca.[14] As zonas na carne refletem diferenças no crescimento durante períodos de baixa umidade diurna e alta umidade noturna, fornecendo um registro razoavelmente preciso do crescimento diário.[16] Os espinhos são densamente agrupados e geralmente decorrentes (estendendo-se ao longo do estipe). Os basidiomas podem exibir uma variedade de cores, de branco a amarelo, verde-oliva, tons de laranja, marrom claro ou marrom escuro com a idade.[14]
Os esporos de Hydnellum são quase esféricos a oblongos e tuberculados, sendo castanhos em massa.[14][12] As basídios (células portadoras de esporos) são estreitamente claviformes e geralmente possuem quatro esporos; não há cistídios em Hydnellum.[17] Três tipos de hifas são encontrados na carne de Hydnellum: hifas generativas (de parede finas, não infladas), hifas esqueléticas (de paredes espessas e estreitas) e hifas gloeoplerosas de paredes finas, que se coram com azul de metila.[18]

Em condições de alta umidade, várias espécies podem formar gotas coloridas impressionantes em píleos em crescimento ativo: gotas vermelhas em H. peckii, H. diabolus, H. ferrugineum e H. cruentum, gotas amarelas em H. caeruleum e gotas cor de café em H. mirabile.[19] Algumas espécies de Hydnellum têm um odor farináceo (como H. mirabile e H. pineticola), semelhante a farinha recém-moída. H. zonatum tem um cheiro de meliloto,[20] enquanto H. suaveolens possui um odor doce que lembra anis ou hortelã. Todos são muito duros e lenhosos para serem comestíveis, e muitos têm um sabor acre.[21]
As diferenças entre as espécies de Hydnellum tendem a ser mais distinguíveis em espécimes jovens. O desenvolvimento do basidioma é fortemente influenciado por fatores ambientais, como níveis de chuva, ventos secos e temperatura.[22] H. caeruleum, por exemplo, desenvolve uma cor azul mais intensa quando cresce durante o outono mais frio.[22] O crescimento ideal ocorre durante períodos de chuvas leves frequentes e alta umidade; se o habitat secar, o crescimento para, mas pode ser retomado após novas precipitações. Esse crescimento intermitente afeta os basidiomas de diferentes espécies em graus variados, levando a grandes variações em forma, textura da superfície e cor.[22] A variabilidade morfológica dos basidiomas e sua dependência de condições ambientais tornaram Hydnellum um grupo difícil de estudar. O micologista canadense Kenneth A. Harrison, que descreveu várias espécies novas da América do Norte, observou: "a notável longevidade de esporóforos individuais de muitas espécies e as mudanças na aparência que ocorrem durante o longo período de seu desenvolvimento confundiram todos os pesquisadores que estudam este grupo".[23] Por exemplo, H. aurantiacum, inicialmente branco, passa por tons de laranja, marrom-ferrugem e marrom-escuro. Seu basidioma começa com uma forma turbinada (semelhante a um coxim) com superfície irregular, tornando-se posteriormente achatado a funiliforme com textura de superfície lisa a corrugada.[15]
Os píleos se formam a partir do topo do estipe curto pelo crescimento e expansão de uma margem arredondada e, posteriormente, pelo espessamento da superfície superior.[15] Os espinhos começam a se formar quando o píleo se projeta ligeiramente sobre o estipe. Eles são brancos em muitas espécies, mas tornam-se castanhos na maturidade, à medida que os esporos castanhos se acumulam na superfície.[22]
Habitat e distribuição
Os fungos de Hydnellum são micorrízicos e geralmente encontrados em florestas de coníferas e mistas.[12][17] As árvores hospedeiras preferidas incluem membros das famílias Fagaceae e Pinaceae.[24] O gênero está amplamente distribuído no Hemisfério Norte, particularmente na Europa e na América do Norte,[25] mas algumas espécies também são encontradas na Ásia tropical.[17] Harrison identificou uma dúzia de novas espécies da América do Norte na década de 1960.[16][26][27] Rudolph Arnold Maas Geesteranus reconheceu 16 espécies europeias em seu tratamento do gênero em 1975,[28] ao qual H. dianthifolium foi recentemente adicionado por Loizides e colegas.[13]
Algumas espécies de Hydnellum, incluindo H. ferrugineum e H. scleropodium, formam um tapete resistente de micélios no húmus e no solo superior de florestas de pinheiros. Esse tapete micelial cresce com árvores mais velhas e pode cobrir uma área de vários metros quadrados. Essas áreas geralmente carecem de arbustos anões e promovem o crescimento vigoroso de musgos; a espécie de líquen Cladonia rangiferina [en] frequentemente ocorre no centro de grandes tapetes. A presença do fungo altera a natureza do solo, resultando em uma camada de húmus mais fina, menor penetração de água subterrânea, diminuição do pH do solo e aumentos no nível de respiração radicular, bem como na quantidade de raízes. O fungo também reduz as concentrações de carbono orgânico e nitrogênio. O solo com o micélio torna-se mais podzolizado do que o solo circundante.[29][30]
Conservação

Algumas espécies de Hydnellum estão em declínio na Europa, incluindo a República Tcheca,[31] Países Baixos,[32] Noruega[33] e Escócia.[34] No Reino Unido, várias espécies estão listadas no plano de ação de biodiversidade para fungos hidnoides com estipe.[35] De acordo com a Lista Vermelha de Espécies Ameaçadas, são listadas como espécies quase ameaçadas: H. versipelle e H. scabrosum. As espécies H. fuligineoviolaceum, H. illudens, H. martioflavum, H. gracilipes e H. mirabile são listadas como vulneráveis. E as espécies H. nemorosum e H. roseoviolaceum já são listadas como em perigo de extinção.[36] H. ferrugineum e H. peckii foram identificados como sensíveis ao aumento da deposição de nitrogênio resultante do corte raso, uma prática florestal usada em algumas áreas da Europa.[37]
Os esforços de conservação para Hydnellum são dificultados pelo fato de que algumas espécies são difíceis de distinguir em campo, tornando complicado determinar um status de conservação apropriado.[12][11] Técnicas baseadas em iniciadores de PCR específicos para espécies e extração de DNA do solo foram desenvolvidas para detectar os micélios de várias espécies de Hydnellum sem depender da presença de basidiomas, o que pode auxiliar nos esforços de conservação e melhorar a compreensão da ecologia subterrânea.[38] Técnicas semelhantes foram usadas para mostrar que, no caso de H. aurantiacum e H. caeruleum, o fungo pode persistir abaixo do solo por pelo menos quatro anos sem produzir basidiomas.[39]
Compostos bioativos
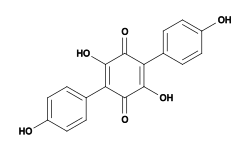
Diversos compostos químicos, alguns com atividade biológica única, foram isolados e identificados de espécies de Hydnellum. Por exemplo, H. peckii contém atromentina, um pigmento com propriedades anticoagulantes semelhantes à heparina.[40] A atromentina também possui atividade antibacteriana, inibindo a enzima enoil-acil transportadora de proteína redutase (essencial para a biossíntese de ácidos graxos) na bactéria Streptococcus pneumoniae.[41]
Algumas espécies são usadas como corantes. H. caeruleum, utilizado na América do Norte e na Escandinávia para tingir seda e lã, produz uma gama de cores, incluindo bege, azul e verde-floresta, dependendo do mordente utilizado. H. peckii produz cores cinza, marrom e oliva.[42] Hidnuferrugina e hidnuferruginina são pigmentos responsáveis pela coloração de H. ferrugineum e H. zonatum.[43] Geogenina é um pigmento amarelo encontrado em H. geogenium [en].[44]
O ácido teleforico está presente em várias espécies de Hydnellum.[45] Esse composto, derivado metabolicamente da via do ácido chiquímico, inibe a enzima prolil endopeptidase, que está envolvida na deterioração de certos neuropeptídeos associados à memória e ao aprendizado.[46] H. caeruleum e H. concrescens possuem vários derivados de para-terfenilo chamados telefantinas (especificamente, variantes telefantinas I–N),[47] alguns dos quais podem inibir a enzima alfa-glicosidase.[48] Os compostos hidnellinas A e B são terfenis encontrados em H. suaveolens e H. geogerirum.[49] Os produtos químicos responsáveis pelo aroma semelhante a anis de H. suaveolens foram identificados como cumarina e para-anisaldeído.[50]
Espécies
A circunscrição original de Karsten de 1879 para Hydnellum continha 19 espécies.[2] Joost Stalpers incluiu 34 espécies de Hydnellum em sua monografia de 1993 sobre Thelephorales.[51] A décima edição do Dictionary of the Fungi (2008) indicava 38 espécies no gênero.[52] Larsson e colaboradores incluíram 12 espécies transferidas para este gênero a partir de Sarcodon em 2019. [53] Em 2024, Douch descreveu mais quatro espécies.[54]
Em agosto de 2025, os bancos de dados Index Fungorum e Mycobank listam aproximadamente 120 espécies em Hydnellum.[55][56] A seguir são listadas algumas das espécies do gênero.
| Imagem | Nome | Distribuição |
|---|---|---|
 |
Hydnellum amygdaliolens [en] (Rubio Casas, Rubio Roldán & Català) E.Larss., K.H.Larss. & Kõljalg | Europa[53] |
_P._Karst_441899.jpg) |
Hydnellum aurantiacum (Batsch) P.Karst. (1879) | Ásia, Europa, América do Norte[17] |
 |
Hydnellum auratile (Britzelm.) Maas Geest. (1959) | Europa, América do Norte[57] |
_P._Karst_466139.jpg) |
Hydnellum caeruleum (Hornem.) P.Karst. (1879) | Ásia, Europa, América do Norte[17] |
| Hydnellum chrysinum K.A.Harrison (1964) | América do Norte[27] | |
| Hydnellum coalitum Maas Geest. (1975) | Europa[28] | |
 |
Hydnellum compactum (Pers.) P.Karst. (1879) | Europa[58] |
| Hydnellum complicatum Banker (1906) | América do Norte[25] | |
| Hydnellum concrescens (Pers.) Banker (1906) | Ásia, Europa, América do Norte[17] | |
| Hydnellum conigenum (Peck) Banker (1906) | América do Norte[59] | |
_Stalpers_358020.jpg) |
Hydnellum cristatum (Bres.) Stalpers (1993) | Europa, América do Norte |
| Hydnellum cruentum K.A.Harrison (1961) | Nova Escócia, Canadá[60] | |
| Hydnellum crustulinum Maas Geest. (1971) | Punjab, Índia[58] | |
| Hydnellum cumulatum K.A.Harrison (1964) | Europa,[61] América do Norte[27] | |
| Hydnellum cyanodon K.A.Harrison (1964) | América do Norte[27] | |
 |
Hydnellum cyanopodium K.A.Harrison (1964) | América do Norte[27] |
.jpg) |
Hydnellum dianthifolium Loizides, Arnolds & P.-A. Moreau (2016) | Sul da Europa[13] |
| Hydnellum earlianum Banker (1906) | América do Norte[25] | |
 |
Hydnellum fennicum [en] (P.Karst.) E.Larss., K.H.Larss. & Kõljalg | Europa[53] |
 |
Hydnellum ferrugineum (Fr.) P.Karst. (1879) | Norte da África, Ásia, Europa, América do Norte[17] |
| Hydnellum floriforme (Schaeff.) Banker (1906) | América do Norte[25] | |
| Hydnellum fraudulentum Maas Geest. (1971) | Austrália[58] | |
| Hydnellum frondosum K.A.Harrison (1961) | Nova Escócia, Canadá[62] | |
 |
Hydnellum fuligineoviolaceum (Kalchbr.) E.Larss., K.H.Larss. & Kõljalg | Europa[53] |
 |
Hydnellum fuscoindicum (K.A.Harrison) E.Larss., K.H.Larss. & Kõljalg | América do Norte[53] |
| Hydnellum gatesiae Douch, L.J. Vaughan & T.W. May | Austrália[54] | |
| Hydnellum geogenium (Fr.) Banker (1913) | Europa, América do Norte[63] | |
 |
Hydnellum glaucopus (Maas Geest. & Nannf.) E.Larss., K.H.Larss. & Kõljalg | Europa[53] |
.jpg) |
Hydnellum gracilipes [en] (P.Karst.) P.Karst. (1879) | Europa[64] |
 |
Hydnellum joeides (Pass.) E.Larss., K.H.Larss. & Kõljalg | Europa, América do Norte[53] |
| Hydnellum lepidum (Maas Geest.) E. Larss., K.H.Larss. & Kõljalg | Europa[53] | |
| Hydnellum longidentatum Coker (1939) | Estados Unidos[65] | |
| Hydnellum lundellii (Maas Geest. & Nannf.) E.Larss., K.H.Larss. & Kõljalg | Europa[53] | |
 |
Hydnellum martioflavum (Snell, K.A.Harrison & H.A.C.Jacks.) E.Larss., K.H.Larss. & Kõljalg | Europa, América do Norte[53] |
 |
Hydnellum mirabile (Fr.) P.Karst. (1879) | Europa, América do Norte[66] |
| Hydnellum multiceps K.A.Harrison (1961) | Nova Escócia, Canadá[62] | |
| Hydnellum nigellum K.A.Harrison (1964) | América do Norte[27] | |
| Hydnellum nothofagacearum Douch & J.A. Cooper | Nova Zelândia[54] | |
| Hydnellum papuanum Maas Geest. (1971) | Papua-Nova Guiné[58] | |
| Hydnellum parvum Banker (1913) | América do Norte[10] | |
 |
Hydnellum peckii Banker (1912) | Europa, América do Norte[17] |
| Hydnellum pseudoioeides Douch & J.A. Cooper | Oceania[54] | |
 |
Hydnellum regium K.A.Harrison (1964) | América do Norte[27] |
| Hydnellum rickeri Banker (1913) | América do Norte[67] | |
.jpg) |
Hydnellum scabrosum (Fr.) E.Larss., K.H.Larss. & Kõljalg | Europa[53] |
| Hydnellum scleropodium K.A.Harrison (1964) | América do Norte[27] | |
 |
Hydnellum scrobiculatum (Fr.) P.Karst. (1879) | Ásia, Europa, América do Norte[17] |
| Hydnellum septentrionale K.A.Harrison (1964) | América do Norte[27] | |
| Hydnellum singeri Maas Geest. (1969) | Colômbia[68] | |
 |
Hydnellum spongiosipes (Peck) Pouzar (1960) | Europa, América do Norte[17] |
| Hydnellum staurastrum Maas Geest. (1971) | Malásia[58] | |
 |
Hydnellum suaveolens (Scop.) P.Karst. (1879) | Ásia, Europa, América do Norte[69] |
| Hydnellum subzonatum K.A.Harrison (1961) | Nova Escócia, Canadá[60] | |
| Hydnellum tardum Maas Geest. (1975) | Europa[28] | |
 |
Hydnellum underwoodii (Banker) E.Larss., K.H.Larss. & Kõljalg | América do Norte[53] |
| Hydnellum variisporum Douch, Robinson & L.J. Vaughan | Austrália[54] | |
 |
Hydnellum versipelle (Fr.) E.Larss., K.H.Larss. & Kõljalg | Europa, América do Norte[53] |
Referências
- ↑ a b «Hydnellum P. Karst. 1879». MycoBank. International Mycological Association. Consultado em 7 de agosto de 2025
- ↑ a b c Karsten PA (1879). «Symbolae ad mycologiam Fennicam. VI». Meddelanden Af Societas Pro Fauna et Flora Fennica. 5: 5–46 (see p. 41)
- ↑ Harrison (1961), p. 16.
- ↑ Karsten PA (1881). «Enumeratio Hydnearum Fr. Fennicarum, systemate novo dispositarum». Revue Mycologique Toulouse (em latim). 3 (9): 19–21
- ↑ Schröter J. (1888). Kryptogamen-Flora von Schlesien. 3–1(4). Lehre, Germany: Cramer. p. 458
- ↑ Donk MA (1961). «Four new families of Hymenomycetes». Persoonia. 1 (4): 405–7
- ↑ Stalpers (1993), p. 22.
- ↑ Binder M, Hibbett DS, Larsson KH, Larsson E, Langer E, Langer G (2005). «The phylogenetic distribution of resupinate forms across the major clades of mushroom-forming fungi (Homobasidiomycetes).». Systematics and Biodiversity. 3 (2): 113–157. doi:10.1017/s1477200005001623
- ↑ Tedersoo L, May T, Smith ME (2010). «Ectomycorrhizal lifestyle in fungi: global diversity, distribution, and evolution of phylogenetic lineages.». Mycorrhiza. 20 (4): 217–263. PMID 20191371. doi:10.1007/s00572-009-0274-x
- ↑ a b c Baird R, Wallace L, Baker G, Scruggs M (2013). «Stipitate hydnoid fungi of the temperate southeastern United States». Fungal Diversity. 62: 41–114. doi:10.1007/s13225-013-0261-6
- ↑ a b Parfitt D, Ainsworth AM, Simpson D, Rogers HJ, Boddy L (2007). «Molecular and morphological discrimination of stipitate hydnoids in the genera Hydnellum and Phellodon». Mycological Research. 111 (7): 761–77. PMID 17681224. doi:10.1016/j.mycres.2007.05.003
- ↑ a b c d e Ainsworth M, Parfitt D, Rogers HJ, Boddy L (2010). «Cryptic taxa within European species of Hydnellum and Phellodon revealed by combined molecular and morphological analysis.». Fungal Ecology. 3 (4): 65–80. doi:10.1016/j.funeco.2009.07.001
- ↑ a b c Loizides M, Alvarado P, Assyov B, Arnolds E, Moreau PA (2016). «Hydnellum dianthifolium sp. nov. (Basidiomycota, Thelephorales), a new tooth-fungus from southern Europe with notes on H. concrescens and H. scrobiculatum». Phytotaxa. 280 (1): 23–35. doi:10.11646/phytotaxa.280.1.2
- ↑ a b c d Baird RE, Khan SR (1986). «The stipitate Hydnums (Thelephoraceae) of Florida USA». Brittonia. 38 (2): 171–84. JSTOR 2807273. doi:10.2307/2807273
- ↑ a b c Harrison (1961), p. 13.
- ↑ a b Harrison KA (1968). «Studies on the Hydnums of Michigan I. Genera Phellodon, Bankera, Hydnellum». Michigan Botanist. 7: 212–64
- ↑ a b c d e f g h i j Pegler DN, Roberts PJ, Spooner BM (1997). British Chanterelles and Tooth Fungi. Kew, UK: Royal Botanic Gardens. pp. 74–88. ISBN 978-1-900347-15-0
- ↑ Stalpers (1997), p. 9.
- ↑ Harrison (1961), p. 15.
- ↑ Rumack BH, Spoerke DG (1994). Handbook of Mushroom Poisoning: Diagnosis and Treatment. [S.l.]: CRC Press. p. 413. ISBN 978-0-8493-0194-0
- ↑ Arora D. (1986). Mushrooms Demystified. Berkeley, California: Ten Speed Press. pp. 623–27. ISBN 978-0-89815-169-5
- ↑ a b c d Harrison (1961), p. 14.
- ↑ Harrison (1961), p. 12.
- ↑ Stalpers (1997), p. 34.
- ↑ a b c d Banker HJ (1906). «A contribution to a revision of the North American Hydnaceae.». Memoirs of the Torrey Botanical Club. 12 (2): 99–194
- ↑ Harrison (1961).
- ↑ a b c d e f g h i Harrison KA (1964). «New or little known North American stipitate Hydnums». Canadian Journal of Botany. 42 (9): 1205–33. doi:10.1139/b64-116
- ↑ a b c Maas Geesteranus RA. (1975). «Die terrestrischen Stachelpilze Europas». Verhandelingen Koninklijke Nederlandse Akademie van Wetenschappen Afdeling Natuurkunde (em alemão). 64 (2): 1–127 (see pp. 95–98)
- ↑ Hintikka V, Näykki O (1967). «Tutkimuksia ruosteorakkaan, Hydnellum ferrugineum, vaikutuksesta metsämaaperään ja-kasvillisuuteen [Notes on the effects of the fungus Hydnellum ferrugineum (Fr.) Karst. on forest soil and vegetation]». Communicationes Instituti Forestalis Fenniae. 62 (2): 1–23
- ↑ Fisher RF (1972). «Spodosol development and nutrient distribution under Hydnaceae fungal mats». Soil Science Society of America Journal. 36 (3): 492–5. Bibcode:1972SSASJ..36..492F. doi:10.2136/sssaj1972.03615995003600030035x
- ↑ Hrouda P. (1999). «Hydnaceous fungi of the Czech Republic and Slovakia». Czech Mycology. 51 (2–3): 99–155. doi:10.33585/cmy.51202
- ↑ Arnolds E. (1989). «Former and present distribution of stipitate hydnaceous fungi (Basidiomycetes) in the Netherlands». Nova Hedwigia. 68: 107–42
- ↑ Gulden G, Hanssen EW (1992). «Distribution and ecology of stipitate hydnaceous fungi in Norway, with special reference to the question of decline». Sommerfeltia. 13: 1–58. doi:10.2478/som-1992-0001

- ↑ Newton AC, Holden E, Davy LM, Ward SD, Fleming LV, Watling R (2002). «Status and distribution of stipitate hydnoid fungi in Scottish coniferous forests». Biological Conservation. 107 (2): 181–92. doi:10.1016/S0006-3207(02)00060-5
- ↑ UK Biodiversity Action Plan (2007). List of UK BAP Priority Fungi Species (including lichens) (PDF). Reino Unido: Joint Nature Conservation Committee
- ↑ «Hydnellum - IUCN Red List». Consultado em 7 de agosto de 2025
- ↑ Arnolds E. (2010). «The fate of hydnoid fungi in The Netherlands and Northwestern Europe». Fungal Ecology. 3 (2): 81–88. doi:10.1016/j.funeco.2009.05.005
- ↑ van der Linde S, Alexander I, Anderson IC (2008). «A PCR-based method for detecting the mycelia of stipitate hydnoid fungi in soil». Journal of Microbiological Methods. 75 (1): 40–46. PMID 18586344. doi:10.1016/j.mimet.2008.04.010
- ↑ van der Linde S, Holden E, Parkin PI, Alexander IJ, Anderson IC (2012). «Now you see it, now you don't: The challenge of detecting, monitoring and conserving ectomycorrhizal fungi». Fungal Ecology. 5 (5): 633–40. doi:10.1016/j.funeco.2012.04.002
- ↑ Khanna JM, Malone MH, Euler KL, Brady LR (1965). «Atromentin – anticoagulant from Hydnellum diabolus». Journal of Pharmaceutical Sciences. 54 (7): 1016–20. PMID 5862512. doi:10.1002/jps.2600540714
- ↑ Zheng CJ, Sohn MJ, Kim WG (2006). «Atromentin and leucomelone, the first inhibitors specific to enoyl-ACP reductase (FabK) of Streptococcus pneumoniae». Journal of Antibiotics. 59 (12): 808–12. PMID 17323650. doi:10.1038/ja.2006.108

- ↑ Roberts P, Evans S (2011). The Book of Fungi. Chicago, Illinois: University of Chicago Press. pp. 469–70. ISBN 978-0-226-72117-0
- ↑ Gripenberg J. (1981). «Fungus pigments. XXIX. The pigments of Hydnellum ferrugineum (Fr.) Karsten and H. zonatum (Batsch) Karsten». Acta Chemica Scandinavica B. 35: 513–9
- ↑ Steglich W, Jendrny B (1979). «Geogenin, ein neuartiger Pyronfarbstoff aus Hydnellum geogenium» [Geogenin, a new kind of pyrone pigment from Hydnellum geogenium]. Beihefte zur Sydowia Annales Mycologici. Series II (em alemão): 378–80
- ↑ Stalpers (1997), p. 7.
- ↑ Kwak JY, Rhee IK, Lee KB, Hwang JS, Yoo ID, Song KS (1999). «Thelephoric acid and kynapcin-9 in mushroom Polyozellus multiplex inhibit prolyl endopeptidase in vitro». Journal of Microbiology and Biotechnology. 9 (6): 798–803
- ↑ Quang DN, Hashimoto T, Hitaka Y, Tanaka M, Nukada M, Yamamoto I, Asakawa Y (2004). «Thelephantins I-N; p-terphenyl derivatives from the inedible mushroom Hydnellum caeruleum». Phytochemistry. 65 (8): 1179–84. Bibcode:2004PChem..65.1179Q. PMID 15110701. doi:10.1016/j.phytochem.2004.02.018
- ↑ Wang SM, Han JJ, Ma K, Jin T, Bao L, Pei YF, Liu HW (2014). «New α-glucosidase inhibitors with p-terphenyl skeleton from the mushroom Hydnellum concrescens». Fitoterapia. 98: 149–55. PMID 25088970. doi:10.1016/j.fitote.2014.07.019
- ↑ Hashimoto T, Quang DN, Kuratsune M, Asakawa Y (2006). «Hydnellins A and B, nitrogen-containing terphenyls from the mushrooms Hydnellum suaveolens and Hydnellum geogerirum». Chemical and Pharmaceutical Bulletin. 54 (6): 912–4. PMID 16755070. doi:10.1248/cpb.54.912

- ↑ Wood WF, DeShazer DA, Largent DL (1988). «The identify and metabolic fate of volatiles responsible for the odor of Hydnellum suaveolens». Mycologia. 80 (2): 252–5. JSTOR 3807803. doi:10.2307/3807803
- ↑ Stalpers (1993).
- ↑ Kirk PM, Cannon PF, Minter DW, Stalpers JA (2008). Dictionary of the Fungi 10th ed. Wallingford, UK: CAB International. p. 324. ISBN 978-0-85199-826-8
- ↑ a b c d e f g h i j k l m Larsson, Svantesson; Miscevic, Kõljalg; Larsson (2019). «Reassessment of the generic limits for Hydnellum and Sarcodon (Thelephorales, Basidiomycota)». MycoKeys (54): 31–47. PMC 6579789
 . PMID 31231164. doi:10.3897/mycokeys.54.35386
. PMID 31231164. doi:10.3897/mycokeys.54.35386
- ↑ a b c d e Douch, James K.; Vaughan, Luke J.; Cooper, Jerry A.; Holmes, Gareth D.; Robinson, Richard; Stefani, Franck; Idnurm, Alexander; May, Tom W. (29 de agosto de 2024). «Taxonomic revision of fleshy species of Hydnellum, Neosarcodon, and Sarcodon (Thelephorales) from Australasia». Mycologia (em inglês). 116 (6): 965–992. ISSN 0027-5514. doi:10.1080/00275514.2024.2363211
- ↑ «Index Fungorum - Search Page». www.indexfungorum.org. Consultado em 7 de agosto de 2025
- ↑ «Page search». www.mycobank.org. Consultado em 7 de agosto de 2025
- ↑ Maas Geesteranus RA. (1959). «Sur un Hydnellum méconnu». Persoonia (em francês). 1 (1): 111–4
- ↑ a b c d e Maas Geesteranus RA. (1971). «Hydnaceous fungi of the eastern old world». Verhandelingen Koninklijke Nederlandse Akademie van Wetenschappen Afdeling Natuurkunde. 60 (3): 1–176 (see pp. 91–106)
- ↑ McKnight KH (1998). A Field Guide to Mushrooms: North America. [S.l.]: Houghton Mifflin Harcourt. p. 94. ISBN 978-0-395-91090-0
- ↑ a b Harrison (1961), p. 37.
- ↑ Ainsworth M. (2011). «Hydnellum cumulatum and H. gracilipes: two overlooked Scottish hydnoids new to Britain». Field Mycology. 12 (4): 139–43. doi:10.1016/j.fldmyc.2011.09.011

- ↑ a b Harrison (1961), p. 45.
- ↑ Phillips R. «Hydnellum geogenium». RogersMushrooms. Consultado em 7 de agosto de 2025. Arquivado do original em 22 de janeiro de 2015
- ↑ Kõljalg U, Renvall P (2000). «Hydnellum gracilipes – a link between stipitate and resupinate Hymenomycetes» (PDF). Karstenia. 40 (1–2): 71–77. doi:10.29203/ka.2000.355

- ↑ Coker WC (1939). «New or noteworthy Basidiomycetes». Journal of the Elisha Mitchell Scientific Society. 55: 373–86
- ↑ Phillips R. «Hydnellum mirabile». RogersMushrooms. Consultado em 7 de agosto de 2025. Arquivado do original em 29 de novembro de 2014
- ↑ Banker HJ (1913). «Type studies in the Hydnaceae – V. The genus Hydnellum». Mycologia. 5 (4): 194–205. JSTOR 3753385. doi:10.2307/3753385
- ↑ Maas Geesteranus RA. (1969). «Notes on Hydnums, VIII». Proceedings van de Koninklijke Nederlandse Akademie van Wetenschappen Section C. 72: 213–21
- ↑ Phillips R. «Hydnellum suaveolens». RogersMushrooms. Consultado em 7 de agosto de 2025. Arquivado do original em 2 de abril de 2015
Bibliografia
- Harrison KA (1961). The Stipitate Hydnums of Nova Scotia. Publications of the Department of Agriculture Canada (Relatório). 1099. Ottawa, Canada: Research Branch, Canada Department of Agriculture. pp. 1–60

- Stalpers JA (1993). «The Aphyllophoraceous fungi I. Keys to the species of the Thelephorales». Studies in Mycology. 35: 1–168. Consultado em 7 de agosto de 2025. Arquivado do original em 21 de fevereiro de 2015

