Dihidrofolato redutase
| dihydrofolate reductase | |||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Identificadores | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Nomes alternativos | |||||||||||||||||||||||||||||||||||||||||||||||||||
| IDs externos | GeneCards: [1] | ||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Wikidata | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
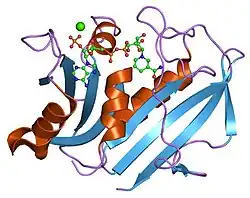
A dihidrofolato redutase ou DHFR é uma enzima que reduz o ácido di-hidrofólico a ácido tetraidrofólico usando NADPH como doador de eletrões, o qual pode converter-se depois nos tipos de cofatores tetraidrofolato utilizados na química de transferência de um carbono. Nos humanos, a enzima DHFR é codificada pelo gene DHFR[1][2] situado na região q14.1 do cromossomo 5.[3] Há duas classes estruturais de DHFR, que não estão relacionadas evolutivamente entre si. O mencionado anteriormente é o que geralmente se chama DHFR e encontra-se em cromossomos bacterianos e de animais. Contudo, nas bactérias, a pressão exercida pelos antibióticos fez com que nesta classe evoluíssem diferentes maneiras de ligar-se a moléculas diamino-heterocíclicas, originando diversos "tipos" incluídos nesta classe, enquanto que os de mamíferos permaneceram com características muito semelhantes.[4] A segunda das classes (as de tipo II) está representada pela R67 codificada em plasmídeos, que é uma enzima diminuta que funciona formando um homotetrâmero.[5]
Função
A dihidrofolato redutase converte o di-hidrofolato em tetraidrofolato, uma lançadeira de prótões necessária para a síntese de novo de purinas, ácido timidílico e certos aminoácidos. Embora o gene funcional da dihidrofolato redutase se tenha mapeado no cromossomo 5, identificaram-se múltiplos pseudogenes processados sem íntrões semelhantes ao da dihidrofolato redutase situados noutros cromossomos.[6]
-
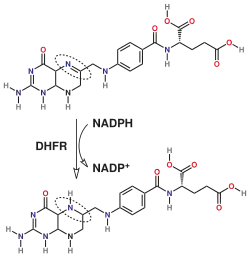 Via de síntese do tetraidrofolato.
Via de síntese do tetraidrofolato.
A DHFR, que se encontra em todos os organismos, tem um papel fundamental na regulação da quantidade de tetraidrofolato da célula. O tetraidrofolato e os seus derivados são essenciais para a síntese de purinas e timidilato, que são importantes para a proliferação e crescimento celular.[7] A DHFR joga um papel central na síntese de precursores de ácidos nucleicos, e observou-se que as células mutantes que carecem completamente de DHFR necessitam para crescer glicina, uma purina e timidina.[8] A DHFR é também uma enzima envolvido no resgate de tetra-hidrobiopterina a partir de di-hidrobiopterina.[9][10]
Estrutura
| Dihidrofolato redutase | |
|---|---|
| Indicadores | |
| Pfam | PF00186 |
| InterPro | IPR001796 |
| PROSITE | PDOC00072 |
| SCOP | 1dhi |
A principal característica do enovelamento do esqueleto polipeptídico da DHFR é uma folha beta de 8 febras.[11] Sete destas febras são paralelas e a oitava discorre antiparalela. Quatro hélices alfa conectam as sucessivas febras beta.[12] Os resíduos 9–24 denominam-se "Met20" ou "alça 1" e, juntamente com outras alças, fazem parte do subdomínio principal que rodeia o sítio ativo.[13] O sítio ativo está situado na metade N-terminal da sequência, que inclui um dipéptido conservado Pro-Trp; o triptofano está envolvido na ligação da enzima com o substrato.[12]
Mecanismo
Mecanismo geral
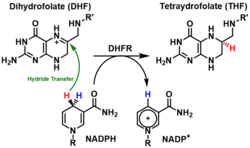
A DHFR catalisa a transferência de um hidreto do NADPH ao di-hidrofolato acompanhada de uma protonação para produzir tetraidrofolato.[7] Ao final, o di-hidrofolato é reduzido a tetraidrofolato e o NADPH é oxidado a NADP+. A grande flexibilidade do Met20 e outras alças próximas ao sítio ativo desempenham um papel na promoção da libertação do produto, o tetraidrofolato. Em concreto, a alça Met20 ajuda a estabilizar o anel de nicotinamida do NADPH para promover a transferência do hidreto do NADPH ao di-hidrofolato.[13] O mecanismo deste enzima funciona passo a passo e é aleatório em estado estacionário. A reação catalítica começa com a ligação do NADPH e do substrato ao sítio ativo da enzima, seguida da protonação e transferência de hidreto do cofator NADPH ao substrato. Contudo, os dois últimos passos não ocorrem simultaneamente no mesmo estado de transição.[14][15] Num estudo em que se usaram estratégias computacionais e experimentais, Liu et al concluíram que o passo de protonação precede a transferência do hidreto.[16]
.png)
O mecanismo enzimático da DHFR é dependente do pH, particularmente o passo da transferência do hidreto, já que as mudanças de pH têm uma considerável influência na eletrostática do sítio ativo e no estado de inonização dos seus resíduos.[16] A acidez do nitrogénio afetado do substrato é importante na ligação do substrato ao sítio de ligação da enzima, que se demonstrou ser hidrófobo apesar de estar em contacto direto com a água.[14][17] O Asp27 é o único resíduo hidrófilo carregado do sítio de ligação, e a neutralização da carga do Asp27 pode alterar o pKa da enzima. O Asp27 joga um papel crítico no mecanismo catlítico ajudando com a protonação do substrato e restringindo o substrato na conformação favorável para a transferência do hidreto.[18][14][17] O passo de protonação está associado com a tautomerização enol mesmo se esta conversão não se considera favorável para doar prótons.[15] Uma molécula de água está envolvida no passo de protonação.[19][20][21] A entrada da molécula de água no sítio ativo da enzima é facilitda pela alça Met20.[22]
Alterações conformacionais da DHFR
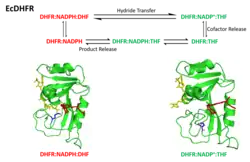
O ciclo catalítico da reação catalisada pela DHFR incorpora cinco intermediários importantes: holoenzima (E:NADPH), complexo de Michaelis (E:NADPH:DHF), complexo ternário do produto (E:NADP+:THF), complexo binário do tetraidrofolato (E:THF), e complexo THF‚NADPH (E:NADPH:THF). O passo da dissociação do produto (THF) do E:NADPH:THF ao E:NADPH é o passo limitante da velocidade durante o recâmbio do estado estacionário.[18] As alterações conformacionais são fundamentais no mecanismo catalítico da DHFR.[23] A alça Met20 da DHFR pode abrir, fechar ou ocluir o sítio ativo.[20][14] Em correspondência, atribuíram-se três conformações ao Met20 classificadas como estados aberto, fechado e ocluído. Além disso, definiu-se uma conformação distorcida extra do Met20 devido ao caráter indistinto dos resultados.[20] A alça Met20 observa-se na sua conformação ocluída nos três intermediários que se ligam ao produto, nos quais o anel de nicotinamida está ocluído do sítio ativo. Esta característica conformacional explica que a substituição do NADP+ por NADPH ocorre antes da dissociação do produto. Desta maneira, pode ocorrer a seguinte ronda de reação depois da ligação do substrato.[18]
DHFR R67
| Dihidrofolato redutase | |
|---|---|
| Indicadores | |
| Pfam | PF06442 |
| InterPro | IPR009159 |
| SCOP | 1vif |
Devido à sua estrutura única e características catalíticas, a DHFR R67 é muito estudada. A DHFR R67 é uma DHFR de tipo II codificada no plasmídeo R sem relação genética ou estrutural com a DHFR cromossómica de Escherichia coli. É um homotetrâmero que possui simetria 222 com um só poro de sítio ativo que está exposto ao solvente.[24] Esta simetria do sítio ativo tem como resultado o modo de ligação diferente que a enzima apresenta: pode ligar-se a duas moléculas de di-hidrofolato (DHF) com cooperatividade positiva ou a duas moléculas de NADPH com cooperatividade negativa, ou a um substrato mais a outro, mas só o último tem a atividade catalítica.[25] Comparado com a DHFR cromossómica de E. coli, tem uma maior Km na ligação do di-hidrofolato (DHF) e NADPH. A cinética catalítica muito menor mostra que a transferência de hidreto é o passo limitante da velocidade e não a libertação do produto (THF).[26]
Na estrutura da DHFR R67, o homotetrâmero forma um poro de sítio ativo. No processo catlítico, o DHF e o NADPH entram no poro a partir de posições opostas. A interação de empilhamento π-π entre o anel de nicotinamida do NADPH e o anel de pteridina do DHF conectam estreitamente dois reagentes no sítio ativo. Contudo, observou-se uma flexibilidade da cauda p-aminobenzoilglutamato do DHF depois da ligação, o qual pode promover a formação do estado de transição.[27]
-
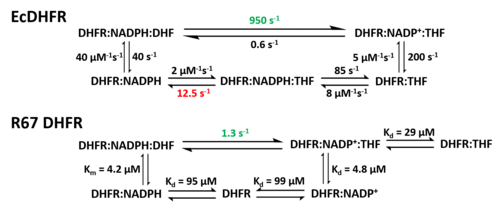 Diferença na estrutura da ligação do substrato em EcDHFR e DHFR R67.
Diferença na estrutura da ligação do substrato em EcDHFR e DHFR R67.
Importância clínica
As mutações na DHFR causam deficiência de di-hidrofolato redutase, uma rara doença congénita autossómica recessiva do metabolismo do folato que tem como resultado anemia megaloblástica, pancitopenia e deficiência de folato cerebral grave. Estes problemas podem ser superados pela suplementação com uma forma reduzida do folato, normalmente ácido folínico.[6][28][29]
Aplicações terapêuticas
A DHFR é um alvo farmacêutico atraente para a inibição pelo seu papel central como precursor da timina para a síntese do ADN. O trimetoprim, um antibiótico, inibe a DHFR bacteriana, enquanto o metotrexato, um agente quimioterápico, inibe a DHFR de mamíferos. Contudo, desenvolveu-se resistência contra alguns destes fármacos, como resultado de alterações mutacionais na própria DHFR.[30]
Cancro
A DHFR é responsável pelos níveis de tetraidrofolato na célula, e a inibição da DHFR pode limitar o crescimento e proliferação de células que são características do cancro e de infeções bacterianas. O metotrexato, um inibidor competitivo da DHFR, é um desses fármacos anticancro que inibe a DHFR.[31] O folato é necessário para o crescimento,[32] e a via do metabolismo do folato é um alvo em tratamentos em desenvolvimento para o cancro. A DHFR é um desses alvos. Um tratamento com fluorouracilo, doxorrubicina e metotrexato prolonga a sobrevivência de pacientes com cancro gástrico avançado.[33] Mais estudos sobre inibidores da DHFR podem dar origem a mais formas de tratar o cancro.
Infeção
As bactérias também necessitam da DHFR para crescer e multiplicar-se e, portanto, os inibidores seletivos para a DHFR bacteriana encontraram aplicação como agentes antibacterianos.[34] O trimetoprim tem atividade contra diversos patógenos bacterianos gram-positivos.[34] Contudo, a resistência ao trimetoprim e outros fármacos dirigidos contra a DHFR pode surgir por diversos mecanismos, limitando o sucesso dos seus usos terapêuticos.[35][36][37] A resistência pode surgir pela amplificação do gene DHFR, mutações na DHFR,[38][39] diminuição na captação desses fármacos, entre outros. Apesar de tudo, o trimetoprim e o sulfametoxazol em combinação foram utilizados como agentes antibacterianos durante décadas.[34] A pirimetamina é um agente antiprotozoário muito usado.[40] Outras classes de compostos que têm como alvo a DHFR em geral, e as DHFRs bacterianas em particular, pertencem a classes como as diaminopteridinas, diaminotriazinas, diaminopirroloquinazolinas, estilbenos, calconas, desoxibenzoínas, diaminoquinazolinas, diaminopirroloquinazolinas, entre outras.
Possível tratamento para o Antraz

A DHDR de Bacillus anthracis (BaDHFR) é um alvo de fármacos validado para o tratamento da doença infecciosa do antraz. A BaDHFR é menos sensível a análogos do trimetoprim do que é a dihidrofolato redutase de outras espécies como Escherichia coli, Staphylococcus aureus e Streptococcus pneumoniae. Um alinhamento estrutural da dihidrofolato redutase dessas quatro espécies mostra que só a BaDHFR tem a combinação de fenilalanina e tirosina nas posições 96 e 102, respetivamente. A resistência da BaDHFR a análogos do trimetoprim deve-se a estes dois resíduos (F96 e Y102), que também lhe melhoram a cinética e a eficiência catalítica.[41] A investigação atual usa sítios ativos na BaDHFR para guiar a otimização de novos inibidores antifolato.[41]
Como ferramenta de investigação
A DHFR utilizou-se como ferramenta para detetar interações proteína-proteína num ensaio de complementação de fragmento de proteína (PCA), usando uma estratégia de proteína dividida.[42] As células CHO carentes de DHFR são a linha celular mais usada para a produção de proteínas recombinantes. Estas células são transfectadas com um plasmídeo que porta o gene dhfr e o gene para a proteína recombinante num só sistema de expressão, e depois são submetidas a condições seletivas e a meio de crescimento sem timidina. Somente sobrevivem as células com o gene DHFR exógeno juntamente com o gene de interesse. A suplementação deste meio com metotrexato, um inibidor competitivo da DHFR, pode fazer uma ulterior seleção das células que expressam os maiores níveis de DHFR, e assim, selecionar os melhores produtores de proteínas recombinantes.[43]
Interacções
A dihidrofolato redutase interacciona com GroEL[44] e Mdm2.[45]
Referências
- ↑ Chen MJ, Shimada T, Moulton AD, Harrison M, Nienhuis AW (dezembro de 1982). «Intronless human dihydrofolate reductase genes are derived from processed RNA molecules». Proceedings of the National Academy of Sciences of the United States of America. 79 (23): 7435–9. Bibcode:1982PNAS...79.7435C. PMC 347354
 . PMID 6961421. doi:10.1073/pnas.79.23.7435
. PMID 6961421. doi:10.1073/pnas.79.23.7435
- ↑ Chen MJ, Shimada T, Moulton AD, Cline A, Humphries RK, Maizel J, Nienhuis AW (março de 1984). «The functional human dihydrofolate reductase gene». The Journal of Biological Chemistry. 259 (6): 3933–43. PMID 6323448. doi:10.1016/S0021-9258(17)43186-3
- ↑ «DHFR dihydrofolate reductase [Homo sapiens (human)]». Gene - NCBI. Consultado em 21 de fevereiro de 2023
- ↑ Smith SL, Patrick P, Stone D, Phillips AW, Burchall JJ (novembro de 1979). «Porcine liver dihydrofolate reductase. Purification, properties, and amino acid sequence». The Journal of Biological Chemistry. 254 (22): 11475–84. PMID 500653. doi:10.1016/S0021-9258(19)86510-9
- ↑ Krahn JM, Jackson MR, DeRose EF, Howell EE, London RE (dezembro de 2007). «Crystal structure of a type II dihydrofolate reductase catalytic ternary complex». Biochemistry. 46 (51): 14878–14888. PMC 3743094
 . PMID 18052202. doi:10.1021/bi701532r
. PMID 18052202. doi:10.1021/bi701532r
- ↑ a b «Entrez Gene: DHFR dihydrofolate reductase»
- ↑ a b Schnell JR, Dyson HJ, Wright PE (2004). «Structure, dynamics, and catalytic function of dihydrofolate reductase». Annual Review of Biophysics and Biomolecular Structure. 33 (1): 119–40. PMID 15139807. doi:10.1146/annurev.biophys.33.110502.133613
- ↑ Urlaub G, Chasin LA (julho de 1980). «Isolation of Chinese hamster cell mutants deficient in dihydrofolate reductase activity». Proceedings of the National Academy of Sciences of the United States of America. 77 (7): 4216–20. Bibcode:1980PNAS...77.4216U. PMC 349802
 . PMID 6933469. doi:10.1073/pnas.77.7.4216
. PMID 6933469. doi:10.1073/pnas.77.7.4216
- ↑ Crabtree MJ, Tatham AL, Hale AB, Alp NJ, Channon KM (outubro de 2009). «Critical role for tetrahydrobiopterin recycling by dihydrofolate reductase in regulation of endothelial nitric-oxide synthase coupling: relative importance of the de novo biopterin synthesis versus salvage pathways». The Journal of Biological Chemistry. 284 (41): 28128–36. PMC 2788863
 . PMID 19666465. doi:10.1074/jbc.M109.041483
. PMID 19666465. doi:10.1074/jbc.M109.041483
- ↑ Harpey JP (1989). «Chapter 17: The Relationship Between Biopterin and Folate Metabolism». In: Zittoun JA, Cooper BA. Folates and Cobalamins. [S.l.]: Springer-Verlag. pp. 215–218. ISBN 978-3-540-50653-9. doi:10.1007/978-3-642-74364-1_17
- ↑ Matthews DA, Alden RA, Bolin JT, Freer ST, Hamlin R, Xuong N, Kraut J, Poe M, Williams M, Hoogsteen K (julho de 1977). «Dihydrofolate reductase: x-ray structure of the binary complex with methotrexate». Science. 197 (4302): 452–5. Bibcode:1977Sci...197..452M. PMID 17920. doi:10.1126/science.17920
- ↑ a b Filman DJ, Bolin JT, Matthews DA, Kraut J (novembro de 1982). «Crystal structures of Escherichia coli and Lactobacillus casei dihydrofolate reductase refined at 1.7 Å resolution. II. Environment of bound NADPH and implications for catalysis». The Journal of Biological Chemistry. 257 (22): 13663–72. PMID 6815179. doi:10.1016/S0021-9258(18)33498-7
- ↑ a b Osborne MJ, Schnell J, Benkovic SJ, Dyson HJ, Wright PE (agosto de 2001). «Backbone dynamics in dihydrofolate reductase complexes: role of loop flexibility in the catalytic mechanism». Biochemistry. 40 (33): 9846–59. PMID 11502178. doi:10.1021/bi010621k
- ↑ a b c d Rod TH, Brooks CL (julho de 2003). «How dihydrofolate reductase facilitates protonation of dihydrofolate». Journal of the American Chemical Society. 125 (29): 8718–9. Bibcode:2003JAChS.125.8718R. PMID 12862454. doi:10.1021/ja035272r
- ↑ a b Wan Q, Bennett BC, Wilson MA, Kovalevsky A, Langan P, Howell EE, Dealwis C (dezembro de 2014). «Toward resolving the catalytic mechanism of dihydrofolate reductase using neutron and ultrahigh-resolution X-ray crystallography». Proceedings of the National Academy of Sciences of the United States of America. 111 (51): 18225–30. Bibcode:2014PNAS..11118225W. PMC 4280638
 . PMID 25453083. doi:10.1073/pnas.1415856111
. PMID 25453083. doi:10.1073/pnas.1415856111
- ↑ a b Liu CT, Francis K, Layfield JP, Huang X, Hammes-Schiffer S, Kohen A, Benkovic SJ (dezembro de 2014). «Escherichia coli dihydrofolate reductase catalyzed proton and hydride transfers: temporal order and the roles of Asp27 and Tyr100». Proceedings of the National Academy of Sciences of the United States of America. 111 (51): 18231–6. Bibcode:2014PNAS..11118231L. PMC 4280594
 . PMID 25453098. doi:10.1073/pnas.1415940111
. PMID 25453098. doi:10.1073/pnas.1415940111
- ↑ a b Czekster CM, Vandemeulebroucke A, Blanchard JS (janeiro de 2011). «Kinetic and chemical mechanism of the dihydrofolate reductase from Mycobacterium tuberculosis». Biochemistry. 50 (3): 367–75. PMC 3074011
 . PMID 21138249. doi:10.1021/bi1016843
. PMID 21138249. doi:10.1021/bi1016843
- ↑ a b c Fierke CA, Johnson KA, Benkovic SJ (junho de 1987). «Construction and evaluation of the kinetic scheme associated with dihydrofolate reductase from Escherichia coli». Biochemistry. 26 (13): 4085–92. PMID 3307916. doi:10.1021/bi00387a052
- ↑ Reyes VM, Sawaya MR, Brown KA, Kraut J (fevereiro de 1995). «Isomorphous crystal structures of Escherichia coli dihydrofolate reductase complexed with folate, 5-deazafolate, and 5,10-dideazatetrahydrofolate: mechanistic implications». Biochemistry. 34 (8): 2710–23. PMID 7873554. doi:10.1021/bi00008a039
- ↑ a b c Sawaya MR, Kraut J (janeiro de 1997). «Loop and subdomain movements in the mechanism of Escherichia coli dihydrofolate reductase: crystallographic evidence». Biochemistry. 36 (3): 586–603. PMID 9012674. doi:10.1021/bi962337c
- ↑ Chen YQ, Kraut J, Blakley RL, Callender R (junho de 1994). «Determination by Raman spectroscopy of the pKa of N5 of dihydrofolate bound to dihydrofolate reductase: mechanistic implications». Biochemistry. 33 (23): 7021–6. PMID 8003467. doi:10.1021/bi00189a001
- ↑ Shrimpton P, Allemann RK (junho de 2002). «Role of water in the catalytic cycle of E. coli dihydrofolate reductase». Protein Science. 11 (6): 1442–51. PMC 2373639
 . PMID 12021443. doi:10.1110/ps.5060102
. PMID 12021443. doi:10.1110/ps.5060102
- ↑ Antikainen NM, Smiley RD, Benkovic SJ, Hammes GG (dezembro de 2005). «Conformation coupled enzyme catalysis: single-molecule and transient kinetics investigation of dihydrofolate reductase». Biochemistry. 44 (51): 16835–43. PMID 16363797. doi:10.1021/bi051378i
- ↑ Narayana N, Matthews DA, Howell EE, Nguyen-huu X (novembro de 1995). «A plasmid-encoded dihydrofolate reductase from trimethoprim-resistant bacteria has a novel D2-symmetric active site». Nature Structural Biology. 2 (11): 1018–25. PMID 7583655. doi:10.1038/nsb1195-1018
- ↑ Bradrick TD, Beechem JM, Howell EE (setembro de 1996). «Unusual binding stoichiometries and cooperativity are observed during binary and ternary complex formation in the single active pore of R67 dihydrofolate reductase, a D2 symmetric protein». Biochemistry. 35 (35): 11414–24. PMID 8784197. doi:10.1021/bi960205d
- ↑ Park H, Zhuang P, Nichols R, Howell EE (janeiro de 1997). «Mechanistic studies of R67 dihydrofolate reductase. Effects of pH and an H62C mutation». The Journal of Biological Chemistry. 272 (4): 2252–8. PMID 8999931. doi:10.1074/jbc.272.4.2252
- ↑ Kamath G, Howell EE, Agarwal PK (outubro de 2010). «The tail wagging the dog: insights into catalysis in R67 dihydrofolate reductase». Biochemistry. 49 (42): 9078–88. PMID 20795731. doi:10.1021/bi1007222
- ↑ Banka S, Blom HJ, Walter J, Aziz M, Urquhart J, Clouthier CM, Rice GI, de Brouwer AP, Hilton E, Vassallo G, Will A, Smith DE, Smulders YM, Wevers RA, Steinfeld R, Heales S, Crow YJ, Pelletier JN, Jones S, Newman WG (fevereiro de 2011). «Identification and characterization of an inborn error of metabolism caused by dihydrofolate reductase deficiency». American Journal of Human Genetics. 88 (2): 216–25. PMC 3035707
 . PMID 21310276. doi:10.1016/j.ajhg.2011.01.004
. PMID 21310276. doi:10.1016/j.ajhg.2011.01.004
- ↑ Nyhan WL, Hoffmann GF, Barshop BA (30 de dezembro de 2011). Atlas of Inherited Metabolic Diseases 3E. [S.l.]: CRC Press. pp. 141–. ISBN 978-1-4441-4948-7
- ↑ Cowman AF, Lew AM (novembro de 1989). «Antifolate drug selection results in duplication and rearrangement of chromosome 7 in Plasmodium chabaudi». Molecular and Cellular Biology. 9 (11): 5182–8. PMC 363670
 . PMID 2601715. doi:10.1128/mcb.9.11.5182
. PMID 2601715. doi:10.1128/mcb.9.11.5182
- ↑ Li R, Sirawaraporn R, Chitnumsub P, Sirawaraporn W, Wooden J, Athappilly F, Turley S, Hol WG (janeiro de 2000). «Three-dimensional structure of M. tuberculosis dihydrofolate reductase reveals opportunities for the design of novel tuberculosis drugs». Journal of Molecular Biology. 295 (2): 307–23. PMID 10623528. doi:10.1006/jmbi.1999.3328
- ↑ Bailey SW, Ayling JE (setembro de 2009). «The extremely slow and variable activity of dihydrofolate reductase in human liver and its implications for high folic acid intake». Proceedings of the National Academy of Sciences of the United States of America. 106 (36): 15424–9. PMC 2730961
 . PMID 19706381. doi:10.1073/pnas.0902072106
. PMID 19706381. doi:10.1073/pnas.0902072106
- ↑ Murad AM, Santiago FF, Petroianu A, Rocha PR, Rodrigues MA, Rausch M (julho de 1993). «Modified therapy with 5-fluorouracil, doxorubicin, and methotrexate in advanced gastric cancer». Cancer. 72 (1): 37–41. PMID 8508427. doi:10.1002/1097-0142(19930701)72:1<37::AID-CNCR2820720109>3.0.CO;2-P
- ↑ a b c Hawser S, Lociuro S, Islam K (março de 2006). «Dihydrofolate reductase inhibitors as antibacterial agents». Biochemical Pharmacology. 71 (7): 941–8. PMID 16359642. doi:10.1016/j.bcp.2005.10.052
- ↑ Narayana N, Matthews DA, Howell EE, Nguyen-huu X (novembro de 1995). «A plasmid-encoded dihydrofolate reductase from trimethoprim-resistant bacteria has a novel D2-symmetric active site». Nature Structural Biology. 2 (11): 1018–25. PMID 7583655. doi:10.1038/nsb1195-1018
- ↑ Huennekens FM (junho de 1996). «In search of dihydrofolate reductase». Protein Science. 5 (6): 1201–8. PMC 2143423
 . PMID 8762155. doi:10.1002/pro.5560050626
. PMID 8762155. doi:10.1002/pro.5560050626
- ↑ Banerjee D, Mayer-Kuckuk P, Capiaux G, Budak-Alpdogan T, Gorlick R, Bertino JR (julho de 2002). «Novel aspects of resistance to drugs targeted to dihydrofolate reductase and thymidylate synthase». Biochimica et Biophysica Acta (BBA) - Molecular Basis of Disease. 1587 (2–3): 164–73. PMID 12084458. doi:10.1016/S0925-4439(02)00079-0
- ↑ Toprak E, Veres A, Michel JB, Chait R, Hartl DL, Kishony R (dezembro de 2011). «Evolutionary paths to antibiotic resistance under dynamically sustained drug selection». Nature Genetics. 44 (1): 101–5. PMC 3534735
 . PMID 22179135. doi:10.1038/ng.1034
. PMID 22179135. doi:10.1038/ng.1034
- ↑ Rodrigues JV, Bershtein S, Li A, Lozovsky ER, Hartl DL, Shakhnovich EI (março de 2016). «Biophysical principles predict fitness landscapes of drug resistance». Proceedings of the National Academy of Sciences of the United States of America. 113 (11): E1470-8. Bibcode:2016PNAS..113E1470R. PMC 4801265
 . PMID 26929328. doi:10.1073/pnas.1601441113
. PMID 26929328. doi:10.1073/pnas.1601441113
- ↑ Benkovic SJ, Fierke CA, Naylor AM (março de 1988). «Insights into enzyme function from studies on mutants of dihydrofolate reductase». Science. 239 (4844): 1105–10. Bibcode:1988Sci...239.1105B. PMID 3125607. doi:10.1126/science.3125607
- ↑ a b Beierlein JM, Karri NG, Anderson AC (outubro de 2010). «Targeted mutations of Bacillus anthracis dihydrofolate reductase condense complex structure−activity relationships». Journal of Medicinal Chemistry. 53 (20): 7327–36. PMC 3618964
 . PMID 20882962. doi:10.1021/jm100727t
. PMID 20882962. doi:10.1021/jm100727t
- ↑ Tarassov K, Messier V, Landry CR, Radinovic S, Serna Molina MM, Shames I, Malitskaya Y, Vogel J, Bussey H, Michnick SW (junho de 2008). «An in vivo map of the yeast protein interactome» (PDF). Science. 320 (5882): 1465–70. Bibcode:2008Sci...320.1465T. PMID 18467557. doi:10.1126/science.1153878
- ↑ Ng SK (2012). «Generation of High-Expressing Cells by Methotrexate Amplification of Destabilized Dihydrofolate Reductase Selection Marker». Protein Expression in Mammalian Cells. Col: Methods in Molecular Biology. 801. [S.l.: s.n.] pp. 161–172. ISBN 978-1-61779-351-6. PMID 21987253. doi:10.1007/978-1-61779-352-3_11
- ↑ Mayhew M, da Silva AC, Martin J, Erdjument-Bromage H, Tempst P, Hartl FU (fevereiro de 1996). «Protein folding in the central cavity of the GroEL-GroES chaperonin complex». Nature. 379 (6564): 420–6. Bibcode:1996Natur.379..420M. PMID 8559246. doi:10.1038/379420a0
- ↑ Maguire M, Nield PC, Devling T, Jenkins RE, Park BK, Polański R, Vlatković N, Boyd MT (maio de 2008). «MDM2 regulates dihydrofolate reductase activity through monoubiquitination». Cancer Research. 68 (9): 3232–42. PMC 3536468
 . PMID 18451149. doi:10.1158/0008-5472.CAN-07-5271
. PMID 18451149. doi:10.1158/0008-5472.CAN-07-5271
Bibliografia
- Joska TM, Anderson AC (outubro de 2006). «Structure-activity relationships of Bacillus cereus and Bacillus anthracis dihydrofolate reductase: toward the identification of new potent drug leads». Antimicrobial Agents and Chemotherapy. 50 (10): 3435–43. PMC 1610094
 . PMID 17005826. doi:10.1128/AAC.00386-06
. PMID 17005826. doi:10.1128/AAC.00386-06 - Chan DC, Fu H, Forsch RA, Queener SF, Rosowsky A (junho de 2005). «Design, synthesis, and antifolate activity of new analogues of piritrexim and other diaminopyrimidine dihydrofolate reductase inhibitors with omega-carboxyalkoxy or omega-carboxy-1-alkynyl substitution in the side chain». Journal of Medicinal Chemistry. 48 (13): 4420–31. PMID 15974594. doi:10.1021/jm0581718
- Banerjee D, Mayer-Kuckuk P, Capiaux G, Budak-Alpdogan T, Gorlick R, Bertino JR (julho de 2002). «Novel aspects of resistance to drugs targeted to dihydrofolate reductase and thymidylate synthase». Biochimica et Biophysica Acta (BBA) - Molecular Basis of Disease. 1587 (2–3): 164–73. PMID 12084458. doi:10.1016/S0925-4439(02)00079-0

- Stockman BJ, Nirmala NR, Wagner G, Delcamp TJ, DeYarman MT, Freisheim JH (janeiro de 1992). «Sequence-specific 1H and 15N resonance assignments for human dihydrofolate reductase in solution». Biochemistry. 31 (1): 218–29. PMID 1731871. doi:10.1021/bi00116a031
- Beltzer JP, Spiess M (dezembro de 1991). «In vitro binding of the asialoglycoprotein receptor to the beta adaptin of plasma membrane coated vesicles». The EMBO Journal. 10 (12): 3735–42. PMC 453108
 . PMID 1935897. doi:10.1002/j.1460-2075.1991.tb04942.x
. PMID 1935897. doi:10.1002/j.1460-2075.1991.tb04942.x - Davies JF, Delcamp TJ, Prendergast NJ, Ashford VA, Freisheim JH, Kraut J (outubro de 1990). «Crystal structures of recombinant human dihydrofolate reductase complexed with folate and 5-deazafolate». Biochemistry. 29 (40): 9467–79. PMID 2248959. doi:10.1021/bi00492a021
- Will CL, Dolnick BJ (dezembro de 1989). «5-Fluorouracil inhibits dihydrofolate reductase precursor mRNA processing and/or nuclear mRNA stability in methotrexate-resistant KB cells». The Journal of Biological Chemistry. 264 (35): 21413–21. PMID 2592384. doi:10.1016/S0021-9258(19)30096-1

- Masters JN, Attardi G (março de 1985). «Discrete human dihydrofolate reductase gene transcripts present in polysomal RNA map with their 5' ends several hundred nucleotides upstream of the main mRNA start site». Molecular and Cellular Biology. 5 (3): 493–500. PMC 366741
 . PMID 2859520. doi:10.1128/mcb.5.3.493
. PMID 2859520. doi:10.1128/mcb.5.3.493 - Miszta H, Dabrowski Z, Lanotte M (novembro de 1988). «In vitro patterns of enzymic tetrahydrofolate dehydrogenase (EC 1.5.1.3) expression in bone marrow stromal cells». Leukemia. 2 (11): 754–9. PMID 3185016
- Oefner C, D'Arcy A, Winkler FK (junho de 1988). «Crystal structure of human dihydrofolate reductase complexed with folate». European Journal of Biochemistry. 174 (2): 377–85. PMID 3383852. doi:10.1111/j.1432-1033.1988.tb14108.x

- Yang JK, Masters JN, Attardi G (junho de 1984). «Human dihydrofolate reductase gene organization. Extensive conservation of the G + C-rich 5' non-coding sequence and strong intron size divergence from homologous mammalian genes». Journal of Molecular Biology. 176 (2): 169–87. PMID 6235374. doi:10.1016/0022-2836(84)90419-4
- Masters JN, Yang JK, Cellini A, Attardi G (junho de 1983). «A human dihydrofolate reductase pseudogene and its relationship to the multiple forms of specific messenger RNA». Journal of Molecular Biology. 167 (1): 23–36. PMID 6306253. doi:10.1016/S0022-2836(83)80032-1
- Chen MJ, Shimada T, Moulton AD, Cline A, Humphries RK, Maizel J, Nienhuis AW (março de 1984). «The functional human dihydrofolate reductase gene». The Journal of Biological Chemistry. 259 (6): 3933–43. PMID 6323448. doi:10.1016/S0021-9258(17)43186-3

- Funanage VL, Myoda TT, Moses PA, Cowell HR (outubro de 1984). «Assignment of the human dihydrofolate reductase gene to the q11----q22 region of chromosome 5». Molecular and Cellular Biology. 4 (10): 2010–6. PMC 369017
 . PMID 6504041. doi:10.1128/mcb.4.10.2010
. PMID 6504041. doi:10.1128/mcb.4.10.2010 - Masters JN, Attardi G (1983). «The nucleotide sequence of the cDNA coding for the human dihydrofolic acid reductase». Gene. 21 (1–2): 59–63. PMID 6687716. doi:10.1016/0378-1119(83)90147-6
- Morandi C, Masters JN, Mottes M, Attardi G (abril de 1982). «Multiple forms of human dihydrofolate reductase messenger RNA. Cloning and expression in Escherichia coli of their DNA coding sequence». Journal of Molecular Biology. 156 (3): 583–607. PMID 6750132. doi:10.1016/0022-2836(82)90268-6
- Bonifaci N, Sitia R, Rubartelli A (setembro de 1995). «Nuclear translocation of an exogenous fusion protein containing HIV Tat requires unfolding». AIDS. 9 (9): 995–1000. PMID 8527095. doi:10.1097/00002030-199509000-00003
- Mayhew M, da Silva AC, Martin J, Erdjument-Bromage H, Tempst P, Hartl FU (fevereiro de 1996). «Protein folding in the central cavity of the GroEL-GroES chaperonin complex». Nature. 379 (6564): 420–6. Bibcode:1996Natur.379..420M. PMID 8559246. doi:10.1038/379420a0
- Gross M, Robinson CV, Mayhew M, Hartl FU, Radford SE (dezembro de 1996). «Significant hydrogen exchange protection in GroEL-bound DHFR is maintained during iterative rounds of substrate cycling». Protein Science. 5 (12): 2506–13. PMC 2143321
 . PMID 8976559. doi:10.1002/pro.5560051213
. PMID 8976559. doi:10.1002/pro.5560051213 - Schleiff E, Shore GC, Goping IS (março de 1997). «Human mitochondrial import receptor, Tom20p. Use of glutathione to reveal specific interactions between Tom20-glutathione S-transferase and mitochondrial precursor proteins». FEBS Letters. 404 (2–3): 314–8. Bibcode:1997FEBSL.404..314S. PMID 9119086. doi:10.1016/S0014-5793(97)00145-2

- Cody V, Galitsky N, Luft JR, Pangborn W, Rosowsky A, Blakley RL (novembro de 1997). «Comparison of two independent crystal structures of human dihydrofolate reductase ternary complexes reduced with nicotinamide adenine dinucleotide phosphate and the very tight-binding inhibitor PT523». Biochemistry. 36 (45): 13897–903. PMID 9374868. doi:10.1021/bi971711l
- Vanguri VK, Wang S, Godyna S, Ranganathan S, Liau G (abril de 2000). «Thrombospondin-1 binds to polyhistidine with high affinity and specificity». The Biochemical Journal. 347 (Pt 2): 469–73. PMC 1220979
 . PMID 10749676. doi:10.1042/0264-6021:3470469
. PMID 10749676. doi:10.1042/0264-6021:3470469