Ciclo catalítico
Catálise é um campo da Química que trata de substâncias capazes de aumentar a velocidade das reações químicas sem serem consumidas permanentemente. Esses materiais, denominados catalisadores, oferecem um caminho reacional alternativo com menor energia de ativação. Catalisadores são empregados em diversos processos industriais e em sistemas biológicos, contribuindo para maior eficiência e para o desenvolvimento de tecnologias voltadas à redução de impactos ambientais.[1]
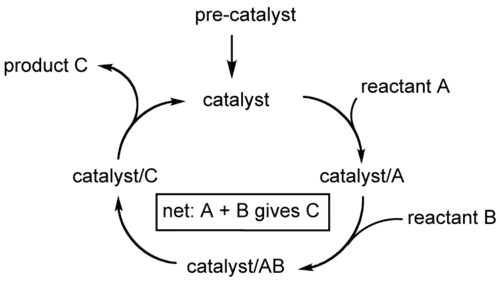
Ciclo catalítico
O ciclo catalítico é o principal método para escrever o papel de catalisadores em bioquímica, química de organometálicos, ciência dos materiais, etc. Além disso, corresponde à sequência de reações pelas quais o catalisador passa, iniciando pela ativação, seguindo por etapas intermediárias e finalizando com sua regeneração, que o devolve à forma original [2].Essa regeneração permite que o catalisador realize múltiplos ciclos, caracterizando parâmetros como a frequência de turnover [3].O conceito é aplicado em diferentes modalidades de catálise — homogênea, heterogênea e enzimática — nas quais a manutenção da atividade e da integridade do catalisador é essencial.
A compreensão dos ciclos catalíticos envolve diversos termos básicos. Um catalisador é a substância que aumenta a velocidade de uma reação química sem ser consumida permanentemente. A energia de ativação é o valor mínimo necessário para que a transformação ocorra. Em catalisadores sólidos, as reações ocorrem em regiões específicas chamadas sítios ativos. O desempenho catalítico é avaliado pela atividade, associada à velocidade reacional, e pela seletividade, que indica a preferência pela formação de um produto. O número de turnover (TON) indica a quantidade total de ciclos realizados pelo catalisador, enquanto a frequência de turnover (TOF) expressa a taxa com que estes ciclos ocorrem. A desativação corresponde à perda de atividade ao longo do
tempo, podendo ser causada por deposição de coque, sinterização, contaminação ou mudanças estruturais. [4],[5],[6]
Mecanismo e etapas gerais
Apesar das diferenças entre sistemas catalíticos, muitos ciclos seguem uma sequência comum. A etapa inicial é a ativação do catalisador, que assume a forma química necessária para participar da reação. Na etapa seguinte ocorre a coordenação do reagente
à espécie catalítica. A transformação química, responsável por quebras e formações de ligações, constitui o núcleo do processo. Ao final, o produto é liberado e o catalisador retorna ao estado original, permitindo o reinício do ciclo.[1] [3]
Etapas na catálise homogênea
Na catálise homogênea, especialmente quando são utilizados complexos de metais de transição como paládio, ródio ou níquel, os mecanismos costumam incluir três etapas elementares: adição oxidativa, inserção migratória e eliminação redutiva.
- Adição oxidativa ocorre quando o metal, em um estado de oxidação mais baixo, reage com um substrato contendo uma ligação A–B, passando a coordenar ambos os fragmentos e sofrendo aumento de duas unidades no estado de oxidação e no número de coordenação.
- Inserção migratória envolve a migração de um grupo alquila ou arila para um ligante insaturado coordenado ao metal, como monóxido de carbono ou olefinas. Nessa etapa, o estado de oxidação do metal tende a permanecer inalterado, embora possa ocorrer alteração no número de ligantes devido a dissociação ou coordenação auxiliar.
- Eliminação redutiva, o estado de oxidação do centro metálico reduz enquanto forma uma nova ligação covalente entre dois ligantes, ou seja, dois grupos adjacentes se combinam e são liberados como produto, enquanto o metal retorna ao estado de oxidação inicial, reiniciando o ciclo catalítico.[5] [6]
Etapas na catálise heterogênea
Na catálise heterogênea, a reação ocorre na superfície do catalisador em estudo, onde estão presentes seus sítios ativos. De modo geral, o processo segue a seguinte sequência: inicialmente, ocorre a difusão dos reagentes da fase fluida até a superfície da partícula catalítica, seguida da difusão dos reagentes para o interior dos poros do catalisador, onde se dá a etapa de adsorção dos reagentes nos centros ativos por meio de uma reação química. Por fim, ocorre a dessorção dos produtos formados e a difusão desses produtos até a superfície externa do catalisador, além da difusão dos produtos da superfície externa para a fase fluida.
Aplicações e sustentabilidade
Os ciclos catalíticos têm papel central em diferentes setores industriais. Na indústria química, participam da produção de polímeros, combustíveis e intermediários petroquímicos, incluindo processos de grande escala, como o Haber–Bosch para síntese de amônia. Na síntese orgânica fina, são fundamentais em reações de acoplamento, oxidações seletivas e hidrogenações utilizadas na fabricação de fármacos e outros compostos de alto valor agregado. No âmbito da sustentabilidade, a catálise contribui para o desenvolvimento de rotas químicas mais eficientes e menos impactantes. Ciclos catalíticos bem estabelecidos permitem reduzir o consumo energético, minimizar a formação de resíduos e diminuir o uso de reagentes de maior toxicidade. Entre as aplicações de interesse ambiental destacam-se a conversão de dióxido de carbono em combustíveis e a transformação de biomassa em produtos químicos úteis .[1][5][6]
Conclusão
Os ciclos catalíticos representam a estrutura base da química moderna, e o seu entendimento detalhado é a chave para o desenvolvimento de materiais mais seletivos, eficientes e sustentáveis.
Referências:
[1]. FERNANDES, R. A.; SILVA, D. M. (org.). Princípios e aplicações em catálise –Volume 1. Belo Horizonte: Editora Poisson, 2020.
[2].WIKIPEDIA. Catalytic cycle. Disponível em:<https://en.wikipedia.org/wiki/Catalytic_cycle>. Acesso em: 6 dez. 2025.
[3]. VANNICE, M. A. Kinetics of Catalytic Reactions. New York: Springer, 2005.
[4].KOZUCH, S.; MARTINS, L.; et al. Trabalhos sobre TON e TOF em catálise homogênea e heterogênea. [Informações adicionais como editora, local e ano são necessárias para completar a referência.
[5]. HARTWIG, J. F. Organotransition Metal Chemistry: From Bonding to Catalysis.University Science Books, 2010.
[6] CRABTREE, R. H. The Organometallic Chemistry of the Transition Metals.Hoboken: Wiley, 2014.
- ↑ Vilas-Bôas, Renata Nazaré; Fernandes, Lindoval Domiciano; Mendes, Marisa Fernandes (2024). «Hidroxiapatita como catalisador heterogêneo para a produção de biodiesel». Editora Poisson. ISBN 978-65-5866-435-2. Consultado em 10 de dezembro de 2025