Inibição competitiva
2OH)
2) para a enzima álcool desidrogenase no fígado quando estão presentes em grandes quantidades. Por esta razão, o etanol é às vezes utilizado como meio para tratar ou prevenir a toxicidade após a ingestão acidental dos outros dois compostos químicos.
A inibição competitiva é a interrupção de uma reação ou via química devido a uma substância química que inibe o efeito de outra ao competir com ela para se ligar quimicamente a uma terceira, seja em enzimologia ou noutros processos químicos. Qualquer sistema metabólico ou mensageiro químico poderia ser afetado por este princípio, mas várias classes de inibição competitiva são especialmente importantes em bioquímica e medicina, incluindo a inibição enzimática de tipo competitivo, a forma competitiva do antagonismo de recetor, a forma competitiva da atividade de antimetabólitos, e a forma competitiva dos envenenamentos (a qual pode incluir qualquer um dos tipos antes mencionados).
Inibição competitiva enzimática
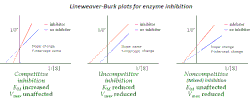
Na inibição competitiva da catálise enzimática, a ligação de um inibidor impede a ligação da molécula sobre a qual a enzima atua, chamada substrato.[1] Isto é realizado bloqueando o local de ligação do substrato – o local ativo – por algum mecanismo. A Vmax indica a velocidade máxima da reação, enquanto que a Km é a quantidade de substância necessária para atingir metade da Vmax. A Km também serve para indicar a tendência do substrato a ligar-se à enzima.[2] A inibição competitiva pode ser superada adicionando mais substrato à reação, o que aumenta as hipóteses de a enzima e o substrato se ligarem. Como resultado, a inibição competitiva altera apenas a Km, deixando a Vmax igual.[3] Isto pode ser demonstrado usando gráficos da cinética enzimática como a de Michaelis-Menten ou a de Lineweaver-Burk. Uma vez que o inibidor se ligou à enzima, a inclinação é alterada, já que a Km faz aumentar ou diminuir a Km original da reação.[4][5][6]
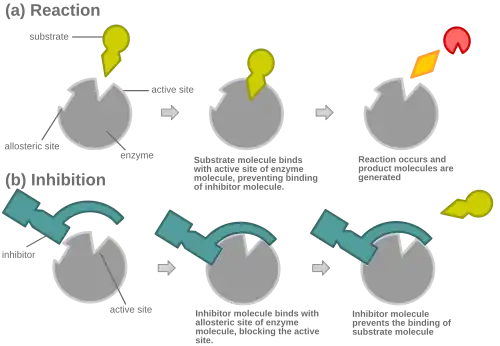
A maioria dos inibidores competitivos funciona ligando-se reversivelmente ao local ativo da enzima.[1] Como resultado, muitas fontes afirmam que esta é a caraterística definidora dos inibidores competitivos.[7] Contudo, isto é uma simplificação excessiva que pode levar à confusão, já que há muitos mecanismos possíveis pelos quais uma enzima pode ligar-se a um inibidor ou ao substrato, mas nunca a ambos ao mesmo tempo.[1] Por exemplo, os inibidores alostéricos podem mostrar inibição competitiva, não-competitiva ou incompetitiva (ou acompetitiva).[1]
Mecanismo
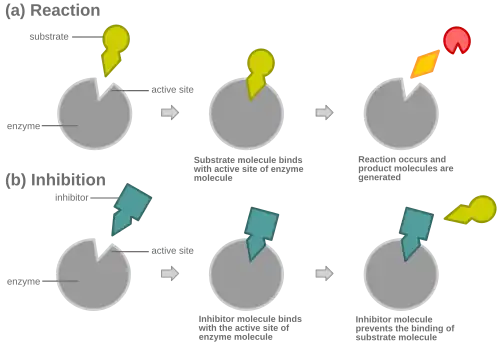
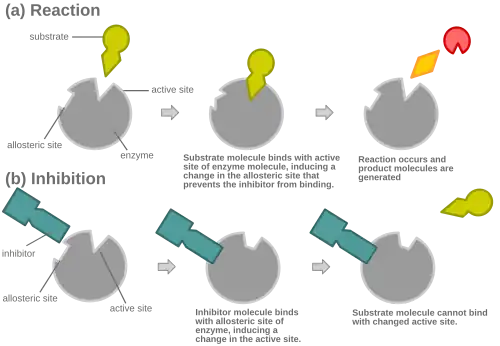
Na inibição competitiva, um inibidor que se assemelha ao substrato normal liga-se à enzima, geralmente no sítio ativo, e impede que o substrato se ligue.[8] Num dado momento, a enzima pode estar ligada ao inibidor, ao substrato, ou a nenhum dos dois, mas não pode estar ligada a ambos ao mesmo tempo. Durante a inibição competitiva, o inibidor e o substrato competem pelo sítio ativo. O sítio ativo é a região da enzima à qual se pode ligar uma determinada proteína ou substrato. O sítio ativo só permite que um dos dois complexos se ligue ao sítio, ou permite que ocorra uma reação ou rendimento de um produto. Na inibição competitiva um inibidor parecido com o substrato ocupa o seu lugar ao ligar-se ao sítio ativo da enzima. Aumentando a concentração de substrato diminuirá a "competição" para que o substrato se ligue corretamente ao sítio ativo e a reação ocorra.[3] Quando o substrato está em maior concentração do que o inibidor competitivo, as probabilidades de ser o substrato a entrar em contacto com o sítio ativo da enzima são maiores do que as que tem o inibidor.
Os inibidores competitivos são frequentemente utilizados para fabricar fármacos.[3] Por exemplo, o metotrexato é um quimioterápico que atua como inibidor competitivo. É estruturalmente semelhante à coenzima, o folato, que se liga à enzima di-hidrofolato redutase.[3] Esta enzima está envolvida na síntese do ADN e ARN, e quando o metotrexato se liga à enzima, esta fica inativa, assim que não se pode sintetizar ADN ou ARN.[3] Nessas circunstâncias, as células cancerosas são, portanto, incapazes de crescer e dividir-se. Outro exemplo: as prostaglandinas são produzidas em grandes quantidades como resposta à dor e podem causar inflamação. Os ácidos gordos essenciais são utilizados para formar as prostaglandinas; quando isto foi descoberto, verificou-se que estes eram também inibidores muito bons dos efeitos das prostaglandinas. Estes ácidos gordos inibidores foram utilizados como fármacos para aliviar a dor porque podem atuar como substrato, e ligar-se à enzima que sintetiza as prostaglandinas, e bloquear a sua produção.[9]
Um exemplo de inibição competitiva não relacionada com fármacos é a que intervém na prevenção do murchamento (escurecimento enzimático) de frutas e vegetais. Por exemplo, a tirosinase, uma enzima dos cogumelos, normalmente liga-se aos seus substratos, os monofenóis, e forma o-quinonas castanhas.[10] Os substratos competitivos, como os benzaldeídos substituídos na posição 4 dos cogumelos, competem com o substrato, diminuindo a quantidade de monofenóis que se ligam. Estes compostos inibidores são adicionados para fazer com que os vegetais se mantenham frescos durante longos períodos de tempo ao diminuírem a ligação de monofenóis que causam o murchamento .[10] Isto permite um aumento da vida do produto nas lojas.
A inibição competitiva pode ser reversível ou irreversível. Se é uma inibição reversível, então os efeitos da inibição podem ser superados aumentando a concentração de substrato.[8] Se é irreversível, a única maneira de superá-lo é produzindo mais enzimas (e degradar ou excretar a enzima inibida irreversivelmente).
Virtualmente em todos os casos, os inibidores competitivos ligam-se no mesmo sítio de ligação (o sítio ativo) que o substrato, mas não é imprescindível que seja o mesmo sítio de ligação. Um inibidor competitivo poderia ligar-se a um sítio alostérico da enzima livre e impedir a ligação do substrato, desde que não se ligue ao sítio alostérico no momento em que o substrato está ligado à enzima. Por exemplo, a estricnina atua como um inibidor alostérico do recetor da glicina na medula espinhal e no tronco cerebral de mamíferos. A glicina é um importante neurotransmissor pós-sináptico com um sítio recetor específico. A estricnina liga-se a um sítio alternativo que reduz a afinidade do recetor da glicina pela glicina, o que resulta em convulsões devido à diminuição da inibição pela glicina.[11]
Na inibição competitiva, a velocidade máxima () não muda, enquanto que a afinidade aparente do substrato com o sítio de ligação diminui (a constante de dissociação aparentemente aumenta). A alteração na (constante de Michaelis-Menten) é paralela à alteração de , já que enquanto uma aumenta a outra deve diminuir. Quando um inibidor competitivo se liga a uma enzima, a aumenta. Isto significa que a afinidade de ligação pela enzima diminui, mas isto pode ser superado aumentando a concentração do substrato.[12] O efeito de qualquer concentração dada de inibidor competitivo pode ser superado aumentando a concentração de substrato. Nesse caso, o substrato reduzirá a disponibilidade de moléculas inibidoras que se possam ligar, e assim, supera na competição ao inibidor na hora de se ligar à enzima.[12]
Exemplos biológicos
Após uma ingestão acidental de uma droga opiácea contaminada, a desmetilprodina, descobriu-se o efeito neurotóxico da 1-metil-4-fenil-1,2,3,6-tetraidropiridina (MPTP). A MPTP pode cruzar a barreira hematoencefálica e entrar nos lisossomas ácidos.[13] A MPTP é ativada biologicamente pela MAO-B, uma isoenzima da monoamina oxidase (MAO) que está concentrada principalmente nos transtornos e doenças neurológicas.[14] Posteriormente, descobriu-se que a MPTP causa sintomas semelhantes à doença de Parkinson. As células do sistema nervoso central (astrócitos) têm MAO-B que oxida MPTP a 1-metil-4-fenilpiridínio (MPP+), que é tóxico.[13] O MPP+ viaja finalmente para o fluido extracelular por meio de um transportador de dopamina, o que em último extremo causa os sintomas de Parkinson. Contudo, a inibição competitiva da enzima MAO-B ou do transportador de dopamina protege contra a oxidação da MPTP a MPP+. Testaram-se alguns compostos para comprovar a sua capacidade de inibir a oxidação da MPTP a MPP+, como o azul de metileno, o 5-nitroindazol, o nor-harman, o 9-metilnor-harman e a menadiona.[14] Estes demonstraram uma redução da neurotoxicidade produzida pela MPTP.
As sulfamidas também atuam como inibidores competitivos. Por exemplo, a sulfanilamida liga-se competitivamente a uma enzima no sítio ativo da di-hidropteroato sintase (DHPS) ao imitar o substrato ácido para-aminobenzoico (PABA).[15] Isto impede que o próprio substrato se ligue, o que interrompe a produção de ácido fólico, um nutriente essencial. As bactérias devem sintetizar ácido fólico porque não têm um transportador para ele. Sem ácido fólico, as bactérias não podem crescer e dividir-se. Portanto, devido à inibição competitiva dos fármacos sulfamidas, estes são excelentes agentes antibacterianos.
Um exemplo de inibição competitiva demonstrou-se experimentalmente na enzima succinato desidrogenase, que catalisa a oxidação do succinato a fumarato no ciclo do ácido cítrico ou de Krebs. O malonato é um inibidor competitivo da succinato desidrogenase. A ligação da succinato desidrogenase ao substrato, o succinato, é inibida competitivamente. Isto acontece porque a química do malonato é semelhante à do succinato. A capacidade do malonato de inibir a ligação da enzima e do substrato está baseada na proporção de malonato para succinato. O malonato liga-se ao sítio ativo da succinato desidrogenase para que o succinato não o possa fazer. Assim, inibe a reação.[16]
Equação
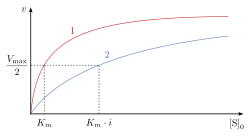
O modelo de Michaelis-Menten pode ser uma ferramenta valiosa para compreender a cinética enzimática. Segundo este modelo, um gráfico da velocidade de reação (V0) associada à concentração de substrato [S] pode então ser utilizado para determinar valores como Vmax, velocidade inicial e Km (Vmax/2 ou afinidade do complexo enzima-substrato).[4] A inibição competitiva aumenta o valor aparente da constante de Michaelis-Menten, , tal que a velocidade da reacção, , é dada por
onde , é a constante de dissociação do inibidor e é a concentração do inibidor.
permanece igual porque a presença do inibidor pode ser superada por uma concentração maior do substrato. , A concentração de substrato que é necessária para atingir , aumenta com a presença de um inibidor competitivo. Isto deve-se a que a concentração de substrato necessária para atingir a com um inibidor é maior do que a concentração de substrato necessária para atingir a sem inibidor.
Derivação
No caso mais simples de uma enzima com um só substrato que obedece à cinética de Michaelis-Menten, o esquema típico :
é modificado para incluir a ligação do inibidor com enzimas livres:
Note-se que o inibidor não se liga ao complexo ES e o substrato não se liga ao complexo EI. Assume-se geralmente que este comportamento é indicativo da ligação de ambos os compostos ao mesmo sítio, mas que não é estritamente necessário. Tal como na derivação da equação de Michaelis-Menten, supõe-se que o sistema está no estado estacionário, ou seja, a concentração de cada uma das espécies de enzima não está a mudar.
Além disso, a concentração de enzima total conhecida é , e a velocidade é medida em condições nas quais as concentrações de substrato e inibidor não mudam substancialmente e se acumulou uma quantidade insignificante de produto. Portanto, podemos utilizar o seguinte sistema de equações:
-
(1)
-
(2)
-
(3)
-
(4)
onde se conhecem
e .
A velocidade inicial define-se como , assim precisamos de definir a desconhecida em relação às e conhecidas.
Da equação (3), podemos definir E em termos de ES rearranjando-a para
Dividindo por dá :
Tal como na derivação da equação de Michaelis-Menten, o termo pode ser substituído por uma constante de velocidade macroscópica :
-
(5)
Substituindo a equação (5) na equação (4), temos :
Operando, obtemos que :
Neste momento, podemos definir a constante de dissociação para o inibidor como , dando
-
(6)
Agora, substituímos a equação (5) e a equação (6) na equação (1):
Operando para isolar ES, temos
-
(7)
Voltando à nossa expressão de , agora temos:
Dado que a velocidade é máxima quando todas as enzimas estão ligadas na forma complexo enzima-substrato, . Substituindo e combinando termos obtemos finalmente a forma convencional:
-
(8)
Para calcular a concentração de inibidor competitivo que produz uma fração da velocidade onde :
-
(9)
Referências
- ↑ a b c d «Types of Inhibition». NIH Center for Translational Therapeutics. Consultado em 2 de abril de 2012. Cópia arquivada em 8 de setembro de 2011
- ↑ Lodish H, Berk A, Zipursky SL, Matsudaira P, Baltimore D, Darnell J (2000). «Functional Design of Proteins». Molecular Cell Biology 4ª ed. [S.l.: s.n.]
- ↑ a b c d e Berg JM, Tymoczko JL, Stryer L (2002). «Enzymes Can Be Inhibited by Specific Molecules» 5ª ed. Biochemistry
- ↑ a b Berg JM, Tymoczko JL, Stryer L (2002). «The Michaelis–Menten Model Accounts for the Kinetic Properties of Many Enzymes». Biochemistry 5ª ed. [S.l.: s.n.]
- ↑ Eadie SG (1942). «The Inhibition of Cholinesterase by Physostigmine and Prostigmine». Journal of Biological Chemistry. 146: 85–93. doi:10.1016/S0021-9258(18)72452-6
- ↑ Berg JM, Tymoczko JL, Stryer L (2002). «Appendix: Vmax and KM Can Be Determined by Double-Reciprocal Plots». Biochemistry 5ª ed. [S.l.: s.n.]
- ↑ Ophardt C. «Virtual Chembook». Elmhurst College. Consultado em 1 setembro de 2015. Cópia arquivada em 17 de outubro de 2015
- ↑ a b «Map: Biochemistry Free & Easy (Ahern and Rajagopal)». Biology LibreTexts. 24 de dezembro de 2014. Consultado em 2 de novembro de 2017
- ↑ Flower RJ (março de 1974). «Drugs which inhibit prostaglandin biosynthesis». Pharmacological Reviews. 26 (1): 33–67. PMID 4208101
- ↑ a b Jiménez M, Chazarra S, Escribano J, Cabanes J, García-Carmona F (agosto de 2001). «Competitive inhibition of mushroom tyrosinase by 4-substituted benzaldehydes». Journal of Agricultural and Food Chemistry. 49 (8): 4060–4063. PMID 11513710. doi:10.1021/jf010194h
- ↑ Dick RM (2011). «Chapter 2. Pharmacodynamics: The Study of Drug Action». In: Ouellette R, Joyce JA. Pharmacology for Nurse Anesthesiology. [S.l.]: Jones & Bartlett Learning. ISBN 978-0-7637-8607-6
- ↑ a b Voet D, Voet JG, Pratt CW (29 de fevereiro de 2016). Fundamentals of biochemistry : life at the molecular level Fifth ed. Hoboken, NJ: [s.n.] ISBN 9781118918401. OCLC 910538334
- ↑ a b Sian J, Youdim MB, Riederer P, Gerlach M (1999). «MPTP-Induced Parkinsonian Syndrome». Basic Neurochemistry: Molecular, Cellular and Medical Aspects. 6ª edição. [S.l.: s.n.]
- ↑ a b Herraiz T, Guillén H (agosto de 2011). «Inhibition of the bioactivation of the neurotoxin MPTP by antioxidants, redox agents and monoamine oxidase inhibitors». Food and Chemical Toxicology. 49 (8): 1773–1781. PMID 21554916. doi:10.1016/j.fct.2011.04.026. hdl:10261/63126
- ↑ «How Sulfa Drugs Work». National Institutes of Health (NIH). 15 de maio de 2015. Consultado em 2 de novembro de 2017. Cópia arquivada em 27 de setembro de 2024
- ↑ Potter VR, Dubois KP (março de 1943). «Studies on the Mechanism of Hydrogen Transport in Animal Tissues». The Journal of General Physiology. 26 (4): 391–404. PMC 2142566
 . PMID 19873352. doi:10.1085/jgp.26.4.391
. PMID 19873352. doi:10.1085/jgp.26.4.391