Ciclo do cloro
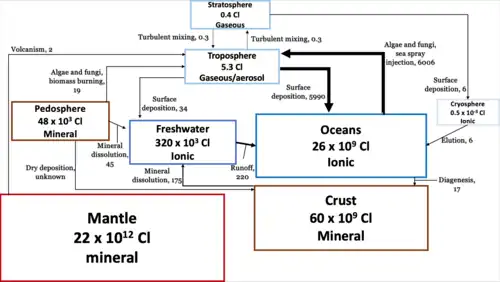
O ciclo do cloro (Cl) é o processo biogeoquímico de circulação do cloro pela atmosfera, hidrosfera, biosfera e litosfera. O cloro é encontrado principalmente na forma de íons cloreto inorgânicos ou em compostos orgânicos clorados. Mais de 5.000 compostos orgânicos clorados produzidos biologicamente já foram identificados.[1][2][3]
O ciclo do cloro na atmosfera e a formação de compostos clorados por fontes antropogênicas têm impactos significativos nas mudanças climáticas e na depleção da camada de ozônio. O cloro desempenha papéis essenciais em diversos processos biológicos, incluindo funções importantes no corpo humano.[6] Ele também atua como um cofator essencial em enzimas envolvidas na fotossíntese das plantas.[3]
Troposfera
O cloro desempenha um papel importante no ciclo atmosférico e no clima, incluindo, mas não se limitando aos clorofluorocarbonetos (CFCs).[7] O principal fluxo de cloro para a troposfera provém do aerossol de sal marinho. Tanto o cloro orgânico quanto o inorgânico são transferidos para a troposfera a partir dos oceanos.[2] A combustão de biomassa é outra fonte de cloro, tanto orgânico quanto inorgânico, para a troposfera a partir do reservatório terrestre.[2] Geralmente, as formas orgânicas de cloro são altamente não reativas e são transferidas da troposfera para a estratosfera. O principal fluxo de cloro da troposfera ocorre por deposição superficial em sistemas aquáticos.
Hidrosfera
Os oceanos são a maior fonte de cloro na hidrosfera terrestre.[2] Na hidrosfera, o cloro existe principalmente como cloreto devido à alta solubilidade do íon Cl−.[3] A maioria dos fluxos de cloro ocorre dentro da hidrosfera devido à solubilidade e reatividade dos íons cloreto em sistemas aquáticos.[2] A criosfera retém parte do cloro depositado por chuvas e neve, mas a maior parte é eluída [en] para os oceanos.
Litosfera
O maior reservatório de cloro está na litosfera, onde 2,2 x 1012 kg de cloro global são encontrados no manto terrestre.[2] Erupções vulcânicas liberam esporadicamente altos níveis de cloro como HCl na troposfera, mas a maior parte do fluxo de cloro terrestre provém de fontes marinhas que se misturam ao manto.[2]
O cloro ligado organicamente é tão abundante quanto os íons cloreto nos sistemas de solo terrestres, ou pedosfera.[1] A descoberta de múltiplos genes mediadores de cloro em microrganismos e plantas indica que diversos processos bióticos utilizam cloreto e produzem compostos orgânicos clorados, assim como processos abióticos.[1][3][4][5] Esses compostos clorados podem ser volatilizados ou lixiviados dos solos, tornando o ambiente do solo um sumidouro global de cloro.[1] Diversos procariontes anaeróbicos contêm genes e exibem atividade para a volatilização de compostos orgânicos clorados.[8]
Processos biológicos
A capacidade do cloro de se dissociar completamente em água é a razão pela qual ele é um eletrólito essencial em muitos processos biológicos.[6] O cloro, junto com o fósforo, é o sexto elemento mais comum na matéria orgânica.[1] As células utilizam cloreto para equilibrar o pH e manter a pressão de turgor em equilíbrio. A alta condutividade elétrica dos íons Cl− é essencial para a sinalização neuronal no cérebro e regula muitas outras funções essenciais em biologia.[9]
Compostos clorados antropogênicos
Os efeitos de depleção dos clorofluorocarbonetos (CFCs) no ozônio sobre a Antártida têm sido amplamente estudados desde a década de 1980.[7] A baixa reatividade dos CFCs permite que eles alcancem a estratosfera superior, onde interagem com a radiação UV-C, formando íons cloreto altamente reativos que interagem com o metano.[7] Esses íons cloreto altamente reativos também interagem com compostos orgânicos voláteis, formando outros ácidos que deplecionam o ozônio.[10]
O cloro-36 é o isótopo radioativo produzido em muitas instalações nucleares como resíduo.[3] Sua meia-vida de 3,01 x 105 anos, mobilidade na pedosfera e capacidade de ser absorvido por organismos tornaram-no um isótopo de grande preocupação entre os pesquisadores.[3] A alta solubilidade e baixa reatividade do 36
Cl–
também o tornaram útil para pesquisas sobre o ciclo biogeoquímico do cloro, sendo frequentemente utilizado como marcador isotópico.[1][3][4][5][7]
Referências
- ↑ a b c d e f g h i Öberg, G. (2002). «The natural chlorine cycle - fitting the scattered pieces». Applied Microbiology and Biotechnology. 58 (5): 565–581. ISSN 0175-7598. PMID 11956738. doi:10.1007/s00253-001-0895-2. Consultado em 29 de maio de 2025
- ↑ a b c d e f g h i j Graedel, Thomas E.; Keene, W. C. (1996). «The Budget and Cycle of Earth's Natural Chlorine». Pure and Applied Chemistry. 68 (9): 1689–1697. ISSN 1365-3075. doi:10.1351/pac199668091689

- ↑ a b c d e f g h i j Svensson, Teresia; Kylin, Henrik; Montelius, Malin; Sandén, Per; Bastviken, David (2021). «Chlorine cycling and the fate of Cl in terrestrial environments». Environmental Science and Pollution Research (em inglês). 28 (7): 7691–7709. ISSN 0944-1344. PMC 7854439
 . PMID 33400105. doi:10.1007/s11356-020-12144-6
. PMID 33400105. doi:10.1007/s11356-020-12144-6
- ↑ a b c d Atashgahi, Siavash; Liebensteiner, Martin G.; Janssen, Dick B.; Smidt, Hauke; Stams, Alfons J. M.; Sipkema, Detmer (2018). «Microbial Synthesis and Transformation of Inorganic and Organic Chlorine Compounds». Frontiers in Microbiology. 9. 3079 páginas. ISSN 1664-302X. PMC 6299022
 . PMID 30619161. doi:10.3389/fmicb.2018.03079
. PMID 30619161. doi:10.3389/fmicb.2018.03079
- ↑ a b c d Vodyanitskii, Yu. N.; Makarov, M. I. (2017). «Organochlorine compounds and the biogeochemical cycle of chlorine in soils: A review». Eurasian Soil Science (em inglês). 50 (9): 1025–1032. Bibcode:2017EurSS..50.1025V. ISSN 1064-2293. doi:10.1134/S1064229317090113. Consultado em 29 de maio de 2025
- ↑ a b Berend, Kenrick; van Hulsteijn, Leonard Hendrik; Gans, Rijk O.B. (2012). «Chloride: The queen of electrolytes?». European Journal of Internal Medicine (em inglês). 23 (3): 203–211. PMID 22385875. doi:10.1016/j.ejim.2011.11.013. Consultado em 29 de maio de 2025
- ↑ a b c d Kim, Ki-Hyun; Shon, Zang-Ho; Nguyen, Hang Thi; Jeon, Eui-Chan (2011). «A review of major chlorofluorocarbons and their halocarbon alternatives in the air». Atmospheric Environment (em inglês). 45 (7): 1369–1382. Bibcode:2011AtmEn..45.1369K. doi:10.1016/j.atmosenv.2010.12.029. Consultado em 29 de maio de 2025
- ↑ Aulenta, Federico; Pera, Antonio; Rossetti, Simona; Petrangeli Papini, Marco; Majone, Mauro (2007). «Relevance of side reactions in anaerobic reductive dechlorination microcosms amended with different electron donors». WaterResearch (em inglês). 41 (1): 27–38. PMID 17107702. doi:10.1016/j.watres.2006.09.019. Consultado em 29 de maio de 2025
- ↑ Vardi (2010). «GABA, Glycine and Cation-Chloride Cotransporters in Retinal Function and Development». Chapter 19 - GABA, Glycine and Cation-Chloride Cotransporters in Retinal Function and Development. [S.l.]: Academic Press. pp. 383–412. ISBN 9780123743732. doi:10.1016/B978-0-12-374373-2.00019-4. Consultado em 29 de maio de 2025
- ↑ Faxon, C. B.; Allen, D. T. (2013). «Chlorine chemistry in urban atmospheres: a review». Environmental Chemistry (em inglês). 10 (3): 221–233. ISSN 1449-8979. doi:10.1071/EN13026
 . Consultado em 29 de maio de 2025
. Consultado em 29 de maio de 2025