Ciclo carbonato-silicato
.jpg)
O ciclo carbonato-silicato, também conhecido como ciclo do carbono inorgânico, descreve a transformação de longo prazo de rochas silicatadas em rochas carbonáticas por meio de intemperismo e sedimentação, e a reconversão de rochas carbonáticas em rochas silicatadas por metamorfismo e vulcanismo.[1][2][3] O dióxido de carbono é removido da atmosfera durante a sedimentação de minerais intemperizados e retornado à atmosfera por meio do vulcanismo. Em escalas de tempo de milhões de anos, o ciclo carbonato-silicato é um fator chave no controle do clima da Terra, pois regula os níveis de dióxido de carbono e, consequentemente, a temperatura global.[3]
A taxa de intemperismo é sensível a fatores que alteram a exposição da superfície terrestre, como o nível do mar, topografia, litologia e mudanças na vegetação.[4] Além disso, essas mudanças geomórficas e químicas atuam em conjunto com forçantes solares, seja por alterações orbitais ou evolução estelar, para determinar a temperatura da superfície global. O ciclo carbonato-silicato também foi considerado uma possível solução para o paradoxo do jovem Sol fraco.[2][3]
Visão geral do ciclo
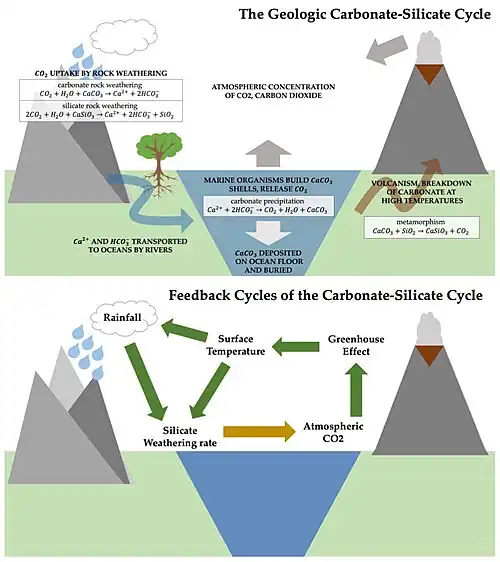
O ciclo carbonato-silicato é o principal controlador dos níveis de dióxido de carbono em escalas de tempo longas.[3] Ele pode ser visto como um ramo do ciclo do carbono, que também inclui o ciclo do carbono orgânico [en], no qual processos biológicos convertem dióxido de carbono e água em matéria orgânica e oxigênio por meio da fotossíntese.[5]
Processos físicos e químicos
O ciclo inorgânico começa com a formação de ácido carbônico (H2CO3) a partir da água da chuva e dióxido de carbono gasoso.[6] Esse processo resulta em chuva com pH em torno de 5,6.[7] O ácido carbônico, embora seja um ácido fraco, pode dissolver rochas silicatadas (e também carbonáticas) em escalas de tempo longas. A maior parte da crosta terrestre (e do manto) é composta por silicatos.[8] Essas substâncias se decompõem em íons dissolvidos. Por exemplo, o silicato de cálcio (CaSiO3), ou wollastonita, reage com dióxido de carbono e água para produzir um íon cálcio, Ca2+, um íon bicarbonato, HCO3−, e sílica dissolvida. Essa reação é representativa do intemperismo geral de minerais silicatados de cálcio.[9] A via química é a seguinte:
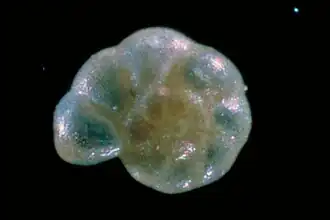
O escoamento fluvial transporta esses produtos para o oceano, onde organismos marinhos calcificantes utilizam Ca2+ e HCO3− para construir suas conchas e esqueletos, em um processo chamado precipitação carbonática:
Duas moléculas de CO2 são necessárias para o intemperismo de rochas silicatadas; a calcificação marinha libera uma molécula de volta à atmosfera. O carbonato de cálcio (CaCO3) contido em conchas e esqueletos afunda após a morte do organismo marinho e é depositado no fundo do oceano.
A etapa final envolve o movimento do fundo oceânico. Em zonas de subducção, os sedimentos carbonáticos são enterrados e forçados de volta ao manto. Alguns carbonatos podem ser levados profundamente ao manto, onde condições de alta pressão e temperatura permitem que se combinem metamorfamente com SiO2 para formar CaSiO3 e CO2, que é liberado do interior para a atmosfera por meio de vulcanismo, aberturas térmicas no oceano ou fontes de soda, que são fontes naturais que contêm gás carbônico ou água com gás:
Essa etapa final devolve a segunda molécula de CO2 à atmosfera, fechando o orçamento do carbono inorgânico. Cerca de 99,6% de todo o carbono na Terra (equivalente a aproximadamente 108 bilhões de toneladas de carbono) está sequestrado no reservatório rochoso de longo prazo. Praticamente todo o carbono já esteve na forma de carbonato. Em contraste, apenas 0,002% do carbono existe na biosfera.[8]
Feedbacks
Alterações na superfície do planeta, como a ausência de vulcões ou níveis mais altos do mar, que reduzem a superfície terrestre exposta ao intemperismo, podem alterar as taxas dos processos desse ciclo.[8] Ao longo de dezenas a centenas de milhões de anos, os níveis de dióxido de carbono na atmosfera podem variar devido a perturbações naturais no ciclo.[10][11][12] De forma mais geral, o ciclo atua como um mecanismo de feedback negativo entre os níveis de dióxido de carbono e as mudanças climáticas.[6][9] Por exemplo, se o CO2 se acumula na atmosfera, o efeito estufa aumenta a temperatura da superfície, o que, por sua vez, eleva a taxa de precipitação e o intemperismo de silicatos, removendo carbono da atmosfera. Assim, em escalas de tempo longas, o ciclo carbonato-silicato estabiliza o clima da Terra, sendo por isso chamado de termostato da Terra.[5][13]
Mudanças ao longo da história da Terra
Aspectos do ciclo carbonato-silicato mudaram ao longo da história da Terra devido à evolução biológica e mudanças tectônicas.[14] Geralmente, a formação de carbonatos superou a de silicatos, removendo dióxido de carbono da atmosfera. A biomineralização de carbonatos próximo ao limite Pré-Cambriano-Cambriano permitiu uma remoção mais eficiente dos produtos de intemperismo do oceano.[15] Processos biológicos no solo podem aumentar significativamente as taxas de intemperismo.[16] As plantas produzem ácidos orgânicos que intensificam o intemperismo, secretados por raízes, fungos micorrízicos e pela decomposição microbiana de plantas. A respiração radicular e a oxidação da matéria orgânica do solo também produzem dióxido de carbono, que se converte em ácido carbônico, aumentando o intemperismo.[17]
Mudanças tectônicas podem induzir alterações no ciclo carbonato-silicato. Por exemplo, o soerguimento de cadeias montanhosas, como o Himalaia e os Andes, é considerado responsável pelo início da Era do Gelo do Cenozoico Tardio [en], devido ao aumento das taxas de intemperismo de silicatos e à redução de dióxido de carbono.[18] O intemperismo do fundo oceânico está ligado à luminosidade solar e à concentração de dióxido de carbono.[19] No entanto, modelar a relação entre taxas de desgaseificação, subducção e mudanças no fundo oceânico é desafiador. Dados de proxies, como núcleos de sedimentos para deduzir níveis passados do mar, não são ideais, pois os níveis do mar mudam por fatores além do ajuste do fundo oceânico.[20] Estudos recentes de modelagem investigaram o papel do intemperismo do fundo oceânico na evolução inicial da vida, mostrando que taxas relativamente rápidas de criação do fundo oceânico reduziram moderadamente os níveis de dióxido de carbono.[21]
Observações de tempos geológicos profundos indicam que a Terra possui um feedback de intemperismo rochoso relativamente insensível, permitindo grandes oscilações de temperatura. Com cerca do dobro de dióxido de carbono na atmosfera, registros paleoclimáticos mostram temperaturas globais até 5 a 6 °C mais altas que as atuais.[22] No entanto, outros fatores, como mudanças em forçantes orbitais ou solares, contribuem para as mudanças de temperatura no registro paleoclimático.
As emissões humanas de CO2 têm aumentado rapidamente em um curto período de tempo.[23] O excesso de carbono na atmosfera dissolvido na água do mar pode alterar as taxas do ciclo carbonato-silicato. O CO2 dissolvido pode reagir com a água para formar íons bicarbonato, HCO3−, e íons hidrogênio, H+. Esses íons hidrogênio reagem rapidamente com carbonato, CO32−, produzindo mais íons bicarbonato e reduzindo os íons carbonato disponíveis, o que dificulta a precipitação carbonática.[24] Em outras palavras, 30% do carbono emitido na atmosfera é absorvido pelos oceanos. Altas concentrações de dióxido de carbono nos oceanos dificultam a precipitação carbonática, produzindo menos CaCO3. Esse processo, que prejudica organismos construtores de conchas, é chamado de acidificação oceânica.[25]
O ciclo em outros planetas
Não se deve assumir que o ciclo carbonato-silicato ocorre em todos os planetas terrestres. Ele requer a presença de um ciclo da água, que se rompe na borda interna da zona habitável do Sistema Solar. Mesmo que um planeta comece com água líquida na superfície, se ficar muito quente, sofrerá um efeito estufa descontrolado, perdendo água superficial. Sem chuva, não há intemperismo para produzir ácido carbônico a partir de CO2 gasoso. Na borda externa, o CO2 pode condensar, reduzindo o efeito estufa e a temperatura da superfície, colapsando a atmosfera em calotas polares.[5]
Marte é um exemplo. Localizado na borda da zona habitável, sua superfície é muito fria para água líquida sem efeito estufa. Com uma atmosfera fina, a temperatura média da superfície de Marte é de 210 K (-63 °C). Para explicar feições topográficas semelhantes a canais fluviais, apesar da radiação solar aparentemente insuficiente, alguns sugerem que um ciclo semelhante ao carbonato-silicato da Terra poderia ter existido, similar a uma recuperação de períodos de Terra bola de neve.[26] Modelos mostram que CO2 e H2O gasosos como gases de efeito estufa não poderiam ter mantido Marte quente em sua história inicial, quando o Sol era mais fraco, pois o CO2 condensaria em nuvens.[27] Embora nuvens de CO2 não reflitam como as de água na Terra,[28] Marte provavelmente não teve um ciclo carbonato-silicato significativo no passado.
Em contrapartida, Vênus, na borda interna da zona habitável, tem uma temperatura média de superfície de 737 K (464 °C). Após perder sua água por fotodissociação e escape de hidrogênio, Vênus parou de remover dióxido de carbono da atmosfera, acumulando-o e sofrendo um efeito estufa descontrolado.
Em exoplanetas com rotação síncrona, a localização do ponto substelar determina a liberação de dióxido de carbono da litosfera.[29]
Ver também
- Bomba biológica
- Ciclo do carbono
- Profundidade de compensação dos carbonatos
- Hipótese de Gaia
- Efeito estufa descontrolado
- Terra bola de neve
- Lago Nyos
- Acidificação oceânica
- Paradoxo do jovem Sol fraco
Referências
- ↑ Urey, H. C. (1952). The planets: their origin and development. Mrs. Hepsa Ely Silliman Memorial Lectures.
- ↑ a b Berner, Robert; Lasaga, Antonio; Garrels, Robert (1983). «The carbonate-silicate geochemical cycle and its effect on atmospheric carbon dioxide over the past 100 million years». American Journal of Science. 283 (7): 641–683. Bibcode:1983AmJS..283..641B. doi:10.2475/ajs.283.7.641

- ↑ a b c d Walker, James C. G.; Hays, P. B.; Kasting, J. F. (1981). «A negative feedback mechanism for the long-term stabilization of Earth's surface temperature». Journal of Geophysical Research: Oceans (em inglês). 86 (C10): 9776–9782. Bibcode:1981JGR....86.9776W. ISSN 2156-2202. doi:10.1029/JC086iC10p09776
- ↑ Walker, James C. G. (1993). «Biogeochemical Cycles of Carbon on a Hierarchy of Timescales». Biogeochemistry of Global Change: Radiatively Active Trace Gases Selected Papers from the Tenth International Symposium on Environmental Biogeochemistry. Boston, MA: Springer. pp. 3–28. ISBN 978-1-4613-6215-9. doi:10.1007/978-1-4615-2812-8_1
- ↑ a b c Sullivan, Woodruff T.; Baross, John A. (2007). «Planetary Atmospheres and Life». Planets and Life. Cambridge, UK: Cambridge University Press. pp. 91–116. ISBN 978-0-521-53102-3
- ↑ a b Bonan, Gordon (2013). Ecological Climatology: Concepts and Applications 2nd ed. New York: Cambridge University Press. pp. 105–128. ISBN 978-0-521-69319-6
- ↑ Environmental Protection Agency (9 de fevereiro de 2016). «What is Acid Rain?». Consultado em 26 de maio de 2025
- ↑ a b c «Geology and Climate: ACS Climate Science Toolkit». American Chemical Society. Consultado em 26 de maio de 2025
- ↑ a b Catling, David C.; Kasting, James F. (2017). Atmospheric Evolution on Inhabited and Lifeless Worlds. Cambridge, UK: Cambridge University Press. pp. 299–326. ISBN 978-0-521-84412-3
- ↑ Berner, Robert A. (1º de abril de 1991). «A model for atmospheric CO2 over Phanerozoic time». American Journal of Science. 291 (4): 339–376. Bibcode:1991AmJS..291..339B. doi:10.2475/ajs.291.4.339

- ↑ Berner, Robert A. (29 de janeiro de 1998). «The carbon cycle and carbon dioxide over Phanerozoic time: the role of land plants». Philosophical Transactions of the Royal Society of London. Series B: Biological Sciences. 353 (1365): 75–82. PMC 1692179
 . doi:10.1098/rstb.1998.0192
. doi:10.1098/rstb.1998.0192
- ↑ Berner, Robert A.; Beerling, David J.; Dudley, Robert; Robinson, Jennifer M.; Wildman, Jr., Richard A. (2003). «Phanerozoic Atmospheric Oxygen». Annual Review of Earth and Planetary Sciences. 31 (31): 105–134. Bibcode:2003AREPS..31..105B. doi:10.1146/annurev.earth.31.100901.141329
- ↑ DiVenere, Vic. «The Carbon Cycle and Earth's Climate». Columbia University. Consultado em 26 de maio de 2025
- ↑ Penman, Donald E.; Caves Rugenstein, Jeremy K.; Ibarra, Daniel E.; Winnick, Matthew J. (Outubro de 2020). «Silicate weathering as a feedback and forcing in Earth's climate and carbon cycle». Earth-Science Reviews (em inglês). 209. 103298 páginas. doi:10.1016/j.earscirev.2020.103298. Consultado em 26 de maio de 2025 – via Esevier Science Direct
- ↑ Ridgewell, A; Zeebe, R (2005). «The role of the global carbonate cycle in the regulation and evolution of the Earth system». Earth and Planetary Science Letters. 234 (3–4): 299–315. ISSN 0012-821X. doi:10.1016/j.epsl.2005.03.006
- ↑ Taylor, Lyla L.; Banwart, Steve A.; Valdes, Paul J.; Leake, Jonathan R.; Beerling, David J. (2012). «Evaluating the effects of terrestrial ecosystems, climate and carbon dioxide on weathering over geological time: a global-scale process-based approach». Philosophical Transactions of the Royal Society B: Biological Sciences. 367 (1588): 565–582. ISSN 0962-8436. PMC 3248708
 . PMID 22232768. doi:10.1098/rstb.2011.0251
. PMID 22232768. doi:10.1098/rstb.2011.0251
- ↑ Berner, Robert A. (1992). «Weathering, plants, and the long-term carbon cycle». Geochimica et Cosmochimica Acta. 56 (8): 3225–3231. Bibcode:1992GeCoA..56.3225B. ISSN 0016-7037. doi:10.1016/0016-7037(92)90300-8

- ↑ Raymo, Maureen E.; Ruddiman, William F.; Froelich, Philip N. (1988). «Influence of late Cenozoic mountain building on ocean geochemical cycles». Geology (em inglês). 16 (7). 649 páginas. Bibcode:1988Geo....16..649R. ISSN 0091-7613. doi:10.1130/0091-7613(1988)016<0649:iolcmb>2.3.co;2
- ↑ Brady, Patrick; Gíslason, Sigurdur R. (Março de 1997). «Seafloor weathering controls on atmospheric CO2 and global climate Author links open overlay panel». Geochimica et Cosmochimica Acta. 61 (5): 965–973. doi:10.1016/S0016-7037(96)00385-7
- ↑ Berner, Robert A.; Lasaga, Antonio C. (Março de 1989). «Modeling the Geochemical Carbon Cycle». Scientific American. 260 (3): 74–81. Bibcode:1989SciAm.260c..74B. doi:10.1038/scientificamerican0389-74
- ↑ Krissansen-Totton, Joshua; Arney, Giada N.; Catling, David C. (17 de abril de 2018). «Constraining the climate and ocean pH of the early Earth with a geological carbon cycle model». PNAS. 115 (16): 4105–4110. Bibcode:2018PNAS..115.4105K. PMC 5910859
 . PMID 29610313. arXiv:1804.00763
. PMID 29610313. arXiv:1804.00763 . doi:10.1073/pnas.1721296115
. doi:10.1073/pnas.1721296115
- ↑ Krissansen-Totton, Joshua; Catling, David C. (22 de maio de 2017). «Constraining climate sensitivity and continental versus seafloor weathering using an inverse geological carbon cycle model». Nature Communications. 8: 15423. Bibcode:2017NatCo...815423K. PMC 5458154
 . PMID 28530231. doi:10.1038/ncomms15423
. PMID 28530231. doi:10.1038/ncomms15423
- ↑ Core Writing Team; R.K. Pachauri; L.A. Meyer, eds. (2014). IPCC, 2014: Climate Change 2014: Synthesis Report. Contribution of Working Groups I, II and III to the Fifth Assessment Report of the Intergovernmental Panel on Climate Change. Geneva, Switzerland: IPCC. Consultado em 26 de maio de 2025
- ↑ «Ocean Acidification». Ocean Carbon and Biogeochemistry. Woods Hole Oceanographic Institute (WHOI). Consultado em 26 de maio de 2025
- ↑ «Carbon Cycle». Earth Observatory. NASA. 16 de junho de 2011. Consultado em 26 de maio de 2025
- ↑ Batalha, Natasha E.; Kopparapu, Ravi Kumar; Haqq-Misra, Jacob; Kasting, James F. (2016). «Climate cycling on early Mars caused by the carbonate-silicate cycle». Earth and Planetary Science Letters. 455: 7–13. arXiv:1609.00602
 . doi:10.1016/j.epsl.2016.08.044
. doi:10.1016/j.epsl.2016.08.044
- ↑ Kasting, J. F. (1991). «CO2 condensation and the climate of early Mars». Icarus. 94 (1): 1–13. Bibcode:1991Icar...94....1K. PMID 11538088. doi:10.1016/0019-1035(91)90137-I
- ↑ Forget, François; Pierrehumbert, Raymond T. (1997). «Warming Early Mars with Carbon Dioxide Clouds that Scatter Infrared Radiation». Science. 278 (5341): 1273–1276. Bibcode:1997Sci...278.1273F. PMID 9360920. doi:10.1126/science.278.5341.1273
- ↑ Edson, Adam R.; Kasting, James F.; Pollard, David; Lee, Sukyoung; Bannon, Peter R. (2012). «The Carbonate-Silicate Cycle and CO2/Climate Feedbacks on Tidally Locked Terrestrial Planets». Astrobiology. 12 (6): 562–571. Bibcode:2012AsBio..12..562E. ISSN 1531-1074. PMID 22775488. doi:10.1089/ast.2011.0762
Ligações externas
- Understanding the long-term carbon-cycle: Weathering of rocks – a vitally important carbon-sink por John Mason, Skeptical Science