Ciclo da sílica

O ciclo da sílica é o ciclo biogeoquímico no qual a sílica biogênica é transportada entre os sistemas da Terra. O silício é um dos elementos mais abundantes na Terra e é considerado necessário para a vida.[2][3] O ciclo da sílica apresenta significativa sobreposição com o ciclo do carbono (ver ciclo carbonato-silicato) e desempenha um papel importante no sequestro de carbono por meio do intemperismo continental, exportação biogênica e soterramento como sedimentos siliciosos em escalas de tempo geológicas.[4]
Visão geral
O silício é o oitavo elemento mais abundante no universo e o segundo mais abundante na crosta terrestre (o mais abundante é o oxigênio). O intemperismo da crosta terrestre por água da chuva rica em dióxido de carbono é um processo chave no controle do dióxido de carbono atmosférico.[5][6] Esse processo resulta na geração de ácido silícico em ambientes aquosos. O ácido silícico, Si(OH)4, é uma forma hidratada de sílica encontrada apenas como uma solução instável em água, mas desempenha um papel central no ciclo da sílica.[1]
Silicificadores são organismos que utilizam ácido silícico para precipitar sílica biogênica, SiO2. A sílica biogênica, também chamada de opala, é precipitada por silicificadores como estruturas internas[7] e/ou externas.[8] Silicificadores estão entre os organismos aquáticos mais importantes. Eles incluem microrganismos como diatomáceas, rizários, silicoflagelados e várias espécies de coanoflagelados, além de macrorganismos como esponjas silicosas [en]. Silicificadores fotótrofos [en], como diatomáceas, consomem globalmente grandes quantidades de silício, juntamente com nitrogênio (N), fósforo (P) e carbono inorgânico (C), conectando a biogeoquímica desses elementos e contribuindo para o sequestro de dióxido de carbono atmosférico no oceano.[9] Organismos heterotróficos, como rizários, coanoflagelados e esponjas, produzem sílica biogênica independentemente do processamento fotoautotrófico de C e N.[1][8][10][11]
As diatomáceas dominam a fixação e exportação de material particulado no ciclo marinho contemporâneo da sílica. Isso inclui a exportação de carbono orgânico da zona eufótica para o oceano profundo por meio da bomba biológica de carbono. Como resultado, diatomáceas e outros organismos secretores de sílica desempenham papéis cruciais no ciclo global do carbono, sequestrando carbono no oceano. A conexão entre a sílica biogênica e o carbono orgânico, juntamente com o potencial de preservação significativamente maior dos compostos siliciosos biogênicos em comparação com o carbono orgânico, torna os registros de acumulação de opala de interesse em paleoceanografia e paleoclimatologia.
Compreender o ciclo da sílica é importante para entender o funcionamento das cadeias alimentares marinhas, ciclos biogeoquímicos e a bomba biológica. O ácido silícico é fornecido ao oceano por seis vias, como ilustrado no diagrama acima, todas derivadas, em última análise, do intemperismo da crosta terrestre.[1][12]
Ciclo da sílica terrestre
A sílica é um nutriente importante utilizado por plantas, árvores e gramíneas na biosfera terrestre. O silicato é transportado por rios e pode ser depositado em solos na forma de vários polimorfos siliciosos. As plantas podem absorver silicato na forma de H4SiO4 para a formação de fitólitos. Os fitólitos são estruturas rígidas minúsculas encontradas dentro das células vegetais que auxiliam na integridade estrutural da planta. Os fitólitos também protegem as plantas do consumo por herbívoros, que não conseguem consumir e digerir eficientemente plantas ricas em sílica.[2] A liberação de sílica pela degradação ou dissolução de fitólitos é estimada em uma taxa dupla em relação ao intemperismo global de minerais de silicato.[3] Considerando o ciclo biogeoquímico dentro dos ecossistemas, a importação e exportação de sílica para e a partir de ecossistemas terrestres é pequena.
Intemperismo
Os minerais de silicato são abundantes em formações rochosas em todo o planeta, compreendendo aproximadamente 90% da crosta terrestre.[4] A principal fonte de silicato para a biosfera terrestre é o intemperismo. O processo e a taxa de intemperismo são variáveis, dependendo da precipitação, escoamento, vegetação, litologia e topografia.
Com tempo suficiente, a água da chuva pode dissolver até mesmo um mineral à base de silicato altamente resistente, como o quartzo.[13] A água quebra as ligações entre os átomos no cristal:[14]
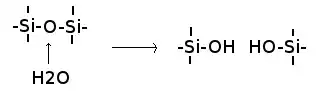
A reação geral para a dissolução do quartzo resulta em ácido silícico:
Outro exemplo de mineral à base de silicato é a enstatita (MgSiO3). A água da chuva intemperiza isso em ácido silícico da seguinte forma:[15]
Intemperismo reverso
Nos últimos anos, o efeito do intemperismo reverso [en] sobre a sílica biogênica tem sido de interesse na quantificação do ciclo da sílica. Durante o intemperismo, a sílica dissolvida é entregue aos oceanos por meio do escoamento glacial e entradas fluviais.[16] Essa sílica dissolvida é absorvida por diversos organismos marinhos, como diatomáceas, e usada para criar conchas protetoras. Quando esses organismos morrem, eles afundam através da coluna de água. Sem a produção ativa de SiO2 biogênico, o mineral começa a diagênese.[16] A conversão dessa sílica dissolvida em argilas de silicato autigênicas [en] por meio do processo de intemperismo reverso constitui a remoção de 20-25% da entrada de silício.[17]
O intemperismo reverso é frequentemente encontrado em deltas fluviais, pois esses sistemas apresentam altas taxas de acumulação de sedimentos e são observados sofrendo rápida diagênese.[18] A formação de argilas de silicato remove a sílica reativa das águas intersticiais dos sedimentos, aumentando a concentração de sílica nas rochas que se formam nesses locais.[18]
O intemperismo de silicatos também parece ser um processo dominante em sedimentos metanogênicos mais profundos, enquanto o intemperismo reverso é mais comum em sedimentos de superfície, mas ocorre em uma taxa menor.[19]
Sumidouros
O principal sumidouro do ciclo da sílica terrestre é a exportação para o oceano por rios. A sílica armazenada em matéria vegetal ou dissolvida pode ser exportada para o oceano por rios. A taxa desse transporte é de aproximadamente 6 Tmol Si/ano.[20][3] Esse é o principal sumidouro do ciclo da sílica terrestre, bem como a maior fonte do ciclo da sílica marinha.[20] Um sumidouro menor para a sílica terrestre é o silicato depositado em sedimentos terrestres e eventualmente exportado para a crosta terrestre.
Entradas marinhas
Fluvias
Até 2021, a melhor estimativa do total de entrada fluvial de ácido silícico é de 6,2 (±1,8) Tmol Si/ano.[12] Isso é baseado em dados que representam 60% da descarga fluvial mundial e uma concentração média ponderada de ácido silícico fluvial de 158 μM−Si.[21][12] No entanto, o ácido silícico não é a única forma pela qual o silício pode ser transferido de sistemas terrestres para fluviais, já que o silício particulado também pode ser mobilizado em formas cristalizadas ou amorfas.[21] De acordo com Saccone e outros em 2007,[22] o termo "sílica amorfa" inclui sílica biogênica (de fitólitos, diatomáceas de água doce, espículas de esponjas), sílica biogênica alterada e silicatos pedogênicos, os quais podem ter solubilidades e reatividades similares. A entrega de sílica amorfa ao sistema fluvial foi revisada por Frings e outros em 2016,[23] que sugeriram um valor de 1,9 (±1,0) Tmol Si/ano. Portanto, a entrada fluvial total é de 8,1 (±2,0) Tmol Si/ano.[1]
Eólica
Nenhum progresso foi feito em relação à deposição de poeira eólica no oceano[24] e subsequente liberação de ácido silícico por meio da dissolução de poeira na água do mar desde 2013, quando Tréguer e De La Rocha somaram o fluxo de sílica dissolvível particulada e a deposição úmida de ácido silícico por precipitação.[12] Assim, a melhor estimativa para o fluxo eólico de ácido silícico, FA, permanece em 0,5 (±0,5) Tmol Si/ano.[1]
Praias arenosas
Um estudo de 2019 propôs que, na zona de surfe das praias, a ação das ondas perturba grãos de areia abióticos e os dissolve ao longo do tempo.[25] Para testar isso, os pesquisadores colocaram amostras de areia em recipientes fechados com diferentes tipos de água e giraram os recipientes para simular a ação das ondas. Eles descobriram que quanto maior a proporção rocha/água dentro do recipiente e mais rápido o recipiente girava, mais sílica se dissolvia na solução. Após analisar e escalonar seus resultados, eles estimaram que entre 3,2 ± 1,0 – 5,0 ± 2,0 Tmol Si/ano de DSi litogênico poderiam entrar no oceano a partir de praias arenosas, um aumento significativo em relação a uma estimativa anterior de 0,3 Tmol Si/ano.[26] Se confirmado, isso representa uma entrada significativa de LSi dissolvido que foi previamente ignorada.[25][1]
Ciclo da sílica marinha
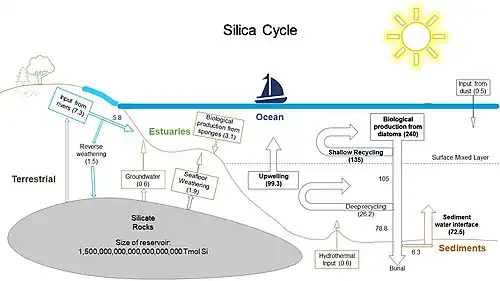
Organismos siliciosos no oceano, como diatomáceas e radiolários, são o principal sumidouro de ácido silícico dissolvido em sílica de opala.[31] Apenas 3% das moléculas de Si dissolvidas no oceano são exportadas e depositadas permanentemente em sedimentos marinhos no fundo do mar a cada ano, demonstrando que a reciclagem do silício é um processo dominante nos oceanos. Essa rápida reciclagem depende da dissolução de sílica em matéria orgânica na coluna de água, seguida pela absorção biológica na zona fótica. O tempo de residência estimado do reservatório biológico de sílica é de cerca de 400 anos.[3] A sílica de opala é predominantemente subssaturada nos oceanos mundiais. Essa subssaturação promove uma rápida dissolução como resultado de reciclagem constante e longos tempos de residência. O tempo de renovação estimado do Si é de 1,5x104 anos. As entradas e saídas líquidas totais de sílica no oceano são de 9,4 ± 4,7 Tmol Si/ano e 9,9 ± 7,3 Tmol Si/ano, respectivamente.[20]
A produção de sílica biogênica na zona fótica é estimada em 240 ± 40 Tmol Si/ano.[20] A dissolução na superfície remove cerca de 135 Tmol Si/ano enquanto o Si restante é exportado para o oceano profundo dentro de partículas que afundam.[3] No oceano profundo, outros 26,2 Tmol Si/ano são dissolvidos antes de serem depositados nos sedimentos como chuva de opala.[3] Mais de 90% da sílica aqui é dissolvida, reciclada e eventualmente refluída para uso novamente na zona eufótica.[3]
Fontes
As principais fontes de sílica marinha incluem rios, fluxo de águas subterrâneas, entradas de intemperismo do fundo do mar, fontes hidrotermais e deposição atmosférica (fluxo eólico).[15] Os rios são, de longe, a maior fonte de sílica para o ambiente marinho, respondendo por até 90% de toda a sílica entregue ao oceano.[15][20][34] Uma fonte de sílica para o ciclo biológico da sílica marinha é a sílica reciclada por ressurgência do oceano profundo e do fundo do mar.
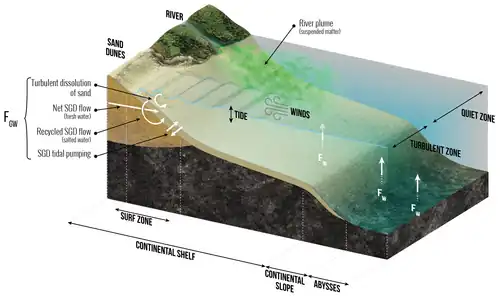
O diagrama sobre processos de baixa temperatura mostra como esses podem controlar a dissolução de minerais siliciosos (seja amorfos ou cristalizados) na água do mar e na zona costeira e no oceano profundo, alimentando a água subterrânea submarina (FGW) e o silício dissolvido na água do mar e sedimentos (FW). Esses processos correspondem a fluxos de energia baixa e média dissipada por volume de uma partícula siliciosa na zona costeira, nas margens continentais e nas zonas abissais, e a fluxos de alta energia dissipada na zona de surfe.[1]
Sumidouros
A rápida dissolução na superfície remove cerca de 135 Tmol de sílica de opala/ano, convertendo-a novamente em ácido silícico solúvel que pode ser usado novamente para biomineralização. A sílica de opala restante é exportada para o oceano profundo em partículas que afundam. No oceano profundo, outros 26,2 Tmol Si/ano são dissolvidos antes de serem depositados nos sedimentos como sílica de opala. Na interface água-sedimento, mais de 90% da sílica é reciclada e refluída para uso novamente na zona fótica.[20] A produção de sílica biogênica na zona fótica é estimada em 240 ± 40 Tmol Si/ano.[35] O tempo de residência em uma escala biológica é estimado em cerca de 400 anos, com cada molécula de sílica reciclada 25 vezes antes do soterramento nos sedimentos.[20]
A deposição no fundo do mar profundo é o maior sumidouro de longo prazo do ciclo da sílica marinha (6,3 ± 3,6 Tmol Si/ano), e é aproximadamente equilibrada pelas fontes de sílica para o oceano.[15] A sílica depositada no oceano profundo está principalmente na forma de sedimento silicioso. Quando a sílica de opala se acumula mais rapidamente do que se dissolve, ela é soterrada e pode fornecer um ambiente diagenético para a formação de cherte marinho.[36] Os processos que levam à formação de cherte foram observados no oceano Antártico, onde a acumulação de sedimento silicioso é mais rápida.[36] A formação de cherte, no entanto, pode levar dezenas de milhões de anos.[37] Fragmentos de esqueletos de organismos siliciosos estão sujeitos à recristalização e cimentação.[36] O cherte é o principal destino do sedimento silicioso soterrado e remove permanentemente a sílica do ciclo da sílica oceânica.
O sedimento silicioso é eventualmente subductado sob a crosta e metamorfizado no manto superior.[38] Sob o manto, minerais de silicato são formados em sedimentos e eventualmente elevados à superfície. Na superfície, a sílica pode entrar novamente no ciclo por meio do intemperismo.[38] Esse processo pode levar dezenas de milhões de anos.[38] O único outro grande sumidouro de sílica no oceano é o soterramento ao longo das margens continentais (3,6 ± 3,7 Tmol Si/ano), principalmente na forma de esponjas siliciosas.[15] Devido aos altos graus de incerteza nas estimativas de fontes e sumidouros, é difícil concluir se o ciclo da sílica marinha está em equilíbrio. O tempo de residência da sílica nos oceanos é estimado em cerca de 10.000 anos.[15] A sílica também pode ser removida do ciclo ao se tornar cherte e ser permanentemente soterrada.
Influências antropogênicas
A intensificação da agricultura nos últimos 400 anos aumentou a exposição de rochas e solos, resultando em taxas elevadas de intemperismo de silicatos. Por sua vez, a lixiviação de estoques de sílica amorfa dos solos também aumentou, entregando maiores concentrações de sílica dissolvida nos rios.[15] Por outro lado, o aumento de barragens levou a uma redução no suprimento de sílica para o oceano devido à absorção por diatomáceas de água doce atrás das barragens. A predominância de fitoplâncton não silicioso devido à carga antropogênica de nitrogênio e fósforo e a dissolução de sílica aprimorada em águas mais quentes tem o potencial de limitar a exportação de sedimentos de silício oceânico no futuro.[15]
Em 2019, um grupo de cientistas sugeriu que a acidificação está reduzindo a produção de sílica por diatomáceas no oceano Antártico.[39][40]

.jpg)
.png)
Papel na regulação climática
O ciclo da sílica desempenha um papel importante na regulação climática global de longo prazo. O ciclo global da sílica também tem grandes efeitos no ciclo global do carbono por meio do ciclo carbonato-silicato.[42] O processo de intemperismo de minerais de silicato transfere CO2 atmosférico para o ciclo hidrológico por meio da reação química exibida acima.[4] Em escalas de tempo geológicas, as taxas de intemperismo mudam devido à atividade tectônica. Durante um período de alta taxa de elevação, o intemperismo de silicatos aumenta, o que resulta em altas taxas de absorção de CO2, compensando emissões aumentadas de CO2 vulcânico associadas à atividade geológica. Esse equilíbrio de intemperismo e vulcões é parte do que controla o efeito estufa e o pH do oceano em escalas de tempo geológicas.
A acumulação de sílica biogênica no fundo do mar contém muitas informações sobre onde a produção de exportação ocorreu no oceano em escalas de tempo que variam de centenas a milhões de anos. Por essa razão, os registros de deposição de opala fornecem informações valiosas sobre reorganizações oceanográficas em grande escala no passado geológico, bem como sobre paleoprodutividade. O tempo médio de residência oceânica para silicato é de aproximadamente 10.000–15.000 anos. Esse tempo de residência relativamente curto torna as concentrações e fluxos de silicato oceânico sensíveis a perturbações glaciais/interglaciais, sendo assim um excelente proxy [en] para avaliar mudanças climáticas.[43][44]
As proporções isotópicas de oxigênio (O18:O16) e silício (Si30:Si28) são analisadas a partir de sílica biogênica preservada em sedimentos lacustres e marinhos para derivar registros de mudanças climáticas passadas e ciclagem de nutrientes (De La Rocha, 2006; Leng e Barker, 2006). Essa é uma abordagem particularmente valiosa considerando o papel das diatomáceas na ciclagem global de carbono. Além disso, análises isotópicas de sílica biogênica são úteis para rastrear mudanças climáticas passadas em regiões como o oceano Antártico, onde poucos carbonatos biogênicos são preservados.
As composições isotópicas de silício em espículas fósseis de esponjas (δ30Si) estão sendo cada vez mais usadas para estimar o nível de ácido silícico em ambientes marinhos ao longo da história geológica, permitindo a reconstrução de ciclos de sílica passados.[45]
Ver também
Referências
- ↑ a b c d e f g h i Tréguer, Paul J.; Sutton, Jill N.; Brzezinski, Mark; Charette, Matthew A.; et al. (2021). «Reviews and syntheses: The biogeochemical cycle of silicon in the modern ocean». Biogeosciences. 18 (4): 1269–1289. Bibcode:2021BGeo...18.1269T. doi:10.5194/bg-18-1269-2021
 . hdl:10261/230297
. hdl:10261/230297
 Material copiado desta fonte, disponível sob a licença Creative Commons Attribution 4.0 International License.
Material copiado desta fonte, disponível sob a licença Creative Commons Attribution 4.0 International License.
- ↑ a b Hunt, J. W.; Dean, A. P.; Webster, R. E.; Johnson, G. N.; Ennos, A. R. (2008). «A Novel Mechanism by which Silica Defends Grasses Against Herbivory». Annals of Botany. 102 (4): 653–656. ISSN 1095-8290. PMC 2701777
 . PMID 18697757. doi:10.1093/aob/mcn130
. PMID 18697757. doi:10.1093/aob/mcn130
- ↑ a b c d e f g h Conley, Daniel J. (Dezembro de 2002). «Terrestrial ecosystems and the global biogeochemical silica cycle». Global Biogeochemical Cycles. 16 (4): 68–1–68–8. Bibcode:2002GBioC..16.1121C. ISSN 0886-6236. doi:10.1029/2002gb001894

- ↑ a b c Defant, Marc J.; Drummond, Mark S. (Outubro de 1990). «Derivation of some modern arc magmas by melting of young subducted lithosphere». Nature. 347 (6294): 662–665. Bibcode:1990Natur.347..662D. ISSN 0028-0836. doi:10.1038/347662a0
- ↑ Berner, Robert A.; Lasaga, Antonio C.; Garrels, Robert M. (1 de setembro de 1983). «The carbonate-silicate geochemical cycle and its effect on atmospheric carbon dioxide over the past 100 million years». American Journal of Science (em inglês) (7): 641–683. doi:10.2475/ajs.283.7.641. Consultado em 28 de maio de 2025
- ↑ Wollast, R.; Mackenzie, F. T. (1989). Berger, A.; Schneider, S.; Duplessy, J. Cl., eds. «Global Biogeochemical Cycles and Climate». Dordrecht: Springer Netherlands: 453–473. ISBN 978-0-7923-0412-8. doi:10.1007/978-94-009-2446-8_26. Consultado em 28 de maio de 2025
- ↑ Moriceau, Brivaëla; Gehlen, Marion; Tréguer, Paul; Baines, Stephen; Livage, Jacques; André, Luc (19 de março de 2019). «Editorial: Biogeochemistry and Genomics of Silicification and Silicifiers». Frontiers in Marine Science. ISSN 2296-7745. doi:10.3389/fmars.2019.00057. Consultado em 28 de maio de 2025
- ↑ a b Maldonado, Manuel; López-Acosta, María; Sitjà, Cèlia; García-Puig, Marta; Galobart, Cristina; Ercilla, Gemma; Leynaert, Aude (2019). «Sponge skeletons as an important sink of silicon in the global oceans» (PDF). Nature Geoscience. 12 (10): 815–822. Bibcode:2019NatGe..12..815M. doi:10.1038/s41561-019-0430-7. Consultado em 28 de maio de 2025
- ↑ Tréguer, Paul; Pondaven, Philippe (2000). «Silica control of carbon dioxide». Nature. 406 (6794): 358–359. PMID 10935620. doi:10.1038/35019236

- ↑ Maldonado, Manuel; Ribes, Marta; Van Duyl, Fleur C. (2012). «Nutrient Fluxes Through Sponges». Advances in Sponge Science: Physiology, Chemical and Microbial Diversity, Biotechnology. Col: Advances in Marine Biology. 62. [S.l.: s.n.] pp. 113–182. ISBN 9780123942838. PMID 22664122. doi:10.1016/B978-0-12-394283-8.00003-5
- ↑ Llopis Monferrer, Natalia; Boltovskoy, Demetrio; Tréguer, Paul; Sandin, Miguel Méndez; Not, Fabrice; Leynaert, Aude (2020). «Estimating Biogenic Silica Production of Rhizaria in the Global Ocean». Global Biogeochemical Cycles. 34 (3). Bibcode:2020GBioC..3406286L. doi:10.1029/2019GB006286
 . hdl:11336/163576
. hdl:11336/163576
- ↑ a b c d Tréguer, Paul J.; de la Rocha, Christina L. (2013). «The World Ocean Silica Cycle». Annual Review of Marine Science. 5: 477–501. PMID 22809182. doi:10.1146/annurev-marine-121211-172346
- ↑ Boggs, Sam (2006). Principles of sedimentology and stratigraphy 4th ed. Upper Saddle River, N.J.: Pearson Prentice Hall. p. 7. ISBN 0131547283
- ↑ Nicholls, G. D. (1963). «Environmental Studies in Sedimentary Geochemistry». Science Progress (1933- ). 51 (201): 12–31. JSTOR 43418626
- ↑ a b c d e f g h Gaillardet, J.; Dupré, B.; Louvat, P.; Allègre, C.J. (Julho de 1999). «Global silicate weathering and CO2 consumption rates deduced from the chemistry of large rivers». Chemical Geology. 159 (1–4): 3–30. Bibcode:1999ChGeo.159....3G. ISSN 0009-2541. doi:10.1016/s0009-2541(99)00031-5
- ↑ a b Loucaides, Socratis; Michalopoulos, Panagiotis; Presti, Massimo; Koning, Erica; Behrends, Thilo; Van Cappellen, Philippe (15 de fevereiro de 2010). «Seawater-mediated interactions between diatomaceous silica and terrigenous sediments: Results from long-term incubation experiments». Chemical Geology. 270 (1–4): 68–79. Bibcode:2010ChGeo.270...68L. doi:10.1016/j.chemgeo.2009.11.006
- ↑ Tréguer, Paul J.; Rocha, Christina L. De La (2 de janeiro de 2013). «The World Ocean Silica Cycle». Annual Review of Marine Science. 5 (1): 477–501. PMID 22809182. doi:10.1146/annurev-marine-121211-172346
- ↑ a b c Aller, R. C. (1 de janeiro de 2014). «Sedimentary Diagenesis, Depositional Environments, and Benthic Fluxes». In: Holland, Heinrich D.; Turekian, Karl K. Treatise on Geochemistry Second ed. Oxford: Elsevier. pp. 293–334. ISBN 9780080983004. doi:10.1016/b978-0-08-095975-7.00611-2
- ↑ Michalopoulos, Panagiotis; Aller, Robert C (1 de março de 2004). «Early diagenesis of biogenic silica in the Amazon delta: alteration, authigenic clay formation, and storage». Geochimica et Cosmochimica Acta. 68 (5): 1061–1085. Bibcode:2004GeCoA..68.1061M. doi:10.1016/j.gca.2003.07.018
- ↑ a b c d e f g h i Tréguer, Paul J.; De La Rocha, Christina L. (3 de janeiro de 2013). «The World Ocean Silica Cycle». Annual Review of Marine Science. 5 (1): 477–501. ISSN 1941-1405. PMID 22809182. doi:10.1146/annurev-marine-121211-172346
- ↑ a b Dürr, H. H.; Meybeck, M.; Hartmann, J.; Laruelle, G. G.; Roubeix, V. (2011). «Global spatial distribution of natural riverine silica inputs to the coastal zone». Biogeosciences. 8 (3): 597–620. Bibcode:2011BGeo....8..597D. doi:10.5194/bg-8-597-2011

- ↑ Saccone, L.; Conley, D. J.; Koning, E.; Sauer, D.; Sommer, M.; Kaczorek, D.; Blecker, S. W.; Kelly, E. F. (2007). «Assessing the extraction and quantification of amorphous silica in soils of forest and grassland ecosystems». European Journal of Soil Science. 58 (6): 1446–1459. doi:10.1111/j.1365-2389.2007.00949.x

- ↑ Frings, Patrick J.; Clymans, Wim; Fontorbe, Guillaume; de la Rocha, Christina L.; Conley, Daniel J. (2016). «The continental Si cycle and its impact on the ocean Si isotope budget». Chemical Geology. 425: 12–36. Bibcode:2016ChGeo.425...12F. doi:10.1016/j.chemgeo.2016.01.020

- ↑ Tegen, I. e Kohfeld, K. E. (2006) "Atmospheric Transport of Silicon". In: The Silicon Cycle: Human Perturbations and Impacts on Aquatic Systems, editado por: Ittekot, V., Unger, D., Humborg, C., e Tac An, N. T., 7: 81–91, Island Press.
- ↑ a b Fabre, Sébastien; Jeandel, Catherine; Zambardi, Thomas; Roustan, Michel; Almar, Rafaël (11 de setembro de 2019). «An Overlooked Silica Source of the Modern Oceans: Are Sandy Beaches the Key?». Frontiers Media SA. Frontiers in Earth Science. 7: 231. Bibcode:2019FrEaS...7..231F. ISSN 2296-6463. doi:10.3389/feart.2019.00231

- ↑ Wollast, R., & Mackenzie, F.T. (1983). "Global Cycle of Silica". In S.R. Aston (Ed.), Silicon Geochemistry and Biogeochemistry, Academic Press, páginas 39–76.
- ↑ Sarmiento, Jorge Louis (2006). Ocean biogeochemical dynamics. Gruber, Nicolas. Princeton: Princeton University Press. ISBN 9780691017075. OCLC 60651167
- ↑ Drever, James I. (1993). «The effect of land plants on weathering rates of silicate minerals». Geochimica et Cosmochimica Acta. 58 (10): 2325–2332. doi:10.1016/0016-7037(94)90013-2
- ↑ De La Rocha, Christina; Conley, Daniel J. (2017), «The Venerable Silica Cycle», ISBN 9783319540542, Springer International Publishing, Silica Stories, pp. 157–176, doi:10.1007/978-3-319-54054-2_9
- ↑ Chadwick, Oliver A.; Ziegler, Karen; Kurtz, Andrew C.; Derry, Louis A. (2005). «Biological control of terrestrial silica cycling and export fluxes to watersheds». Nature. 433 (7027): 728–731. Bibcode:2005Natur.433..728D. PMID 15716949. doi:10.1038/nature03299
- ↑ a b Yool, Andrew; Tyrrell, Toby (2003). «Role of diatoms in regulating the ocean's silicon cycle». Global Biogeochemical Cycles. 17 (4): 14.1–14.22. Bibcode:2003GBioC..17.1103Y. CiteSeerX 10.1.1.394.3912
 . doi:10.1029/2002GB002018
. doi:10.1029/2002GB002018
- ↑ DeMaster, David (2002). «The accumulation and cycling of biogenic silica in the Southern Ocean: revisiting the marine silica budget». Deep Sea Research Part II. 49 (16): 3155–3167. Bibcode:2002DSRII..49.3155D. doi:10.1016/S0967-0645(02)00076-0
- ↑ Sutton, Jill N.; Andre, Luc; Cardinal, Damien; Conley, Daniel J.; de Souza, Gregory F.; Dean, Jonathan; Dodd, Justin; Ehlert, Claudia; Ellwood, Michael J. (2018). «A Review of the Stable Isotope Bio-geochemistry of the Global Silicon Cycle and Its Associated Trace Elements». Frontiers in Earth Science. 5: 112. Bibcode:2018FrEaS...5..112S. ISSN 2296-6463. doi:10.3389/feart.2017.00112
 . hdl:1885/250959
. hdl:1885/250959
- ↑ Huebner, J. Stephen (Novembro de 1982). «Rock-Forming Minerals. Volume 2A: Single-Chain Silicates. W. A. Deer, R. A. Howie, J. Zussman». The Journal of Geology. 90 (6): 748–749. ISSN 0022-1376. doi:10.1086/628736
- ↑ Van Cappellen, P. (Janeiro de 2003). «Biomineralization and Global Biogeochemical Cycles». Reviews in Mineralogy and Geochemistry. 54 (1): 357–381. Bibcode:2003RvMG...54..357V. CiteSeerX 10.1.1.499.4327
 . doi:10.2113/0540357
. doi:10.2113/0540357
- ↑ a b c Marshall, John; Plumb, R. Alan (2013). Atmosphere, Ocean and Climate Dynamics: an Introductory Text. Burlington: Elsevier Science. ISBN 978-0-08-095987-0. OCLC 911000821
- ↑ Burckle, Lloyd H.; Cirilli, Jerome (1987). «Origin of Diatom Ooze Belt in the Southern Ocean: Implications for Late Quaternary Paleoceanography». Micropaleontology. 33 (1). 82 páginas. JSTOR 1485529. doi:10.2307/1485529
- ↑ a b c Gaillardet, J.; Dupré, B.; Allègre, C.J. (Dezembro de 1999). «Geochemistry of large river suspended sediments: silicate weathering or recycling tracer?». Geochimica et Cosmochimica Acta. 63 (23–24): 4037–4051. ISSN 0016-7037. doi:10.1016/s0016-7037(99)00307-5
- ↑ New threat from ocean acidification emerges in the Southern Ocean, Phys.org, 26 de agosto de 2019. Acesso em 28 de maio de 2025.
- ↑ Petrou, K., Baker, K.G., Nielsen, D.A. et al. (2019) "Acidification diminishes diatom silica production in the Southern Ocean". Nature: Climate Change, 9: 781–786. doi:10.1038/s41558-019-0557-y Acesso em 28 de maio de 2025.
- ↑ Information, US Department of Commerce, NOAA National Centers for Environmental. «World Ocean Atlas 2009». www.nodc.noaa.gov. Consultado em 28 de maio de 2025
- ↑ Berner, Robert (Agosto de 1992). «Weathering, plants, and the long-term carbon cycle». Geochimica et Cosmochimica Acta. 56 (8): 3225–3231. Bibcode:1992GeCoA..56.3225B. doi:10.1016/0016-7037(92)90300-8

- ↑ DeMaster, D.J. (1981). "The supply and accumulation of silica in the marine environment". Geochimica et Cosmochimica Acta 45: 1715–1732.
- ↑ Cortese, G., Gersonde, R. (2004). "Opal sedimentation shifts in the World Ocean over the last 15 Myr". Earth and Planetary Science Letters 224: 509–527.
- ↑ Łukowiak, Magdalena (2020). «Utilizing sponge spicules in taxonomic, ecological and environmental reconstructions: A review». PeerJ. 8: e10601. PMC 7751429
 . PMID 33384908. doi:10.7717/peerj.10601
. PMID 33384908. doi:10.7717/peerj.10601
 Material copiado desta fonte, disponível sob a licença Creative Commons Attribution 4.0 International License.
Material copiado desta fonte, disponível sob a licença Creative Commons Attribution 4.0 International License.