Ascocoryne sarcoides
Ascocoryne sarcoides
| |||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||
| Classificação científica | |||||||||||||||||
| |||||||||||||||||
| Nome binomial | |||||||||||||||||
| Ascocoryne sarcoides (Jacq.) J.W.Groves & D.E.Wilson (1967) | |||||||||||||||||
| Sinónimos | |||||||||||||||||
| |||||||||||||||||
A Ascocoryne sarcoides é uma espécie de fungo da família Helotiaceae. Anteriormente conhecida como Coryne sarcoides, sua história taxonômica é complexa devido à capacidade de apresentar formas sexuadas e assexuadas. Este fungo comum se manifesta como uma massa gelatinosa de discos rosados ou roxos. Amplamente distribuído na América do Norte, Eurásia e Oceania,[1] o A. sarcoides é um fungo saprófito que cresce em grupos nos troncos e galhos em uma variedade de madeiras mortas. Estudos de campo indicam que a colonização do cerne de Picea mariana por A. sarcoides confere certa resistência a infecções adicionais por fungos causadores de podridão.
Taxonomia

A história taxonômica deste fungo é complicada pelo fato de seu ciclo de vida permitir tanto uma forma assexuada (produzindo esporos assexuados, ou conídios) quanto uma forma sexuada (produzindo esporos sexuados); ao longo do tempo, diferentes autores atribuíram nomes a uma ou outra forma, muitas vezes em desacordo com as regras aceitas de nomenclatura fúngica. Foi originalmente descrito em 1781 pelo cientista holandês Nikolaus Joseph von Jacquin como Lichen sarcoides.[2] Christian Hendrik Persoon o chamou de Peziza sarcoides em 1801. Elias Magnus Fries, em sua publicação de 1822, Systema Mycologicum,[3] descreveu o estado assexuado do fungo como Tremella sarcoides. O nome de gênero Coryne foi usado pela primeira vez em 1851 por Bonorden, que propôs Coryne sarcoides para o estado assexuado; em 1865, os irmãos Tulasne (Charles e Louis René) usaram Coryne para se referir tanto às formas sexuadas quanto assexuadas. Foi designado como espécie-tipo do gênero em uma publicação de 1931 por Clements e Shear.
Décadas depois, ficou evidente que o nome Coryne sarcoides violava as convenções de nomenclatura impostas pelos taxonomistas de fungos — especificamente, a espécie foi nomeada com base no estado assexuado. Assim, em 1967, Groves e Wilson propuseram o novo nome de gênero Ascocoryne para acomodar o estado sexuado.[4] O estado conidial deste fungo é Coryne dubia Persoon ex S.F. Gray (sinônimo de Pirobasidium sarcoides von Hoehnel).[5] O epíteto específico deriva do grego sarkodes e significa "carnoso, semelhante a carne", vindo de σάρξ (sarx, sarc- em compostos), "carne", e o sufixo adjetival comum -οειδής (-oeides), "semelhante".[6]
Descrição


Este fungo é caracterizado por um apotécio de cor roxo-rosada e consistência mais ou menos gelatinosa. Os apotécios, com diâmetro geralmente entre 0,5 e 1,5 cm, começam com uma forma aproximadamente esférica, depois se achatam, tornando-se em forma de taça rasa com borda ondulada e superfície superior lisa. A superfície inferior pode ser coberta por pequenas partículas (granulada), e os apotécios são fixados diretamente à superfície de crescimento (sésseis) ou possuem um estipe rudimentar.[7] Os apotécios são acompanhados por uma forma conidial, na qual esporos assexuados são gerados. A forma conidial consiste em esporodóquios, uma massa de apotécio assexuado em forma de almofada composta por conidióforos curtos (estruturas especializadas que produzem conídios). Os esporodóquios têm cor e consistência semelhantes aos apotécios, mas variam muito em forma, geralmente sendo em formato de clava, colher ou língua, e carregam conídios minúsculos, cilíndricos, retos ou curvados.[4] Conforme o fungo amadurece e os apotécios crescem e se pressionam uns contra os outros, eles se fundem, formando uma massa gelatinosa e irregular.[8] A carne, semelhante à aparência do fungo, é roxo-rosada e gelatinosa. O odor e o sabor de A. sarcoides não são marcantes[7] e não é considerado comestível.[7]
Características microscópicas
Os esporos são translúcidos (hialinos), lisos, têm forma elipsoide e dimensões de 12–16 por 3–5 μm. Os esporos contêm uma ou duas gotículas de óleo. A esporada é branca.[9] A forma assexuada (conidial) do fungo produz esporos lisos e hialinos com 3–3,5 por 1–2 μm.[10] Os ascos (células que produzem esporos sexuados) têm formato cilíndrico, com dimensões de 115–125 por 8–10 μm. As paráfises (células filamentosas estéreis entre os ascos) são cilíndricas com pontas ligeiramente inchadas e poucas ramificações.[7]
Espécies semelhantes
A Ascocoryne cylichnium, outra espécie pequena e gelatinosa de cor violeta, possui apotécios mais frequentemente em forma de taça e esporos maiores (20–24 por 5,5–6 μm).[7] Devido à semelhança com fungos gelatinosos, a A. sarcoides já foi confundida com as espécies de basidiomicetos Auricularia auricula e Tremella foliacea. A T. foliacea é maior, marrom e tem aparência folhosa. A A. auricula também é maior, geralmente marrom, em forma de disco ou orelha, com a superfície inferior nervurada. Microscopicamente, Tremella foliacea e A. auricula são facilmente distinguidas de A. sarcoides pela presença de basídios (em vez de ascos).[10]
Outras espécies semelhantes incluem Bulgaria inquinans e Exidia glandulosa,[11] e algumas do gênero Pachyella (geralmente produzindo discos mais escuros, largos e achatados).[9]
Habitat e distribuição
Esta espécie tem ampla distribuição em áreas florestais da América do Norte e Europa. Como fungo saprófito, obtém nutrientes de matéria orgânica em decomposição e, por isso, é geralmente encontrado crescendo em tocos e troncos de árvores decíduas caídas. No entanto, também aparece em várias árvores vivas. Por exemplo, na Europa, foi encontrado nos caules de Picea abies na Finlândia,[12] França,[13] Grã-Bretanha,[14] Noruega,[15] e Alemanha.[16]
Outros locais de coleta incluem Austrália,[17] Chile,[18] China,[19] Cuba,[20] Islândia,[21] Coreia,[22] e Taiwan.[23] No Havaí, cresce em troncos caídos de Cibotium[24] e Aleurites.[25] A A. sarcoides ocorre com mais frequência no final do verão e no outono.[7]
Papel na decomposição de árvores

Diversos estudos de campo realizados na região da floresta boreal do norte de Ontário (Canadá) mostraram que a A. sarcoides está frequentemente associada a várias árvores decíduas e coníferas afetadas pela doença fúngica conhecida como podridão do cerne; essa descoberta foi considerada incomum, pois a maioria das infecções fúngicas em árvores é causada por basidiomicetos, não por ascomicetos.[26][27][28][29] No caso da espécie comercialmente valiosa Picea mariana, determinou-se que a colonização prévia por A. sarcoides reduz a incidência de infecções subsequentes por patógenos fúngicos comuns, como Fomes pini e Scytinostroma galactina; além disso, a A. sarcoides pode existir na madeira sem efeitos nocivos perceptíveis ao hospedeiro.[26] Uma relação semelhante foi demonstrada posteriormente com Pinus banksiana, onde a A. sarcoides inibiu Peniophora pseudopini, mas teve pouco efeito no crescimento subsequente de Fomes pini.[30] O estudo também mostrou que a A. sarcoides é isolada mais frequentemente de madeira defeituosa à medida que a idade da árvore aumenta (as árvores examinadas tinham mais de 80 anos) e que pode infectar tanto o cerne não infectado quanto madeira previamente decomposta; neste último caso, geralmente coexiste com outros fungos causadores da decomposição.
Pesquisa
Compostos bioativos
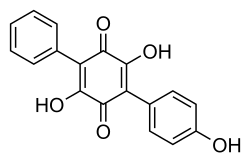
Os terfenilquinonas são compostos químicos amplamente distribuídos entre os fungos. O Ascocoryne sarcoides contém uma terfenilquinona chamada ascocorynina — um derivado do composto benzoquinona. Esse pigmento, quando em solução alcalina, torna-se violeta escuro, semelhante à cor dos apotécios do fungo. A ascocorynina possui atividade antibiótica moderada e demonstrou, em testes de laboratório, inibir o crescimento de várias bactérias gram-positivas, incluindo o organismo comum de deterioração de alimentos Bacillus stearothermophilus; no entanto, não afeta o crescimento de bactérias gram-negativas nem possui atividade antifúngica.[5]
Compostos orgânicos voláteis
Em 2008, um isolado de A. sarcoides foi observado produzindo uma série de voláteis, incluindo álcoois, cetonas e alcanos de 6 a 9 carbonos.[31] Essa mistura foi chamada de "micodiesel" devido à semelhança com algumas misturas de combustível existentes. Os pesquisadores sugeriram que isso, combinado com sua capacidade de digerir celulose, o torna uma fonte potencial de biocombustível. O isolado foi originalmente identificado como Gliocladium roseum, mas sua taxonomia foi posteriormente revisada para Ascocoryne sarcoides.[32] Seu genoma foi sequenciado em 2012 para determinar a base genética da produção desses voláteis.[33]
Ver também
- Anaptychia ciliaris
- Calycina citrina
- Leotia lubrica
- Paragyromitra infula
- Parmelia barrenoae
- Peltigera castanea
- Pulchrocladia retipora
- Spathularia flavida
- Wynnea americana
Referências
- ↑ Wiltshire R and Gates G. (2018). FungiFlip. Hobart: University of Tasmania Biological Sciences. p. 2
- ↑ Jacquin NJ. (1781). Miscellanea austriaca ad botanicum, chemiam et historiam naturalem spectantia (em latim). 2. [S.l.: s.n.] p. 20
- ↑ «New Zealand Fungi Names Databases - Fries, E.M. 1822: Systema Mycologicum. 2(1). Ex Officina Berlingiana». NZFUNGI - New Zealand Fungi (and Bacteria). Landcare Research. Consultado em 31 de março de 2025. Cópia arquivada em 13 de março de 2022
- ↑ a b Groves JW, Wilson DE (1967). «The nomenclatural status of Coryne» 1 ed. Taxon. 16: 35–41. JSTOR 1217104. doi:10.2307/1217104
- ↑ a b Quack W, Scholl H, Budzikiewicz H (1982). «Ascorynin, a terphenylquinone from Ascocoryne sarcoides» 12 ed. Phytochemistry. 21: 2921–23. doi:10.1016/0031-9422(80)85069-2
- ↑ Stearn WT. (1973). Botanical Latin 2ª anotada e revisada ed. Newton Abbot: David & Charles. pp. 265–266, 278
- ↑ a b c d e f Jordan M. (2004). The Encyclopedia of Fungi of Britain and Europe. Londres: Frances Lincoln. p. 64. ISBN 978-0-7112-2378-3
- ↑ Emberger G. «Ascocoryne sarcoides». Fungi on Wood. Messiah College. Consultado em 31 de março de 2025. Cópia arquivada em 29 de janeiro de 2009
- ↑ a b Audubon (2023). Mushrooms of North America. [S.l.]: Knopf. p. 63. ISBN 978-0-593-31998-7
- ↑ a b Wood M, Stevens F. «Ascocoryne sarcoides». California Fungi. MycoWeb. Consultado em 31 de março de 2025. Cópia arquivada em 28 de junho de 2009
- ↑ Davis, R. Michael; Sommer, Robert; Menge, John A. (2012). Field Guide to Mushrooms of Western North America. Berkeley: University of California Press. p. 400. ISBN 978-0-520-95360-4. OCLC 797915861
- ↑ Kallio T, Tamminen P (1974). «Decay of spruce (Picea abies [L.] Karst.) in the Åland Islands». Acta Forestalia Fennica. 138: 1–42
- ↑ Delatour C.; Sylvestre, Gilberte (1976). «Microflore interne de tissus ligneux de l'epicéa commun sur pied» 4 ed. Annales des Sciences Forestières (em francês). 33: 199–219. doi:10.1051/forest/19760402

- ↑ Pawsey RG. (1971). «Some recent observations on decay of conifers associated with extraction damage, and on butt rot caused by Polyporus sehweinitzii and Sparassis crispa». Quarterly Journal of Forestry. 65: 193–208
- ↑ Roll-Hansen F, Roll-Hansen H (1976). «Microflora of sound-looking wood in Picea abies stems» 5 ed. European Journal of Forest Pathology. 9: 308–16. doi:10.1111/j.1439-0329.1979.tb00693.x
- ↑ Zycha H, Dimitri L (1968). «Ausmaß und Ursache der Kernfäule in einer Fichtenprobefläche in Reinhausen (Niedersachsen)» 1 ed. Forstwiss. CBL. (em alemão). 87: 331–41. doi:10.1007/BF02735875
- ↑ Fuhrer BA. (1985). A Field Companion to Australian Fungi. Fitzroy, Vic., Austrália: Five Mile Press. pp. 144–45. ISBN 978-0-86788-063-2
- ↑ Stinson, M., Ezra, D., Hess, W.M., Sears, J., and Strobel, G. (2003). An endophytic Gliocladium sp. of Eucryphia cordifolia producing selective volatile antimicrobial compounds. Plant Science 165, 913–922.
- ↑ Zhuang W-Y. (1999). «Discomycetes of tropical China. VI. Additional species from Guangxi» (PDF). Fungal Diversity. 3: 187–96. Consultado em 31 de março de 2025. Cópia arquivada (PDF) em 24 de julho de 2011
- ↑ Dennis RWG. (1954). «Some inoperculate Discomycetes of Tropical America» 2 ed. Kew Bulletin. 9: 289–348. JSTOR 4114399. doi:10.2307/4114399
- ↑ Hallgrimsson H, Gotzsche HF (1990). «Notes on Ascomycetes. II. Discomycetes». Acta Botanica Islandica. 10: 31–36
- ↑ Lee JB, Kim SC, Oh DC (2000). «Higher fungal flora of Jeju-do (3): Unrecorded fungi (Ascomycota)» 4 ed. Mycobiology (Resumo de reunião). 28: 232–32
- ↑ Liou SC, Chen ZC (1977). «Notes on Taiwan discomycetes. Part I: Pezizales and Helotiales». Tawainia. 22: 29–43
- ↑ Gilbertson RL, Hemmes DE (1997). «Notes on fungi on Hawaiian tree ferns». Mycotaxon. 62: 465–87
- ↑ Cash EK. (1938). «New records of Hawaiian discomycetes» 1 ed. Mycologia. 38: 97–107. JSTOR 3754484. doi:10.2307/3754484
- ↑ a b Basham JT. (1973). «Heart rot of black spruce in Ontario. I. Stem rot, hidden rot, and management considerations» 1 ed. Canadian Journal of Forest Research. 3: 95–104. doi:10.1139/x73-014
- ↑ Etheridge DE. (1970). «Ascocoryne sarcoides (Jacq. ex Gray) Groves and Wilson and its association with decay of conifers». Fonds Rech. For. Univ. Laval. 13: 19–26
- ↑ Basham JT. (1973). «Heart rot of black spruce in Ontario. 2. Mycoflora in defective and normal wood of living trees» 7 ed. Canadian Journal of Botany. 51: 1379–92. doi:10.1139/b73-173
- ↑ Etheridge DE, Morin LA (1967). «The microbiological condition of wood of living balsam fir and black spruce in Quebec» 7 ed. Canadian Journal of Botany. 45: 1003–10. doi:10.1139/b67-104
- ↑ Basham JT. (1975). «Heart rot of Jack Pine in Ontario. IV. Heartwood-inhabiting fungi, their entry and interactions with living tree» 4 ed. Canadian Journal of Forest Research. 5: 706–21. doi:10.1139/x75-097
- ↑ Strobel, G.A.; Knighton, B.; Kluck, K.; Ren, Y.; Livinghouse, T.; Griffin, M.; Spakowicz, D.; Sears, J. (2008). «The production of myco-diesel hydrocarbons and their derivatives by the endophytic fungus Gliocladium roseum (NRRL 50072)» 11 ed. Microbiology. 154: 3319–28. PMID 18957585. doi:10.1099/mic.0.2008/022186-0

- ↑ Griffin, MA; Spakowicz, DJ; Gianoulis, TA; Strobel, SA (Dez 2010). «Volatile organic compound production by organisms in the genus Ascocoryne and a re-evaluation of myco-diesel production by NRRL 50072» 12 ed. Microbiology. 156: 3814–29. PMC 7336539
 . PMID 20705658. doi:10.1099/mic.0.041327-0
. PMID 20705658. doi:10.1099/mic.0.041327-0
- ↑ Gianoulis, T.A.; Griffin, M.A.; Spakowicz, D.J.; Dunican, B.F.; Alpha, C.J.; Sboner, A.; Sismour, A.M.; Kodira, C.; Egholm, M.; Church, G.M. (2012). «Genomic Analysis of the Hydrocarbon-Producing, Cellulolytic, Endophytic Fungus Ascocoryne sarcoides» 3 ed. PLOS Genet. 8: e1002558. PMC 3291568
 . PMID 22396667. doi:10.1371/journal.pgen.1002558
. PMID 22396667. doi:10.1371/journal.pgen.1002558