Cap 5'
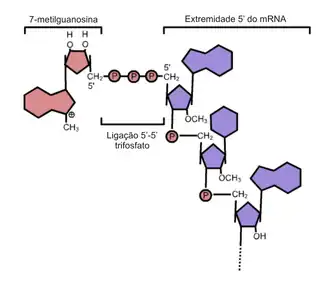
Cap 5' é uma estrutura típica de mRNA eucariótico, a qual é gerada pela ligação 5'-5' trifosfato entre a extremidade 5' de uma molécula de mRNA precursora e um nucleotídeo alterado (GMP metilado). O Cap 5' protege o mRNA contra a ação de ribonucleases, proteção contra a ação de fosfatases e também é responsável por interagir com complexos protéicos que processam, exportam o mRNA para o citosol e promovem a ligação deste com os ribossomos.[1][2]
É um nucleótido especialmente alterado localizado na extremidade 5′ do RNA mensageiro precursor e de alguns outros transcritos primários encontrados em eucariotas. É também designado por cap 7-metilguanosina ou cap m7G, cap de RNA m7G ou cap 5′. O processo de formação do cap 5′ é vital para a criação do mRNA maduro, que pode então sofrer tradução em proteínas. A formação do cap garante a estabilidade do mRNA durante a tradução e é um processo altamente regulado que ocorre exclusivamente no núcleo celular, razão pela qual os mRNA dos mitocôndrias e cloroplastos não possuem um cap 5′.[3][4]
Estrutura da cap 5′
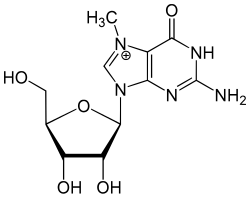
O cap 5′ está localizado na extremidade 5′ de uma molécula de mRNA e consiste numa única molécula de nucleótido com guanina ligada ao mRNA através de uma ligação trifosfato 5′-5′ invulgar. Esta guanosina é metilada in vivo no nitrogénio em posição 7, logo após a formação do cap, por uma metiltransferase, criando uma carga positiva neste azoto. Por esta razão, o cap é também designado por 7-metilguanosina ou 7-metilguanilato, abreviado como m7G.
Outras modificações incluem a possível metilação dos grupos hidroxilo 2′ das duas primeiras riboses na extremidade 5′ do mRNA. A metilação de ambos os grupos hidroxilo é apresentada no primeiro diagrama. A extremidade 5′ (cap) assemelha-se à extremidade 3′ (cap) de um RNA (o carbono da ribose na extremidade 5′ do cap está ligado, enquanto o da extremidade 3′ não). Isto confere à molécula uma resistência significativa às exonucleases 5′. As moléculas de mRNA podem perder os seus caps 5′ num processo denominado "decapagem" do mRNA.
Os pequenos ARN nucleares contêm caps 5′ únicos. Os pequenos ARN nucleares da classe Sm possuem caps com 5′-trimetilguanosina, enquanto os da classe Lsm possuem caps com 5′-monometilfosfato.[5]
Formação do Cap
O ponto de partida para a formação do cap, ou "capagem", é a extremidade 5' inalterada de uma molécula de mRNA. Esta possui um nucleótido final ligado a três grupos fosfato no carbono 5’.
Um dos grupos fosfato terminais é removido por uma fosfatase de RNA terminal, restando apenas dois fosfatos.
- Uma guanilil transferase utiliza um GTP como substrato para adicionar um GMP a estes dois fosfatos terminais. No processo, perdem-se dois grupos fosfato do GTP, pelo que o que é realmente adicionado é GMP. Como o GMP já se ligou aos dois grupos fosfato da extremidade através do seu único fosfato, forma-se uma ligação trifosfato 5'-5'.
- O azoto na posição 7 da base azotada guanina do GMP é então metilado por uma metiltransferase.
- As metilações podem também ocorrer em nucleótidos adjacentes ao cap, geralmente o segundo e o terceiro nucleótidos. Se a segunda base a contar da extremidade for uma 2’-O-ribose metil-adenosina, esta pode ser adicionalmente metilada na posição N6, formando N6-metiladenosina.[6] A terceira base a contar da extremidade também costuma ser metilada (10-15% das vezes).
Enzimas envolvidas
O Complexo Enzimático de Capeamento (CEC), necessário para a formação do cap, está ligado à RNA polimerase II antes do início da transcrição genética. À medida que a extremidade 5’ do novo transcrito emerge durante a transcrição, as enzimas transferem-se para a mesma e iniciam o capeamento (este é um mecanismo semelhante ao que ocorre na poliadenilação).[7][8][9][10]
As enzimas responsáveis pela formação do cap apenas se podem ligar à RNA polimerase II, garantindo assim a especificidade apenas para os transcritos que são quase exclusivamente mRNA.[8][10]
Função do cap 5′
O cap 5′ tem 4 funções principais:
- Regulação da exportação nuclear de mRNA.[11][12]
- Prevención da degradación por exonucleases do ARNm.[13][14][15]
- Promoção da tradução do mRNA.)[6][16][17]
- Promoção da excisão do intrão mais próximo da extremidade 5′.[18][19]
A exportação nuclear do RNA é regulada pelo complexo de ligação ao cap (CBC), que se liga exclusivamente aos RNAs com cap. O CBC é então reconhecido pelo complexo do poro nuclear e exportado. Uma vez no citoplasma após a primeira ronda de tradução do mRNA, o CBC é substituído pelo fatores de transcrição eIF-4E e eIF-4G. Este complexo é então reconhecido pela maquinaria de iniciação da tradução, incluindo o ribossoma.[20]
O cap 5' impede a degradação do RNA de duas formas. Em primeiro lugar, como referido acima, a degradação do mRNA pelas exonucleases 5’ é impedida porque a extremidade 5’ protegida pelo cap se assemelha funcionalmente a uma extremidade 3’. Em segundo lugar, o complexo CBC e o fator eIF-4E/eIF-4G bloqueiam o acesso ao cap pelas enzimas removedoras do cap. Isto aumenta a meia-vida do mRNA, o que é essencial nos eucariotas, uma vez que o processo de exportação é muito demorado.
A remoção do cap de um mRNA é catalisada por um complexo enzimático formado por pelo menos Dcp1 e Dcp2, que competem com o eIF-4E pela ligação ao cap. Assim, o cap 5’ é um marcador de mRNA em tradução ativa e é utilizado pelas células para regular o tempo de semivida dos mRNA em resposta a novos estímulos. Os mRNA indesejáveis são enviados para os corpos P para armazenamento temporário ou remoção do cap, cujos detalhes ainda não são conhecidos.[21]
O mecanismo de promoção da excisão do intrão 5’ proximal não está bem esclarecido, mas o cap 5’ parece formar um laço em torno do spliceossoma e interagir com este durante o processo de splicing, o que promoveria a excisão do intrão.
Ver também
Referências
- ↑ ALBERTS, B.; JOHNSON, A.; LEWIS, J.; RAFF, M.; ROBERTS, K.; WALTER, P.. Molecular Biology of the Cell. 5 ed. New York: Garland science, Taylor & Francis Group, 2008. 1268 p. ISBN 9780815341062
- ↑ NELSON, D. L.; COX, M. M.. Lehninger Principles of Biochemistry. 4 ed. W.H. Freeman & Co, 2004. 1100 p. ISBN 9780716764380
- ↑ Temperley, Richard J.; Wydro, Mateusz; Lightowlers, Robert N.; Chrzanowska-Lightowlers, Zofia M. (junho de 2010). «Human mitochondrial mRNAs—like members of all families, similar but different». Biochimica et Biophysica Acta (BBA) - Bioenergetics. 1797 (6-7): 1081–1085. doi:10.1016/j.bbabio.2010.02.036. Consultado em 12 de dezembro de 2014
- ↑ Monde, Rita A; Schuster, Gadi; Stern, David B (7 de junho de 2000). «Processing and degradation of chloroplast mRNA». Biochimie. 82 (6-7): 573–582. doi:10.1016/S0300-9084(00)00606-4. Consultado em 12 de dezembro de 2014
- ↑ Matera, A. Gregory; Terns, Rebecca M.; Terns, Michael P. (março de 2007). «Non-coding RNAs: lessons from the small nuclear and small nucleolar RNAs». Nature Reviews Molecular Cell Biology. 8 (3): 209–220. doi:10.1038/nrm2124. Consultado em 12 de dezembro de 2014
- ↑ a b Shatkin, A (Dezembro de 1976). "Capping of eukaryotic mRNAs". Cell 9 (4): 645–653. doi:10.1016/0092-8674(76)90128-8.
- ↑ Cho, E.-J.; Takagi, T.; Moore, C. R.; Buratowski, S. (15 de dezembro de 1997). «mRNA capping enzyme is recruited to the transcription complex by phosphorylation of the RNA polymerase II carboxy-terminal domain». Genes & Development. 11 (24): 3319–3326. doi:10.1101/gad.11.24.3319. Consultado em 23 de novembro de 2014
- ↑ a b Fabrega, Carme; Shen, Vincent; Shuman, Stewart; Lima, Christopher D. (junho de 2003). «Structure of an mRNA Capping Enzyme Bound to the Phosphorylated Carboxy-Terminal Domain of RNA Polymerase II». Molecular Cell. 11 (6): 1549–1561. doi:10.1016/S1097-2765(03)00187-4. Consultado em 23 de novembro de 2014
- ↑ Ho, C. (15 de dezembro de 1999). «An essential surface motif (WAQKW) of yeast RNA triphosphatase mediates formation of the mRNA capping enzyme complex with RNA guanylyltransferase». Nucleic Acids Research. 27 (24): 4671–4678. doi:10.1093/nar/27.24.4671. Consultado em 23 de novembro de 2014
- ↑ a b Hirose, Yutaka; Manley, James L (2000). «RNA polymerase II and the integration of nuclear events». Genes & Dev. 14: 1415–1429. doi:10.1101/gad.14.12.1415. Consultado em 23 de novembro de 2014
- ↑ Visa, N.; Izaurralde, E.; Ferreira, J.; Daneholt, B.; Mattaj, I. W. (1 de abril de 1996). «A nuclear cap-binding complex binds Balbiani ring pre-mRNA cotranscriptionally and accompanies the ribonucleoprotein particle during nuclear export». The Journal of Cell Biology. 133 (1): 5–14. doi:10.1083/jcb.133.1.5. Consultado em 23 de novembro de 2014
- ↑ Lewis, Joe D.; Izaurralde, Elisa (15 de julho de 1997). «The Role of the Cap Structure in RNA Processing and Nuclear Export». European Journal of Biochemistry. 247 (2): 461–469. doi:10.1111/j.1432-1033.1997.00461.x. Consultado em 23 de novembro de 2014
- ↑ Evdokimova, Valentina; Ruzanov, Peter; Imataka, Hiroaki; Raught, Brian; Svitkin, Yuri; Ovchinnikov, Lev P.; Sonenberg, Nahum (1 de outubro de 2001). «The major mRNA-associated protein YB-1 is a potent 5' cap-dependent mRNA stabilizer». The EMBO Journal. 20 (19): 5491–5502. doi:10.1093/emboj/20.19.5491. Consultado em 23 de novembro de 2014
- ↑ Gao, Min; Fritz, David T.; Ford, Lance P.; Wilusz, Jeffrey (março de 2000). «Interaction between a Poly(A)-Specific Ribonuclease and the 5′ Cap Influences mRNA Deadenylation Rates In Vitro». Molecular Cell. 5 (3): 479–488. doi:10.1016/S1097-2765(00)80442-6. Consultado em 23 de novembro de 2014
- ↑ Burkard, K. T. D.; Butler, J. S. (15 de janeiro de 2000). «A Nuclear 3'-5' Exonuclease Involved in mRNA Degradation Interacts with Poly(A) Polymerase and the hnRNA Protein Npl3p». Molecular and Cellular Biology. 20 (2): 604–616. doi:10.1128/MCB.20.2.604-616.2000. Consultado em 23 de novembro de 2014. Cópia arquivada em 6 de novembro de 2018
- ↑ Banerjee, A K (Junho 1980). "Estrutura do cap 5'-terminal em ácidos ribonucleicos mensageiros eucarióticos". Microbiol Rev 44(2): 175–205.
- ↑ Sonenberg, Nahum; Gingras, Anne-Claude (April 1998). "The mRNA 5′ cap-binding protein eIF4E and control of cell growth". Current Opinion in Cell Biology 10 (2): 268–275. doi:10.1016/S0955-0674(98)80150-6. [1] Arquivado em 2015-09-24 no Wayback Machine
- ↑ Konarska, Maria M.; Padgett, Richard A.; Sharp, Phillip A. (outubro de 1984). «Recognition of cap structure in splicing in vitro of mRNA precursors». Cell. 38 (3): 731–736. doi:10.1016/0092-8674(84)90268-X. Consultado em 12 de dezembro de 2014
- ↑ «Recognition of cap structure in splicing in vitro of mRNA precursors». Consultado em 11 de dezembro de 2012. Arquivado do original em 22 de fevereiro de 2014
- ↑ Kapp, L.D.; Lorsch, J.R. (2004). «The Molecular Mechanics of Eukaryotic Translation» (PDF). Annual Review of Biochemistry. 73 (1): 657–704. PMID 15189156. doi:10.1146/annurev.biochem.73.030403.080419. Consultado em 3 de abril de 2013. Cópia arquivada (PDF) em 20 de fevereiro de 2012
- ↑ Parker, R.; Sheth, U. (2007). «P Bodies and the Control of mRNA Translation and Degradation» (w). Molecular Cell. 25 (5): 635–646. PMID 17349952. doi:10.1016/j.molcel.2007.02.011