Modificação pós-transcricional
O processamento do RNA é o conjunto de modificações co-transcricionais e pós-transcricionais que o transcrito primário de um RNA sofre durante e após a sua transcrição, principalmente nas células eucarióticas, para se tornar um RNA maduro e totalmente funcional. Um exemplo notável é a conversão do ARNm precursor em mRNA maduro, que inclui a sua splicing e a modificação das suas extremidades antes da síntese proteica. Este processo é vital para a tradução adequada do genoma, uma vez que, nos eucariotas, os genes e os transcritos primários de mRNA contêm intrões (regiões não codificantes) que necessitam de ser removidos.[1] O processamento também afeta outros tipos de RNA. É um processo tipicamente eucariótico, uma vez que as bactérias não possuem intrões no mRNA, mas também ocorre processamento do RNA nos procariontes. Outra forma de modificação dos transcritos de RNA é a sua edição, que consiste na realização de inserções, deleções e substituições de bases nucleotídicas na molécula de RNA após a sua transcrição.
Processamento do mRNA
Nos procariontes, o mRNA não é modificado e pode ser traduzido diretamente (por vezes, a tradução começa a partir de uma extremidade quando a outra ainda não completou a transcrição). Em contraste, nos eucariotas, o mRNA sofre extensas modificações no núcleo antes de ir para o citoplasma para iniciar a tradução. Nos eucariotas, a molécula de pré-mRNA sofre três modificações principais: formação do cap 5' (ou "capagem" 5'), poliadenilação e splicing, que ocorrem no núcleo celular antes de o RNA ser traduzido.[2]
Processamento 5'
Formação da Cap 5'
A formação da Cap 5' ou capping no pre-ARNm a adição de uma molécula de 7-metilguanosina (m7G) à extremidade 5’ do RNA é um processo que ocorre quando o fosfato terminal 5’ é removido, o que é feito com o auxílio da enzima fosfatase. A enzima guanosiltransferase catalisa a reacção, produzindo o difosfato na extremidade 5’. Este difosfato ataca, então, o átomo de fósforo gama da molécula de GTP (que perde dois fosfatos) para adicionar o resíduo de GMP, formando uma ligação trifosfato 5’5’. A enzima (guanina-N7-)-metiltransferase ("cap MTase") transfere um grupo metilo da S-adenosilmetionina para o anel da guanina..[3] Este tipo de tampa, que tem simplesmente o (m7G) em posição, é designado por estrutura "tampa 0". A ribose do nucleótido adjacente também pode ser metilada para dar uma "tampa 1". A metilação de nucleótidos "a jusante" da molécula de RNA produz as estruturas "tampa 2", "tampa 3" e assim por diante. Em todos estes casos, os grupos metilo são adicionados aos grupos 2' OH do açúcar ribose. A tampa 5' protege a extremidade 5' do transcrito primário de RNA do ataque de ribonucleases que têm especificidade para ligações fosfodiéster 3'-5'.[4]
Processamento 3'
Clivagem e Poliadenilação
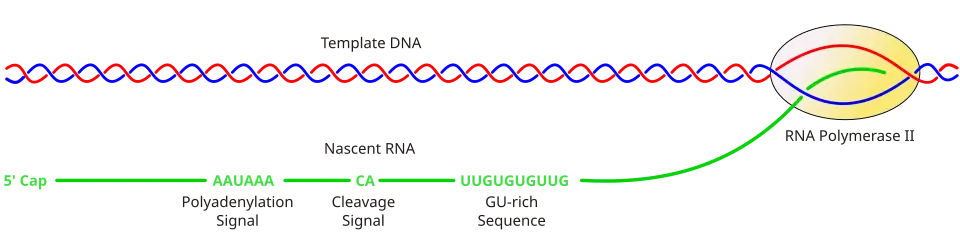
O processamento do pré-mRNA na extremidade 3’ da molécula de RNA envolve a clivagem (corte) dessa extremidade e a subsequente adição de cerca de 200 resíduos de adenosina monofosfato (AMP) para formar a chamada cauda poli(A). As reações de clivagem e adenilação ocorrem se uma sequência sinal de poliadenilação (5’-AAUAAA-3’) estiver localizada junto à extremidade 3’ do RNA, seguida de outra sequência, geralmente 5’-CA-3’. O segundo sinal é o local de clivagem. Uma sequência rica em GU também costuma estar presente no RNA um pouco mais a jusante. De seguida, duas proteínas multissubunitárias denominadas fator de especificidade de poliadenilação e clivagem (CPSF) e fator de estimulação de clivagem (CstF) são transferidas da RNA polimerase II para a molécula de RNA. Ambos os fatores se ligam aos elementos de sequência do RNA. Forma-se um complexo proteico, contendo fatores de clivagem adicionais e a enzima poliadenilato polimerase (PAP). Este complexo cliva o RNA entre a sequência de poliadenilação e a sequência rica em GU no local de clivagem marcado pelas sequências 5’-CA-3’. A poli(A) polimerase adiciona então cerca de 200 unidades de AMP à nova extremidade 3’ do RNA, utilizando moléculas de adenosina trifosfato (ATP) como precursor. À medida que a cauda poli(A) é sintetizada, muitas cópias da proteína de ligação à poli(A) são ligadas a esta, protegendo a extremidade 3’ da digestão por ribonucleases.[5]
Splicing
O splicing do RNA é o processo pelo qual os intrões (regiões não codificadoras de proteínas) de um pré-mRNA são removidos, restando apenas os éxons (regiões codificadoras), que são unidos para formar uma única molécula contínua de RNA. Embora a maior parte do splicing do RNA ocorra após a molécula de pré-mRNA estar totalmente sintetizada e com o cap 5’ adicionado, os transcritos com muitos éxons podem sofrer splicing co-transcricional.[6] A reação de splicing é catalisada por um grande complexo proteico denominado spliceossoma, que é um conjunto de proteínas e pequenas moléculas de RNA nuclear que reconhecem o sítio de splicing na sequência do pré-mRNA. Muitos pré-mRNA, incluindo os que codificam anticorpos, podem ser processados por splicing de diversas formas, produzindo diferentes mRNA maduros, que codificam diferentes estruturas primárias de proteínas (diferentes anticorpos no exemplo), através de um processo conhecido como splicing alternativo, que permite a produção de uma grande variedade de proteínas a partir de uma quantidade limitada de ADN.
Processamento do ARNr
Nos procariontes, existem sete genes de ARNr, cada um dos quais dá origem a um ARN precursor 30S, que contém os três tipos de ARNr (ARNr 23S, ARNr 16S e ARNr 5S) e até algum ARNt, separados por sequências espaçadoras. Esta longa transcrição é depois cortada para dar origem aos ARNr finais, um processo denominado "aparamento", que é realizado pelas enzimas ribonuclease P e ribonuclease III.[7]
Nos eucariotas, o processo é semelhante, mas aqui a molécula precursora é o 45S (contém apenas três ARN ribossómicos: 28S rRNA, 18S rRNA e 5,8S rRNA, mas não o 5S rRNA, que é transcrito separadamente, nem o tRNA). Os eucariotas possuem centenas de genes precursores do 45S rRNA, que são transcritos no nucléolo pela RNA polimerase I. A clivagem endonucleolítica separa os RNA ribossómicos e remove os espaçadores entre eles. Nos eucariotas, o ARNr 5.8S estabelece o emparelhamento de bases com o ARNr 28S quando ambos são libertados e formam as subunidades ribossómicas.[7]
As modificações pós-transcricionais que um ARNr sofre podem também afetar as modificações de bases e ocorrem tanto em eucariotas como em procariotas. Podem ser de três tipos básicos: metilação de bases, metilação de riboses e pseudouridilação. A metilação de bases ocorre em regiões conservadas do RNA; na subunidade ribossómica menor dos procariotas, esta metilação não é essencial, mas melhora a eficiência da tradução.[8] A metilação da ribose ocorre sempre no carbono 2' e é muito mais frequente nos eucariotas do que nas bactérias, mas na arquea "Sulfolobus solfataricus" é comparável à dos eucariotas;[9] a metilação da ribose não é essencial para a função do RNA, mas mutações que a impedem nos microrganismos afectam o crescimento[10] A pseudouridilação (introdução de pseudouridilação ou Ψ) é comum nos eucariotas e mais rara nos procariontes.
Estas modificações foram melhor estudadas em Escherichia coli, onde foram encontrados 11 locais de modificação no rRNA 16S, 24 no 23S e nenhum no 5S.[11][12]
Os genes do ARNr de alguns eucariotas e procariontes contêm intrões.[13]
Processamento de tRNA
Os tRNAs nos procariontes têm origem como transcritos longos contendo vários tRNAs, que são depois clivados para gerar os tRNAs finais. Os genes dos tRNA estão agrupados no genoma e os transcritos iniciais contêm dois a sete tRNA (alguns tRNA podem também estar contidos no transcrito inicial dos rRNA nos procariontes). As ribonucleases P (atuando na extremidade 5’) e D (atuando na extremidade 3’) clivam os transcritos, libertando os diferentes tRNA. Na extremidade 3’, uma estrutura em alça-tronco é clivada e, por vezes, parte dos nucleótidos adjacentes à sequência CAA característica dos tRNA, ou a própria sequência, é eliminada. De seguida, a sequência CCA é adicionada à extremidade 3’ nos tRNA que a perderam na clivagem anterior, processo realizado pela tRNA nucleotidiltransferase. De seguida, o tRNA sofre uma modificação das suas bases, principalmente metilações, mas também tiolações e transformação de uracilo em di-hidrouracilo ou pseudouracilo.[7][14] Nos eucariotas, o tRNA também é formado como um longo precursor que é depois clivado de forma semelhante aos procariotas. Nos mamíferos, a metilação do tRNA precursor parece ocorrer no núcleo, mas a clivagem e a ligação da sequência CAA são citoplasmáticas.[15] Em mamíferos, também foram estudadas modificações de bases nos tRNA mitocondriais.[16][17] Nos eucariotas, alguns genes de tRNA contêm intrões, que são removidos durante o processamento; por exemplo, na levedura, 10 tRNAs têm os seus intrões removidos durante o processamento.
Processamento de outros RNA
Outros pequenos ARN na célula também sofrem processamento em eucariotas. Por exemplo, os microRNAs (miRNAs) são inicialmente transcritos como pré-miRNAs de 70 nucleótidos com um cap 5’ e uma cauda poli(A), têm uma forma de alça-tronco e são processados pela enzima Drosha e pela proteína Pasha, que atuam no núcleo. O processamento continua no citoplasma pela endonuclease Dicer, que dá origem ao miRNA maduro.
Processamento de outros RNA
Outros pequenos ARN na célula também sofrem processamento em eucariotas. == Degradação do RNA == Uma vez que tenha cumprido a sua função, o RNA é degradado enzimaticamente, por exemplo, por complexos enzimáticos como o exossomo (em eucariotas e arqueias) e o degradosoma (em bactérias). Outras nucleases também podem destruir o RNA. O exossoma desempenha também um papel no processamento do RNA nuclear pequeno, do RNA nucleolar pequeno e do rRNA 5.8S.[18]
Referências
- ↑ Berg, Tymoczko & Stryer 2007, p. 836
- ↑ Berg, Tymoczko & Stryer 2007, p. 841
- ↑ Yamada-Okabe, Toshiko; Mio, Toshiyuki; Matsui, Mitsuaki; Arisawa, Mikio; Yamada-Okabe, Hisafumi (novembro de 1999). «The Candida albicans gene for mRNA 5'-cap methyltransferase: identification of additional residues essential for catalysis» (PDF). Microbiology. 145. ISSN 1350-0872. PMID 10589710. Consultado em 7 de janeiro de 2011
- ↑ Hames & Hooper 2006, p. 221
- ↑ Diana F. Colgan, James L. Manley. Mechanism and regulation of mRNA polyadenylation. Genes & Development. 1997. doi 10.1101/gad.11.21.2755. [1]
- ↑ Lodish HF, Berk A, Kaiser C, Krieger M, Scott MP, Bretscher A, Ploegh H, Matsudaira PT (2007). «Chapter 8: Post-transcriptional Gene Control». Molecular Cell .Biology. San Francisco: WH Freeman. ISBN 0-7167-7601-4
- ↑ a b c Victor L. Davidson,Donald B. Sittman. Biochemistry. Páxina 154 e ss. Google books. [2]
- ↑ Raue, H., Klootwijk, J., & Musters, W. (1988). Evolutionary conservation of structure and function of high molecular weight ribosomal RNA. Prog Biophys Mol Biol, 51, 77-129.
- ↑ Noon, K. R., Bruenger, E., & McCloskey, J. A. (1998). Modificações pós-transcritas nos rRNAs 16S e 23S do hipertermófilo arqueal Sulfolobus solfataricus. J. Bacteriol., 180, 2883-2888.
- ↑ Tollervey, D., Lehtonen, H., Jansen, R., Kern, H., & Hurt, E. C. (1993). Mutações sensíveis à temperatura demonstram o papel da fibrilarina de levedura no processamento do pré-rRNA, na metilação do pré-rRNA e na montagem do ribossoma. Cell, 72, 443-457.
- ↑ Kowalak, J.A., Pomerantz, S.C., Crain, P.F. and McCloskey, J.A. (1993) A novel method for the determination of post-transcriptional modification in RNA by mass spectrometry. Nucleic Acids Res, 21, pp. 4577-85. PMID 8233793
- ↑ Kowalak, J.A., Bruenger, E. and McCloskey, J.A. (1995) Posttranscriptional modification of the central loop of domain V in Escherichia coli 23 S ribosomal RNA. J Biol Chem, 270, pp. 17758-64. PMID 7629075
- ↑ Verena Salmana, Rudolf Amanna, David A. Shubb, and Heide N. Schulz-Vogta. Multiple self-splicing introns in the 16S rRNA genes of giant sulfur bacteria. PNAS [3] Arquivado em 2019-09-15 no Wayback Machine
- ↑ Post-transcriptional processing og rRNA and tRNA
- ↑ «Biochemistry for medics». Consultado em 26 de julho de 2014. Arquivado do original em 30 de julho de 2014
- ↑ Suzuki T, Suzuki T. A complete landscape of post-transcriptional modifications in mammalian mitochondrial tRNAs. Nucleic Acids Res. 2014;42(11):7346-57. doi: 10.1093/nar/gku390. Epub 2014 May 15. PMID 24831542
- ↑ Suzuki T1, Nagao A, Suzuki T. Human mitochondrial tRNAs: biogenesis, function, structural aspects, and diseases. Annu Rev Genet. 2011;45:299-329. doi: 10.1146/annurev-genet-110410-132531. Epub 2011 Sep 6. PMID 21910628
- ↑ Allmang et al.. "Functions of the exosome in rRNA, snoRNA and snRNA synthesis". EMBO Journal. DOI:10.1093/emboj/18.19.5399. PMID 10508172.
Leitura adicional
- Berg JM, Tymoczko JL, Stryer L (2007). Biochemistry 6 ed. New York: WH Freeman & Co. ISBN 978-0-7167-6766-4
- Hames D, Hooper N (2006). Instant Notes Biochemistry. Annales de Biologie Clinique. 58 3 ed. Leeds: Taylor and Francis. 767 páginas. ISBN 978-0-415-36778-3. PMID 11098183
- Sun WJ, Li JH, Liu S, Wu J, Zhou H, Qu LH, Yang JH (janeiro de 2016). «RMBase: a resource for decoding the landscape of RNA modifications from high-throughput sequencing data». Nucleic Acids Research. 44 (D1): D259-65. PMC 4702777
 . PMID 26464443. doi:10.1093/nar/gkv1036
. PMID 26464443. doi:10.1093/nar/gkv1036 - Machnicka MA, Milanowska K, Osman Oglou O, Purta E, Kurkowska M, Olchowik A, Januszewski W, Kalinowski S, Dunin-Horkawicz S, Rother KM, Helm M, Bujnicki JM, Grosjean H (janeiro de 2013). «MODOMICS: a database of RNA modification pathways--2013 update». Nucleic Acids Research. 41 (Database issue): D262-7. PMC 3531130
 . PMID 23118484. doi:10.1093/nar/gks1007
. PMID 23118484. doi:10.1093/nar/gks1007 - Cantara WA, Crain PF, Rozenski J, McCloskey JA, Harris KA, Zhang X, Vendeix FA, Fabris D, Agris PF (janeiro de 2011). «The RNA Modification Database, RNAMDB: 2011 update». Nucleic Acids Research. 39 (Database issue): D195-201. PMC 3013656
 . PMID 21071406. doi:10.1093/nar/gkq1028
. PMID 21071406. doi:10.1093/nar/gkq1028