Dimorfismo sexual
Em biologia, o dimorfismo sexual é considerado quando há ocorrência de indivíduos do sexo masculino e feminino de uma espécie com características físicas não sexuais marcadamente diferentes. Pode ocorrer em qualquer grupo de seres vivos, protistas, plantas, ou animais, que apresentem espécies com indivíduos unissexuais. A função destas diferenças, em muitos casos, está relacionada à luta dos indivíduos pelo direito de se reproduzir, usando tais caracteres para lutar por um(a) parceiro(a), ou impressioná-lo(a) com os seus dotes. Em algumas plantas, especificamente, as diferenças são puramente funcionais, e não competitivas.
O oposto do dimorfismo é o monomorfismo, quando ambos os sexos biológicos são fenotipicamente indistinguíveis um do outro. Muitos répteis, por exemplo, com os órgãos sexuais internos, não demonstram notórias diferenças externas entre os espécimes de sexos diferentes.[1]
-
 Dimorfismo sexual: A diferença entre um faisão fêmea (menor, à esquerda) e macho (à direita)
Dimorfismo sexual: A diferença entre um faisão fêmea (menor, à esquerda) e macho (à direita) -
 Monomorfismo sexual: Pássaros da espécie Philetairus socius não exibem dimorfismo sexual visível aos olhos humanos
Monomorfismo sexual: Pássaros da espécie Philetairus socius não exibem dimorfismo sexual visível aos olhos humanos
Exemplos
Um tipo comum de dimorfismo é ornamentação. Um componente frequente de tal ornamentação dimórfico é dicromatismo sexual, o que significa que os sexos de uma mesma espécie diferem na coloração, como é o caso em muitas espécies de aves e répteis.[2][3]
Características dimórficas exageradas são utilizados predominantemente na competição entre companheiros.[4] A ornamentação pode ser cara para se produzir ou manter, o que tem implicações evolutivas complexas[5] mas os custos e implicações variam, dependendo da natureza da ornamentação (tal como o mecanismo de cor envolvido).
Na maioria das espécies de insetos, aranhas, peixes, anfíbios, répteis, aves de rapina, corujas, etc., as fêmeas são maiores que os machos, enquanto nos mamíferos o macho é geralmente o maior, às vezes de forma muito perceptível.
-
 O pavão, à direita, cortejando sua fêmea a esquerda
O pavão, à direita, cortejando sua fêmea a esquerda -
 Macho, (em baixo) e fêmea (ao topo) do pato-real
Macho, (em baixo) e fêmea (ao topo) do pato-real -
 Macho (esquerda) e fêmea (direita) da traça da espécie Orgyia antiqua. Note que o macho é alado enquanto a fêmea não
Macho (esquerda) e fêmea (direita) da traça da espécie Orgyia antiqua. Note que o macho é alado enquanto a fêmea não -
 Fêmea adulta (esquerda, vista ventral) e macho adulto (direita, vista dorsal) da aranha da espécie Argiope appensa, exibindo diferenças sexuais típicas em aranhas, com machos dramaticamente menores
Fêmea adulta (esquerda, vista ventral) e macho adulto (direita, vista dorsal) da aranha da espécie Argiope appensa, exibindo diferenças sexuais típicas em aranhas, com machos dramaticamente menores -
 Elefante-marinho fêmea (esquerda) e macho (direita)
Elefante-marinho fêmea (esquerda) e macho (direita) -
-
_female_%2526_male.jpg) Tartarugas da espécie Graptemys pseudogeographica kohni, fêmea adulta (esquerda) e macho adulto (direita)
Tartarugas da espécie Graptemys pseudogeographica kohni, fêmea adulta (esquerda) e macho adulto (direita) -
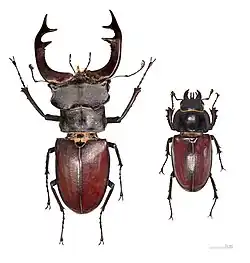 Vaca-loura. À esquerda o macho, à direita a fêmea.
Vaca-loura. À esquerda o macho, à direita a fêmea. -
Orangotango-de-sumatra. À esquerda o macho adulto, à direita a fêmea adulta. Entre os dois pode se ver um filhote.
-
 Diferenças de barbatanas dorsais entre uma orca macho (na frente, mais próxima da câmera) e fêmea (ao topo, mais distante da câmera)
Diferenças de barbatanas dorsais entre uma orca macho (na frente, mais próxima da câmera) e fêmea (ao topo, mais distante da câmera) -
.png) Fêmea de Cryptopsaras couesii, uma espécie de tamboril, com o macho preso perto da cloaca (seta). Algumas espécies de tamboril apresentam extremo dimorfismo sexual
Fêmea de Cryptopsaras couesii, uma espécie de tamboril, com o macho preso perto da cloaca (seta). Algumas espécies de tamboril apresentam extremo dimorfismo sexual
Plantas
A maioria das plantas são hermafroditas, mas cerca de 6% têm machos e fêmeas separados (dioicia).[6] Machos e fêmeas em espécies dependentes da polinização de insetos geralmente são semelhantes porque as plantas fornecem recompensas (por exemplo, néctar) que incentivam os polinizadores a visitarem outra flor semelhante, completando a polinização. As orquídeas Catasetum são uma exceção a esta regra, a Catasetum macho se anexa pólens às abelhas então evitam que outras flores masculinas, mas podem visitar uma flor fêmea, que tem a aparência diferente das flores macho.[7]
Humanos
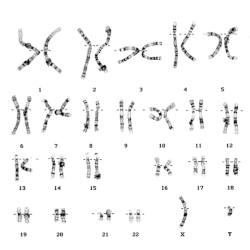
De acordo com Clark Spencer Larsen, o Homo sapiens moderno mostra uma gama de dimorfismo sexual, com massa corporal média entre os sexos diferindo em aproximadamente 15%.[8] De acordo com Daly e Wilson, "Os sexos diferem mais nos seres humanos do que nos mamíferos monogâmicos, mas muito menos do que nos mamíferos extremamente polígamos".[9]
Os seres humanos exibem dimorfismo sexual em muitas características, muitas não apresentam nenhuma ligação direta com a habilidade reprodutiva, porém a maioria destas características têm um papel na atração sexual. O dimorfismo sexual em seres humanos se observa sobretudo por cinco fatores ao nascer: a presença ou ausência do cromossomo Y, o tipo de gônadas, hormônios sexuais, anatomia reprodutiva interna (como o útero nas fêmeas) e a genitália externa.[10]
No cérebro humano, foi observada uma diferença entre os sexos na transcrição do par de genes PCDH11X / Y exclusivo do Homo sapiens.[11]
Alguns estudos mostram que os primeiros hominidae eram muito dimórficos e que esta tendência se reduziu ao longo da evolução humana, sugerindo que os humanos se tornaram mais monógamos. Ao contrário por exemplo dos gorilas, que vivem em haréns com um único macho e várias fêmeas e que demostram um dimorfismo sexual muito maior (ver: homininae).[12]
Insetos

Os insetos apresentam uma grande variedade de dimorfismo sexual entre os táxons, incluindo tamanho, ornamentação e coloração.[13] O dimorfismo sexual de tamanho com predominância feminina observado em muitos táxons evoluiu apesar da intensa competição entre machos por parceiras.[14] Na alverneira-ruiva [en] (Osmia rufa), por exemplo, a fêmea é maior/mais larga que os machos, com os machos tendo 8–10 mm de tamanho e as fêmeas 10–12 mm.[15] Em Asterocampa celtis, as fêmeas são igualmente maiores que os machos.[16] A razão para o dimorfismo sexual deve-se ao tamanho da massa de provisão, em que as fêmeas consomem mais pólen do que os machos.[17]
Em algumas espécies, há evidências de dimorfismo masculino, mas parece ser para distinção de papéis. Isso é observado na espécie de abelha Macrotera portalis [en], na qual há uma morfologia de cabeça pequena, capaz de voar, e uma morfologia de cabeça grande, incapaz de voar, para os machos.[18] Anthidium manicatum também apresenta dimorfismo sexual com predominância masculina. A seleção por tamanho maior nos machos em vez das fêmeas nesta espécie pode ter resultado devido ao seu comportamento territorial agressivo e subsequente sucesso diferencial no acasalamento.[19] Outro exemplo é Lasioglossum hemichalceum [en], uma espécie de abelha do suor que apresenta dimorfismos físicos drásticos entre os descendentes machos.[20] Nem todo dimorfismo tem que ter uma diferença drástica entre os sexos. Andrena agilissima [en] é uma abelha mineira em que as fêmeas têm apenas uma cabeça ligeiramente maior do que os machos.[21]
Referências
- ↑ «Dictionary of Human Evolution and Biology». Human-biology.key-spot.ru. Consultado em 3 de novembro de 2017. Arquivado do original em 7 de novembro de 2017
- ↑ A. Johnsen, K. Delhey, S. Andersson & B. Kempenaers (2003). «Plumage colour in nestling blue tits: sexual dichromatism, condition dependence and genetic effects» (PDF). Proceedings of the Royal Society B. 270 (1521): 1263–1270. JSTOR 3558810. PMC 1691364
 . PMID 12816639. doi:10.1098/rspb.2003.2375
. PMID 12816639. doi:10.1098/rspb.2003.2375
- ↑ Bill Branch (1988). Bill Branch's Field Guide to the Snakes and Other Reptiles of Southern Africa. Cape Town: Struik. ISBN 978-0-86977-639-1
- ↑ Andersson 1994
- ↑ Amotz Zahavi (1975). «Mate selection – a selection for a handicap» (PDF). Journal of Theoretical Biology. 53 (1): 205–214. PMID 1195756. doi:10.1016/0022-5193(75)90111-3
- ↑ Renner, Susanne; Ricklefs, Robert E (1995). «Dioecy and its correlates in the flowering plants». Americal Journal of Botany. 82 (5): 596–606
- ↑ Romero, Gustavo; Nelson, Craig E. (1986). «Sexual Dimorphism in Catasetum Orchids: Forcible Pollen Emplacement and Male Flower Competition». Science. 232 (4757): 1538–1540. Bibcode:1986Sci...232.1538R. doi:10.1126/science.232.4757.1538
- ↑ Larsen CS (Agosto de 2003). «Equality for the sexes in human evolution? Early hominid sexual dimorphism and implications for mating systems and social behavior». Proceedings of the National Academy of Sciences of the United States of America. 100 (16): 9103–4. Bibcode:2003PNAS..100.9103L. PMC 170877
 . PMID 12886010. doi:10.1073/pnas.1633678100
. PMID 12886010. doi:10.1073/pnas.1633678100
- ↑ Daly M, Wilson M (1996). «Evolutionary psychology and marital conflict». In: Buss DM, Malamuth NM. Sex, Power, Conflict: Evolutionary and Feminist Perspectives. [S.l.]: Oxford University Press. p. 13. ISBN 978-0-19-510357-1
- ↑ Knox, David; Schacht, Caroline. Choices in Relationships: An Introduction to Marriage and the Family. 11 ed. Cengage Learning; 2011-10-10 [cited 17 June 2013]. ISBN 9781111833220. p. 64–66.
- ↑ Lopes, Alexandra M.; Ross, Norman; Close, James; Dagnall, Adam; Amorim, António; Crow, Timothy J. (1 de abril de 2006). «Inactivation status of PCDH11X: sexual dimorphisms in gene expression levels in brain». Human Genetics (em inglês). 119 (3): 267–275. ISSN 1432-1203. doi:10.1007/s00439-006-0134-0
- ↑ Principles of Human Evolution, by Roger Lewin, Robert Foley.
- ↑ Bonduriansky R (janeiro de 2007). «The evolution of condition-dependent sexual dimorphism». The American Naturalist. 169 (1): 9–19. Bibcode:2007ANat..169....9B. PMID 17206580. doi:10.1086/510214
- ↑ Barreto FS, Avise JC (Agosto de 2011). "The genetic mating system of a sea spider with male-biased sexual size dimorphism: evidence for paternity skew despite random mating success". Behavioral Ecology and Sociobiology. 65 (8): 1595–1604. Bibcode:2011BEcoS..65.1595B. doi:10.1007/s00265-011-1170-x. PMC 3134710. PMID 21874083.
- ↑ Gruber B, Eckel K, Everaars J, Dormann CF (30 de Junho de 2011). "On managing the red mason bee (Osmia bicornis) in apple orchards" (PDF). Apidologie. 42 (5) 564: 564–576. doi:10.1007/s13592-011-0059-z. ISSN 0044-8435. S2CID 22935710.
- ↑ "hackberry emperor – Asterocampa celtis (Boisduval & Leconte)". entnemdept.ufl.edu. Recuperado em 15 de novembro de 2017.
- ↑ Rust R, Torchio P, Trostle G (1989). "Late embryogenesis and immature development of Osmia rufa cornigera (Rossi) (Hymenoptera: Megachilidae)". Apidologie. 20 (4): 359–367. doi:10.1051/apido:19890408.
- ↑ Danforth B (1991). "The morphology and behavior of dimorphic males in Perdita portalis (Hymenoptera: Andrenidae)". Behavioral Ecology and Sociobiology. 29 (4): 235–247. Bibcode:1991BEcoS..29..235D. doi:10.1007/bf00163980. S2CID 37651908.
- ↑ Jaycox Elbert R (1967). "Territorial Behavior Among Males of Anthidium Bamngense". Journal of the Kansas Entomological Society. 40 (4): 565–570.
- ↑ Kukuk PF (1 de Outubro de 1996). "Male Dimorphism in Lasioglossum (Chilalictus) hemichalceum: The Role of Larval Nutrition". Journal of the Kansas Entomological Society. 69 (4): 147–157. JSTOR 25085712.
- ↑ Paxton RJ, Giovanetti M, Andrietti F, Scamoni E, Scanni B (1 de Outubro de 1999). "Mating in a communal bee, Andrena agilissima (Hymenoptera Andrenidae)". Ethology Ecology & Evolution. 11 (4): 371–382. Bibcode:1999EtEcE..11..371P. doi:10.1080/08927014.1999.9522820. ISSN 0394-9370.