Yersinia pestis
Yersinia pestis
| |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||
| Classificação científica | |||||||||||||||
| |||||||||||||||
| Nome binomial | |||||||||||||||
| Yersinia pestis (Lehmann & Neumann, 1896) | |||||||||||||||
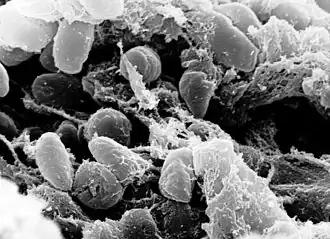
Yersinia pestis[1] (anteriormente denominada Pasteurella pestis) é um cocobacilo gram-negativo, em forma de bastonete, imóvel e sem esporos. É um organismo anaeróbico facultativo que pode infectar o ser humano por via da pulga Xenopsylla cheopis.[2] A bactéria é a causa da doença peste, que pode assumir uma de três formas: peste pulmonar, peste septicémica ou peste bubónica.[2][3][4]
Estas três formas foram responsáveis por diversas epidemias de elevada mortalidade ao longo da História, entre as quais a Praga de Justiniano , a Peste negra, que dizimou um terço da população europeia entre 1347 e 1353, e a Terceira Pandemia, com origem na China em 1855 e que matou cerca de 10 milhões de pessoas.[5][6][7][8][9] Estas pestes tiveram provavelmente origem na China, tendo sido transmitidas para a Europa através das rotas comerciais.[8][10] A Y. pestis foi descoberta em 1894 por Alexandre Yersin, um médico franco-suíço do Instituto Pasteur, durante uma epidemia de peste em Hong Kong.[11]
A Organização Mundial de Saúde reporta milhares de casos de peste todos os anos, embora hoje, com um tratamento adequado e rápido, o prognóstico das vítimas tenha melhorado muito. Durante a Guerra do Vietname os casos na Ásia aumentaram 5 ou 6 vezes, possivelmente devido à destruição dos ecossistemas e à maior proximidade entre humanos e animais. A peste tem também um efeito muito prejudicial sobre outros mamíferos (furões, cães-da-pradaria, etc.).
Características Gerais
E. pestis é um bacilo anaeróbico facultativo com um padrão de coloração bipolar (que lhe dá a aparência de um alfinete).[12] Semelhante a outros membros do género Yersinia, é negativo no teste da urease, fermentação da lactose e indol.[13] A especie máis próxima é o patóxeno gastrointestinal Yersinia pseudotuberculosis, e máis afastada está Yersinia enterocolitica.
Genoma
A sequência genómica completa de Y. pestis está disponível para duas das três subespécies de Y. pestis: estirpe KIM (de biovar Medievalis),[14] e estirpe CO92 (da biovar Orientalis, obtida a partir de um isolado clínico nos Estados Unidos).[15] Em 2006, foi concluída a sequenciação genómica da estirpe biovar Antiqua.[16] Tal como outras camadas patogénicas, existem sinais de mutações de perda de função. O cromossoma da camada KIM tem 4.600.755 pares de bases; o cromossoma da estirpe CO92 tem 4.653.728 pares de bases. Assim como os seus parentes próximos Y. pseudotuberculosis e Y. enterocolitica, Y. pestis contém o plasmídeo pCD1. Além disso, contém dois outros plasmídeos, o pPCP1 (também designado por pPla ou pPst) e o pMT1 (também designado por pFra), que não estão presentes noutras espécies de Yersinia. O plasmídeo pFra codifica a fosfolipase D, que é importante para a capacidade do Y. pestis para ser transmitido por pulgas.[17] O pPla codifica uma protease, o Pla, que activa o plasminogénio nos hospedeiros humanos e é um factor de virulência muito importante na peste pneumónica.[18] Juntamente com estes plasmídeos e uma ilha de patogenicidade denominada HPI, o genoma também codifica várias proteínas que causam a patogénese, que são muito características do Y. praga. Entre outras coisas, estes fatores de virulência são necessários para a adesão bacteriana e injeção de proteínas na célula hospedeira, invasão bacteriana da célula hospedeira (através do sistema de secreção tipo III) e para a absorção e ligação do ferro dos glóbulos vermelhos (através de sideróforos).
E. Acredita-se que Y. pestis seja descendente de Y. pseudotuberculosis, da qual difere apenas pela presença de plasmídeos de virulência específicos.
Em 2006, foi realizada uma análise proteómica abrangente e comparativa da estirpe KIM de Y. praga.[19] A análise centrou-se no momento da transição para o crescimento semelhante ao crescimento nas células hospedeiras.
Patogénese e imunidade

Nos ciclos urbano e florestal (selvagem) do Y. pestis, a maioria das transmissões ocorre entre roedores e pulgas. No ciclo da selva, são roedores selvagens, mas, no ciclo urbano, os roedores são domésticos (vivem em casas). Além das pulgas, os animais infetados podem transmitir a infeção aos humanos através do contacto com tecido epitelial. Os humanos também podem transmitir a bactéria uns aos outros através de espirros, tosse ou contacto direto com tecido infetado.
Nos hospedeiros do reservatório
Os reservatórios de Y. pestis são várias espécies de roedores. Nas estepes, pensa-se que as espécies reservatório são maioritariamente marmotas. Na América do Norte, pensa-se que várias espécies de roedores são reservatórios de Y. praga. No entanto, a dinâmica esperada da doença não foi observada em nenhuma espécie de roedor, e sabe-se que estas populações de roedores têm uma resistência variável à bactéria, tornando alguns indivíduos suscetíveis e outros portadores assintomáticos.[20] Existem evidências de que as pulgas de outros mamíferos também desempenham um papel nas epidemias de peste humana.[21]
Esta falta de conhecimento sobre a dinâmica da peste em espécies de mamíferos também ocorre entre roedores suscetíveis, como os cães-da-pradaria-de-cauda-preta (Cynomys ludovicianus), nos quais a peste pode provocar o colapso de toda a colónia, causando um efeito maciço na teia alimentar de que fazem parte.[22] No entanto, a dinâmica de transmissão nos cães-da-pradaria parece não depender de pulgas com o trato digestivo obstruído, mas sim de cadáveres, pulgas desobstruídas ou outros vetores.[23]
Noutras regiões do mundo, o reservatório de infecção não está claramente identificado, o que complica os programas de prevenção e alerta precoce. Um exemplo é a epidemia de 2003 na Argélia.[24]
Vector
A transmissão de Y. pestis pelas pulgas está bem caracterizada.[25] A transmissão inicial do Y. pestis pelo vetor ocorre durante a alimentação. Várias proteínas contribuem para a manutenção das bactérias no trato digestivo da pulga, incluindo o sistema de armazenamento hemina (Hms) e a toxina murina Yersinia (Ymt).
Embora a toxina murina da Yersinia seja muito tóxica para os roedores e se acreditasse anteriormente que era produzida para garantir a reinfeção de novos hospedeiros, o que foi demonstrado é que a Ymt é importante para a sobrevivência da Y. pestis em pulgas.[17]
O sistema Hms desempenha um papel importante na transmissão do Y. pestis para o hospedeiro mamífero.[26] Enquanto que no inseto vetor, as proteínas codificadas pelos loci genéticos Hms induzem a formação de biofilmes no proventrículo, uma válvula que liga o intestino médio ao esófago do inseto.[27] A agregação no biofilme impede a alimentação, pois forma-se uma massa de sangue coagulado e bactérias ingeridas (denominada "bloco de Bacot").[28]) A transmissão do Y. pestis ocorre durante as tentativas inúteis da pulga se alimentar de sangue que não consegue engolir. O sangue ingerido é bombeado para o esófago, onde remove algumas das bactérias que formam o tampão proventrículo, e o sangue com as bactérias é regurgitado na ferida da mordedura do hospedeiro, e as bactérias passam para o seu sistema circulatório. Como as pulgas não se conseguem alimentar, ficam com fome e picam com mais frequência.
Em humanos e outros hospedeiros suscetíveis
A patogénese devido à infecção com Y. pestis dos hospedeiros mamíferos é produzido por vários fatores, como a capacidade da bactéria suprimir e evitar respostas normais do sistema imunitário, como a fagocitose e a produção de anticorpos. A picada da pulga permite que a bactéria ultrapasse a barreira da pele. E. pestis expressa o produto do gene yadBC, que é semelhante às adesina de outras espécies de Yersinia, facilitando a adesão e a invasão das células epiteliais.[29] E. pestis expressa um ativador de plasminogénio que é um importante fator de virulência para a peste pneumónica e que pode degradar a coágulos sanguíneos para facilitar a invasão sistémica.[18] Muitos dos fatores de virulência das bactérias são antifagocíticos. Dois antigénios antifagocíticos importantes, designados por F1 (Fracção 1) e V ou LcrV, são importantes para a virulência.[12] Estes antigénios são produzidos pelas bactérias à temperatura normal do corpo humano. Além disso, Y. pestis sobrevive e produz antigénios F1 e V no interior dos glóbulos brancos, como os monócitos, mas não nos neutrófilos. A imunidade natural ou induzida é conseguida pela produção de anticorpos opsonínicos específicos contra os antigénios F1 e V; anticorpos contra F1 e V induzem fagocitose pelos neutrófilos.[30]
Além disso, o tipo III (T3SS) permite que o Y. pestis injecta proteínas nos macrófagos e noutras células imunes. Estas proteínas injetadas pelo T3SS são designadas por Yops (Yersinia Outer Proteins) e entre elas está a Yop B/D, que forma poros na membrana plasmática do hospedeiro e tem sido associada à citólise. YopO, YopH, YopM, YopT, YopJ e YopE são injetados no citoplasma da célula hospedeira pelo T3SS através de poros criados em parte por YopB e YopD.[31] As proteínas Yop injetadas limitam a fagocitose e as vias de sinalização celular importantes para o sistema imunitário inato. Além disso, algumas estirpes de Y. pestis são capazes de interferir com a sinalização imunitária (por exemplo, impedindo a libertação de algumas citocinas).
A Yersinia pestis prolifera no interior dos linfonodos, onde pode evitar a destruição por células imunitárias, como os macrófagos. A capacidade de Y. A capacidade do pestis de inibir a fagocitose permite-lhe crescer nos gânglios linfáticos e causar linfadenopatias. A YopH é uma proteína tirosina fosfatase que contribui para esta capacidade de Y. pestis para escapar à ação das células imunes.[32] Nos macrófagos, a YopH desfosforila p130Cas, Fyb (proteína de ligação Fyn) SKAP-HOM, e Pyk, uma tirosina quinase homóloga da FAK. O YopH liga-se também à subunidade p85 da fosfoinositídeo 3-quinase, Gab1, às proteínas adaptadoras Gab2 e ao fator de troca de nucleótidos guanina Vav.
A YopE funciona como uma proteína ativadora da GTPase para os membros da família Rho de GTPases como a RAC1. A YopT é uma cisteína-protease que inibe a RhoA removendo o grupo isoprenil, que é importante para a localização da proteína na membrana plasmática. Foi proposto que YopE e YopT podem funcionar limitando a citólise induzida por YopB/D.[33] Isto poderia limitar a função do YopB/D de criar os poros utilizados para a inserção do Yop nas células do hospedeiro e impedir a rutura das células do hospedeiro induzida pelo YopB/D e a libertação de conteúdo celular, o que atrairia e estimularia as respostas imunitárias.
Imunidade
Não existem vacinas eficazes contra a doença. Algumas vacinas foram utilizadas com pouca eficácia e que poderiam causar inflamações graves, como a vacina inativada com formaldeído, que já não é utilizada. Estão a ser realizadas experiências com técnicas de engenharia genética para vacinas baseadas nos antigénios F1 e V e parecem promissoras. No entanto, as bactérias sem o antigénio F1 permanecem virulentas, e os antigénios V são suficientemente variáveis para que uma vacina composta por eles não seja totalmente protetora.[34][35][36]
Aspectos clínicos
Sintomas e progressão da doença
- Peste bubónica
- Período de incubação de 2 a 6 dias, quando a bactéria está a replicar ativamente.
- Mal-estar geral
- Febre
- Dor de cabeça e arrepios que surgem subitamente no final do período de incubação
- Inchaço dos gânglios linfáticos que dão origem aos bubões, especialmente nas virilhas, que é o sintoma clássico da peste bubónica.
- Praga septicémica
- Hipotensão
- Hepatoesplenomegalia
- Delírio
- Convulsões em crianças
- Choque
- Mal-estar geral
- Febre
- Os sintomas das pestes bubónica e pneumónica nem sempre estão presentes
- Nota: O doente pode morrer antes que surja qualquer sintoma
- Peste pneumónica (transmitida de pessoa para pessoa)
A peste pneumónica pode ocorrer por inalação de aerossóis com a bactéria (primária) ou pode atingir os pulmões através do sangue (secundária). Como a bactéria é transportada no sangue, vários órgãos podem ser afetados, como o baço e o cérebro. A infeção difusa pode causar uma cascata imunológica que resulta em coagulação intravascular disseminada, que por sua vez produz hemorragias e necrose na pele e nos tecidos. Uma infecção disseminada deste tipo aumenta a mortalidade para 22%. A pneumonia progride em 2 a 4 dias e, se o tratamento precoce não for iniciado, os doentes podem morrer em apenas 36 horas.
Com excepção dos bubões, os sintomas iniciais da peste são muito semelhantes aos de muitas outras doenças, dificultando o diagnóstico.[38]
OMS Os códigos CID-9 para as doenças causadas por Y. peste:
- 020.0 Peste bubónica
- 020.2 Peste septicémica
- 020.5 Peste pneumónica inespecífica
- 020.3 Peste pneumónica primária
- 020.4 Peste pneumónica secundária.
Determinação clínica
A coloração de Gram pode confirmar a presença de bacilos gram-negativos e, em alguns casos, a identificação de formas duplamente curvadas. Um teste serológico anti-F1 pode diferenciar entre diferentes espécies de Yersinia, e a reação em cadeia da polimerase (PCR) pode ser utilizada para identificar Y. praga.
A proteína H da fibra da cauda do bacteriófago fago Yersinia L-413C permite a diferenciação entre Y. pestis e Y. pseudotuberculose.[39]
Tratamento
O tratamento tradicional de primeira linha contra o Y. pestis são os antibióticos estreptomicina,[40][41] cloranfenicol, tetraciclina,[42] e as fluoroquinolonas. Existem também boas evidências que suportam o uso de doxiciclina ou gentamicina.[43] Foram isoladas estirpes resistentes, pelo que o tratamento deve ser orientado pela sensibilidade aos antibióticos sempre que possível. O tratamento com antibióticos por si só é insuficiente para alguns doentes, que podem também necessitar de suporte circulatório, respiratório ou renal.[44]
Referências
- ↑ Sutyak, Katya. "Yersinia Pestis." University of Connecticut, 10 Nov. 2015.
- ↑ a b Ryan KJ, Ray CG, eds. (2004). Sherris Medical Microbiology 4th ed. [S.l.]: McGraw Hill. pp. 484–488. ISBN 0-8385-8529-9
- ↑ http://hisz.rsoe.hu/alertmap/site/index.php?pageid=event_desc&edis_id=BH-20150621-48754-USA
- ↑ CDC https://www.cdc.gov/plague/
- ↑ Austin Alchon, Suzanne (2003). A pest in the land: new world epidemics in a global perspective. [S.l.]: University of New Mexico Press. p. 21. ISBN 0-8263-2871-7
- ↑ Harbeck, Michaela; Seifert, Lisa; Hänsch, Stephanie; Wagner, David M.; Birdsell, Dawn; Parise, Katy L.; Wiechmann, Ingrid; Grupe, Gisela; Thomas, Astrid; Keim, Paul; Zöller, Lothar; Bramanti, Barbara; Riehm, Julia M.; Scholz, Holger C. (2013). «Yersinia pestis DNA from Skeletal Remains from the 6th Century AD Reveals Insights into Justinianic Plague | Science. New SeriesPLoS Pathogens». 9 (5): e1003349. PMC 3642051
 . PMID 23658525. doi:10.1371/journal.ppat.1003349. Resumo divulgativo – ScienceDaily
. PMID 23658525. doi:10.1371/journal.ppat.1003349. Resumo divulgativo – ScienceDaily
- ↑ Carter, Adam (27 de janeiro de 2014). «Black Death mysteries unlocked by McMaster scientists». CBC News
- ↑ a b Nicholas Wade (31 de outubro de 2010). «Europe's Plagues Came From China, Study Finds». New York Times. Consultado em 1 de novembro de 2010
- ↑ «Plague Helped Bring Down Roman Empire : DNews». DNews. Consultado em 28 de junho de 2013 (em inglês)
- ↑ Morelli, G.; Song, Y.; Mazzoni, C.J.; Eppinger, M.; Roumagnac, P.; Wagner, D.M.; Feldkamp, M.; Kusecek, B.; Vogler, A.J.; Li, Y.; Cui, Y.; Thomson, N.R.; Jombart, T.; Leblois, R.; Lichtner, P.; Rahalison, L.; Petersen, J.M.; Balloux, F.; Keim, Pl; Wirth, T.; Ravel, J.; Yang, R.; Carniel, E.; Achtman, M. (dezembro de 2010). «Yersinia pestis genome sequencing identifies patterns of global phylogenetic diversity». Nature Genetics. 42 (12): 1140–1143. PMC 2999892
 . PMID 21037571. doi:10.1038/ng.705
. PMID 21037571. doi:10.1038/ng.705
- ↑ Bockemühl J (1994). «100 years after the discovery of the plague-causing agent – importance and veneration of Alexandre Yersin in Vietnam today». Immun Infekt. 22 (2): 72–75. PMID 7959865
- ↑ a b Collins FM (1996). Pasteurella, Yersinia, and Francisella. In: Baron's Medical Microbiology (Baron S et al, eds.) 4th ed. [S.l.]: Univ. of Texas Medical Branch. ISBN 0-9631172-1-1
- ↑ Stackebrandt, Erko; Dworkin, Martin; Falkow, Stanley; Rosenberg, Eugene; Karl-Heinz Schleifer (2005). The Prokaryotes: A Handbook on the Biology of Bacteria:Volume 6: Proteobacteria: Gamma Subclass. Berlin: Springer. ISBN 0-387-25499-4
- ↑ Deng W; et al. (2002). «Genome Sequence of Yersinia pestis KIM». Journal of Bacteriology. 184 (16): 4601–4611. PMC 135232
 . PMID 12142430. doi:10.1128/JB.184.16.4601-4611.2002
. PMID 12142430. doi:10.1128/JB.184.16.4601-4611.2002
- ↑ Parkhill J; et al. (2001). «Genome sequence of Yersinia pestis, the causative agent of plague». Nature. 413 (6855): 523–527. PMID 11586360. doi:10.1038/35097083
- ↑ Chain PS; Hu P; Malfatti SA; et al. (2006). «Complete Genome Sequence of Yersinia pestis Strains Antiqua and Nepal516: Evidence of Gene Reduction in an Emerging Pathogen». J. Bacteriol. 188 (12): 4453–63. PMC 1482938
 . PMID 16740952. doi:10.1128/JB.00124-06
. PMID 16740952. doi:10.1128/JB.00124-06
- ↑ a b Hinnebusch BJ, Rudolph AE, Cherepanov P, Dixon JE, Schwan TG, Forsberg A (2002). «Role of Yersinia murine toxin in survival of Yersinia pestis in the midgut of the flea vector». Science. 296 (5568): 733–5. PMID 11976454. doi:10.1126/science.1069972
- ↑ a b Lathem WW, Price PA, Miller VL, Goldman WE (2007). «A plasminogen-activating protease specifically controls the development of primary pneumonic plague». Science. 315 (5811): 509–13. PMID 17255510. doi:10.1126/science.1137195
- ↑ Hixson K; et al. (2006). «Biomarker candidate identification in Yersinia pestis using organism-wide semiquantitative proteomics». Journal of Proteome Research. 5 (11): 3008–3017. PMID 16684765. doi:10.1021/pr060179y
- ↑ MEYER KF (1957). «The natural history of plague and psittacosis: The R. E. Dyer Lecture». Public Health Rep. 72 (8): 705–19. PMC 2031327
 . PMID 13453634. doi:10.2307/4589874
. PMID 13453634. doi:10.2307/4589874
- ↑ von Reyn CF; Weber NS; Tempest B; et al. (1977). «Epidemiologic and clinical features of an outbreak of bubonic plague in New Mexico». J. Infect. Dis. 136 (4): 489–94. PMID 908848. doi:10.1093/infdis/136.4.489
- ↑ Pauli JN, Buskirk SW, Williams ES, Edwards WH (2006). «A plague epizootic in the black-tailed prairie dog (Cynomys ludovicianus)». J. Wildl. Dis. 42 (1): 74–80. PMID 16699150
- ↑ Webb CT, Brooks CP, Gage KL, Antolin MF (2006). «Classic flea-borne transmission does not drive plague epizootics in prairie dogs». Proc. Natl. Acad. Sci. U.S.A. 103 (16): 6236–41. PMC 1434514
 . PMID 16603630. doi:10.1073/pnas.0510090103
. PMID 16603630. doi:10.1073/pnas.0510090103
- ↑ Bertherat E; Bekhoucha S; Chougrani S; et al. (2007). «Plague Reappearance in Algeria after 50 Years, 2003». Emerging Infect. Dis. 13 (10): 1459–1462. PMC 2851531
 . PMID 18257987
. PMID 18257987
- ↑ Zhou D, Han Y, Yang R (2006). «Molecular and physiological insights into plague transmission, virulence and etiology». Microbes Infect. 8 (1): 273–84. PMID 16182593. doi:10.1016/j.micinf.2005.06.006
- ↑ B.J. Hinnebusch, R.D. Perry and T.G. Schwan (1996). «Role of the Yersinia pestis hemin storage (hms) locus in the transmission of plague by fleas». Science. 273 (5237): 367–70. PMID 8662526. doi:10.1126/science.273.5273.367
- ↑ Erickson, D. L., N. R. Waterfield, V. Vadyvaloo, D. Long, E. R. Fischer, R. ffrench-Constant, and B. J. Hinnebusch (2007). «Acute oral toxicity of yersinia pseudotuberculosis to fleas: Implications for the evolution of vector-borne transmission of plague». Cellular Microbiology. 9 (11): 2658–2666. PMID 17587333. doi:10.1111/j.1462-5822.2007.00986.x
- ↑ Pepper, C., M. Nascarella, E. Marsland, J. Montford, L. Wood, S. Cox, C. Bradford, T. Burns, and S. Presley. 2004. Threatened or endangered? Keystone species or public health threat? The black-tailed prairie dog, the Endangered Species Act, and the imminent threat of bubonic plague. Journal of Land, Resources, and Environmental Law 24: 355-391.
- ↑ Forman S, Wulff CR, Myers-Morales T, Cowan C, Perry RD, Straley SC (2008). «yadBC of Yersinia pestis, a New Virulence Determinant for Bubonic Plague». Infect. Immun. 76 (2): 578–87. PMC 2223446
 . PMID 18025093. doi:10.1128/IAI.00219-07
. PMID 18025093. doi:10.1128/IAI.00219-07
- ↑ Salyers AA, Whitt DD (2002). Bacterial Pathogenesis: A Molecular Approach 2nd ed. [S.l.]: ASM Press. pp. 207-12
- ↑ Viboud GI, Bliska JB (2005). «Yersinia outer proteins: role in modulation of host cell signaling responses and pathogenesis». Annu. Rev. Microbiol. 59: 69–89. PMID 15847602. doi:10.1146/annurev.micro.59.030804.121320
- ↑ de la Puerta ML, Trinidad AG, del Carmen Rodríguez M, Bogetz J, Sánchez Crespo M, Mustelin T, Alonso A, Bayón Y (2009). Bozza, Patricia, ed. «Characterization of New Substrates Targeted By Yersinia Tyrosine Phosphatase YopH». PLoS ONE. 4 (2): e4431. PMC 2637541
 . PMID 19221593. doi:10.1371/journal.pone.0004431
. PMID 19221593. doi:10.1371/journal.pone.0004431
- ↑ Mejía E, Bliska JB, Viboud GI (2009). «Yersinia Controls Type III Effector Delivery into Host Cells by Modulating Rho Activity». PLoS ONE. 4 (2): e4431. PMC 2186360
 . PMID 18193942. doi:10.1371/journal.ppat.0040003
. PMID 18193942. doi:10.1371/journal.ppat.0040003
- ↑ Welkos S; et al. (2002). «Determination of the virulence of the pigmentation-deficient and pigmentation-/plasminogen activator-deficient strains of Yersinia pestis in non-human primate and mouse models of pneumonic plague». Vaccine. 20 (17–18): 2206–2214. PMID 12009274. doi:10.1016/S0264-410X(02)00119-6
- ↑ Pitt ML (14 de outubro de 2004). «Non-human primates as a model for pneumonic plague. In: Animals Models and Correlates of Protection for Plague Vaccines Workshop» (PDF). Consultado em 26 de julho de 2013. Cópia arquivada (PDF) em 21 de fevereiro de 2006
- ↑ Jefferson T, Demicheli V, Pratt M (2000). «Vaccines for preventing plague». Cochrane Database Syst Rev (2): CD000976. PMID 10796565. doi:10.1002/14651858.CD000976
- ↑ Informação retirada de "Harrison's Principles of Internal Medicine 16th Edition"
- ↑ Prentice MB, Rahalison L (2007). «Praga». 369 9568 ed. Lancet. pp. 1196–207. PMID 17416264. doi:10.1016/S0140-6736(07)60566-2
- ↑ Garcia, E; Chain, P; Elliott, JM; Bobrov, AG; Motin, VL; Kirillina, O; Lao, V; Calendar, R; Filippov, AA (2008). «Molecular characterization of L-413C, a P2-related plague diagnostic bacteriophage». Virology. 372 (1): 85–96. PMID 18045639. doi:10.1016/j.virol.2007.10.032
- ↑ Wagle PM. (1948). «Recent advances in the treatment of bubonic plague». Indian J Med Sci. 2: 489–94
- ↑ Meyer KF. (1950). «Modern therapy of plague». JAMA. 144 (12): 982–5. PMID 14774219
- ↑ Kilonzo BS, Makundi RH, Mbise TJ. (1992). «A decade of plague epidemiology and control in the Western Usambara mountains, north-east Tanzania». Acta Tropica. 50 (4): 323–9. PMID 1356303. doi:10.1016/0001-706X(92)90067-8
- ↑ Mwengee W; Butler T; Mgema S; et al. (2006). «Treatment of plague with gentamicin or doxycycline in a randomized clinical trial in Tanzania». Clin Infect Dis. 42 (5): 614–21. PMID 16447105. doi:10.1086/500137
- ↑ Jameson, J. N. St C.; Dennis L. Kasper; Harrison, Tinsley Randolph; Braunwald, Eugene; Fauci, Anthony S.; Hauser, Stephen L; Longo, Dan L. (2005). Harrison's principles of internal medicine. New York: McGraw-Hill Medical Publishing Division. ISBN 0-07-140235-7