Trímero de proteína

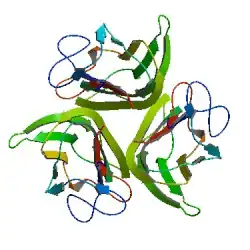
Em bioquímica, um trímero de proteína é um complexo macromolecular formado por três macromoléculas, geralmente ligadas de forma não covalente, como proteínas ou ácidos nucleicos. Um trímero de proteína geralmente ocorre a partir da montagem da estrutura quaternária de uma proteína.[1] As interações não covalentes entre as regiões hidrofóbicas e hidrofílicas nas unidades polipeptídicas ajudam a estabilizar a estrutura quaternária. Como um trímero de proteína é composto de múltiplas subunidades polipeptídicas, ele é considerado um oligômero.[2]
Um homotrímero seria formado por três moléculas idênticas.[3] Um heterotrímero seria formado por três macromoléculas diferentes. O colágeno tipo II é um exemplo de proteína homotrimérica, enquanto o colágeno tipo I é uma proteína heterotrimérica do tipo AAB.[4]
As porinas geralmente se organizam em membranas como trímeros.[5]
Fibra da cauda do bacteriófago T4
Várias cópias de um polipeptídeo codificado por um gene geralmente podem formar um agregado denominado multímero.[6] Quando um multímero é formado a partir de polipeptídeos produzidos por dois alelos mutantes diferentes de um gene específico, o multímero misto pode exibir maior atividade funcional do que os multímeros não misturados formados por cada um dos mutantes isoladamente. Quando um multímero misto apresenta maior funcionalidade em relação aos multímeros não misturados, o fenômeno é chamado de complementação intragênica. A porção distal de cada uma das fibras da cauda do bacteriófago T4 é codificada pelo gene 37 e os mutantes defeituosos neste gene sofrem complementação intragênica.[7]
Essa descoberta indicou que as fibras distais da cauda são um multímero do polipeptídeo codificado pelo gene 37. Uma análise dos dados de complementação indicou ainda que os polipeptídeos que compõem o multímero foram dobrados sobre si mesmos na forma de um grampo de cabelo. Uma análise adicional da estrutura cristalina de alta resolução da fibra da cauda distal indicou que os polipeptídeos do gene 37 estão presentes como um trímero e que cada polipeptídeo do trímero é dobrado sobre si mesmo em uma configuração de grampo de cabelo.[8]
Ver também
Notas
- Este artigo foi inicialmente traduzido, total ou parcialmente, do artigo da Wikipédia em inglês cujo título é «Protein trimer».
Referências
- ↑ Godbey, W.T. (2014), «Proteins», ISBN 978-1-907568-28-2, Elsevier, An Introduction to Biotechnology: 9–33, doi:10.1016/b978-1-907568-28-2.00002-2, consultado em 3 de maio de 2024
- ↑ Pelley, John W. (1 de janeiro de 2012), Pelley, John W., ed., «3 - Protein Structure and Function», ISBN 978-0-323-07446-9, Philadelphia: W.B. Saunders, Elsevier's Integrated Review Biochemistry (Second Edition): 19–28, doi:10.1016/b978-0-323-07446-9.00003-9, consultado em 3 de maio de 2024
- ↑ Cha, S.S.; et al. (1998). «High resolution crystal structure of a human tumor necrosis factor-alpha mutant with low systemic toxicity». J. Biol. Chem. 273 (4): 2153–60. PMID 9442056. doi:10.1074/jbc.273.4.2153

- ↑ Fallas, Jorge A.; Gauba, Varun; Hartgerink, Jeffrey D. (25 de setembro de 2009). «Solution Structure of an ABC Collagen Heterotrimer Reveals a Single-register Helix Stabilized by Electrostatic Interactions *». Journal of Biological Chemistry (em inglês) (39): 26851–26859. ISSN 0021-9258. PMC 2785373
 . PMID 19625247. doi:10.1074/jbc.M109.014753. Consultado em 3 de maio de 2025
. PMID 19625247. doi:10.1074/jbc.M109.014753. Consultado em 3 de maio de 2025
- ↑ Heldt, Hans-Walter; Piechulla, Birgit (1 de janeiro de 2021). Heldt, Hans-Walter; Piechulla, Birgit, eds. «Chapter 1 - Leaf Cells Consist of Several Metabolic Compartments». Academic Press: 1–41. ISBN 978-0-12-818631-2. Consultado em 3 de maio de 2025
- ↑ Crick, F. H. C.; Orgel, L. E. (1 de janeiro de 1964). «The theory of inter-allelic complementation». Journal of Molecular Biology (1): 161–165. ISSN 0022-2836. doi:10.1016/S0022-2836(64)80156-X. Consultado em 3 de maio de 2025
- ↑ Bernstein, H.; Edgar, R. S.; Denhardt, G. H. (junho de 1965). «INTRAGENIC COMPLEMENTATION AMONG TEMPERATURE SENSITIVE MUTANTS OF BACTERIOPHAGE T4D». Genetics (6): 987–1002. ISSN 0016-6731. PMC 1210828
 . PMID 14337770. doi:10.1093/genetics/51.6.987. Consultado em 3 de maio de 2025
. PMID 14337770. doi:10.1093/genetics/51.6.987. Consultado em 3 de maio de 2025
- ↑ Bartual, Sergio G.; Otero, José M.; Garcia-Doval, Carmela; Llamas-Saiz, Antonio L.; Kahn, Richard; Fox, Gavin C.; van Raaij, Mark J. (23 de novembro de 2010). «Structure of the bacteriophage T4 long tail fiber receptor-binding tip». Proceedings of the National Academy of Sciences (em inglês) (47): 20287–20292. ISSN 0027-8424. PMC 2996694
 . PMID 21041684. doi:10.1073/pnas.1011218107. Consultado em 3 de maio de 2025
. PMID 21041684. doi:10.1073/pnas.1011218107. Consultado em 3 de maio de 2025