Porina
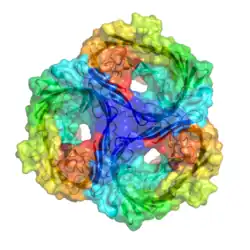
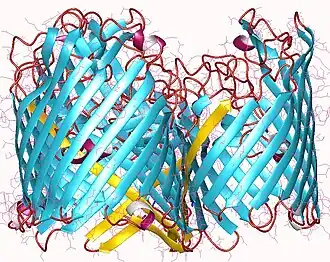
As porinas são proteínas com estrutura de barril beta que abrangem toda a espessura de uma membrana celular e funcionam como um poro através do qual pode ocorrer a difusão passiva de certas moléculas.[1][2] Ao contrário de outras proteínas de transporte membranar, as porinas são grandes o suficiente para permitir a difusão passiva através delas, ou seja, atuam como canais que são específicos para diferentes tipos de moléculas. Estão presentes na membrana externa das bactérias Gram-negativas e também em algumas Gram-positivas do grupo Mycolata (actinomicetos que contêm ácido micólico), nas mitocôndrias e nos cloroplastos.
A descoberta das porinas foi atribuída a Hiroshi Nikaido, a quem foi dado o apelido de "o porinólogo".[3]
Estrutura
As porinas são compostas por cadeias β, que estão, geralmente, ligadas por voltas beta no lado citoplasmático e por longos laços de aminoácidos no outro. As cadeias β dispõem-se de modo antiparalelo e formam um tubo cilíndrico, chamado barril β.[4] A composição de aminoácidos das cadeias β das porinas é peculiar, pois os resíduos de aminoácidos polares e não polares são alternantes. Isto significa que os resíduos não polares ficam virados para fora e interagem com a membrana lipídica apolar, enquanto os resíduos polares estão orientados para dentro, voltados para o interior do barril beta, para interagirem com o canal aquoso.
O canal da porina está parcialmente bloqueado por um laço (o olho do poro), que se projeta para dentro da cavidade. Em geral, encontra-se entre as cadeias 5 e 6 de cada barril, e define o tamanho dos solutos que podem atravessar o canal. Está revestido quase exclusivamente por aminoácidos carregados, dispostos a cada lado do canal, criando um campo elétrico transversal através do poro. O olho do poro tem um excedente local de cargas negativas por ter quatro resíduos de ácido glutâmico e sete de ácido aspártico (juntamente com um resíduo de histidina, duas lisinas e três argininas, que não o compensam), e é parcialmente compensado pela ligação de dois iões cálcio. Pensa-se que esta disposição assimétrica da molécula influencia a seleção das moléculas que podem passar através do canal.[5]
Funções celulares
Nas bactérias Gram-negativas, a membrana interna é a principal barreira de permeabilidade, enquanto a membrana externa contém porinas, que a tornam muito permeável a moléculas de aproximadamente 1500 daltons. As moléculas de tamanho médio ou carregadas que necessitam de ser transportadas através da membrana movem-se através das porinas.
As porinas controlam tipicamente a difusão de pequenos metabolitos como açúcares, iões e aminoácidos.
As porinas são quimicamente seletivas, transportando apenas um grupo de compostos (por exemplo, carboidratos[6]), ou podem mesmo ser específicas para um único composto[7]. Os antibióticos beta-lactâmicos e a fluoroquinolona devem passar através das porinas para atingir os seus alvos nas bactérias Gram-negativas[8][9]. As bactérias podem desenvolver resistência a estes antibióticos através de mutações no Gene que codifica as porinas.
Outras "porinas"
Existem outras proteínas que formam poros ou canais nas membranas que contêm o nome porina, mas que são completamente distintas. As nucleoporinas são proteínas que facilitam o transporte através dos poros nucleares do envoltório nuclear eucariota, sendo, portanto, distintas das porinas de tipo bacteriano e classificadas separadamente. As aquaporinas são outro tipo de proteínas que formam canais aquosos nas membranas das células, também totalmente diferentes das bacterianas, com uma estrutura formada por hélices alfa.
Referências
- ↑ B. K. Jap and P. J. Walian. Structure and functional mechanism of porins. APS. Phisiological Reviews. [1] Arquivado em 2016-04-04 no Wayback Machine
- ↑ MeshName - Porins
- ↑ Klebba PE (2005). «The porinologist». Journal of Bacteriology. 187 (24): 8232–6. PMC 1317029
 . PMID 16321927. doi:10.1128/JB.187.24.8232-8236.2005
. PMID 16321927. doi:10.1128/JB.187.24.8232-8236.2005
- ↑ Schirmer T (1998). «General and specific porins from bacterial outer membranes». Journal of Structural Biology. 121 (2): 101–9. PMID 9615433. doi:10.1006/jsbi.1997.3946
- ↑ Branden and Tooze, Introduction to Protein Structure, second edition
- ↑ EMBL-EBI. Carbohydrate-selective porin OprB (IPR007049)
- ↑ Transporter classification database
- ↑ Pagès, Jean-Marie; James, Chloë E.; Winterhalter, Mathias (dezembro de 2008). «The porin and the permeating antibiotic: a selective diffusion barrier in Gram-negative bacteria». Nature Reviews Microbiology (em inglês). 6 (12): 893–903. ISSN 1740-1526. doi:10.1038/nrmicro1994
- ↑ Jean-Marie Pagès, Chloë E. James & Mathias Winterhalter. The porin and the permeating antibiotic: a selective diffusion barrier in Gram-negative bacteria. Nature Reviews Microbiology 6, 893-903 (dezembro de 2008). doi:10.1038/nrmicro1994. [2]