Lumiracoxib
Lumiracoxib
| |
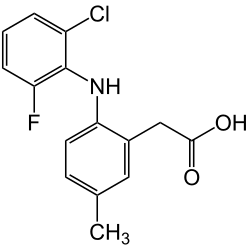 | |
Nome IUPAC (sistemática)
| |
| {2-[(2-chloro-6-fluorophenyl)amino]-5-methylphenyl} acetic acid | |
Identificadores
| |
| M01H06 | |
| 151166 | |
Informação química
| |
| 293,72 g/mol | |
Farmacocinética
| |
| 74% (oral) | |
| >98% | |
| 4 hours | |
| Renal e fecal | |
Considerações terapêuticas
| |
| per os | |
Lumiracoxib é um anti-inflamatório não estereoidal de classe coxib (anti-inflamatórios inibidores seletivos da COX-2), fabricada pela multinacional Novartis, que oferece além de uma potente eficácia analgésica e anti-inflamatória, diz-se que também disponibiliza segurança tanto gastrointestinal (reduzindo os problemas como úlceras e complicações) quanto cardiovascular (alteração dos níveis pressóricos) em relação a outros medicamentos do mesmo tipo.
Propriedades
Este medicamento, assim como os demais inibidores seletivos da COX-2, apesar da referência à redução de problemas gastrointestinais, pode causar problemas de estômago se tomado por prazos superiores a 4 dias ou dosagens superiores a 1 comprimido ao dia.
Indicações
- Artrite
- Osteoartrite
- Dismenorreia
- Cefaleia grave
- Entorses
- Cervicalgias
- Lombalgia
- Quadro inflamatório tanto a nível muscular quanto esquelético
Proibição de venda
No mês de julho de 2008, a Vigilância Sanitária do Estado de São Paulo fez a interdição de todos lotes do medicamento, sob alegação de reações adversas, cardiovasculares e hepática.[1] Precisamente no dia 22 de julho de 2008, a Anvisa, cancelou o registro do medicamento em todo o país. De julho de 2005 até abril de 2008 foram 3585 situações de reações adversas.[2]
Em 11 de agosto de 2007, a Austrália, proibiu sua comercialização pela morte de pacientes que usavam o medicamento. O FDA, não havia aprovado seu uso em humanos.
Ligações externas
Referências
- ↑ http://www.diariodecuiaba.com.br/detalhe.php?cod=322059
- ↑ «Cópia arquivada». Consultado em 24 de julho de 2008. Arquivado do original em 26 de julho de 2008