Nimesulida
Nimesulida
| |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||
| Nomes | |||||||||||||||||||
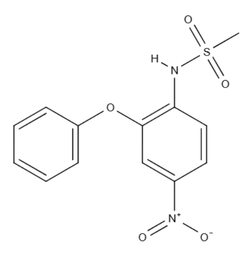
| Nome IUPAC | N-(4-Nitro-2-phenoxyphenyl)methanesulfonamide | ||||||||||||||||||
| |||||||||||||||||||
| |||||||||||||||||||
| |||||||||||||||||||
| Página de dados suplementares | |||||||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||||||
A Nimesulida é um fármaco anti-inflamatório não esteroide (AINE) pertencente à classe das sulfonanilidas. O medicamento apresenta propriedades anti-inflamatórias, antipiréticas (redução da febre) e analgésicas (alívio da dor).
Estudos comparativos indicam que a nimesulida possui atividade anti-inflamatória superior à do ácido acetilsalicílico, fenilbutazona e indometacina. Sua capacidade antipirética é equivalente à do diclofenaco e da dipirona (metamizol), sendo potencialmente superior à do acetaminofeno (paracetamol).[1]
Ela ocupa uma posição singular e controversa na farmacopeia moderna. Sua molécula distingue-se estrutural e farmacologicamente dos AINEs tradicionais, como os derivados do ácido propiônico (ibuprofeno, naproxeno) ou do ácido acético (diclofenaco), por apresentar um grupo funcional sulfonanilida em vez da função ácido carboxílico comum à maioria dos seus pares terapêuticos. Desde a sua introdução no mercado farmacêutico em 1985, a nimesulida ganhou rápida e vasta aceitação clínica em mais de 50 países, consolidando-se como uma ferramenta terapêutica de primeira linha para o tratamento de condições inflamatórias agudas, dor osteoarticular e dismenorreia primária, devido ao seu início de ação notavelmente rápido e potente atividade analgésica.[2]
O perfil farmacodinâmico da nimesulida é caracterizado por uma inibição preferencial da isoforma 2 da enzima ciclooxigenase (COX-2) em detrimento da ciclooxigenase-1 (COX-1). Esta seletividade relativa foi desenhada para maximizar a eficácia anti-inflamatória enquanto, teoricamente, minimizaria os efeitos adversos gastrointestinais decorrentes da supressão das prostaglandinas citoprotetoras geradas pela COX-1. Adicionalmente, a nimesulida exibe um mecanismo de ação multifatorial complexo, que transcende a simples inibição da síntese de prostaglandinas, atuando na modulação de radicais livres, na inibição da libertação de histamina e na proteção contra a degradação da cartilagem. [3][4]
Entretanto, a trajetória clínica da nimesulida tem sido marcada por um intenso escrutínio regulatório e científico. A emergência de relatos de hepatotoxicidade grave e idiossincrática,variando de elevações assintomáticas das enzimas hepáticas a hepatite fulminante requerendo transplante de fígado ou resultando em óbito, precipitou uma fragmentação no seu status global. Enquanto agências reguladoras em países como Espanha, Finlândia e Irlanda optaram pela retirada do medicamento do mercado, outras, como no Brasil, Itália e Índia, mantiveram a sua comercialização sob restrições rigorosas de dosagem e duração de tratamento.[5]
História e Desenvolvimento
A história da nimesulida é um reflexo da evolução do entendimento científico sobre a inflamação e reflete as mudanças nos paradigmas de segurança farmacêutica ao longo das últimas quatro décadas. O desenvolvimento da molécula não seguiu a rota tradicional de descoberta dos AINEs ácidos, emergindo, em vez disso, de pesquisas focadas em mecanismos antioxidantes e na química das sulfonanilidas.
A descoberta da nimesulida ocorreu nos laboratórios de pesquisa da Riker Laboratories, uma empresa farmacêutica inovadora sediada em Northridge, Califórnia. A Riker foi adquirida pelo conglomerado industrial 3M (Minnesota Mining and Manufacturing Company) em meados da década de 1960, tornando-se a divisão farmacêutica da empresa (posteriormente conhecida como 3M Pharmaceuticals).
No final dos anos 1960 e início dos anos 1970, o mecanismo exato de ação da aspirina e dos AINEs ainda não estava completamente elucidado, a descoberta fundamental de que estes fármacos inibem a biosíntese de prostaglandinas só seria publicada por Sir John Vane em 1971. Consequentemente, a pesquisa na Riker Laboratories, liderada pelo Dr. George G. I. Moore (químico medicinal e inventor principal), juntamente com o Dr. Karl F. Swingle (farmacologista) e o Dr. Robert Scherrer, baseava-se em hipóteses alternativas sobre a patogénese da inflamação.
A equipe científica postulava que os radicais livres de oxigénio desempenhavam um papel central na perpetuação da inflamação crónica e no dano tecidual. Assim, o objetivo primário não era necessariamente encontrar um inibidor da ciclooxigenase, mas sim identificar compostos capazes de neutralizar ou "varrer" (scavenge) estes radicais tóxicos. A classe química das sulfonanilidas foi selecionada para investigação devido a observações históricas de atividade antirreumática em compostos análogos. Através de uma extensa análise de relação estrutura-atividade (SAR), a equipe sintetizou e testou centenas de variantes, culminando na identificação do composto codificado como R-805, que viria a ser nomeado nimesulida.
A patente original da nimesulida (US Patent 3,840,597) foi concedida em 1974, protegendo a estrutura química das fenoximetanossulfonanilidas substituídas. O trabalho do Dr. Moore e sua equipe foi pioneiro ao introduzir um AINE que não dependia da função ácido carboxílico para a sua atividade, uma característica que influenciaria profundamente as propriedades físico-químicas e a tolerabilidade gástrica do fármaco.
Lançamento Comercial e Expansão Global
Apesar da descoberta nos Estados Unidos, a estratégia de desenvolvimento clínico e comercialização da nimesulida focou-se na Europa. A Helsinn Healthcare, uma empresa farmacêutica suíça, adquiriu os direitos de licenciamento e conduziu o desenvolvimento final do produto.
Em 1985, a nimesulida obteve a sua primeira autorização de introdução no mercado na Itália, sendo lançada sob as marcas Aulin e Mesulid. O sucesso na Itália foi imediato, impulsionado pela eficácia do fármaco e pela percepção de uma melhor tolerabilidade gástrica em comparação com os AINEs prevalentes na época, como a indometacina e o piroxicam.
Nas décadas seguintes (1990-2000), a nimesulida expandiu-se rapidamente para mais de 50 países, tornando-se um dos anti-inflamatórios mais prescritos em regiões como:
- Europa do Sul e Oriental: Portugal, Grécia, França, Espanha, Polônia, República Checa, Bulgária e Rússia.
- América Latina: Brasil (onde se tornou líder de mercado), México, Venezuela, Equador e Colômbia.
- Ásia: Índia (mercado massivo com múltiplas marcas genéricas), China, Tailândia e Vietnã.
É notável que a nimesulida nunca foi submetida para aprovação à Food and Drug Administration (FDA) nos Estados Unidos. As razões exatas para esta decisão estratégica por parte da 3M/Riker e dos seus licenciados não são publicamente detalhadas, mas especula-se que envolvessem questões de priorização de portfólio, a expiração iminente da patente durante o período de desenvolvimento ou a antecipação de exigências regulatórias rigorosas quanto à segurança hepática num mercado litigioso como o norte-americano.
A Crise de Segurança e a Fragmentação do Mercado
O início do século XXI marcou um ponto de inflexão na história da nimesulida. Em 2002, a agência de medicamentos da Finlândia suspendeu a comercialização do fármaco após receber 109 relatos de reações adversas, incluindo 66 casos de lesão hepática e dois transplantes de fígado. A Espanha seguiu o mesmo caminho pouco depois. Estes eventos desencadearam a primeira grande revisão de segurança pelo Comitê de Medicamentos para Uso Humano (CHMP) da Agência Europeia de Medicamentos (EMA).
A revisão da EMA de 2004 concluiu que o benefício-risco da nimesulida permanecia favorável, desde que o seu uso fosse restrito. No entanto, a controvérsia ressurgiu em 2007, quando a Irlanda retirou o medicamento do mercado após novos casos de falência hepática fulminante. Uma segunda revisão mais aprofundada da EMA, concluída em 2010/2011, resultou na manutenção da autorização de mercado, mas com restrições severas: proibição do uso crónico, limitação a 15 dias de tratamento e contraindicação absoluta em pacientes com patologia hepática prévia. Esta decisão criou o cenário atual, onde o fármaco é banido em certos países europeus e amplamente utilizado em outros, ilustrando as complexidades da farmacovigilância e da avaliação de risco em escala global.[6][7][8]
Propriedades Físico-Químicas e Estrutura Molecular
Estrutura Molecular
A molécula de nimesulida apresenta três componentes estruturais críticos que definem a sua reatividade e interação biológica:
Grupo sulfonamida
A nimesulida é um ácido fraco com um (constante de acidez) de aproximadamente 6.5. Diferentemente dos AINEs ácidos carboxílicos (como o ibuprofeno, ~4.5) que estão quase totalmente ionizados no pH fisiológico (7.4), a nimesulida possui uma fração significativa na forma não ionizada em ambientes neutros. Esta característica físico-química facilita a sua passagem através das membranas lipídicas e permite uma distribuição ampla nos tecidos. A moiety sulfonanilida é o farmacóforo responsável pela ligação ao sítio ativo da ciclooxigenase, mimetizando a estrutura do estado de transição da reação de ciclooxigenação.
Grupo Nitro na posição para
Localizado no anel benzénico principal, o grupo nitro é um forte retirador de elétrons. Do ponto de vista toxicológico, este é o "calcanhar de Aquiles" da molécula. A redução metabólica deste grupo nitro (por nitroredutases bacterianas ou hepáticas) pode gerar intermediários reativos, como derivados nitroso e hidroxilamina, que estão implicados na indução de stress oxidativo mitocondrial. No entanto, este grupo também contribui para a potência anti-inflamatória através da modulação do potencial redox celular.
Grupo Éter Fenóxi na posição orto
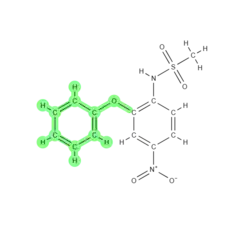
Este segundo anel aromático, ligado através de uma ponte de oxigénio, confere lipofilicidade à molécula e fornece volume estérico. Esta conformação espacial é crucial para o encaixe seletivo no canal hidrofóbico da enzima COX-2, que é ligeiramente mais largo do que o da COX-1. A presença deste grupo éter também influencia a estabilidade metabólica do anel principal.
Síntese Química
A síntese industrial da nimesulida é um processo multi-etapas refinado ao longo de décadas para maximizar o rendimento e pureza. As rotas sintéticas descritas na literatura de patentes (como as da Riker e Helsinn) geralmente seguem a seguinte lógica retrossintética:
- Formação do Núcleo Difenil Éter: A reação inicial envolve tipicamente a condensação de um halonitrobenzeno (como o 2-cloro-1,4-dinitrobenzeno ou similar) com fenol ou fenolato de sódio. Esta substituição nucleofílica aromática cria a espinha dorsal do éter difenílico.
- Redução Seletiva: Se o precursor contiver múltiplos grupos nitro, pode ser necessária uma redução seletiva (usando hidrogénio catalítico ou reagentes químicos como ferro/ácido) para converter um grupo nitro específico numa amina primária (), mantendo o outro grupo nitro intacto, se necessário, ou introduzindo o grupo funcional na posição correta.
- Sulfonilação: A amina aromática resultante (uma anilina substituída) é então reagida com cloreto de metanossulfonilo () na presença de uma base (como piridina ou trietilamina) para formar a ligação sulfonamida final.
- Purificação: O produto bruto é purificado por recristalização em solventes adequados para remover subprodutos e atingir o grau farmacêutico exigido.
Pesquisas também exploraram a síntese de derivados da nimesulida, como compostos N-acilados, visando melhorar o perfil de segurança ou solubilidade, utilizando reações de acilação direta da nimesulida ou redução prévia do grupo nitro para gerar novas entidades químicas com potencial antitumoral.[9][10]
Farmacologia Clínica
Farmacodinâmica
A nimesulida não é apenas "mais um AINE". O seu perfil farmacodinâmico é complexo, envolvendo interações enzimáticas seletivas e modulação direta de processos celulares inflamatórios.
Inibição Preferencial da COX-2
O mecanismo canônico de ação dos AINEs é a inibição das enzimas ciclooxigenases (COX), que catalisam a conversão do ácido araquidónico em prostaglandinas (), precursores de prostaciclinas e tromboxanos.
- COX-1 (Constitutiva): Expressa basalmente na maioria dos tecidos, gera prostaglandinas responsáveis pela proteção da mucosa gástrica, regulação do fluxo sanguíneo renal e agregação plaquetária.
- COX-2 (Induzível): Rapidamente suprarregulada em resposta a citocinas pró-inflamatórias () e fatores de crescimento nos locais de inflamação.
A nimesulida exibe uma seletividade preferencial pela COX-2. Estudos in vitro e ex vivo demonstram que a nimesulida inibe a COX-2 em concentrações 5 a 16 vezes menores do que as necessárias para inibir a COX-1. Embora não seja tão altamente seletiva quanto os "coxibes" modernos (celecoxibe, etoricoxibe), esta preferência confere uma vantagem terapêutica significativa: potente atividade anti-inflamatória com menor propensão a causar úlceras gástricas e sangramentos em comparação com inibidores não seletivos como a aspirina ou indometacina. No entanto, em doses elevadas, a seletividade perde-se e a inibição da COX-1 torna-se clinicamente relevante.
Mecanismos Multifatoriais Independentes de COX
A singularidade da nimesulida reside na sua capacidade de modular a inflamação por vias que não dependem das prostaglandinas. Estes mecanismos "adicionais" podem explicar a sua eficácia em condições onde outros AINEs falham ou têm ação limitada.
- Controlo do Stress Oxidativo (Neutrófilos): Durante a fase aguda da inflamação, os neutrófilos ativados libertam grandes quantidades de ânions superóxido () num processo conhecido como "explosão respiratória" (respiratory burst), causando dano tecidual colateral. A nimesulida inibe diretamente a enzima NADPH oxidase na membrana dos neutrófilos, reduzindo a produção de superóxido. Além disso, atua como um "scavenger" direto de ácido hipocloroso (HOCl), neutralizando agentes oxidantes sem afetar a quimiotaxia ou a fagocitose bacteriana.
- Inibição da Fosfodiesterase IV (PDE4): A nimesulida inibe a isoforma IV da fosfodiesterase, uma enzima que degrada o AMP cíclico (cAMP). O aumento dos níveis intracelulares de cAMP nos leucócitos reduz a sua ativação, diminuindo a libertação de mediadores pró-inflamatórios como leucotrienos e citocinas.
- Inibição de Metaloproteinases (MMPs): Em pacientes com osteoartrite, a degradação da cartilagem é mediada por enzimas como a estromelisina e a colagenase. A nimesulida demonstrou inibir a síntese e atividade destas metaloproteinases, sugerindo um efeito condroprotetor que retarda a destruição articular, além de apenas aliviar a dor.
- Modulação da Histamina: Estudos indicam que a nimesulida inibe a libertação de histamina de mastócitos e basófilos, o que contribui para a redução do edema e da resposta alérgica vascular.
- Ação Antineoplásica Potencial: Pesquisas recentes sugerem que a nimesulida pode ter propriedades anticancerígenas. Estudos em linhas celulares de cancro do pulmão (A549), cervical (HeLa) e ovário mostraram que a nimesulida pode induzir apoptose e inibir a proliferação celular, possivelmente através da inibição da COX-2 (que é frequentemente superexpressa em tumores) e da ativação de caspases, independentemente da via COX. A modulação de proteínas de choque térmico (HSP27) e recetores de fator de crescimento também foi observada.[9]
| Alvo / Processo | Ação Farmacológica | Benefício Clínico Potencial |
|---|---|---|
| Neutrófilos (Stress Oxidativo) |
Inibe a enzima NADPH oxidase e atua como varredor (scavenger) direto do ácido hipocloroso (HOCl). | Reduz o dano tecidual causado por radicais livres durante a inflamação aguda, sem prejudicar a capacidade de fagocitose bacteriana. |
| Fosfodiesterase IV (PDE4) |
Inibe a degradação do AMP cíclico (cAMP) nos leucócitos. | A elevação do cAMP reduz a ativação leucocitária e diminui a liberação de mediadores como histamina e citocinas, contribuindo para redução de edema e reações alérgicas. |
| Metaloproteinases (MMPs) |
Inibe a síntese e atividade de enzimas como estromelisina e colagenase. | Condroproteção: Pode retardar a degradação da cartilagem em pacientes com osteoartrite, oferecendo benefício além da analgesia simples. |
| Modulação da Histamina | Bloqueia a liberação de histamina por mastócitos e basófilos. | Potencializa o efeito anti-inflamatório em tecidos moles e reduz a permeabilidade vascular. |
| Ação Antineoplásica (Investigacional) |
Indução de apoptose e inibição da proteína de choque térmico (HSP27) e proliferação celular. | Observada em estudos in vitro (câncer de pulmão, colo do útero, ovário), sugerindo um papel antiproliferativo independente da COX-2. |
Farmacocinética
A farmacocinética da nimesulida é ideal para o tratamento de condições agudas dolorosas, caracterizada por rápida absorção e eliminação moderada, evitando acumulação excessiva.
| Parâmetro | Valor Médio | Notas Clínicas |
|---|---|---|
| Biodisponibilidade Oral (F) | ~100% | Absorção rápida e completa pelo trato gastrointestinal. |
| Tempo para Pico (Tmax) | 1,22 – 2,75 horas | Início de ação analgésica rápido (< 30 min). A presença de alimentos pode retardar o Tmax, mas não reduz a absorção total. |
| Ligação a Proteínas | > 97,5% | Liga-se principalmente à Albumina (Sítio II). Risco de interações medicamentosas por deslocamento. |
| Volume de Distribuição (Vd) | 0,18 – 0,39 L/kg | Boa distribuição no compartimento extracelular; penetra bem em tecidos inflamatórios. |
| Meia-vida de Eliminação (t1/2) | 1,8 – 4,7 horas | Permite posologia bid (duas vezes ao dia). Curta o suficiente para minimizar acumulação. |
| Excreção Urinária | ~50% | Principalmente como metabolitos conjugados hidrofílicos. Apenas 1-3% é excretado inalterado. |
| Excreção Fecal | ~29% | Via de eliminação secundária importante. |
.png)
Metabolismo Hepático e Bioativação
O metabolismo da nimesulida ocorre quase exclusivamente no fígado e é um processo crítico tanto para a depuração do fármaco quanto para a geração de toxicidade.
- Vias Enzimáticas: A principal enzima responsável pela biotransformação é o Citocromo P450 2C9 (CYP2C9). A isoforma CYP1A2 desempenha um papel auxiliar.
- Metabolito Ativo (M1): O principal produto metabólico é a 4-hidroxi-nimesulida (referido na literatura como M1). Este composto retém atividade farmacológica inibitória sobre a COX-2 e contribui significativamente para o efeito terapêutico global, dado que circula no plasma em concentrações relevantes.
- Metabolitos Reativos e Risco (M2): O metabolismo oxidativo subsequente do M1 (mediado por CYP2C19 e CYP1A2) pode levar à formação de um intermediário quimicamente reativo: a diiminoquinona (M2). Este eletrófilo é capaz de reagir com grupos tiol (sulfidrilo) de proteínas e glutationa. A conjugação com glutationa é a via de detoxificação normal; contudo, se a produção de M2 exceder a capacidade de detoxificação ou se os níveis de glutationa estiverem depletados, ocorre ligação covalente a proteínas hepáticas essenciais, desencadeando necrose celular. Este mecanismo de bioativação é central para a hipótese da hepatotoxicidade idiossincrática.[11][12]
Efeitos Adversos
Reações Adversas Classificadas por Frequência[1]
| Frequência | Reações Observadas |
|---|---|
| Muito comuns (> 1/10) |
Diarreia, náusea e vômito. |
| Incomuns (> 1/1.000 e < 1/100) |
Prurido, rash e sudorese aumentada; constipação, flatulência e gastrite; tonturas e vertigens; hipertensão; edema. |
| Raras (> 1/10.000 e < 1/1.000) |
Eritema e dermatite; ansiedade, nervosismo e pesadelo; visão borrada; hemorragia, flutuação da pressão sanguínea e fogachos; disúria, hematúria e retenção urinária; anemia e eosinofilia; hipersensibilidade; hipercalemia; mal-estar e astenia. |
| Muito raras (< 1/10.000) |
Urticária, edema angioneurótico, edema facial, eritema multiforme e casos isolados de Síndrome de Stevens-Johnson e necrólise epidérmica tóxica; dor abdominal, dispepsia, estomatite, melena, úlceras pépticas e perfuração ou hemorragia gastrintestinal (podem ser graves); cefaleia, sonolência e casos isolados de encefalopatia (Síndrome de Reye); outros distúrbios visuais e vertigem; falência renal, oligúria e nefrite intersticial; casos isolados de púrpura, pancitopenia e trombocitopenia; anafilaxia; casos isolados de hipotermia. |
Reações de Frequência Indeterminada
A literatura médica registra ainda eventos adversos cuja incidência exata não pôde ser calculada a partir dos dados disponíveis, incluindo:
Distúrbios Hepatobiliares: É comum observar elevações nas enzimas hepáticas (transaminases), que tendem a ser reversíveis e transitórias. Contudo, existem registros de quadros severos, incluindo colestase, icterícia e hepatite aguda. Em casos raros e idiossincráticos, a condição pode evoluir para insuficiência hepática fulminante, com desfechos fatais.
Distúrbios Respiratórios: Podem ocorrer manifestações de hipersensibilidade respiratória, tais como dispneia (falta de ar), crises asmáticas e broncoespasmo. O risco é acentuado em pacientes que já apresentam reatividade cruzada ao ácido acetilsalicílico (aspirina) ou a outros anti-inflamatórios não esteroides.[1]
Aplicações Terapêuticas e Posologia
Indicações Aprovadas
As indicações da nimesulida variam conforme o registro sanitário local, mas convergem globalmente para o tratamento sintomático de curto prazo:
| Indicação Clínica | Detalhes e Restrições de Uso |
|---|---|
| Dor Aguda | Tratamento de processos inflamatórios dolorosos, incluindo:
Traumas (entorses, distensões e contusões); Dor pós-operatória (ex: cirurgias odontológicas). |
| Osteoartrite Dolorosa | Indicada apenas para o tratamento sintomático de crises agudas de artrose.
Contraindicação Implícita: Devido às restrições de segurança, não deve ser utilizada como terapia de manutenção prolongada para doenças articulares crônicas. |
| Dismenorreia Primária | Alívio da dor pélvica associada à menstruação (cólicas) em pacientes acima de 12 anos.
A rápida absorção ( reduzido) e a potente ação sobre as prostaglandinas uterinas tornam o fármaco particularmente eficaz nesta indicação. |
Posologia e Administração
| Parâmetro | Recomendação | Observações de Segurança |
|---|---|---|
| Dose Padrão | 100 mg | Administrar por via oral, duas vezes ao dia (a cada 12 horas). |
| Dose Máxima Diária | 200 mg/dia | Doses superiores não aumentam a eficácia analgésica linearmente, mas elevam exponencialmente o risco de hepatotoxicidade. |
| Duração do Tratamento | Máximo de 15 dias | O uso deve ser limitado ao menor tempo possível. Ciclos superiores a 15 dias consecutivos são contraindicados. |
Formas Farmacêuticas Disponíveis
- O fármaco é comercializado em diversas apresentações para facilitar a adesão e absorção:
- Comprimidos e granulado para solução oral;
- Supositórios e gel tópico;
- Formulações com Beta-ciclodextrina: Variantes complexadas que aumentam a solubilidade em água e aceleram a absorção gastrointestinal, proporcionando alívio mais rápido da dor.
Contraindicações
| População / Condição | Status | Justificativa Clínica e Riscos |
|---|---|---|
| Pediátrico (< 12 anos) |
CONTRAINDICADO | O uso foi banido globalmente nesta faixa etária devido à forte associação com casos de hepatotoxicidade fatal e risco de Síndrome de Reye (encefalopatia grave associada a disfunção hepática). |
| Insuficiência Hepática | CONTRAINDICADO | Proibido em qualquer grau de comprometimento hepático, bem como em pacientes com histórico de reações hepatotóxicas a outros AINEs. |
| Gravidez (3º Trimestre) |
CONTRAINDICADO | Risco de fechamento prematuro do ducto arterioso e desenvolvimento de hipertensão pulmonar fetal. Também pode inibir as contrações uterinas, atrasando o trabalho de parto. |
| Lactação | CONTRAINDICADO | Não há dados suficientes sobre a excreção no leite humano; devido ao perfil de segurança, o uso é desaconselhado durante a amamentação. |
Interações Medicamentosas
A nimesulida apresenta interações clinicamente relevantes, principalmente devido à sua alta afinidade por proteínas plasmáticas e metabolismo pelo CYP2C9.[1]
| Fármaco/Classe | Mecanismo da Interação | Consequência Clínica | Recomendação |
| Varfarina e Anticoagulantes | Competição pelo CYP2C9 e deslocamento da ligação à albumina (embora a nimesulida prefira o Sítio II, interações alostéricas ou competição em altas doses podem ocorrer). | Aumento da fração livre de varfarina e inibição do seu metabolismo, elevando o INR e o risco de hemorragia grave. | Monitoramento rigoroso do INR. Evitar a associação se possível. Pacientes com polimorfismos do CYP2C9 (2/3) estão em maior risco. |
| Metotrexato | Inibição da secreção tubular renal (via transportadores OAT) e deslocamento de proteínas. | Aumento tóxico dos níveis séricos de metotrexato. Risco de pancitopenia, nefrotoxicidade e hepatotoxicidade. | Contraindicado ou Precaução Extrema. Suspender nimesulida 24h antes e depois da dose de metotrexato. |
| Lítio | Redução da depuração renal de lítio (efeito mediado por prostaglandinas renais). | Aumento da litemia com risco de toxicidade (tremores, confusão, danos renais). | Monitorar níveis séricos de lítio. |
| Diuréticos (Furosemida) e Anti-hipertensivos (IECA/BRA) | Inibição da síntese de prostaglandinas vasodilatadoras renais (). | Redução do efeito diurético e anti-hipertensivo. Risco aumentado de insuficiência renal aguda em desidratados. | Hidratação adequada e monitoramento da função renal e pressão arterial. |
| Outros AINEs e Corticosteroides | Sinergismo farmacodinâmico na inibição de prostaglandinas gástricas. | Risco exponencialmente aumentado de ulceração gastrointestinal e sangramento. | Evitar associação. |
Regulação e Farmacovigilância Global
A nimesulida ilustra a heterogeneidade das decisões regulatórias baseadas na avaliação benefício-risco. O mapa global de disponibilidade da nimesulida é fragmentado.[13]
União Europeia: A Posição da EMA
A Agência Europeia de Medicamentos conduziu revisões formais (Referrals sob o Artigo 31) em 2002, 2007 e 2010.[13]
- Decisão Final (2011/2012): A EMA concluiu que o benefício da nimesulida no tratamento da dor aguda supera os riscos, desde que medidas de minimização de risco sejam implementadas.
- Restrições Impostas: Remoção da indicação para osteoartrite dolorosa crónica; restrição da dose a 100 mg bid; limite máximo de 15 dias de tratamento; obrigação de advertências de segurança nas embalagens.
- Status Nacional: Apesar da aprovação centralizada condicional, países individuais mantiveram proibições nacionais baseadas em dados locais. O medicamento não é comercializado na Finlândia, Espanha, Irlanda, Bélgica e Reino Unido.
Ásia: O Caso da Índia
A Índia é um dos maiores mercados para a nimesulida, mas também palco de intervenções regulatórias recentes e significativas.
- 2011: O Ministério da Saúde e Bem-Estar da Família proibiu o uso de nimesulida em crianças menores de 12 anos, seguindo o consenso global.
- 2024/2025: Num movimento recente de farmacovigilância, o governo indiano, sob recomendação do ICMR (Indian Council of Medical Research), emitiu notificações proibindo a fabricação e venda de formulações orais de nimesulida de liberação imediata acima de 100 mg (doses altas) e de combinações de dose fixa irracionais. O alerta citou riscos hepáticos e a disponibilidade de alternativas mais seguras como justificativa para restringir ainda mais o acesso. [14]
Brasil: A Postura da Anvisa
No Brasil, a nimesulida permanece como um dos anti-inflamatórios mais populares e acessíveis. A Agência Nacional de Vigilância Sanitária (Anvisa) adota uma postura de monitoramento e restrição, sem banimento total para adultos.[1]
- Uso Pediátrico: A Resolução RE nº 3.238 proibiu o uso em menores de 12 anos. A Anvisa tem atuado ativamente na interdição de lotes (ex: suspensões orais) que não cumprem os requisitos de teor de princípio ativo, reforçando o controle de qualidade.
- Prescrição: O medicamento é classificado como "Venda Sob Prescrição Médica" (Tarja Vermelha), embora a fiscalização na ponta da venda varie. A bula profissional brasileira contém advertências explícitas (Black Box Warnings) sobre hepatotoxicidade, contraindicando o uso concomitante com outros fármacos lesivos ao fígado ou álcool.
Estados Unidos e Outros
A ausência da nimesulida nos EUA, Austrália e Canadá deve-se à não submissão de pedido de registro (nos primórdios) ou à recusa baseada no perfil de segurança hepática comparado aos AINEs já estabelecidos nesses mercados (como naproxeno e ibuprofeno). A FDA nunca aprovou o uso de nimesulida. [15]
Referências
- ↑ a b c d e «Consultas - Agência Nacional de Vigilância Sanitária». consultas.anvisa.gov.br. Consultado em 21 de janeiro de 2026
- ↑ Mattia, C.; Ciarcia, S.; Muhindo, A.; Coluzzi, F. (agosto de 2010). «[Nimesulide: 25 years later]». Minerva Medica (4): 285–293. ISSN 0026-4806. PMID 21030939. Consultado em 21 de janeiro de 2026
- ↑ «What is the mechanism of Nimesulide?». synapse.patsnap.com (em inglês). Consultado em 21 de janeiro de 2026
- ↑ «Nimesulide: Critical Appraisal of Safety and Efficacy in Acute Pain». japi.org (em inglês). Consultado em 21 de janeiro de 2026
- ↑ «Nimesulide - referral | European Medicines Agency (EMA)». www.ema.europa.eu (em inglês). 13 de maio de 2004. Consultado em 21 de janeiro de 2026
- ↑ Bansode Shreya S; Bhukan Priyanka V; Sole Prashant (novembro de 2025). «GLOBAL BAN ON NIMESULIDE: PHARMACOLOGICAL INSIGHS, SAFETY CORNERS, AND REGULATORY PRESPECIVE» 11 ed. International Research Journal of Modernization in Engineering Technology and Science. 07: 3534-3544. ISSN 2582-5208. Consultado em 21 de janeiro de 2026 line feed character character in
|título=at position 58 (ajuda) - ↑ PubChem. «Nimesulide». pubchem.ncbi.nlm.nih.gov (em inglês). Consultado em 21 de janeiro de 2026
- ↑ Rainsford, Kim D., ed. (2005). Nimesulide — Actions and Uses. Col: SpringerLink Bücher. Basel: Birkhäuser Basel. ISBN 978-3-7643-7068-8
- ↑ a b Güngör, Tuğba; Ozleyen, Adem; Yılmaz, Yakup Berkay; Siyah, Pinar; Ay, Mehmet; Durdağı, Serdar; Tumer, Tugba Boyunegmez (outubro de 2021). «New nimesulide derivatives with amide/sulfonamide moieties: Selective COX-2 inhibition and antitumor effects». European Journal of Medicinal Chemistry (em inglês). 113566 páginas. doi:10.1016/j.ejmech.2021.113566. Consultado em 22 de janeiro de 2026
- ↑ Pericherla, Sandhya; Mareddy, Jyoti; Rani D. P., Geetha; Gollapudi, Padmavathi V.; Pal, Sarbani (abril de 2007). «Chemical modifications of nimesulide». Journal of the Brazilian Chemical Society (em inglês) (2): 384–390. ISSN 0103-5053. doi:10.1590/S0103-50532007000200021. Consultado em 22 de janeiro de 2026
- ↑ Van Booven, Derek; Marsh, Sharon; McLeod, Howard; Carrillo, Michelle Whirl; Sangkuhl, Katrin; Klein, Teri E.; Altman, Russ B. (abril de 2010). «Cytochrome P450 2C9-CYP2C9». Pharmacogenetics and Genomics (em inglês) (4): 277–281. ISSN 1744-6872. doi:10.1097/FPC.0b013e3283349e84. Consultado em 23 de janeiro de 2026
- ↑ Ferreira, Roseane Guimarães; Narvaez, Luis Eduardo Mosquera; Espíndola, Kaio Murilo Monteiro; Rosario, Amanda Caroline R. S.; Lima, Wenddy Graziela N.; Monteiro, Marta Chagas (20 de julho de 2021). «Can Nimesulide Nanoparticles Be a Therapeutic Strategy for the Inhibition of the KRAS/PTEN Signaling Pathway in Pancreatic Cancer?». Frontiers in Oncology. ISSN 2234-943X. doi:10.3389/fonc.2021.594917. Consultado em 23 de janeiro de 2026
- ↑ a b «Sale of Nimulid in the Country». www.pib.gov.in. Consultado em 23 de janeiro de 2026. Cópia arquivada em 31 de dezembro de 2025
- ↑ «Govt bans high-dose nimesulide painkiller pills citing health risk». The Times of India. 1 de janeiro de 2026. ISSN 0971-8257. Consultado em 23 de janeiro de 2026
- ↑ McCormick, Pa; Kennedy, F; Curry, M; Traynor, O (janeiro de 1999). «COX 2 inhibitor and fulminant hepatic failure». The Lancet (em inglês) (9146): 40–41. doi:10.1016/S0140-6736(05)74867-4. Consultado em 23 de janeiro de 2026