Hidroxilamina
Hidroxilamina
| |||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||||||||||
 | |||||||||||||||||||||||||||
| Nomes | |||||||||||||||||||||||||||
| Nome IUPAC | Hidroxilamina | ||||||||||||||||||||||||||
| Nome sistemático | Hidroxilamina[1] | ||||||||||||||||||||||||||
| Outros nomes | Aminol Azanol | ||||||||||||||||||||||||||
| |||||||||||||||||||||||||||
| |||||||||||||||||||||||||||
| |||||||||||||||||||||||||||
| |||||||||||||||||||||||||||
| |||||||||||||||||||||||||||
| |||||||||||||||||||||||||||
| Página de dados suplementares | |||||||||||||||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||||||||||||||
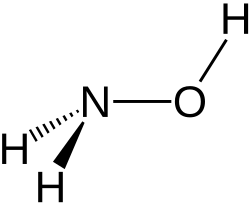
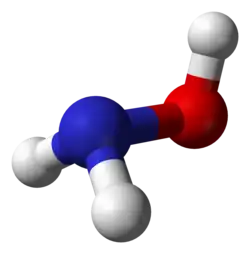
Hidroxilamina é um composto inorgânico de fórmula NH2OH. O material puro é um composto cristalino instável e higroscópico.[4] de qualquer forma, hidroxilamina é quase sempre disponível e usada em solução aquosa. É usada para preparar oximas, um importante grupo funcional. É também um intermediário na nitrificação biológica. A oxidação da amônia (NH3) é mediada pela enzima hidroxilamina oxiredutase (HAO).
Produção
NH2OH pode ser produzida de várias formas. A principal é pela síntese de Raschig: nitrito de amônio aquoso é reduzido por HSO4− e SO2 a 0 °C para formar o ânion hidroxilamido-N,N-dissulfato:
- NH4NO2 + 2 SO2 + NH3 + H2O → 2 NH4+ + N(OH)(OSO2)22−
Este ânion é então hidrolisado para (NH3OH)2SO4:
- N(OH)(OSO2)22− + H2O → NH(OH)(OSO2)− + HSO4−
- 2 NH(OH)(OSO2)− + 2 H2O → (NH3OH)2SO4 + SO42-
NH2OH sólido pode ser coletado pelo tratamento com amônia. Sulfato de amônio, (NH4)2SO4, um co-produto insolúvel em amônia líquida, é removido por filtração; a amônialíquida é evaporada para dar o produto desejado.[4]
A reação global é: 2NO2- + 4SO2 + 6H2O + 6NH3 → 4SO42- + 6NH4+ + 2NH2OH
Sais de hidroxilamônio podem ser convertidos a hidroxilamina por neutralização:
- (NH3OH)Cl + NaOBu → NH2OH + NaCl + BuOH[4]
Hidroxilamina pode também ser produzida pela redução de ácido nitroso ou nitrito de potássio por bissulfito:
- HNO2 + 2 HSO3− → N(OH)(OSO2)22− + H2O → NH(OH)(OSO2)− + HSO4−
- NH(OH)(OSO2)− + H3O+ (100 °C/1 h) → NH3(OH)+ + HSO4−
Reações
Hidroxilamina reage com eletrófilos, tais como agentes alquilantes, os quais podem se ligar ao nitrogênio ou ao oxigênio:
- R-X + NH2OH → R-ONH2 + HX
- R-X + NH2OH → R-NHOH + HX
A reação de NH2OH com um aldeído ou uma cetona produz uma oxima.
- R2C=O + NH2OH∙HCl , NaOH → R2C=NOH + NaCl + H2O
Ver também
Referências
- ↑ «Hydroxylamine - PubChem Public Chemical Database». The PubChem Project. USA: National Center for Biotechnology Information
- ↑ Predefinição:RubberBible87th
- ↑ Martel, B.; Cassidy, K. (2004). Chemical Risk Analysis: A Practical Handbook. [S.l.]: Butterworth–Heinemann. 362 páginas. ISBN 1-903996-65-1
- ↑ a b c Greenwood and Earnshaw. Chemistry of the Elements. 2nd Edition. Reed Educational and Professional Publishing Ltd. pp. 431-432. 1997.
Leitura posterior
- Hydroxylamine
- Walters, Michael A. and Andrew B. Hoem. "Hydroxylamine." e-Encyclopedia of Reagents for Organic Synthesis. 2001.
- Schupf Computational Chemistry Lab
- M. W. Rathke A. A. Millard "Boranes in Functionalization of Olefins to Amines: 3-Pinanamine" Organic Syntheses, Coll. Vol. 6, p. 943; Vol. 58, p. 32. (preparação do ácido hidroxilamino-O-sulfônico).