Peróxido de lítio
Peróxido de lítio
| |||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
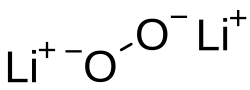 | |||||||||||||||||
| Nomes | |||||||||||||||||
| Outros nomes | Peróxido de dilítio Peróxido de lítio (I) | ||||||||||||||||
| |||||||||||||||||
| |||||||||||||||||
| |||||||||||||||||
| |||||||||||||||||
| |||||||||||||||||
| Página de dados suplementares | |||||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||||
Peróxido de lítio (Li2O2) é um composto químico. Peróxido de lítio reage com, e deve ser mantido destes isolado, água, vapor, agentes redutores, material orgânico, óxidos metálicos e sais.
Produção
Por conversão do hidróxido de lítio com peróxido de hidrogênio e posterior evaporação da água ao vácuo:
Aplicações
- Peróxido de lítio encontra uso como endurecedor para polímeros especiais.
- Produção de óxido de lítio de alta pureza por decomposição térmica do peróxido de lítio a 195 °C:
- É usado em purificadores de ar e meios de regeneração para sistemas de suporte de vida em naves espaciais e submarinos para absorver dióxido de carbono e liberar oxigênio na reação:
Nesta reação, um grama de peróxido de lítio absorve 490 mL de dióxido de carbono e libera aproximadamente 240 mL de oxigênio livre, resultando em carbonato de lítio como resíduo sólido.
Ver também
Ligações externas
