Di-isopropilamida de lítio
Di-isopropilamida de lítio
| |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||
 | |||||||||||||
| Nomes | |||||||||||||
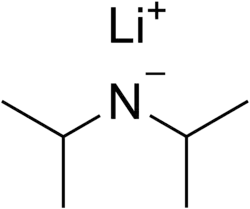
| Nome IUPAC | Lithium diisopropylamide | ||||||||||||
| Outros nomes | LDA | ||||||||||||
| |||||||||||||
| |||||||||||||
| |||||||||||||
| |||||||||||||
| Página de dados suplementares | |||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||
Di-isopropilamida de lítio é o composto químico com a fórmula [(CH3)2CH]2NLi. Geralmente abreviado LDA (do inglês lithium diisopropylamide), é uma base forte usada em química orgânica para a deprotonação de compostos fracamente ácidos. O reagente tem sido amplamente aceito porque é solúvel em solventes orgânicos não polares e é não pirofórico. O LDA é uma base não nucleofílica. A di-isopropilamida de potássio (KDA) é um composto similar, mas possuindo um cátion potássio ao invés de uma cátion lítio. O LDA é mais barato que o KDA e é mais amplamente usado.
Preparação e estrutura
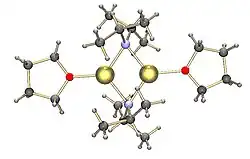
LDA é normalmente formado pelo tratamento de uma solução de tetraidrofurano (THF) resfriada (0 a −78 °C) de di-isopropilamina com n-butil-lítio.[3]
Referências
- ↑ a b Catálogo da Sigma-Aldrich, Di-isopropilamida de lítio, consultado em 9 de fevereiro de 2010.
- ↑ David Evans Research Group
- ↑ Smith, A. P.; Lamba, J. J. S.; Fraser, C. L. (2004). «Efficient Synthesis of Halomethyl-2,2'-Bipyridines: 4,4'-Bis(chloromethyl)-2,2'-Bipyridine». Org. Synth.; Coll. Vol., 10