para-Metoxianfetamina
para-Metoxianfetamina
| |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||
 | |||||||||||||||
| Nomes | |||||||||||||||
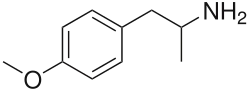
| Nome IUPAC | 1-(4-methoxyphenyl)propan-2-amine | ||||||||||||||
| Outros nomes | para-Metoxianfetamina; p-Metoxianfetamina; 4-Metoxianfetamina | ||||||||||||||
| |||||||||||||||
| |||||||||||||||
| |||||||||||||||
| Página de dados suplementares | |||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||
para-Metoxianfetamina (PMA), também conhecida como 4-metoxianfetamina (4-MA), é uma droga sintética da classe das anfetaminas com efeitos serotoninérgicos.[2][3] Diferentemente de outras substâncias dessa classe, a PMA não produz efeitos estimulantes, euforizantes ou entactogênicos,[4] comportando-se mais como um antidepressivo,[5] embora possua propriedades psicodélicas leves em dosagens mais elevadas.[6][7]
A PMA tem sido encontrada em comprimidos vendidos como metilenodioxianfetamina (MDMA, ecstasy),[8][9][10][11] embora seus efeitos sejam significativamente distintos daqueles provocados pelà metilenodioxianfetamina. Geralmente, PMA é sintetizada a partir do anetol, um composto aromatizante presente no anis e no funcho, devido à menor disponibilidade do safrol, a matéria-prima tradicionalmente utilizaada para a produção de MDMA, em consequência de restrições impostas pelas autoridades, o que levou aos produtores ilegais a adltarem o anetol como alternativa.[12]
Efeitos
De acordo com Alexander Shulgin, em seu livro PiHKAL, os efeitos da PMA em doses de 50 a 80 mg incluíram hipertensão e efeitos semelhantes aos da dietiltriptamina (DET): pós-imagens [en], parestesia leve e uma intoxicação comparável à do álcool, sem efeitos psicodélicos marcantes.[2][13]
Em ensaios clínicoss, a PMA provocou excitação [en], outros efeitos centrais e efeitos simpaticomiméticos, mas nenhum efeito psicotomimético.[13] Testes com animais sugerem que a PMA tenha efeitos psicodélicos parciais, mas não há consenso de que o efeito se estenda a humanos.[13] A PMA substituiu apenas parcialmente o psicoestimulante anfetamina em testes de discriminação de drogas [en].[13][14] Não produziu efeitos semelhantes aos do MDMA em roedores, sugerindo ausência de propriedades entactogênicas.[14]
Efeitos colaterais
A PMA tem sido associada a inúmeras reações adversas, incluindo morte.[15][16] Os efeitos da ingestão de PMA se relacionam ais produzidos por anfetaminas alucinógenas, como batimentos cardíacos acelerados (taquicardia) e irregulares, visão turva e uma forte sensação de intoxicação, muitas vezes desagradável. Em altas doses podem ocorrer outros efeitos negativos, como náuseas e vômitos, hipertermia grave e alucinações. Os efeitos da PMA também parecem ser muito mais imprevisíveis e variáveis entre indivíduos do que os do MDMA, e indivíduos sensíveis podem morrer devido a uma dose de PMA pela qual uma pessoa menos suscetível pode ser apenas levemente afetada.[17]
Embora a PMA por si só possa causar toxicidade significativa, a combinação de PMA com MDMA tem um efeito sinérgico apontado como particularmente perigoso.[18] Como a PMA tem um início de ação lento, ocorreram várias mortes quando as pessoas tomaram uma pílula contendo PMA, seguida de uma pílula contendo MDMA posteriormente, por pensarem que a primeira pílula não era ativa.[19]
Sobredosagem
A overdose de PMA pode causar uma emergência médica grave, mesmo com doses apenas ligeiramente superiores à faixa recreativa usual, e especialmente quando a PMA é combinada com outros estimulantes, como cocaína ou MDMA. Os sintomas característicos são hipertermia pronunciada, taquicardia e hipertensão, em conjunto com agitação, confusão e convulsões. A overdose de PMA também tende a provocar hipoglicemia e hipercalemia, o que pode ajudar a distingui-la de uma overdose de MDMA. Em alguns casos, podem surgir complicações mais sérias, como rabdomiólise e hemorragia intracerebral, exigindo cirurgia de emergência. Não há antídoto específico, de modo que o tratamento é sintomático, geralmente envolvendo resfriamento externo e também resfriamento interno por meio de infusão intravenosa de solução salina gelada (soro fisiológico). Inicialmente, osbenzodiazepínicos são usados para controlar as convulsões, e anticonvulsivantes mais potentes, como fenitoína ou tiopental, podem ser aplicados caso as convulsões persistam. A pressão arterial pode ser reduzida com uma combinação de alfabloqueadores e betabloqueadores (ou um bloqueador misto alfa/beta) ou com outros medicamentos, como nifedipina ou nitroprussiato. Antagonistas de serotonina podem ser considerados caso necessário. Apesar da gravidade da condição, a maioria das pessoas sobrevivem se o tratamento for administrado a tempo. No entanto, pacientes com temperatura corporal superior a 40 °C no momento em que buscam atendimento tendem a apresentar um prognóstico desfavorável.[20]
Farmacologia
Farmacodinâmica
| Composto | 5-HT | NE | DA | Ref |
|---|---|---|---|---|
| d-Anfetamina | 698–1,765 | 6.6–7.2 | 5.8–24.8 | [21][22] |
| d-Metanfetamina | 736–1,292 | 12.3–13.8 | 8.5–24.5 | [21][23] |
| 2-Methoxyamphetamine | SD | 473 | 1,478 | [24] |
| 3-Metoxianfetamina | SD | 58.0 | 103 | [24] |
| para-Metoxianfetamina (PMA) | SD | 166 | 867 | [24][25] |
| PMMA | SD | SD | SD | SD |
| (S)-PMMA | 41 | 147 | 1,000 | [14][26][25] |
| (R)-PMMA | 134 | >14,000 | 1,600 | [14][26][25] |
| 4-Metilanfetamina (4-MA) | 53.4 | 22.2 | 44.1 | [27][28][24] |
| 4-Metilmetanfetamina (4-MMA) | 67.4 | 66.9 | 41.3 | [29][30] |
| para-Cloroanfetamina (PCA) | 28.3 | 23.5–26.2 | 42.2–68.5 | [28][24][31][32] |
| para-Clorometanfetamina (PCMA) | 29.9 | 36.5 | 54.7 | [31][32] |
| Metedrona (4-MeO-MC) | 120–195 | 111 | 506–881 | [33][34][35][36][37] |
| Mefedrona (4-MMC) | 118.3–122 | 58–62.7 | 49.1–51 | [23][22][34][36][37] |
| Notas: Quanto menor o valor, mais fortemente a substância libera o neurotransmissor. Os bioensaios foram realizados em sinaptossomaS de cérebro de rato, e as potências em humanos podem ser diferentes. Refs:[38][39] | ||||
A PMA atua como um agente seletivo de liberação de serotonina (SSRA), com efeitos fracos sobre os transportadores de dopamina (DAT) e de noradrenalina (NET).[40][41][42][43] Seus valores de concentração necessária para atingir 50% do efeito máximo (EC50) para indução de liberação de monoamina são 166 nM para dopamina e 867 nM para norepinefrina em sinaptossomas cerebrais de ratos, enquanto a serotonina não foi relatada.[24]«Dopamine-releasing agents». Dopamine Transporters: Chemistry, Biology and Pharmacology. Hoboken [NJ]: Wiley. Julho de 2008. pp. 305–320. ISBN 978-0-470-11790-3. OCLC 181862653. OL 18589888W</ref>[25] Foi descoberto que o medicamento aumenta fortemente os níveis de serotonina no cérebro e aumenta fracamente os níveis de dopamina no cérebro em roedores in vivo.[44] Em relação ao MDMA, a PMA parece ser consideravelmente menos eficaz como liberador de serotonina, com propriedades mais semelhantes às de um inibidor da recaptação de serotonina em comparação.[45]
A PMA também atua como um inibidor da monoamina oxidase (IMAO) potente, mais especificamente como um inibidor reversível da enzima monoamina oxidase A (MAO-A), sem efeitos significativos sobre a monoamina oxidase B (MAO-B).[46][47] O valor de concentração inibitória média (IC50) da PMA para a inibição da MAO-A foi reportado como variando entre 300 e 600 nM.[48]
A PMA apresenta afinidades muito baixas para os receptores de serotonina 5-HT1A, 5-HT2A e 5-HT2C.[43] Suas afinidades por esses receptores foram relatadas como sendo, respectivamente, >20.000 nM, 11.200 nM e >13.000 nM,.[43] Por outro lado, em camundongos e rato, a PMA apresenta afinidades mais altas pelo receptor associado às aminas-traço do tipo 1 (TAAR1).[43]
A para-Metoxianfetamina provoca hipertermia acentuada em roedores, e exerce efeitos leves sobre hiperatividade e neurotoxicidade serotoninérgica [en] e somente em doses elevadas, sendo substancialmente menor do que, por exemplo, o potencial de neurotoxicidade causada por MDMA.[41][42][45]
Evidências limitadas sugerem que a PMA eleva a temperatura corporal de forma drástica; e suspeita-se que esse efeito esteja relacionado à capacidade desta droga em inibir a MAO-A, ao mesmo tempo em que promove a liberação de serotonina, o que aumenta o risco de desencadear uma síndrome serotoninérgica.[45][47]
História
A PMA entrou em circulação no início da década de 1970, quando passou a ser utilizada como droga substituta do LSD.[2]
Na década de 1990, diversas mortes que inicialmente foram atribuídas ao uso de MDMA na Austrália, agora são consideradas como tendo sido provocadas por PMA. As pessoas não sabiam que estavam ingerindo PMA em vez de MDMA.[11] Desde então, houve uma série de mortes induzidas por PMA em todo o mundo.[49][50]
Ver também
Referências
- ↑ Anvisa (24 de julho de 2023). «RDC Nº 804 - Listas de Substâncias Entorpecentes, Psicotrópicas, Precursoras e Outras sob Controle Especial». Diário Oficial da União. Consultado em 27 de agosto de 2023
- ↑ a b c «#97 4-MA». Pihkal: A Chemical Love Story. [S.l.]: Transform Press. 1991. ISBN 978-0-9630096-0-9
|wayb=requer|url=(ajuda); - ↑ «Warning of possible shift to killer drug». Sydney Morning Herald. Fairfax. 7 de abril de 2008. Consultado em 29 de junho de 2008. Arquivado do original em 2 de julho de 2008
- ↑ Corrigall WA, Robertson JM, Coen KM, Lodge BA (janeiro de 1992). «The reinforcing and discriminative stimulus properties of para-ethoxy- and para-methoxyamphetamine». Pharmacology, Biochemistry, and Behavior. 41 (1): 165–169. CiteSeerX 10.1.1.670.6929
 . PMID 1539067. doi:10.1016/0091-3057(92)90077-S
. PMID 1539067. doi:10.1016/0091-3057(92)90077-S
- ↑ Preve M, Suardi NE, Godio M, Traber R, Colombo RA (abril de 2017). «Paramethoxymethamphetamine (Mitsubishi turbo) abuse: Case report and literature review». European Psychiatry. 41 (S1): s875. doi:10.1016/j.eurpsy.2017.01.1762
- ↑ Hegadoren KM, Martin-Iverson MT, Baker GB (abril de 1995). «Comparative behavioural and neurochemical studies with a psychomotor stimulant, an hallucinogen and 3,4-methylenedioxy analogues of amphetamine». Psychopharmacology. 118 (3): 295–304. PMID 7617822. doi:10.1007/BF02245958
- ↑ Winter JC (fevereiro de 1984). «The stimulus properties of para-methoxyamphetamine: a nonessential serotonergic component». Pharmacology, Biochemistry, and Behavior. 20 (2): 201–203. PMID 6546992. doi:10.1016/0091-3057(84)90242-9
- ↑ «EcstasyData.org: Results : Lab Test Results for Recreational Drugs». www.ecstasydata.org. Consultado em 15 de fevereiro de 2015. Arquivado do original em 15 de fevereiro de 2015
- ↑ «Warning over fake ecstasy tablets after seven people die in Scotland». The Guardian. 10 de julho de 2013. Consultado em 10 de julho de 2013. Arquivado do original em 2 de fevereiro de 2020
- ↑ «Four Dead Amid Fears Of Dodgy Batch Of 'Superman' Ecstasy Hitting The UK». HuffPost UK. 2 de janeiro de 2015. Consultado em 12 de junho de 2022. Arquivado do original em 21 de abril de 2022
- ↑ a b Byard RW, Gilbert J, James R, Lokan RJ (setembro de 1998). «Amphetamine derivative fatalities in South Australia--is "Ecstasy" the culprit?». The American Journal of Forensic Medicine and Pathology. 19 (3): 261–265. PMID 9760094. doi:10.1097/00000433-199809000-00013
- ↑ Waumans D, Bruneel N, Tytgat J (abril de 2003). «Anise oil as para-methoxyamphetamine (PMA) precursor». Forensic Science International. 133 (1–2): 159–170. PMID 12742705. doi:10.1016/S0379-0738(03)00063-X
- ↑ a b c d The Shulgin Index, Volume One: Psychedelic Phenethylamines and Related Compounds. 1. Berkeley: Transform Press. 2011. ISBN 978-0-9630096-3-0. Consultado em 2 de novembro de 2024
- ↑ a b c d Glennon RA (abril de 2017). «The 2014 Philip S. Portoghese Medicinal Chemistry Lectureship: The "Phenylalkylaminome" with a Focus on Selected Drugs of Abuse». J Med Chem. 60 (7): 2605–2628. PMC 5824997
 . PMID 28244748. doi:10.1021/acs.jmedchem.7b00085
. PMID 28244748. doi:10.1021/acs.jmedchem.7b00085
- ↑ Martin TL (outubro de 2001). «Three cases of fatal paramethoxyamphetamine overdose». Journal of Analytical Toxicology. 25 (7): 649–651. PMID 11599618. doi:10.1093/jat/25.7.649

- ↑ Becker J, Neis P, Röhrich J, Zörntlein S (março de 2003). «A fatal paramethoxymethamphetamine intoxication». Legal Medicine. 5 (Suppl 1): S138–S141. PMID 12935573. doi:10.1016/s1344-6223(02)00096-2
- ↑ Smets G, Bronselaer K, De Munnynck K, De Feyter K, Van de Voorde W, Sabbe M (agosto de 2005). «Amphetamine toxicity in the emergency department». European Journal of Emergency Medicine. 12 (4): 193–197. PMID 16034267. doi:10.1097/00063110-200508000-00010
- ↑ Lora-Tamayo C, Tena T, Rodríguez A, Moreno D, Sancho JR, Enseñat P, Muela F (março de 2004). «The designer drug situation in Ibiza». Forensic Science International. 140 (2–3): 195–206. PMID 15036441. doi:10.1016/j.forsciint.2003.11.021
- ↑ Dams R, De Letter EA, Mortier KA, Cordonnier JA, Lambert WE, Piette MH, et al. (1 de julho de 2003). «Fatality due to combined use of the designer drugs MDMA and PMA: a distribution study». Journal of Analytical Toxicology. 27 (5): 318–322. PMID 12908947. doi:10.1093/jat/27.5.318

- ↑ Caldicott DG, Edwards NA, Kruys A, Kirkbride KP, Sims DN, Byard RW, Prior M, Irvine RJ (2003). «Dancing with "death": p-methoxyamphetamine overdose and its acute management». Journal of Toxicology. Clinical Toxicology. 41 (2): 143–154. PMID 12733852. doi:10.1081/CLT-120019130
- ↑ a b Rothman RB, Baumann MH, Dersch CM, Romero DV, Rice KC, Carroll FI, Partilla JS (janeiro de 2001). «Amphetamine-type central nervous system stimulants release norepinephrine more potently than they release dopamine and serotonin». Synapse. 39 (1): 32–41. PMID 11071707. doi:10.1002/1098-2396(20010101)39:1<32::AID-SYN5>3.0.CO;2-3
- ↑ a b Baumann MH, Partilla JS, Lehner KR, Thorndike EB, Hoffman AF, Holy M, Rothman RB, Goldberg SR, Lupica CR, Sitte HH, Brandt SD, Tella SR, Cozzi NV, Schindler CW (2013). «Powerful cocaine-like actions of 3,4-methylenedioxypyrovalerone (MDPV), a principal constituent of psychoactive 'bath salts' products». Neuropsychopharmacology. 38 (4): 552–562. PMC 3572453
 . PMID 23072836. doi:10.1038/npp.2012.204
. PMID 23072836. doi:10.1038/npp.2012.204
- ↑ a b Baumann MH, Ayestas MA, Partilla JS, Sink JR, Shulgin AT, Daley PF, Brandt SD, Rothman RB, Ruoho AE, Cozzi NV (2012). «The designer methcathinone analogs, mephedrone and methylone, are substrates for monoamine transporters in brain tissue». Neuropsychopharmacology. 37 (5): 1192–1203. PMC 3306880
 . PMID 22169943. doi:10.1038/npp.2011.304
. PMID 22169943. doi:10.1038/npp.2011.304
- ↑ a b c d e f «Dopamine-releasing agents». Dopamine Transporters: Chemistry, Biology and Pharmacology. Hoboken [NJ]: Wiley. Julho de 2008. pp. 305–320. ISBN 978-0-470-11790-3. OCLC 181862653. OL 18589888W
- ↑ a b c d Vekariya, Rakesh (2012). «Towards Understanding the Mechanism of Action of Abused Cathinones». VCU Theses and Dissertations. doi:10.25772/AR93-7024
- ↑ a b «Drug Discrimination and Mechanisms of Drug Action». Drug Discrimination. [S.l.]: Wiley. 5 de agosto de 2011. pp. 183–216. ISBN 978-0-470-43352-2. doi:10.1002/9781118023150.ch6
- ↑ Wee S, Anderson KG, Baumann MH, Rothman RB, Blough BE, Woolverton WL (maio de 2005). «Relationship between the serotonergic activity and reinforcing effects of a series of amphetamine analogs». The Journal of Pharmacology and Experimental Therapeutics. 313 (2): 848–854. PMID 15677348. doi:10.1124/jpet.104.080101
- ↑ a b Forsyth, Andrea N (22 de maio de 2012). «Synthesis and Biological Evaluation of Rigid Analogues of Methamphetamines». ScholarWorks@UNO. Consultado em 4 de novembro de 2024
- ↑ Solis E, Partilla JS, Sakloth F, Ruchala I, Schwienteck KL, De Felice LJ, Eltit JM, Glennon RA, Negus SS, Baumann MH (setembro de 2017). «N-Alkylated Analogs of 4-Methylamphetamine (4-MA) Differentially Affect Monoamine Transporters and Abuse Liability». Neuropsychopharmacology. 42 (10): 1950–1961. PMC 5561352
 . PMID 28530234. doi:10.1038/npp.2017.98
. PMID 28530234. doi:10.1038/npp.2017.98
- ↑ Sakloth, Farhana. Psychoactive synthetic cathinones (or 'bath salts'): Investigation of mechanisms of action (Tese). doi:10.25772/AY8R-PW77
- ↑ a b Fitzgerald LR, Gannon BM, Walther D, Landavazo A, Hiranita T, Blough BE, Baumann MH, Fantegrossi WE (março de 2024). «Structure-activity relationships for locomotor stimulant effects and monoamine transporter interactions of substituted amphetamines and cathinones». Neuropharmacology. 245. 109827 páginas. PMID 38154512. doi:10.1016/j.neuropharm.2023.109827
- ↑ a b Nicole, Lauren (2022). «In vivo Structure-Activity Relationships of Substituted Amphetamines and Substituted Cathinones». ProQuest. Consultado em 5 de dezembro de 2024
- ↑ Baumann MH, Walters HM, Niello M, Sitte HH (2018). «Neuropharmacology of Synthetic Cathinones». Handb Exp Pharmacol. Handbook of Experimental Pharmacology. 252: 113–142. ISBN 978-3-030-10560-0. PMC 7257813
 . PMID 30406443. doi:10.1007/164_2018_178
. PMID 30406443. doi:10.1007/164_2018_178
- ↑ a b Blough BE, Decker AM, Landavazo A, Namjoshi OA, Partilla JS, Baumann MH, Rothman RB (março de 2019). «The dopamine, serotonin and norepinephrine releasing activities of a series of methcathinone analogs in male rat brain synaptosomes». Psychopharmacology. 236 (3): 915–924. PMC 6475490
 . PMID 30341459. doi:10.1007/s00213-018-5063-9
. PMID 30341459. doi:10.1007/s00213-018-5063-9
- ↑ Shalabi, Abdelrahman R. Structure-Activity Relationship Studies of Bupropion and Related 3-Substituted Methcathinone Analogues at Monoamine Transporters (Tese). doi:10.25772/M4E1-3549
- ↑ a b Walther D, Shalabi AR, Baumann MH, Glennon RA (janeiro de 2019). «Systematic Structure-Activity Studies on Selected 2-, 3-, and 4-Monosubstituted Synthetic Methcathinone Analogs as Monoamine Transporter Releasing Agents». ACS Chem Neurosci. 10 (1): 740–745. PMC 8269283
 . PMID 30354055. doi:10.1021/acschemneuro.8b00524
. PMID 30354055. doi:10.1021/acschemneuro.8b00524
- ↑ a b Bonano JS, Banks ML, Kolanos R, Sakloth F, Barnier ML, Glennon RA, Cozzi NV, Partilla JS, Baumann MH, Negus SS (maio de 2015). «Quantitative structure-activity relationship analysis of the pharmacology of para-substituted methcathinone analogues». Br J Pharmacol. 172 (10): 2433–2444. PMC 4409897
 . PMID 25438806. doi:10.1111/bph.13030
. PMID 25438806. doi:10.1111/bph.13030
- ↑ Rothman RB, Baumann MH (outubro de 2003). «Monoamine transporters and psychostimulant drugs». Eur J Pharmacol. 479 (1–3): 23–40. PMID 14612135. doi:10.1016/j.ejphar.2003.08.054
- ↑ Rothman RB, Baumann MH (2006). «Therapeutic potential of monoamine transporter substrates». Current Topics in Medicinal Chemistry. 6 (17): 1845–1859. PMID 17017961. doi:10.2174/156802606778249766
- ↑ Menon MK, Tseng LF, Loh HH (maio de 1976). «Pharmacological evidence for the central serotonergic effects of monomethoxyamphetamines». The Journal of Pharmacology and Experimental Therapeutics. 197 (2): 272–279. PMID 946817. doi:10.1016/S0022-3565(25)30506-9
- ↑ a b Hitzemann RJ, Loh HH, Domino EF (outubro de 1971). «Effect of para-methoxyamphetamine on catecholamine metabolism in the mouse brain». Life Sciences. 10 (19 Pt. 1): 1087–1095. PMID 5132700. doi:10.1016/0024-3205(71)90227-x
- ↑ a b Tseng LF, Menon MK, Loh HH (maio de 1976). «Comparative actions of monomethoxyamphetamines on the release and uptake of biogenic amines in brain tissue». The Journal of Pharmacology and Experimental Therapeutics. 197 (2): 263–271. PMID 1271280. doi:10.1016/S0022-3565(25)30505-7
- ↑ a b c d Simmler LD, Rickli A, Hoener MC, Liechti ME (abril de 2014). «Monoamine transporter and receptor interaction profiles of a new series of designer cathinones». Neuropharmacology. 79: 152–160. PMID 24275046. doi:10.1016/j.neuropharm.2013.11.008
- ↑ Matsumoto T, Maeno Y, Kato H, Seko-Nakamura Y, Monma-Ohtaki J, Ishiba A, Nagao M, Aoki Y (agosto de 2014). «5-hydroxytryptamine- and dopamine-releasing effects of ring-substituted amphetamines on rat brain: a comparative study using in vivo microdialysis». Eur Neuropsychopharmacol. 24 (8): 1362–1370. PMID 24862256. doi:10.1016/j.euroneuro.2014.04.009
- ↑ a b c Daws LC, Irvine RJ, Callaghan PD, Toop NP, White JM, Bochner F (agosto de 2000). «Differential behavioural and neurochemical effects of para-methoxyamphetamine and 3,4-methylenedioxymethamphetamine in the rat». Progress in Neuro-Psychopharmacology & Biological Psychiatry. 24 (6): 955–977. PMID 11041537. doi:10.1016/S0278-5846(00)00113-5
- ↑ Green AL, El Hait MA (abril de 1980). «p-Methoxyamphetamine, a potent reversible inhibitor of type-A monoamine oxidase in vitro and in vivo». The Journal of Pharmacy and Pharmacology. 32 (4): 262–266. PMID 6103055. doi:10.1111/j.2042-7158.1980.tb12909.x
- ↑ a b Ask AL, Fagervall I, Ross SB (setembro de 1983). «Selective inhibition of monoamine oxidase in monoaminergic neurons in the rat brain». Naunyn-Schmiedeberg's Archives of Pharmacology. 324 (2): 79–87. PMID 6646243. doi:10.1007/BF00497011
- ↑ Reyes-Parada M, Iturriaga-Vasquez P, Cassels BK (2019). «Amphetamine Derivatives as Monoamine Oxidase Inhibitors». Front Pharmacol. 10. 1590 páginas. PMC 6989591
 . PMID 32038257. doi:10.3389/fphar.2019.01590
. PMID 32038257. doi:10.3389/fphar.2019.01590
- ↑ Galloway JH, Forrest AR (setembro de 2002). «Caveat Emptor: Death involving the use of 4-methoxyamphetamine». Journal of Clinical Forensic Medicine. 9 (3). 160 páginas. PMID 15274949. doi:10.1016/S1353-1131(02)00043-3
- ↑ Lamberth PG, Ding GK, Nurmi LA (abril de 2008). «Fatal paramethoxy-amphetamine (PMA) poisoning in the Australian Capital Territory». The Medical Journal of Australia. 188 (7). 426 páginas. PMID 18393753. doi:10.5694/j.1326-5377.2008.tb01695.x