Matriz mitocondrial
Na mitocôndria, a matriz é o espaço dentro da membrana interna. Também pode ser chamado de fluido mitocondrial. A palavra "matriz" vem do fato de que esse espaço é viscoso, comparado ao citoplasma relativamente aquoso. A matriz mitocondrial contém o DNA mitocondrial, ribossomos, enzimas solúveis, pequenas moléculas orgânicas, cofatores de nucleotídeos e íons inorgânicos. As enzimas na matriz facilitam as reações responsáveis pela produção de ATP, como o ciclo do ácido cítrico, a fosforilação oxidativa, a oxidação do piruvato e a beta oxidação dos ácidos graxos.[1]
A composição da matriz baseada em suas estruturas e conteúdos produz um ambiente que permite que as vias anabólicas e catabólicas ocorram favoravelmente. A cadeia de transporte de elétrons e as enzimas na matriz desempenham um papel importante no ciclo do ácido cítrico e na fosforilação oxidativa. O ciclo do ácido cítrico produz NADH e FADH2 por oxidação que serão reduzidos na fosforilação oxidativa para produzir ATP.[2][3]
O compartimento citosólico, espaço intermembranar, tem um conteúdo aquoso:proteína mais alto de cerca de 3,8 μL/mg de proteína em relação ao que ocorre na matriz mitocondrial, onde tais níveis normalmente estão próximos de 0,8 μL/mg de proteína.[4] Não se sabe como as mitocôndrias mantêm o equilíbrio osmótico através da membrana mitocondrial interna, embora a membrana contenha aquaporinas que se acredita serem condutores para o transporte regulado de água. A matriz mitocondrial tem um pH de cerca de 7,8, que é superior ao pH do espaço intermembranar da mitocôndria, que é em torno de 7,0–7,4.[5] O DNA mitocondrial foi descoberto por Nash e Margit em 1963. Uma ou muitas fitas duplas de DNA, principalmente circulares, estão presentes na matriz mitocondrial. O DNA mitocondrial representa 1% do DNA total de uma célula. É rico em guanina e citosina e, em humanos, é de origem materna. As mitocôndrias dos mamíferos têm ribossomos 55S.[6]
Composição
Metabólitos
A matriz hospeda uma grande variedade de metabólitos envolvidos em processos dentro da matriz. O ciclo do ácido cítrico envolve acil-CoA, piruvato, acetil-CoA, citrato, isocitrato, α-cetoglutarato, succinil-CoA, fumarato, succinato, L-malato e oxaloacetato.[2] O ciclo da ureia faz uso de L-ornitina, fosfato de carbamoil e L-citrulina.[4] A cadeia de transporte de elétrons oxida as coenzimas NADH e FADH2 . A síntese de proteínas faz uso de DNA mitocondrial, RNA e tRNA.[5] A regulação dos processos faz uso de íons (Ca2+/K+/Mg+).[7] Metabólitos adicionais presentes na matriz são CO2, H2O, O2 , ATP, ADP e Pi.[1]
Enzimas
Enzimas de processos que ocorrem na matriz. O ciclo do ácido cítrico é facilitado pela piruvato desidrogenase, citrato sintase, aconitase, isocitrato desidrogenase, α-cetoglutarato desidrogenase, succinil-CoA sintetase, fumarase e malato desidrogenase.[2] O ciclo da ureia é facilitado pela carbamoil fosfato sintetase I e pela ornitina transcarbamilase.[4] A β-oxidação utiliza piruvato carboxilase, acil-CoA desidrogenase e β-cetotiolase.[1] A produção de aminoácidos é facilitada pelas transaminases.[8] O metabolismo dos aminoácidos é mediado por proteases, como a protease de pré-sequência.[9]
Componentes da membrana interna
A membrana interna é uma bicamada fosfolipídica que contém os complexos de fosforilação oxidativa. que contém a cadeia de transporte de elétrons encontrada nas cristas da membrana interna e consiste em quatro complexos de proteínas e ATP sintase. Esses complexos são o complexo I (NADH:coenzima Q oxidorredutase), o complexo II (succinato:coenzima Q oxidorredutase), o complexo III (coenzima Q: citocromo c oxidorredutase) e o complexo IV (citocromo c oxidase).[7]
Controle da membrana interna sobre a composição da matriz
A cadeia de transporte de elétrons é responsável por estabelecer um pH e um gradiente eletroquímico que facilita a produção de ATP através do bombeamento de prótons. O gradiente também fornece controle da concentração de íons como Ca2+ impulsionada pelo potencial da membrana mitocondrial.[1] A membrana permite que apenas moléculas não polares, como CO2 e O2, e pequenas moléculas polares não carregadas, como H2O, entrem na matriz. As moléculas entram e saem da matriz mitocondrial por meio de proteínas de transporte e transportadores de íons. As moléculas são então capazes de deixar as mitocôndrias através da porina.[10] Essas características atribuídas permitem o controle sobre as concentrações de íons e metabólitos necessários para a regulação e determinam a taxa de produção de ATP.[11][12]
Processos
Ciclo do ácido cítrico
Após a glicólise, o ciclo do ácido cítrico é ativado pela produção de acetil-CoA. A oxidação do piruvato pela piruvato desidrogenase na matriz produz CO 2, acetil-CoA e NADH. A beta oxidação de ácidos graxos serve como uma via catabólica alternativa que produz acetil-CoA, NADH e FADH2.[1] A produção de acetil-CoA inicia o ciclo do ácido cítrico enquanto as coenzimas produzidas são utilizadas na cadeia de transporte de elétrons.[12]
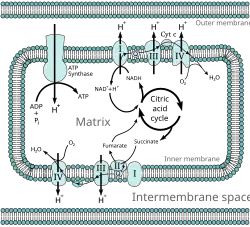
Todas as enzimas do ciclo do ácido cítrico estão na matriz (por exemplo, citrato sintase, isocitrato desidrogenase, α-cetoglutarato desidrogenase, fumarase e malato desidrogenase), exceto a succinato desidrogenase, que está na membrana interna e faz parte do complexo proteico II na cadeia de transporte de elétrons . O ciclo produz coenzimas NADH e FADH 2 por meio da oxidação de carbonos em dois ciclos. A oxidação de NADH e FADH 2 produz GTP a partir da succinil-CoA sintetase.[2]
Fosforilação oxidativa
NADH e FADH2 são produzidos na matriz ou transportados através de porinas e proteínas de transporte para sofrer oxidação por fosforilação oxidativa.[1] NADH e FADH 2 sofrem oxidação na cadeia de transporte de elétrons transferindo elétrons para regenerar NAD+ e FAD. Os prótons são puxados para o espaço intermembrana pela energia dos elétrons que passam pela cadeia de transporte de elétrons. Quatro elétrons são finalmente aceitos pelo oxigênio na matriz para completar a cadeia de transporte de elétrons. Os prótons retornam à matriz mitocondrial através da proteína ATP sintase. A energia é usada para girar a ATP sintase, o que facilita a passagem de um próton, produzindo ATP. Uma diferença de pH entre a matriz e o espaço intermembranar cria um gradiente eletroquímico pelo qual a ATP sintase pode passar um próton para a matriz de forma favorável.[7]
Ciclo da ureia
As duas primeiras etapas do ciclo da ureia ocorrem dentro da matriz mitocondrial das células do fígado e dos rins. Na primeira etapa, a amônia é convertida em fosfato de carbamoil por meio do investimento de duas moléculas de ATP. Esta etapa é facilitada pela carbamoil fosfato sintetase I. A segunda etapa facilitada pela ornitina transcarbamilase converte carbamoil fosfato e ornitina em citrulina. Após essas etapas iniciais, o ciclo da ureia continua no espaço da membrana interna até que a ornitina entre novamente na matriz através de um canal de transporte para continuar as primeiras etapas dentro da matriz.[13]
Transaminação
O α-cetoglutarato e o oxaloacetato podem ser convertidos em aminoácidos dentro da matriz através do processo de transaminação. Essas reações são facilitadas pelas transaminases para produzir aspartato e asparagina a partir do oxaloacetato. A transaminação do α-cetoglutarato produz glutamato, prolina e arginina. Esses aminoácidos são então usados dentro da matriz ou transportados para o citosol para produzir proteínas.[8][14]
Regulação
A regulação dentro da matriz é controlada principalmente pela concentração de íons, concentração de metabólitos e carga energética. A disponibilidade de íons como Ca2+ controla várias funções do ciclo do ácido cítrico. na matriz ativa a piruvato desidrogenase, a isocitrato desidrogenase e a α-cetoglutarato desidrogenase, o que aumenta a taxa de reação no ciclo.[15] A concentração de intermediários e coenzimas na matriz também aumenta ou diminui a taxa de produção de ATP devido aos efeitos anapleróticos e catapleróticos. NADH pode atuar como um inibidor de α-cetoglutarato, isocitrato desidrogenase, citrato sintase e piruvato desidrogenase. A concentração de oxaloacetato em particular é mantida baixa, de modo que quaisquer flutuações nessas concentrações servem para impulsionar o ciclo do ácido cítrico.[2] A produção de ATP também serve como um meio de regulação, agindo como um inibidor da isocitrato desidrogenase, da piruvato desidrogenase, dos complexos de proteínas da cadeia de transporte de elétrons e da ATP sintase. O ADP atua como um ativador.[1]
Síntese de proteínas
A mitocôndria contém seu próprio conjunto de DNA usado para produzir proteínas encontradas na cadeia de transporte de elétrons. O DNA mitocondrial codifica apenas cerca de treze proteínas que são usadas no processamento de transcrições mitocondriais, proteínas ribossômicas, RNA ribossômico, RNA de transferência e subunidades de proteínas encontradas nos complexos de proteínas da cadeia de transporte de elétrons.[16][17]
Ver também
Notas
- Este artigo foi inicialmente traduzido, total ou parcialmente, do artigo da Wikipédia em inglês cujo título é «Mitochondrial matrix».
Referências
- ↑ a b c d e f g Voet, Donald; Voet, Judith; Pratt, Charlotte (2013). Fundamentals of Biochemistry Life at the Molecular Level. New York City: John Wiley & Sons, Inc. pp. 582–584. ISBN 978-1118129180
- ↑ a b c d e Stryer, L; Berg, J; Tymoczko, JL (2002). Biochemistry. San Francisco: W.H. Freeman. pp. 509–527, 569–579, 614–616, 638–641, 732–735, 739–748, 770–773. ISBN 978-0-7167-4684-3
- ↑ Mitchell, Peter; Moyle, Jennifer (14 de janeiro de 1967). «Chemiosmotic Hypothesis of Oxidative Phosphorylation». Nature (em inglês). 213 (5072): 137–139. Bibcode:1967Natur.213..137M. PMID 4291593. doi:10.1038/213137a0
- ↑ a b c Soboll, S; Scholz, R; Freisl, M; Elbers, R; Heldt, H.W. (1976). Distribution of metabolites between mitochondria and cytosol of perfused liver. New york: Elsevier. pp. 29–40. ISBN 978-0-444-10925-5
- ↑ a b Porcelli, Anna Maria; Ghelli, Anna; Zanna, Claudia; Pinton, Paolo; Rizzuto, Rosario; Rugolo, Michela (28 de janeiro de 2005). «pH difference across the outer mitochondrial membrane measured with a green fluorescent protein mutant». Biochemical and Biophysical Research Communications. 326 (4): 799–804. PMID 15607740. doi:10.1016/j.bbrc.2004.11.105
- ↑ Ahmad, S. I. (2019). Handbook of Mitochondrial Dysfunction 1 ed. [S.l.: s.n.] ISBN 9781032178004
- ↑ a b c Dimroth, P.; Kaim, G.; Matthey, U. (1 de janeiro de 2000). «Crucial role of the membrane potential for ATP synthesis by F(1)F(o) ATP synthases». The Journal of Experimental Biology. 203 (Pt 1): 51–59. Bibcode:2000JExpB.203...51D. ISSN 0022-0949. PMID 10600673. doi:10.1242/jeb.203.1.51
- ↑ a b Karmen, A.; Wroblewski, F.; Ladue, J. S. (1 de janeiro de 1955). «Transaminase activity in human blood». The Journal of Clinical Investigation. 34 (1): 126–131. ISSN 0021-9738. PMC 438594
 . PMID 13221663. doi:10.1172/JCI103055
. PMID 13221663. doi:10.1172/JCI103055
- ↑ King, John V.; Liang, Wenguang G.; Scherpelz, Kathryn P.; Schilling, Alexander B.; Meredith, Stephen C.; Tang, Wei-Jen (8 de julho de 2014). «Molecular basis of substrate recognition and degradation by human presequence protease». Structure. 22 (7): 996–1007. ISSN 1878-4186. PMC 4128088
 . PMID 24931469. doi:10.1016/j.str.2014.05.003
. PMID 24931469. doi:10.1016/j.str.2014.05.003
- ↑ Alberts, Bruce; Johnson, Alexander; Lewis, julian; Roberts, Keith; Peters, Walter; Raff (1994). Molecular Biology of the Cell. New york: Garland Publishing Inc. ISBN 978-0-8153-3218-3
- ↑ Anderson, S.; Bankier, A. T.; Barrell, B. G.; de Bruijn, M. H. L.; Coulson, A. R.; Drouin, J.; Eperon, I. C.; Nierlich, D. P.; Roe, B. A. (9 de abril de 1981). «Sequence and organization of the human mitochondrial genome». Nature (em inglês). 290 (5806): 457–465. Bibcode:1981Natur.290..457A. PMID 7219534. doi:10.1038/290457a0
- ↑ a b Iuchi, S.; Lin, E. C. C. (1 de julho de 1993). «Adaptation of Escherichia coli to redox environments by gene expression». Molecular Microbiology (em inglês). 9 (1): 9–15. ISSN 1365-2958. PMID 8412675. doi:10.1111/j.1365-2958.1993.tb01664.x
- ↑ Tuchman, Mendel; Plante, Robert J. (1 de janeiro de 1995). «Mutations and polymorphisms in the human ornithine transcarbamylase gene: Mutation update addendum». Human Mutation (em inglês). 5 (4): 293–295. ISSN 1098-1004. PMID 7627182. doi:10.1002/humu.1380050404

- ↑ Kirsch, Jack F.; Eichele, Gregor; Ford, Geoffrey C.; Vincent, Michael G.; Jansonius, Johan N.; Gehring, Heinz; Christen, Philipp (15 de abril de 1984). «Mechanism of action of aspartate aminotransferase proposed on the basis of its spatial structure». Journal of Molecular Biology. 174 (3): 497–525. PMID 6143829. doi:10.1016/0022-2836(84)90333-4
- ↑ Denton, Richard M.; Randle, Philip J.; Bridges, Barbara J.; Cooper, Ronald H.; Kerbey, Alan L.; Pask, Helen T.; Severson, David L.; Stansbie, David; Whitehouse, Susan (1 de outubro de 1975). «Regulation of mammalian pyruvate dehydrogenase». Molecular and Cellular Biochemistry (em inglês). 9 (1): 27–53. ISSN 0300-8177. PMID 171557. doi:10.1007/BF01731731
- ↑ Fox, Thomas D. (1 de dezembro de 2012). «Mitochondrial Protein Synthesis, Import, and Assembly». Genetics. 192 (4): 1203–1234. ISSN 0016-6731. PMC 3512135
 . PMID 23212899. doi:10.1534/genetics.112.141267
. PMID 23212899. doi:10.1534/genetics.112.141267
- ↑ Grivell, L.A.; Pel, H.J. (1994). «Protein synthesis in mitochondria» (PDF). Mol. Biol. Rep. 19 (3): 183–194. PMID 7969106. doi:10.1007/bf00986960