História da bioquímica
A história da bioquímica pode ser considerada como tendo comecado com os antigos Gregos, que estavam interessados na composição e nos processos da vida, embora a bioquímica enquanto disciplina científica específica tenha tido o seu início em princípios do século XIX.[1] Alguns defenderam que o começo da bioquímica pode ter tido por base a descoberta da primeira enzima, a diastase (hoje chamada amilase), em 1833 por Anselme Payen,[2] enquanto outros consideraram que a origem da bioquímica deu-se com a primeirasdemonstração de um processo bioquímico complexo, a fermentação alcoólica em extratos livres de células por Eduard Buchner.[3][4] Alguns também podem apontar para o influente trabalho de Justus von Liebig de 1842, Animal chemistry, or, Organic chemistry in its applications to physiology and pathology (Química animal, ou, Química orgânica nas suas aplicações à fisiologia e patologia), que apresentou uma teoria química do metabolismo,[1] ou ainda mais cedo para os estudos do século XVIII sobre fermentação e respiração por Antoine Lavoisier.[5][6]
O próprio termo bioquímica deriva da forma combinada bio-, que significa 'vida', e química. A palavra é registada pela primeira vez em inglês em 1848,[7] enquanto em 1877, Felix Hoppe-Seyler usou o termo (Biochemie em alemão) no prefácio da primeira edição do Zeitschrift für Physiologische Chemie (Jornal de Química Fisiológica) como um sinónimo de química fisiológica e defendeu a criação de institutos dedicados aos seus estudos.[8][9] No entanto, várias fontes citam o químico alemão Carl Neuberg como tendo cunhado o termo para a nova disciplina em 1903,[10][11] e alguns creditam-no a Franz Hofmeister.[12]
O objeto de estudo na bioquímica são os processos químicos em organismos vivos, e a sua história envolve a descoberta e compreensão dos componentes complexos da vida e o esclarecimento das vias dos processos bioquímicos. Grande parte da bioquímica lida com as estruturas e funções de componentes celulares, como proteínas, carboidratos, lípidos, ácidos nucleicos e outras biomoléculas; as suas vias metabólicas e o fluxo de energia química através do metabolismo; como as moléculas biológicas dão origem aos processos que ocorrem dentro das células vivas; foca-se também nos processos bioquímicos envolvidos no controlo do fluxo de informação através da sinalização bioquímica, e como estes se relacionam com o funcionamento de organismos inteiros. Nos últimos 40 anos esta área científica teve sucesso em explicar processos vivos, de tal forma que agora quase todas as áreas das ciências da vida, desde a botânica à medicina, estão envolvidas na investigação bioquímica.
Entre o vasto número de diferentes biomoléculas, muitas são moléculas complexas e grandes (chamadas polímeros), que são compostas por subunidades repetidas semelhantes (chamadas monómeros). Cada classe de biomolécula polimérica tem um conjunto diferente de tipos de subunidades. Por exemplo, uma proteína é um polímero cujas subunidades são selecionadas a partir de um conjunto de vinte ou mais aminoácidos, os carboidratos são formados a partir de açúcares conhecidos como monossacarídeos, oligossacarídeos e polissacarídeos, os lípidos são formados a partir de ácidos gordos e gliceróis, e os ácidos nucleicos são formados a partir de nucleotídeos. A bioquímica estuda as propriedades químicas de moléculas biológicas importantes, como as proteínas, e em particular a química das reações catalisadas por enzimas. A bioquímica do metabolismo celular e do sistema endócrino tem sido extensivamente descrita. Outras áreas da bioquímica incluem o código genético (DNA, RNA), a síntese proteica, o transporte pela membrana celular e a transdução de sinal.
Proto-bioquímica
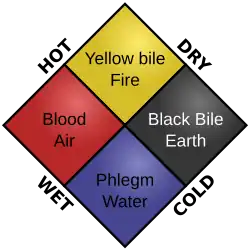
De certo modo, o estudo da bioquímica pode ser considerado como tendo começado em tempos antigos, por exemplo, quando a biologia começou pela primeira vez a interessar a sociedade—como os antigos Chineses desenvolveram um sistema de medicina baseado no yin e yang, e também nas cinco fases,[13] que resultaram ambas de interesses alquímicos e biológicos. O seu início na antiga cultura Indiana estava ligado a um interesse pela medicina, ao desenvolverem o conceito de três humores que eram semelhantes aos quatro humores dos Gregos (ver humorismo). Eles também se aprofundaram no interesse de que os corpos eram compostos por tecidos. A conceção dos antigos Gregos sobre bioquímica estava ligada às suas ideias sobre matéria e doença, onde se pensava que a boa saúde provinha de um equilíbrio dos quatro elementos e dos quatro humores no corpo humano.[14] Tal como na maioria das ciências iniciais, o mundo Islâmico contribuiu significativamente para os primeiros avanços biológicos, bem como para os avanços alquímicos; especialmente com a introdução de ensaios clínicos e farmacologia clínica apresentados no O Cânone da Medicina de Avicena.[15] No lado da química, os primeiros avanços foram fortemente atribuídos à exploração de interesses alquímicos, mas também incluíram: metalurgia, o método científico e as primeiras teorias do atomismo. Em tempos mais recentes, o estudo da química foi marcado por marcos como o desenvolvimento da tabela periódica de Mendeleev, o modelo atómico de Dalton e a teoria da conservação da massa. Esta última menção tem a maior importância das três, devido ao facto de esta lei entrelaçar a química com a termodinâmica de forma intercalada.
Enzimas

Já no final do século XVIII e início do século XIX, a digestão da carne por secreções estomacais[16] e a conversão de amido em açúcares por extratos de plantas e saliva eram conhecidas. No entanto, o mecanismo pelo qual isso ocorria não tinha sido identificado.[17] No século XIX, ao estudar a fermentação do açúcar em álcool por levedura, Louis Pasteur concluiu que essa fermentação era catalisada por uma força vital contida nas células de levedura chamada fermentos, que ele pensava funcionar apenas dentro de organismos vivos. Ele escreveu que "a fermentação alcoólica é um ato correlacionado com a vida e organização das células de levedura, e não com a morte ou putrefação das células."[18]
Em 1833 Anselme Payen descobriu a primeira enzima, a diastase,[19] e em 1878 o fisiologista alemão Wilhelm Kühne (1837–1900) cunhou o termo enzima, que vem do grego ενζυμον 'em levedura', para descrever este processo. A palavra enzima foi usada mais tarde para se referir a substâncias não-vivas, como a pepsina, e a palavra fermento foi usada para se referir à atividade química produzida por organismos vivos.
Em 1897 Eduard Buchner começou a estudar a capacidade de extratos de levedura fermentarem açúcar, apesar da ausência de células de levedura vivas. Numa série de experiências na Universidade de Berlim, ele descobriu que o açúcar era fermentado mesmo quando não havia células de levedura vivas na mistura.[20] Ele chamou à enzima que efetuava a fermentação da sacarose de zimase.[21] Em 1907 ele recebeu o Prémio Nobel da Química "pela sua investigação bioquímica e a sua descoberta da fermentação livre de células". Seguindo o exemplo de Buchner; as enzimas são geralmente nomeadas de acordo com a reação que realizam. Tipicamente, o sufixo -ase é adicionado ao nome do substrato (e.g., a lactase é a enzima que cliva a lactose) ou ao tipo de reação (e.g., a DNA polimerase forma polímeros de DNA).
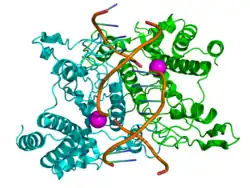
Tendo demonstrado que as enzimas podiam funcionar fora de uma célula viva, o próximo passo foi determinar a sua natureza bioquímica. Muitos investigadores iniciais notaram que a atividade enzimática estava associada a proteínas, mas vários cientistas (como o laureado com o Nobel Richard Willstätter) argumentaram que as proteínas eram meramente transportadoras para as verdadeiras enzimas e que as proteínas per se eram incapazes de catálise. No entanto, em 1926, James B. Sumner demonstrou que a enzima urease era uma proteína pura e a cristalizou; Sumner fez o mesmo para a enzima catalase em 1937. A conclusão de que proteínas puras podem ser enzimas foi definitivamente provada por Northrop e Stanley, que trabalharam nas enzimas digestivas pepsina (1930), tripsina e quimiotripsina. Estes três cientistas foram premiados com o Prémio Nobel da Química de 1946.[22]
Esta descoberta, de que as enzimas podiam ser cristalizadas, significou que os cientistas podiam eventualmente resolver as suas estruturas por cristalografia de raios-X. Isto foi feito pela primeira vez para a lisozima, uma enzima encontrada em lágrimas, saliva e clara de ovo que digere o revestimento de algumas bactérias; a estrutura foi resolvida por um grupo liderado por David Chilton Phillips e publicada em 1965.[23] Esta estrutura de alta resolução da lisozima marcou o início do campo da biologia estrutural e o esforço para entender como as enzimas funcionam a um nível atómico em detalhe.
Referências
- ↑ a b Ton van Helvoort (2000). Arne Hessenbruch, ed. Reader's Guide to the History of Science. [S.l.]: Fitzroy Dearborn Publishing. p. 81. ISBN 978-1-134-26294-6
- ↑ Hunter (2000), p. 75.
- ↑ Jacob Darwin Hamblin (2005). Science in the Early Twentieth Century: An Encyclopedia. [S.l.]: ABC-CLIO. p. 26. ISBN 978-1-85109-665-7
- ↑ Hunter (2000), pp. 96–98.
- ↑ Clarence Peter Berg (1980). The University of Iowa and Biochemistry from Their Beginnings. [S.l.]: Iowa Biochemistry. pp. 1–2. ISBN 978-0-87414-014-9
- ↑ Frederic Lawrence Holmes (1987). Lavoisier and the Chemistry of Life: An Exploration of Scientific Creativity. [S.l.]: University of Wisconsin Press. p. xv. ISBN 978-0-299-09984-8
- ↑ «biochemistry, n.». OED Online. Oxford University Press. Consultado em 8 de abril de 2015
- ↑ Anne-Katrin Ziesak; Hans-Robert Cram (18 de outubro de 1999). Walter de Gruyter Publishers, 1749–1999. [S.l.]: Walter de Gruyter & Co. p. 169. ISBN 978-3-11-016741-2
- ↑ Horst Kleinkauf; Hans von Döhren; Lothar Jaenicke (1988). The Roots of Modern Biochemistry: Fritz Lippmann's Squiggle and its Consequences. [S.l.]: Walter de Gruyter & Co. p. 116. ISBN 978-3-11-085245-5
- ↑ Mark Amsler (1986). The Languages of Creativity: Models, Problem-solving, Discourse. [S.l.]: University of Delaware Press. p. 55. ISBN 978-0-87413-280-9
- ↑ Advances in Carbohydrate Chemistry and Biochemistry, Volume 70. [S.l.]: Academic Press. 28 de novembro de 2013. p. 36. ISBN 978-0-12-408112-3
- ↑ Koscak Maruyama (1988). Horst Kleinkauf; Hans von Döhren; Lothar Jaenickem, eds. The Roots of Modern Biochemistry: Fritz Lippmann's Squiggle and its Consequences. [S.l.]: Walter de Gruyter & Co. p. 43. ISBN 978-3-11-085245-5
- ↑ Magner. A History of Life Sciences. [S.l.: s.n.] p. 4
- ↑ W. F. Bynum; Roy Porter, eds. (20 de junho de 2013). Companion Encyclopedia of the History of Medicine. [S.l.]: Routledge. ISBN 978-1-136-11044-3
- ↑ Brater, D. Craig; Walter J. Daly (2000). «Clinical pharmacology in the Middle Ages: Principles that presage the 21st century». Clinical Pharmacology and Therapeutics. 67 (5): 447–450. PMID 10824622. doi:10.1067/mcp.2000.106465
- ↑ de Réaumur, RAF (1752). «Observations sur la digestion des Oiseaux». Histoire de l'Académie Royale des Sciences. 1752: 266, 461
- ↑ Williams, H. S. (1904) A History of Science: in Five Volumes. Volume IV: Modern Development of the Chemical and Biological Sciences Harper and Brothers (New York)
- ↑ Dubos J. (1951). «Louis Pasteur: Free Lance of Science, Gollancz. Quoted in Manchester K. L. (1995) Louis Pasteur (1822–1895)--chance and the prepared mind.». Trends Biotechnol. 13 (12): 511–515. PMID 8595136. doi:10.1016/S0167-7799(00)89014-9
- ↑ A. Payen and J.-F. Persoz (1833) "Mémoire sur la diastase, les principaux produits de ses réactions et leurs applications aux arts industriels" (Memória sobre a diastase, os principais produtos das suas reações e as suas aplicações às artes industriais), Annales de chimie et de physique, 2nd series, vol. 53, pages 73–92.
- ↑ Biografia do Laureado com o Nobel Eduard Buchner em http://nobelprize.org
- ↑ Texto da palestra do Nobel de 1907 de Eduard Buchner em http://nobelprize.org
- ↑ Laureados com o Prémio Nobel da Química de 1946 em http://nobelprize.org
- ↑ Blake CC, Koenig DF, Mair GA, North AC, Phillips DC, Sarma VR (1965). «Structure of hen egg-white lysozyme. A three-dimensional Fourier synthesis at 2 Angstrom resolution.». Nature. 206 (4986): 757–761. Bibcode:1965Natur.206..757B. PMID 5891407. doi:10.1038/206757a0