Guanidina
Guanidina
| |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||
 | |||||||||||
| Nomes | |||||||||||
| Nome IUPAC | Guanidine | ||||||||||
| |||||||||||
| |||||||||||
| |||||||||||
| |||||||||||
| Página de dados suplementares | |||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||
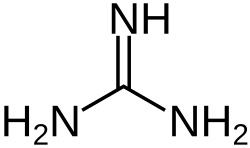
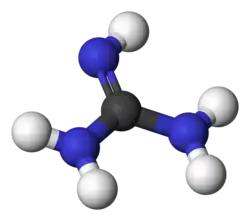
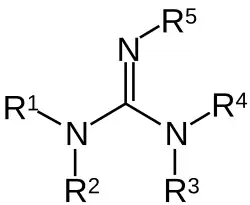
As guanidinas são uma espécie de substâncias puras cristalinas muito alcalinas, formadas a partir da oxidação da guanina. Se encontram de maneira natural na urina como um produto normal do metabolismo das proteínas. Não devem ser confundidas com a guanosina, uma das bases que formam o ADN. Possuem a fórmula genérica (R1R2N)(R3R4N)C=N-R5.
É a amidina do ácido amidocarbônico, ocorrendo naturalmente no suco de beterraba.
A guanidina propriamente dita é a mais simples das guanidinas e tem fórmula CH5N3. Se usa na fabricação de plásticos, borrachas e explosivos.
Obtenção
A guanidina propriamente dita foi primeiramente preparada em 1861 por A . Strecker, que oxidou guanina com ácido clorídrico e clorato de potássio. Pode também ser obtida por ação de iodeto de amônio sobre cianamida:
- CN•NH2 + NH4I → CN3H5•HI
Por aquecer ésteres de ácido orto-carbônico com amônia, mas de melhor maneira por aquecer tiocianato de amônio a 180° a 190°C, quando a tiouréia primeiro formada é convertida em tiocinato de guanidina.
- 2CS(NH2)2=HN → C(NH2)2•HCNS+H2S .
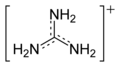
Cátion guanidínio
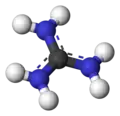
Com um pKa de 12.5, guanidina é protonada em condições fisiológicas, com uma carga +1. Este ácido conjugado de guanidina é chamado cátion guanidínio, [CH6N3]+.
-
-
-
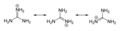
formas canônicas
Notáveis sais de guanidina incluem cloridrato de guanidina, o qual tem propriedades caotrópicas e é usado para denaturar proteínas. Empiricamente, o cloridrato guanidina é conhecido em denaturação de proteínas com uma relação linear entre concentração e energia livre de desprendimento. Outro sal é o tiocianato de guanidínio.
Aplicações
Derivados de guanidina têm sido usados em formulações de produtos para alisamento de cabelos.
Ligações externas
- GUANIDINE HYDROCHLORIDE - MSDS - www.jtbaker.com (em inglês)
- CN3H5 GUANIDINE - encyclopedia.jrank.org (em inglês)
Referências
Ver também
- Cloridrato de guanidina
- Tiocianato de guanidínio
- Nitrato de guanidina
- Carbonato de Guanidina