Tiocinato de guanidina
Tiocinato de guanidina
| |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||
| Nomes | |||||||||||||
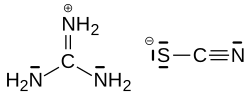
| Nome IUPAC | Tiocinato de guanidina | ||||||||||||
| |||||||||||||
| |||||||||||||
| |||||||||||||
| Página de dados suplementares | |||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||
O tiocianato de guanidina ou isotiocianato de guanidina (GITC) é um composto químico utilizado como desnaturante proteico em geral, sendo, portanto, um agente caotrópico, embora seja mais comumente usado como um protetor de ácido nucléico na extração de DNA e RNA das células.[1]
Usos
O tiocianato de guanidínio pode ser usado para desativar vírus, como o vírus influenza, no qual é mais utilizado, para que possa ser estudado com segurança. O tiocianato de guanidínio também é usado para lisar células e vírus em extrações de RNA e DNA, onde sua função, além de sua ação de lise, é impedir a atividade de enzimas RNase e enzimas DNase, desnaturando-as. Essas enzimas danificariam o extrato.
Um método comumente usado é a extração com tiocianato de guanidina-fenol-clorofórmio. Não é estritamente necessário usar fenol ou clorofórmio se extrair RNA para a analise de Northern blot ou DNA para análise de Southern blot porque a eletroforese em gel seguida de transferência para uma membrana separará o RNA/DNA das proteínas. Além do mais, como esses métodos usam sondas para se ligarem a seus conjugados, os peptídeos que passam pelo processo geralmente não oferecem interferências nas analises, a menos que um peptídeo seja uma RNase ou DNase, e somente se a enzima conseguir renaturar, o que não deve ocorrer se protocolos apropriados sejam aplicados. Uma possível exceção pode ser ao trabalhar com temperaturas extremófilas, porque algumas enzimas desses organismos podem permanecer estáveis sob circunstâncias extraordinárias.[2]
Referências
- ↑ «The hydration structure of guanidinium and thiocyanate ions: Implications for protein stability in aqueous solution»
- ↑ Shimomura, O; Masugi, T; Johnson, FH; Haneda, Y (março de 1978). «Properties and reaction mechanism of the bioluminescence system of the deep-sea shrimp Oplophorus gracilorostris.». Biochemistry. 17: 994–8. PMID 629957. doi:10.1021/bi00599a008