Nitrato de guanidina
Nitrato de guanidina
| |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
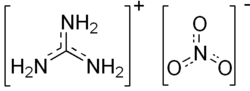 | |||||||||||||||
 | |||||||||||||||
| Nomes | |||||||||||||||
| Nome IUPAC | Nitrato de guanidinio | ||||||||||||||
| |||||||||||||||
| |||||||||||||||
| |||||||||||||||
| |||||||||||||||
| Página de dados suplementares | |||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||
O nitrato de guanidina, ou nitrato de guanidinio é um composto químico com a fórmula [C(NH2)3]NO3. É um sal incolor solúvel em água. É produzido em grande escala como combustível de alta energia usado como gerador de gás e aplicações de propelente sólido para foguetes.
Propriedades e produção
Embora seja o sal formado pela neutralização da guanidina com ácido nítrico, o nitrato de guanidina é produzido industrialmente pela reação da cianoguanidina com nitrato de amônio.[1]
Foi usado como um monopropelente em motores Jetex para aeromodelos, sendo atraente pelo fato de possuir um alto débito de gás e baixa temperatura de chama. Tem um impulso específico relativamente alto de 177 segundos (1,7 kN·s/kg).
A decomposição explosiva do nitrato de guanidina é dada pela seguinte equação: H6N4CO3(s)→ 3h2O(g) + 2 N2(g) + C(s)
Segurança
O composto é uma substância perigosa, sendo um explosivo e oxidante. Também é prejudicial para os olhos, pele e trato respiratório.[1]
Referências
- ↑ a b Thomas Güthner, Bernd Mertschenk and Bernd Schulz "Guanidine and Derivatives" in Ullmann's Encyclopedia of Industrial Chemistry, 2006, Wiley-VCH, Weinheim. doi:10.1002/14356007.a12_545.pub2
Ligações externas
- Jetex: Propellants
- PhysChem: Guanidine Nitrate MSDS
