Formiga-de-fogo-vermelha
Formiga-de-fogo
| |||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||
 | |||||||||||||||||
| Classificação científica | |||||||||||||||||
| |||||||||||||||||
| Nome binomial | |||||||||||||||||
| Solenopsis invicta Buren, 1972 | |||||||||||||||||
| Distribuição geográfica | |||||||||||||||||
 | |||||||||||||||||
| Sinónimos[1] | |||||||||||||||||
| |||||||||||||||||
A formiga-de-fogo[2] ou formiga-de-fogo-vermelha[3] (nome científico: Solenopsis invicta) é uma espécie de formiga do gênero Solenopsis e subfamília dos mirmicíneos (Myrmicinae) nativa da América do Sul (Brasil, Argentina, Uruguai e Paraguai). Foi descrita pelo entomologista suíço Felix Santschi como uma variante de Solenopsis saevissima em 1916. Seu nome específico atual invicta foi dado à formiga em 1972 como uma espécie separada. No entanto, a variante e a espécie eram a mesma formiga, e o nome foi preservado devido ao seu amplo uso. Embora de origem sul-americana, a formiga-de-fogo-vermelha foi acidentalmente introduzida na Austrália, Nova Zelândia, vários países asiáticos e caribenhos e nos Estados Unidos. É polimórfica, pois as operárias aparecem em diferentes formas e tamanhos. As cores da formiga são vermelhas e um pouco amareladas com um gáster marrom ou preto, mas os machos são totalmente pretos. São dominantes em áreas alteradas e vivem numa grande variedade de habitats. Podem ser encontrados em florestas tropicais, áreas perturbadas, desertos, pastagens, ao longo de estradas e edifícios e em equipamentos elétricos. As colônias formam grandes montes construídos a partir do solo sem entradas visíveis porque os túneis de forrageamento são construídos e as operárias emergem longe do ninho.
Essas formigas exibem grande variedade de comportamentos, como construir jangadas quando percebem que o nível da água está subindo. Também mostram comportamento necrofórico, onde companheiros de ninho descartam restos ou formigas mortas em pilhas de lixo fora do ninho. O forrageamento ocorre em dias quentes ou mornos, embora possam permanecer ao ar livre à noite. As operárias se comunicam por uma série de semioquímicos e feromônios, que são usados para recrutamento, forrageamento e defesa. São onívoras e comem mamíferos mortos, artrópodes, insetos, sementes e substâncias doces, como melada de insetos hemípteros com os quais desenvolveram relações. Os predadores incluem aracnídeos, pássaros e muitos insetos, incluindo outras formigas, libélulas, lacrainhas (dermápteros) e besouros (coleópteros). A formiga é hospedeira de parasitas e de vários patógenos, nematoides e vírus, que têm sido vistos como potenciais agentes de controle biológico. O voo nupcial ocorre durante as estações quentes, e os alados podem acasalar por até 30 minutos. A fundação da colônia pode ser feita por uma única rainha ou por um grupo de rainhas, que mais tarde disputam o domínio assim que surgem as primeiras operárias. As operárias podem viver vários meses, enquanto as rainhas podem viver anos; o número de colônias pode variar de 100 a 250 mil indivíduos. Existem duas formas de sociedade na formiga-de-fogo-vermelha: colônias poligínicas (ninhos com várias rainhas) e colônias monogínicas (ninhos com uma rainha).
O veneno desempenha papel importante na vida da formiga, pois é usado para capturar presas ou para defesa.[4] Cerca de 95% do veneno consiste em alcaloides de piperidina insolúveis em água conhecidos como solenopsinas, com o restante compreendendo uma mistura de proteínas tóxicas que podem ser particularmente potentes em humanos sensíveis. Mais de 14 milhões de pessoas são picadas por elas nos Estados Unidos anualmente, onde se espera que muitos desenvolvam alergia ao veneno. A maioria das vítimas apresenta queimação e inchaço intensos, seguidos pela formação de pústulas estéreis, que podem permanecer por vários dias. No entanto, 0,6% a 6,0% das pessoas podem sofrer de anafilaxia, que pode ser fatal se não for tratada. Os sintomas comuns incluem tontura, dor no peito, náusea, sudorese intensa, pressão arterial baixa, perda de ar e fala arrastada. Mais de 80 mortes foram registradas em ataques de formigas-de-fogo. O tratamento depende dos sintomas; aqueles que apenas sentem dor e formação de pústulas não requerem atenção médica, mas aqueles que sofrem de anafilaxia recebem epinefrinas. A imunoterapia com extrato de corpo inteiro é usada para tratar vítimas e é considerada altamente eficaz.[5]
A formiga é vista como praga notória, causando bilhões de dólares em danos anualmente e impactando a vida selvagem. As formigas prosperam em áreas urbanas, então sua presença pode impedir atividades ao ar livre. Os ninhos podem ser construídos sob estruturas como pavimentos e fundações, o que pode causar problemas estruturais ou derrubá-los. Não apenas podem danificar ou destruir estruturas, mas também podem danificar equipamentos e infraestrutura e afetar os valores de negócios, terrenos e propriedades. Na agricultura, podem danificar plantações e máquinas e ameaçar pastagens. São conhecidas por invadir grande variedade de culturas e montes construídos em terras agrícolas podem impedir a colheita. Também representam ameaça aos animais e o gado, podendo causar ferimentos graves ou matá-los, especialmente animais jovens, fracos ou doentes. Apesar disso, podem ser benéficas porque consomem insetos-praga comuns nas plantações. Métodos comuns de controle dessas formigas incluem iscas e fumigação; outros métodos podem ser ineficazes ou perigosos. Devido à sua notoriedade e importância, a formiga tornou-se um dos insetos mais estudados do planeta, rivalizando até com a abelha-europeia (Apis mellifera).[6][7] É atualmente uma das mais importantes pragas invasoras em alguns lugares do planeta. Foi uma das primeiras formigas a ter o genoma publicado, na revista científica americana PNAS.[8][9] Consta em octogésimo sexto na lista das 100 das espécies exóticas invasoras mais daninhas do mundo da União Internacional para a Conservação da Natureza (UICN).[10]
Etimologia e nome comum
O epíteto específico da formiga-de-fogo-vermelha, invicta, deriva do latim e significa "invencível".[11][12][13] O epíteto se origina da frase Roma invicta, usada como citação inspiradora até a Queda do Império Romano do Ocidente em 476. O nome genérico, Solenopsis, se traduz como "aparência" ou "rosto" do grego antigo. É um composto de duas palavras do grego antigo - solen, que significa "cachimbo" ou "canal", e opsis, que significa "aparência" ou "visão".[14][15] Nos Estados Unidos é comumente conhecida como formiga-de-fogo-importada-vermelha (abreviada como RIFA). Outro nome popular, "lava-pés", é por causa da sensação de queimação causada por sua picada.[16][17] Nomes alternativos incluem: a "formiga-de-fogo", "formiga-vermelha" ou "formiga-vagabunda".[18][19] No Brasil é chamada toicinhera, que deriva da palavra portuguesa toicinho (gordura de porco).[20]
Taxonomia


A formiga-de-fogo-vermelha foi descrita pela primeira vez pelo entomólogo suíço Felix Santschi num artigo de jornal de 1916 publicado pela Physis.[21] Originalmente chamada Solenopsis saevissima wagneri de uma operária sintípica coletada em Santiago del Estero, Argentina, Santschi acreditava que a formiga era uma variante de Solenopsis saevissima; o epíteto específico, wagneri, deriva do sobrenome de E. R. Wagner, que coletou os primeiros espécimes.[22] O material tipo está atualmente alojado no Museu de História Natural de Basileia, Suíça, mas operárias tipo adicionais possivelmente estão alojadas no Museu Nacional de História Natural, Paris.[23] Em 1930, o mirmecólogo americano William Creighton revisou o gênero Solenopsis e reclassificou o táxon como Solenopsis saevissima electra wagneri no nível infrassubespecífico, notando que não poderia coletar nenhuma operária que se referisse à descrição original de Santschi.[24] Em 1952, o complexo de espécies de S. saevissima foi examinado e, junto com nove outros nomes de grupos de espécies, S. saevissima electra wagneri foi sinonimizado com S. saevissima saevissima.[25] Essa reclassificação foi aceita pelo entomólogo australiano George Ettershank em sua revisão do gênero e no catálogo de formigas neotropicais de Walter Kempf de 1972.[26][27]
Em 1972, o entomólogo americano William Buren descreveu o que pensava ser uma nova espécie, chamando-a de Solenopsis invicta.[28] Buren coletou uma operária holotípica de Cuiabá, em Mato Grosso, Brasil, e forneceu a primeira descrição oficial da formiga num artigo de jornal publicado pela Sociedade Entomológica da Geórgia. Acidentalmente escreveu invicta como invica [sic] acima das páginas de descrição da espécie, embora estivesse claro que invicta era a grafia pretendida por causa do uso constante do nome no artigo.[29][30] O material tipo está atualmente alojado no Museu Nacional de História Natural, Washington, D.C..[28]
Numa revisão de 1991 do complexo de espécies, o entomólogo americano James Trager sinonimizou S. saevissima electra wagneri e S. wagneri. Trager cita incorretamente Solenopsis saevissima electra wagneri como o nome original, acreditando erroneamente que o nome S. wagneri não estava disponível e usou o nome de Buren S. invicta. Trager acreditava anteriormente que S. invicta era coespecífico com S. saevissima até comparar o material com S. wagneri. Trager observa que, embora S. wagneri tenha prioridade sobre S. invicta, o nome nunca foi usado acima da classificação infrasubespecífica. O uso do nome desde Santschi não foi associado a espécimes coletados e, como resultado, é nomen nudum.[29] Em 1995, o mirmecólogo inglês Barry Bolton corrigiu o erro de Trager, reconhecendo S. wagneri como o nome válido e sinonimizando S. invicta.[31] Ele afirma que Trager erroneamente classificou S. wagneri como um nome indisponível e cita S. saevissima electra wagneri como o táxon original. Ele conclui que S. wagneri é, de fato, o nome original e tem prioridade sobre S. invicta.[31][32]
Em 1999, Steve Shattuck e colegas propuseram conservar o nome S. invicta. Desde a primeira descrição de S. invicta, mais de 1 800 artigos científicos usando o nome foram publicados discutindo ampla gama de tópicos sobre seu comportamento ecológico, genética, comunicação química, impactos econômicos, métodos de controle, população e fisiologia. Afirmam que o uso de S. wagneri é uma "ameaça" à estabilidade nomenclatural para cientistas e não cientistas; os taxonomistas podem ter sido capazes de se adaptar a tal mudança de nome, mas a confusão de nomes pode surgir se tal caso ocorrer. Devido a isso, Shattuck e seus colegas propuseram a continuação do uso de S. invicta e não de S. wagneri, já que esse nome raramente é usado; entre 1995 e 1998, mais de 100 artigos foram publicados usando S. invicta e apenas três usando S. wagneri. Solicitaram que a Comissão Internacional de Nomenclatura Zoológica (CINZ) usasse poderes plenos para suprimir S. wagneri para fins do princípio de prioridade e não ao princípio de homonímia. Além disso, solicitaram que o nome S. invicta fosse adicionado à Lista Oficial de Nomes Específicos em Zoologia e que S. wagneri fosse adicionado ao Índice Oficial de Nomes Específicos Inválidos Rejeitados em Zoologia.[23] Após a revisão, a proposta foi votada pela comunidade entomológica e foi apoiada por todos, exceto um eleitor. Observam que não há justificativa para suprimir S. wagneri; em vez disso, seria melhor dar precedência a S. invicta sobre S. wagneri sempre que um autor os tratasse como coespecíficos. O CINZ iria conservar S. invicta e suprimir S. wagneri numa revisão de 2001.[33] De acordo com a classificação atual, a formiga-de-fogo-vermelha é um membro do gênero Solenopsis na tribo dos solenopsidinos (Solenopsidini), subfamília dos mirmicíneos (Myrmicinae). É um membro da família dos formicídeos (Formicidae), pertencente à ordem dos himenópteros (Hymenoptera), uma ordem de insetos que contém formigas, abelhas e vespas.[34]
Filogenia


A formiga-de-fogo-vermelha é um membro do grupo de espécies S. saevissima. Os membros podem ser distinguidos por seus clubes de duas juntas no final do funículo em operárias e rainhas, e o segundo e terceiro segmentos do funículo são duas vezes mais longos e largos em operárias maiores. O polimorfismo ocorre em todas as espécies e as mandíbulas possuem quatro dentes.[28] O seguinte cladograma mostra a posição da formiga-de-fogo-vermelha entre outros membros do grupo de espécies S. saevissima: [a][35]
| Solenopsis |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Dados fenotípicos e genéticos sugerem que a formiga-de-fogo-vermelha e a formiga-de-fogo-preta (Solenopsis richteri) diferem uma da outra, mas compartilham uma relação genética próxima.[36][37][38][39] A hibridação entre as duas formigas ocorre em áreas onde fazem contato, com a zona híbrida localizada no Mississípi. Tal hibridização resultou do contato secundário entre essas duas formigas várias décadas atrás, quando se encontraram pela primeira vez no sul do Alabama.[36][40] Com base no DNA mitocondrial, os haplótipos examinados não formam um clado monofilético. Alguns dos haplótipos examinados formam uma relação mais próxima com S. megergates, S. quinquecuspis e S. richteri do que com outros haplótipos de S. invicta. A ocorrência de um possível agrupamento parafilético sugere que a formiga-de-fogo-vermelha e S. quinquecuspis são possíveis grupos de espécies crípticas compostas por várias espécies que não podem ser distinguidas morfologicamente.[39][41]
Genética
Estudos mostram que a variação do DNA mitocondrial ocorre substancialmente em sociedades poligínicas (ninhos com múltiplas rainhas),[42] mas nenhuma variação é detectada em sociedades monogínicas (ninhos com uma única rainha).[43] A triploidia (uma anormalidade cromossômica) ocorre em altas taxas de formigas-de-fogo-vermelhas (até 12% em fêmeas não reprodutivas), que está ligada à alta frequência de machos diploides.[44] É é a primeira espécie a possuir um gene de barba verde, pelo qual a seleção natural pode favorecer o comportamento altruísta. As operárias que contêm esse gene são capazes de distinguir entre rainhas que o contêm e aquelas que não o possuem, aparentemente usando pistas de odor. As operárias matam as rainhas que não contêm o gene.[45][46] Em 2011, os cientistas anunciaram que tinham sequenciado completamente o genoma da formiga-de-fogo-vermelha de um macho.[9]
Descrição


Operárias de formigas-de-fogo-vermelhas variam em tamanho de pequeno a médio, tornando-as polimórficas. Medem entre 2,4 e 6,0 milímetros (0,094 e 0,236 polegada).[47] A cabeça mede de 0,66 a 1,41 milímetro (0,026 a 0,056 polegada) e tem de 0,65 a 1,43 milímetro (0,026 a 0,056 polegada) de largura. Nas operárias maiores, suas cabeças medem de 1,35 a 1,40 milímetro (0,053 a 0,055 polegada) e de 1,39 a 1,42 milímetro (0,055 a 0,056 polegada) de largura. Os escapos da antena medem de 0,96 a 1,02 milímetro (0,038 a 0,040 polegada) e o comprimento torácico é de 1,70 a 1,73 milímetro (0,067 a 0,068 polegada). A cabeça torna-se mais larga atrás dos olhos com lóbulos occipitais arredondados presentes e, ao contrário da formiga-de-fogo-preta de aparência semelhante, os lóbulos atingem o pico além da linha média, mas a excisão occipital não é tão semelhante a um vinco. Os escapos das operárias maiores não se estendem além do pico occipital em um ou dois diâmetros do escapo; esta característica é mais perceptível nas formigas-de-fogo-pretas. Nas operárias de médio porte, os escapos atingem os picos occipitais e ultrapassam a borda posterior nas operárias menores. Em operárias pequenas e médias, a cabeça tende a ter lados mais elípticos. A cabeça das operárias pequenas é mais larga na frente do que atrás. Nas operárias maiores, o pronoto não possui ombros angulares, nem possui área posteromediana rebaixada. O promesonoto é convexo e a base do propódeo é arredondada e também convexa. A base e o declive têm o mesmo comprimento. A sutura do promesonoto é forte ou fraca em operárias maiores. O pecíolo tem uma escama grossa e rombuda; se observado por trás, não é tão arredondado na parte superior em contraste com a formiga-de-fogo-preta e, às vezes, pode ser subtruncado. O pós-pecíolo é grande e largo e, nas operárias maiores, é mais largo que o comprimento. O pós-pecíolo tende a ser menos largo na frente e mais largo atrás. No lado posterior da superfície dorsal, uma impressão transversal está presente. Na formiga-de-fogo-preta esta característica também está presente, mas muito mais fraca.[28]
A escultura é muito semelhante à formiga-de-fogo-preta. As perfurações são de onde surge a pilosidade, muitas vezes alongadas nas porções dorsal e ventral da cabeça. No tórax, estrias estão presentes, mas são menos gravadas com menos pontos do que na formiga-de-fogo-preta. No pecíolo, os pontuados estão localizados nas laterais. O pós-pecíolo, quando visto de cima, tem chagrim forte com punctostrias transversais distintas. As laterais são cobertas por perfurações profundas, onde parecem menores, porém mais profundas. Na formiga-de-fogo-preta, as perfurações são maiores e mais rasas. Isso dá uma aparência mais opaca à superfície. Em alguns casos, punctostrias podem estar presentes ao redor da porção posterior. A pilosidade parece semelhante à da formiga-de-fogo-preta. Esses pelos são eretos e variam em comprimento, aparecendo longos em cada lado do pronoto e do mesonoto; na cabeça, os cabelos longos são vistos em fileiras longitudinais. Numerosos pelos pubescentes reprimidos estão na escala peciolar; isso é o oposto na formiga-de-fogo-preta, já que esses pelos são esparsos.[28] As operárias aparecem vermelhas e um tanto amareladas com um gáster marrom ou completamente preto.[21] Às vezes, manchas gástricas são vistas em operárias maiores, onde não são tão coloridas quanto as da formiga-de-fogo-preta. A mancha gástrica geralmente cobre uma pequena porção do primeiro tergito gástrico. O tórax é concolor, variando de marrom-avermelhado claro a marrom-escuro. As pernas e coxas são geralmente levemente sombreadas. A cabeça tem um padrão de cor consistente em operárias grandes, com o occipital e o vértice aparecendo em marrom. Outras partes da cabeça, incluindo a frente, genas e a região central do clípeo, são amareladas ou marrom-amareladas. As bordas anteriores das genas e mandíbulas são marrom-escuras; ambos também parecem compartilhar o mesmo tom de cor com o occipital. Os escapos e funículos variam de ser da mesma cor que a cabeça ou compartilham a mesma tonalidade com o occipital. As áreas claras da cabeça em operárias de pequeno e médio porte são restritas apenas à região frontal, com uma marca escura semelhante a uma flecha ou foguete presente. Ocasionalmente, os ninhos podem ter uma série de cores diferentes. Por exemplo, as operárias podem ser muito mais escuras e a mancha gástrica pode estar completamente ausente ou parecer marrom-escura.[28]

As rainhas têm comprimento de cabeça de 1,27 a 1,29 milímetro (0,050 a 0,051 polegada) e largura de 1,32 a 1,33 milímetro (0,052 a 0,052 polegada). Os escapos medem de 0,95 a 0,98 milímetro (0,037 a 0,039 polegada) e o tórax é de 2,60 a 2,63 milímetros (0,102 a 0,104 polegada). A cabeça é quase indistinguível da formiga-de-fogo-preta, mas a excisão occipital é menos parecida com um vinco e os escapos são consideravelmente mais curtos. Sua escama peciolar é convexa e lembra a da formiga-de-fogo-preta. O pós-pecíolo tem lados retos que nunca são côncavos, ao contrário da formiga-de-fogo-preta, onde eles são côncavos. O tórax é quase idêntico, mas o espaço claro entre a área estriada metapleural e os espiráculos propodeais é uma prega estreita ou não está presente. As porções laterais do pecíolo são puntiformes. Os lados do pós-pecíolo são opacos com perfurações presentes, mas nenhuma rugosidade irregular é vista. A parte anterior do dorso é chagrim, e as regiões média e posterior apresentam punctostrias transversais. Todas essas regiões possuem pelos eretos. As porções anteriores do pecíolo e do pós-pecíolo têm pubescência aprimorada que também é vista no propódeo. A cor da rainha é semelhante à de uma operária: o gáster é marrom escuro e as pernas, escapos e tórax são marrom claro com estrias escuras no mesoscuto. A cabeça é amarelada ou marrom-amarelada em torno das regiões centrais, o occipital e as mandíbulas são de uma cor semelhante ao tórax e as veias das asas variam de incolores a marrom claro. Os machos parecem semelhantes à formiga-de-fogo-preta, mas as bordas superiores das escamas peciolares são mais côncavas. Em ambas as espécies, os espiráculos do pós-pecíolo e do pecíolo projetam-se fortemente. Todo o corpo do macho é preto concolor, mas as antenas são esbranquiçadas. Como a rainha, as veias das asas são incolores ou marrom-claras.[28]
A formiga-de-fogo-vermelha pode ser erroneamente identificada como a similar formiga-de-fogo-preta. As duas espécies podem ser distinguidas uma da outra através de exames morfológicos da cabeça, tórax e pós-pecíolo. Na formiga-de-fogo-preta, os lados da cabeça são amplamente elípticos e a forma cordada vista na formiga-de-fogo-vermelha está ausente. A região dos lóbulos occipitais que estão situadas perto da linha média e da excisão occipital aparecem mais como vincos na formiga-de-fogo-preta do que na formiga-de-fogo-vermelha. Os escapos da formiga-de-fogo-preta são mais longos do que na formiga-de-fogo-vermelha, e o pronoto tem fortes ombros angulados. Tal personagem está quase ausente na formiga-de-fogo-vermelha. Uma área rasa, mas afundada, é conhecida apenas nas operárias maiores da formiga-de-fogo-preta, localizadas na região posterior do dorso do pronoto. Esse recurso está completamente ausente em formigas-de-fogos-vermelhas maiores. O promesonoto da formiga-de-fogo-vermelha é fortemente convexo, enquanto esta característica é fracamente convexa na formiga-de-fogo-preta. Ao exame, a base do propódeo é alongada e reta na formiga-de-fogo-preta, enquanto convexa e mais curta na formiga-de-fogo-vermelha. Ele também tem pós-pecíolo largo com lados retos ou divergentes. O pós-pecíolo na formiga-de-fogo-preta é mais estreito com lados convergentes. Na formiga-de-fogo-preta, a impressão transversal na porção posterodorsal do pós-pecíolo é forte, mas fraca ou ausente na formiga-de-fogo-vermelha.[28] Além disso, as operárias da formiga-de-fogo-preta são 15% maiores que as operárias de formigas-de-fogo-vermelhas, são marrom-escuras e possuem uma faixa amarela no lado dorsal do gáster.[48][49]
Ninhada

Os ovos são minúsculos e de formato oval, permanecendo do mesmo tamanho por cerca de uma semana. Após uma semana, o ovo assume a forma de um embrião e forma uma larva quando a casca do ovo é removida.[50] As larvas medem 3 milímetros (0,12 polegadas). Apresentam aparência semelhante às larvas de S. geminata, mas podem ser distinguidas pelo tegumento com espínulos no topo da porção dorsal dos somitos posteriores. Os pelos do corpo medem 0,063 a 0,113 milímetro (0,0025 a 0,0044 polegada) com uma ponta denticulada. As antenas têm duas ou três sensilas. O labro é menor com dois pelos na superfície anterior que são de 0,013 milímetro (0,00051 polegada). A maxila tem uma faixa esclerotizada entre o cardo e os estipes. O lábio também tem uma pequena faixa esclerotizada.[51] Os tubos das glândulas labiais são conhecidos por produzir ou secretar uma substância proteica que possui rico nível de enzimas digestivas, que inclui proteases e amilases que funcionam como digestão extraintestinal de alimentos sólidos. O intestino médio também contém amilases, roteases e upases. As células estreitas em seu reservatório têm pouca ou nenhuma função na secreção.[52] As pupas se assemelham a adultos de qualquer casta, exceto que suas pernas e antenas são mantidas firmemente contra o corpo. Parecem brancas, mas com o tempo, as pupas ficam mais escuras quando estão quase prontas para amadurecer.[53]
Quatro ínstares larvais foram descritos com base em caracteres morfológicos distintos.[50][54] As larvas das operárias menores e maiores são impossíveis de distinguir antes do instar final, quando as diferenças de tamanho se tornam aparentes. Após a pupação, uma diferença maior na largura da cabeça entre as castas torna-se mais evidente. As larvas reprodutivas são maiores que as larvas de operárias e apresentam diferenças morfológicas discretas nas peças bucais. As larvas de quarto ínstar de machos e rainhas podem ser diferenciadas com base em sua forma relativa e coloração do corpo, e também os discos imaginais gonopodais internos podem diferir.[55]
Polimorfismo
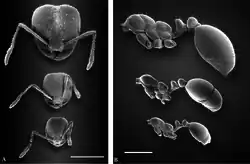
A formiga-de-fogo-vermelha é polimórfica com duas castas diferentes de operárias: operárias menores e operárias maiores (soldados). Como muitas formigas que exibem polimorfismo, formigas jovens e menores não forrageiam e cuidam da ninhada, enquanto as operárias maiores saem e forrageiam.[56][57][58][59] Nas colônias incipientes, não existe polimorfismo, mas são ocupadas por operárias monomórficas chamadas "mínimas" ou "naníticas". A largura média da cabeça nas colônias testadas aumenta durante os primeiros seis meses de desenvolvimento.[60] Em colônias com cinco anos de idade, a largura da cabeça das operárias menores diminui, mas às operárias maiores, a largura da cabeça permanece a mesma. O peso total de uma operária maior é o dobro do de uma operária menor quando eles chegam e, aos seis meses, as operárias maiores são quatro vezes mais pesadas do que as operárias menores. Uma vez que as grandes operárias se desenvolvem, elas podem constituir uma grande parte da força de trabalho, com até 35% sendo grandes operárias em uma única colônia.[61] Isso não afeta o desempenho da colônia, pois colônias polimórficas e ninhos com pequenas operárias produzem ninhadas aproximadamente na mesma taxa, e o polimorfismo não é uma vantagem ou desvantagem quando as fontes de alimento não são limitadas. No entanto, colônias polimórficas são energeticamente mais eficientes e, sob condições em que o alimento é limitado, o polimorfismo pode fornecer uma pequena vantagem na produção de cria, mas isso depende dos níveis de estresse alimentar.[62]
À medida que as formigas operárias crescem para tamanhos maiores, a forma da cabeça muda, devido ao comprimento da cabeça crescer ao mesmo tempo que o comprimento total do corpo, e a largura da cabeça pode crescer em 20%. O comprimento das antenas só cresce lentamente; as antenas podem crescer apenas 60% mais quando o corpo dobra seu comprimento, portanto, o comprimento relativo da antena diminui em 20% conforme o comprimento do corpo dobra. Todas as pernas individuais do corpo são isométricas com o comprimento do corpo, o que significa que mesmo quando o comprimento do corpo dobra, as pernas também dobram. No entanto, nem todas as pernas têm o mesmo comprimento; a porção protorácica representa 29% do comprimento da perna, a mesotorácica 31% e a metatorácica 41%. Os dois primeiros pares de pernas têm o mesmo comprimento entre si, enquanto o par final é mais longo. No geral, a aparência morfológica de uma operária muda drasticamente quando cresce. A cabeça exibe a maior mudança de formato e a altura do alinoto cresce mais rápido que seu comprimento, onde uma relação altura/comprimento de 0,27 em operárias menores e 0,32 em operárias maiores é observada. Devido a isso, as operárias maiores tendem a ter uma forma corcunda e um alinoto robusto em contraste com as operárias menores. Nenhum segmento do pecíolo exibe qualquer alteração na forma à medida que o tamanho do corpo muda. A largura do gáster cresce mais rapidamente do que seu comprimento, onde a largura pode ser de 96% de seu comprimento, mas aumenta para 106%.[60]
Fisiologia

Assim como outros insetos, a formiga-de-fogo-vermelha respira por um sistema de tubos cheios de gás chamados traqueias conectados ao ambiente externo por meio de espiráculos. Os ramos traqueais terminais (traqueolas) fazem contato direto com órgãos e tecidos internos. O transporte de oxigênio às células (e dióxido de carbono para fora das células) ocorre por meio da difusão de gases entre as traqueolas e o tecido circundante e é auxiliado por uma troca gasosa descontínua.[63] Assim como ocorre com outros insetos, a comunicação direta entre o sistema traqueal e os tecidos elimina a necessidade de uma rede de fluido circulante para transportar oxigênio.[64] Assim, as formigas-de-fogo-vermelhas e outros artrópodes podem ter um sistema circulatório modesto, embora tenham demandas metabólicas altamente altas.[65]
O sistema excretor consiste em três regiões. A região basal possui três células encontradas na porção posterior do intestino médio. As cavidades anterior e superior são formadas pelas bases dos quatro túbulos de Malpighi. A cavidade superior se abre no lume do intestino delgado. O reto é um saco grande, mas de paredes finas, que ocupa o quinto posterior das larvas. A liberação de resíduos é controlada pelas válvulas retais que levam ao ânus.[66] Às vezes, as larvas secretam um líquido que consiste em ácido úrico, água e sais.[67] Esses conteúdos são frequentemente levados para fora pelas operárias e ejetados, mas colônias sob estresse hídrico podem consumir os conteúdos.[66] No sistema reprodutivo, as rainhas liberam um feromônio que impede a transacção e a oogênese nas fêmeas virgens; aqueles testados em colônias sem uma rainha começam o desenvolvimento do oócito após o tratamento e assumem a função de postura de ovos.[68] A degeneração dos músculos de voo é iniciada pelos hormônios juvenis e de acasalamento e evitada pela alatectomia do corpo.[69][70] A histólise começa com a dissolução da miofibrila e a lenta quebra dos miofilamentos. Tal dissolução continua até atingir os únicos materiais livres da linha Z, que também desapareceriam; apenas os núcleos e os corpos lamelares permanecem.[66] Em um estudo, os aminoácidos aumentam na hemolinfa após a inseminação.[71]
O sistema glandular contém quatro glândulas: as glândulas mandibular, maxilar, labial e pós-faríngea.[66] A pós-faríngea é bem desenvolvida na rainha, enquanto as outras glândulas são maiores nas operárias. A glândula pós-faríngea funciona como vácuo para absorver ácidos graxos e triglicerídeos, bem como um ceco gástrico.[72] As funções das outras glândulas permanecem pouco compreendidas. Em um estudo discutindo as enzimas do sistema de digestão de formigas adultas, foi encontrada atividade de lipase nas glândulas mandibulares e labiais, bem como atividade de invertase. A glândula de Dufour encontrada na formiga atua como fonte de feromônios de trilha, embora os cientistas acreditassem que a glândula de veneno era a fonte do feromônio da rainha.[66][73][74] O neuropeptídeo ativador da biossíntese do feromônio do neurohormônio é encontrado na formiga que ativa a biossíntese dos feromônios da glândula de Dufour.[75] A glândula espermateca é encontrada em rainhas, que funciona na manutenção do esperma. Os machos parecem não ter essas glândulas, mas aquelas associadas à cabeça são morfologicamente semelhantes às encontradas nas operárias, mas essas glândulas podem agir de maneira diferente.[72]
A formiga enfrenta muitos desafios respiratórios devido ao seu ambiente altamente variável, que pode causar maior dessecação, hipóxia e hipercapnia. Climas quentes e úmidos causam aumento na frequência cardíaca e na respiração, o que aumenta a perda de energia e água.[64][76] A hipóxia e a hipercapnia podem resultar de colônias de formigas-de-fogo-vermelhas que vivem em montes termorreguladores mal ventilados e ninhos subterrâneos. A troca gasosa descontínua (DGE) pode permitir que as formigas sobrevivam às condições hipercápnicas e hipóxicas frequentemente encontradas em suas tocas;[63] é ideal para se adaptar a essas condições porque permite que as formigas aumentem o período de ingestão de oxigênio e expulsão de dióxido de carbono independentemente através da manipulação do espiráculo. O sucesso da invasão da formiga-de-fogo-vermelha possivelmente pode estar relacionado à sua tolerância fisiológica ao estresse abiótico, sendo mais tolerante ao calor e mais adaptável ao estresse por dessecação do que a formiga-de-fogo-preta. Isso significa que a formiga é menos vulnerável ao estresse por calor e dessecação. Embora a formiga-de-fogo-preta tenha maior conteúdo de corpo de água do que a formiga-de-fogo-vermelha, a formiga-de-fogo-preta é mais vulnerável ao estresse de dessecação. A menor sensibilidade à dessecação se deve a uma menor taxa de perda de água.[77] As colônias que vivem em locais não sombreados e mais quentes tendem a ter tolerância ao calor mais alta do que aquelas que vivem em locais sombreados e mais frios.[78]
A taxa metabólica, que afeta indiretamente a respiração, também é influenciada pela temperatura ambiente. O pico do metabolismo ocorre em cerca de 32 °C.[79] O metabolismo e, portanto, a taxa de respiração, aumenta consistentemente com o aumento da temperatura. O DGE para acima de 25 °C, embora a razão para isso seja atualmente desconhecida. A taxa de respiração também parece ser significativamente influenciada pela casta. Os machos apresentam taxa de respiração consideravelmente maior do que as fêmeas e as operárias, devido, em parte, à sua capacidade de voo e maior massa muscular. Em geral, os machos têm mais músculos e menos gordura, resultando numa maior demanda metabólica de oxigênio.[80] Embora a taxa metabólica seja mais alta a 32 °C, as colônias geralmente prosperam em temperaturas ligeiramente mais baixas (cerca de 25 °C). A alta taxa de atividade metabólica associada a temperaturas mais quentes é um fator limitante no crescimento da colônia porque a necessidade de consumo de alimentos também é aumentada. Como resultado, colônias maiores tendem a ser encontradas em condições mais frias porque as demandas metabólicas necessárias para sustentar uma colônia são reduzidas.[79]
Distribuição e habitat

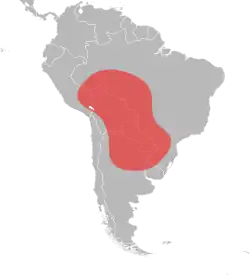
As formigas-de-fogo-vermelhas são nativas das áreas tropicais da América Central e do Sul, onde têm ampla distribuição geográfica que se estende do sudeste do Peru até o centro da Argentina e ao sul do Brasil.[81][82][83][84] Em contraste com sua distribuição geográfica na América do Norte, sua distribuição na América do Sul é significativamente diferente. Tem distribuição norte-sul extremamente longa, mas uma distribuição leste-oeste muito estreita. O registro mais ao norte é Porto Velho, no Brasil, e seu registro mais ao sul é Resistência, na Argentina; esta é uma distância de cerca de 3 mil quilômetros (1 900 milhas). Em comparação, a largura de sua faixa estreita é de cerca de 350 quilômetros (220 milhas), e é mais provável que seja mais estreita no sul da Argentina e Paraguai e nas áreas do norte da bacia do rio Amazonas. A maioria dos registros conhecidos da formiga-de-fogo-vermelha estão na região do Pantanal brasileiro. No entanto, o interior dessa área não foi examinado a fundo, mas é certo que a espécie ocorre em locais favoráveis ao seu redor. A região do Pantanal é considerada a pátria original da formiga-de-fogo-vermelha; a dispersão de hidrocoro via balsas flutuantes de formigas poderia facilmente explicar as populações do extremo sul ao redor dos rios Paraguai e Guaporé. A extensão ocidental de seu alcance não é conhecida exatamente, mas sua abundância pode ser limitada. Pode ser extensa no extremo leste da Bolívia, devido à presença da região do Pantanal.[85]
Essas formigas são nativas da Argentina, e a formiga-de-fogo-vermelha provavelmente veio daqui quando invadiram os Estados Unidos; em particular, populações dessas formigas foram encontradas nas províncias de Chaco, Corrientes, Formosa, Santiago del Estero, Santa Fé e Tucumã.[29][85][86] As regiões do nordeste da Argentina são o palpite mais confiável de onde as formigas invasoras se originam.[83] No Brasil, são encontrados no norte de Mato Grosso e em Rondônia e no estado de São Paulo. A formiga-de-fogo-vermelha e S. saevissima são parapátricas no Brasil, com zonas de contato conhecidas em Mato Grosso do Sul, Paraná e São Paulo.[82][87] No Paraguai, encontram-se em todo o território nacional, tendo sido registrados nos departamentos de Boquerón, Caaguazú, Canindeyú, Central, Guairá, Ñeembucú, Paraguarí e Presidente Hayes; Trager afirma que a formiga está distribuída em todas as regiões do país.[88][89][90] Também são encontradas em grande parte do nordeste da Bolívia e, em menor escala, no noroeste do Uruguai.[85][91]
A formiga-de-fogo-vermelha é capaz de dominar áreas alteradas e viver numa variedade de habitats. Pode sobreviver ao clima extremo da floresta tropical sul-americana e, em áreas perturbadas, os ninhos são vistos com frequência ao longo de estradas e edifícios.[92][93] Tem sido observada com frequência ao redor das várzeas do rio Paraguai.[94] Em áreas onde a água está presente, são comumente encontradas ao redor de: canais de irrigação, lagos, lagoas, reservatórios, rios, riachos, margens de rios e manguezais.[88][92] Os ninhos são encontrados em áreas agrícolas, zonas costeiras, pântanos, remanescentes de dunas costeiras, desertos, florestas, pradarias, florestas naturais, bosques de carvalhos, florestas mésicas, serrapilheira, margens de praias, matagais, ao longo de ferrovias e estradas e em áreas urbanas.[95][96] Em particular, são encontradas em terras cultivadas, florestas e plantações manejadas, áreas perturbadas, sistemas de produção pecuária intensiva e estufas.[92][97] Verificou-se que formigas-de-fogo-vermelhas invadem edifícios, incluindo instalações médicas. Em áreas urbanas, as colônias vivem em áreas abertas, especialmente se a área estiver ensolarada. Isso inclui: jardins urbanos, áreas para piquenique, gramados, parques infantis, pátios escolares, parques e campos de golfe.[88][98] Em algumas áreas, há em média 200 montes por acre.[99] Durante o inverno, as colônias se movem sob calçadas ou em edifícios, e as rainhas recém-casadas se mudam para pastagens.[92][98] As formigas-de-fogo-vermelhas são encontradas principalmente em altitudes entre 5 e 145 metros (16 e 476 pés) acima do nível do mar.[88]
Os montes variam de pequenos a grandes, medindo 10 a 60 centímetros (3,9 a 23,6 polegadas) de altura e 46 centímetros (18 polegadas) de diâmetro, sem entradas visíveis.[92][100] As operárias só conseguem acessar seus ninhos por uma série de túneis que se projetam da região central. Tais saliências podem se estender por até 25 pés de distância do monte central, diretamente para baixo no chão ou, mais comumente, lateralmente do monte original.[101] Construídos a partir do solo, os montes são orientados de modo que as longas porções do monte fiquem voltadas para o sol durante o início da manhã e antes do pôr do sol.[92][100] Os montes são geralmente de forma oval com o longo eixo do ninho orientando-se na direção norte-sul.[102] Essas formigas também gastam grandes quantidades de energia na construção do ninho e no transporte da cria, o que está relacionado com a termorregulação. A ninhada é transportada para áreas onde as temperaturas são altas; as operárias rastreiam os padrões de temperatura do monte e não dependem de hábitos comportamentais.[103] Dentro dos ninhos, os montes contêm uma série de túneis horizontais estreitos, com poços e nós subterrâneos atingindo raízes de grama de 10 a 20 centímetros (3,9 a 7,9 polegadas) abaixo da superfície; esses poços e nós conectam os túneis do monte às câmaras subterrâneas. Essas câmaras têm cerca de 5 centímetros quadrados (0,77 polegada quadrada) e atingem profundidades de 10 a 80 centímetros (3,9 a 31,5 polegadas). O número médio de formigas em uma única câmara subterrânea é de cerca de 200.[104][105][106]
Introduções


As formigas-de-fogo-vermelhas estão entre as piores espécies invasoras do mundo.[10][107] Alguns cientistas consideram-na uma "especialista em distúrbios"; a perturbação humana ao meio ambiente pode ser um fator importante por trás do impacto das formigas (elas tendem a favorecer áreas perturbadas). Isso é demonstrado por meio de um experimento, demonstrando que cortar e arar nas áreas estudadas diminuiu a diversidade e abundância de espécies de formigas nativas, enquanto as formigas-de-fogo-vermelhas encontradas em áreas florestais não perturbadas diminuíram apenas algumas espécies.[108][109]
Nos Estados Unidos, chegou pela primeira vez ao porto marítimo de Mobile, Alabama, em um cargueiro entre 1933 e 1945.[110][111][85][112][b][c] Chegando com uma estimativa 9 a 20 rainhas não relacionadas,[113][114] era rara na época, pois os entomólogos não conseguiram coletar nenhum espécime (com as primeiras observações feitas em 1942, precedidas por uma expansão populacional em 1937); a população dessas formigas explodiu na década de 1950.[115][116][117] Desde sua introdução nos Estados Unidos, se espalhou pelos estados do sul e nordeste do México, afetando negativamente a vida selvagem e causando danos econômicos.[81][118][119][120] A expansão das formigas-de-fogo-vermelhas pode ser limitada, uma vez que são quase eliminadas durante os invernos do Tenessi, portanto, podem estar atingindo seu alcance mais ao norte.[121][122][123] No entanto, o aquecimento global pode permitir que expanda seu alcance geográfico.[124] A partir de 2004, a formiga é encontrada em 13 estados e ocupa mais de 128 milhões de hectares de terra, e até 400 montes podem ser encontrados em um único acre de terra.[125][126] O Departamento de Agricultura dos Estados Unidos estima que se expandem 120 milhas (193 quilômetros) para o oeste por ano.[98] Provavelmente devido à ausência de competidores sul-americanos - e menor número de competidores nativos - domina mais nectários extraflorais e fontes de melada de hemípteros no sul dos Estados Unidos do que em sua área de origem.[127]
Formigas-de-fogo-vermelhas foram descobertas pela primeira vez em Queenslândia, Austrália, em 2001.[128][129] Acredita-se que as formigas estavam presentes em contêineres que chegavam ao porto de Brisbane, provavelmente da América do Norte.[130] Evidências anedóticas sugerem que as formigas podem ter estado presentes na Austrália por seis a oito anos antes da identificação formal. O dano potencial da formiga-de-fogo-vermelha levou o governo australiano a responder rapidamente. Um financiamento conjunto estadual e federal de A$ 175 milhões foi concedido para um programa de erradicação de seis anos.[131][132][133] Após anos de erradicação, foram relatadas taxas de erradicação superiores a 99% de propriedades previamente infestadas. O programa recebeu financiamento estendido da Comunidade das Nações de cerca de A$ 10 milhões por pelo menos mais dois anos para tratar as infestações residuais encontradas mais recentemente.[134] Em dezembro de 2014, um ninho foi identificado em Port Botany, Sydney, em Nova Gales do Sul. O porto foi colocado em quarentena e uma operação de remoção ocorreu.[135] Em setembro de 2015, populações originárias dos Estados Unidos foram encontradas num aeroporto de Brisbane.[136]
As formigas-de-fogo-vermelhas se espalharam além da América do Norte. O Invasive Species Specialist Group (ISSG) relata a formiga habitando três das ilhas Caimã. No entanto, as fontes citadas pelo ISSG não fornecem nenhum relatório sobre elas na ilha, mas coletas recentes indicam que estão presentes. Em 2001, formigas foram descobertas na Nova Zelândia, mas foram erradicadas com sucesso vários anos depois.[81][137] Também foram relatadas na Índia,[138] Malásia,[139] Filipinas[140] e Singapura.[81] No entanto, esses relatórios foram considerados incorretos, pois as formigas coletadas lá foram identificadas incorretamente. Em Singapura, as formigas provavelmente também foram identificadas incorretamente. Na Índia, após as formigas serem pesquisadas no taluca de Satur, o país confirmou altas populações; entretanto, nenhum relato da formiga foi feito fora da área pesquisada. Em 2016, os cientistas afirmam que, apesar de não haver presença da formiga na Índia, provavelmente encontrará habitats adequados no ecossistema da Índia se tiver a oportunidade.[141] Os relatórios nas Filipinas provavelmente identificaram erroneamente o material coletado, já que nenhuma população foi encontrada.[81] Foi descoberta em Honcongue e na China continental em 2004, onde se espalhou por várias províncias, bem como Macau e Taiuã.[142][143][144][145] Nenhuma barreira geográfica ou climática impede que se espalhem ainda mais, portanto, pode se espalhar pelas regiões tropicais e subtropicais da Ásia.[126][146] Na Europa, um único ninho foi encontrado na Holanda em 2002.[84]
Por volta de 1980, formigas-de-fogo-vermelhas começaram a se espalhar pelas Índias Ocidentais, onde foram relatadas pela primeira vez em Porto Rico e nas Ilhas Virgens Americanas.[147][148] Entre 1991 e 2001, foram registrada em Trindade e Tobago, várias áreas nas Baamas, Ilhas Virgens Britânicas, Antígua e Ilhas Turcas e Caicos.[149][150] Desde então, foram registradas em mais ilhas e regiões, com novas populações descobertas em: Anguila, São Martinho, Barbuda, Monserrate, São Cristóvão, Neves, Aruba e Jamaica. As formigas registradas em Aruba e Jamaica só foram encontradas em campos de golfe; esses cursos importam grama da Flórida, portanto, essa importação pode ser uma maneira importante para a formiga se espalhar pelas Índias Ocidentais.[81]
As populações encontradas fora da América do Norte são originárias dos Estados Unidos. Em 2011, o DNA de espécimes da Austrália, China e Taiuã foi analisado com resultados mostrando que estão relacionados aos dos Estados Unidos.[151] Apesar de sua disseminação, S. geminata tem distribuição geográfica maior do que a formiga-de-fogo-vermelha, mas pode ser facilmente deslocada por ela. Por causa disso, quase todo o seu alcance exótico na América do Norte foi perdido e a formiga quase desapareceu lá. Em estradas na Flórida, 83% desses locais tinham S. geminata presente quando a formiga-de-fogo-vermelha estava ausente, mas apenas 7% quando estava presente. Isso significa que a formiga provavelmente pode invadir muitas regiões tropicais e subtropicais onde as populações de S. geminata estão presentes.[81]
Comportamento e ecologia

As formigas-de-fogo-vermelhas são extremamente resistentes e se adaptaram para lidar com condições de inundação e seca. Se as formigas sentem o aumento dos níveis de água em seus ninhos, se unem e formam uma bola ou jangada que flutua, com as operárias do lado de fora e a rainha do lado de dentro.[152][153][154] A ninhada é transportada à superfície mais alta. Também são usados como estrutura de fundação da jangada, com exceção dos ovos e larvas menores. Antes de submergir, as formigas se jogam na água e cortam as conexões com a terra seca. Em alguns casos, os trabalhadores podem remover deliberadamente todos os machos da jangada, resultando no afogamento dos machos. A longevidade de uma jangada pode chegar a 12 dias. As formigas que estão presas debaixo d'água escapam subindo à superfície usando bolhas que são coletadas do substrato submerso.[155] Devido à sua maior vulnerabilidade a predadores, as formigas-de-fogo-vermelhas são significativamente mais agressivas no rafting. Os trabalhadores tendem a fornecer doses mais altas de veneno, o que reduz a ameaça de ataque de outros animais. Devido a isso, e porque uma força de trabalho maior de formigas está disponível, as jangadas são potencialmente perigosas para aqueles que as encontram.[156]
Comportamento necrofórico ocorre na formiga-de-fogo-vermelha. As operárias descartam alimentos não consumidos e outros resíduos do ninho. O componente ativo não foi identificado, mas os ácidos graxos acumulados como resultado da decomposição foram implicados e pedaços de papel revestidos com ácido oleico sintético normalmente provocaram resposta necrofórica. O processo por trás desse comportamento em formigas-de-fogo-vermelhas foi confirmado por Blum (1970): gorduras insaturadas, como ácido oleico, provocam comportamento de remoção de cadáveres.[157] As operárias também apresentam respostas diferenciadas em relação a operárias e pupas mortas. Operárias mortas geralmente são retiradas do ninho, enquanto as pupas podem levar um dia para ocorrer resposta necrófora. As pupas infectadas por Metarhizium anisopliae são geralmente descartadas pelas operárias numa taxa maior; 47,5% dos cadáveres não afetados são descartados num dia, mas para cadáveres afetados esse número é de 73,8%.[158]
As formigas-de-fogo-vermelhas têm impactos negativos na germinação das sementes. A extensão do dano, no entanto, depende de quanto tempo as sementes são vulneráveis (secar e germinar) e da abundância de formigas.[159] Um estudo mostrou que, enquanto essas formigas são atraídas e removem sementes que se adaptaram à dispersão de formigas, formigas-de-fogo-vermelhas danificam essas sementes ou as movem para locais desfavoráveis para germinação. Em sementes dadas a colônias, 80% das sementes de Sanguinaria canadensis foram escarificadas e 86% das sementes de Viola rotundifolia foram destruídas.[160] Pequenas porcentagens de sementes de pinheiro-longo (Pinus palustris) depositadas por operárias germinam com sucesso, fornecendo assim evidências de que as formigas-de-fogo-vermelhas ajudam no movimento das sementes no ecossistema do pinheiro-longo. As sementes portadoras de elaiossoma são coletadas numa taxa mais alta em contraste com as sementes não portadoras de elaiossoma e não as armazenam em seus ninhos, mas sim em pilhas de lixo na superfície nas proximidades do monte.[161]
Forrageamento e comunicação

As colônias da formiga-de-fogo-vermelha têm superfícies de túneis que se projetam das superfícies onde as operárias se alimentam.[162][163] Essas áreas de protuberância tendem a estar dentro de seu próprio território, mas uma maior colonização de formigas pode afetar isso.[164] Os túneis são projetados para permitir interações eficazes do corpo, membros e antenas com as paredes, e uma operária também pode se mover excepcionalmente rápido dentro deles (mais de nove comprimentos de corpo por segundo).[165] Os buracos saem de qualquer ponto do território da colônia e as operárias forrageiras podem precisar viajar meio metro para chegar à superfície. Supondo que uma forrageadora média percorra cinco metros, mais de 90% do tempo de forrageamento ocorre dentro dos túneis durante o dia e raramente à noite. As operárias se alimentam em temperaturas do solo que atingem 27 °C (80 °F) e temperaturas de superfície de 12–51 °C (53–123 °F). Operárias expostas a temperaturas de 42 °C (107 °F) correm o risco de morrer por causa do calor. A taxa de operárias em busca de alimento cai rapidamente no outono e raramente emergem durante o inverno. Isto pode ser devido aos efeitos da temperatura do solo e à diminuição da preferência por fontes alimentares. Estas preferências só diminuem quando a produção de crias é baixa. Nas regiões do norte dos Estados Unidos, as áreas são muito frias à formiga se alimentar, mas em outras áreas, como Flórida e Texas, a forragem pode ocorrer durante todo o ano. Quando está chovendo, as operárias não forrageiam ao ar livre, pois os buracos de saída ficam temporariamente bloqueados, os rastros de feromônios são eliminados e as forrageadoras podem ser fisicamente atingidas pela chuva. A umidade do solo também pode afetar o comportamento de forrageamento das operárias.[162]
Quando as operárias estão em busca de alimento, isso é caracterizado por três etapas: busca, recrutamento e transporte. Tendem a procurar mel com mais frequência do que outras fontes de alimento, e o peso dos alimentos não tem impacto no tempo de procura. Podem recrutar outras companheiras de ninho se a comida que encontrarem for muito pesada, demorando até 30 minutos para que o número máximo de operárias recrutadas chegue. Fontes de alimentos mais leves levam menos tempo e geralmente são transportadas rapidamente.[166] As operárias forrageiras tornam-se batedoras e procuram apenas comida fora da superfície, podendo posteriormente morrer duas semanas depois de velhice.[167]
As operárias se comunicam por meio de uma série de semioquímicos e feromônios. Esses métodos de comunicação são usados numa variedade de atividades, como recrutamento de companheiras de ninho, forrageamento, atração e defesa; por exemplo, uma operária pode secretar feromônios de trilha se uma fonte de alimento descoberta for grande demais para ser transportada.[168] Esses feromônios são sintetizados pela glândula de Dufour e podem seguir desde a fonte de alimento descoberta até o ninho.[169][170] Os componentes desses feromônios de trilha também são específicos da espécie apenas para esta formiga, em contraste com outras formigas com feromônios de cauda comuns.[171] O saco de veneno nesta espécie foi identificado como sendo o novo local de armazenamento do feromônio rainha; esse feromônio é conhecido por provocar orientação em operárias, resultando na deposição de crias.[73][172] É também um atrativo, onde as operárias se agregam em áreas onde o feromônio foi liberado. Um feromônio de cria está possivelmente presente, já que as operárias são capazes de segregar a cria por idade e casta, o que é seguido por lambidas, escovação e antenação.[168] Se uma colônia estiver sob ataque, as operárias liberarão feromônios de alarme.[173] No entanto, esses feromônios são pouco desenvolvidos nas operárias. As operárias podem detectar pirazinas produzidas pelos alados; essas pirazinas podem estar envolvidas no voo nupcial, bem como em uma resposta de alarme.[174]
As formigas-de-fogo-vermelhas podem distinguir companheiras de ninho e não companheiras de ninho por meio de comunicação química e odores específicos de colônias.[168] As operárias preferem cavar materiais de ninho de sua própria colônia e não do solo de áreas não aninhadas ou de outras colônias de formigas-de-fogo-vermelhas. Um estudo sugere que, como a dieta de uma colônia é semelhante, a única diferença entre o solo aninhado e o não aninhado era a nidificação das próprias formigas. Portanto, as operárias podem transferir o odor das colônias ao solo.[175] O odor das colônias pode ser afetado pelo ambiente, pois as operárias em colônias criadas em laboratório são menos agressivas do que aquelas na natureza.[176] Sinais derivados da rainha são capazes de regular o reconhecimento dos companheiros de ninho nas operárias e nos níveis de aminas. No entanto, estas pistas não desempenham um papel importante no reconhecimento ao nível da colônia, mas podem servir como forma de reconhecimento de castas dentro dos ninhos.[177][178] As operárias que vivem em sociedades monogínicas tendem a ser extremamente agressivas e atacam intrusos de ninhos vizinhos. Em colônias sem rainha, a adição de rainhas ou operárias estrangeiras não aumenta a agressão entre a população.[179]
Dieta
As formigas-de-fogo-vermelhas são onívoras e as forrageadoras são consideradas necrófagas e não predadoras. A dieta das formigas consiste em mamíferos mortos, artrópodes,[180] insetos, minhocas, vertebrados e alimentos sólidos, como sementes. No entanto, esta espécie prefere alimentos líquidos a sólidos. O alimento líquido que as formigas coletam são substâncias doces de plantas ou hemípteros produtores de melada.[100][181][182][183] As presas dos artrópodes podem incluir adultos dípteros, larvas e pupas e cupins. Sabe-se que o consumo de aminoácidos de açúcar afeta o recrutamento de operárias para plantar néctares. Plantas mímicas com açúcar raramente têm operárias para se alimentar delas, enquanto aquelas com açúcar e aminoácidos têm números consideráveis.[184][185] Os habitats onde vivem podem determinar os alimentos que mais recolhem; por exemplo, as taxas de sucesso de forragem para alimentos sólidos são mais altas em locais à beira de lagos, enquanto altos níveis de fontes líquidas foram coletados em locais de pastagem.[186] Dietas específicas também podem alterar o crescimento de uma colônia, com colônias de laboratório apresentando alto crescimento se alimentadas com água com mel. As colônias que se alimentam de insetos e de água com açúcar podem crescer excepcionalmente num curto período de tempo, enquanto as que não se alimentam de água com açúcar crescem substancialmente mais lentamente. As colônias que não se alimentam de insetos cessam totalmente a produção de crias.[183] Ao todo, o volume de alimento digerido pelos companheiros de ninho é regulado dentro das colônias. As larvas são capazes de exibir apetites independentes por fontes como proteínas sólidas, soluções de aminoácidos e soluções de sacarose, e também preferem essas fontes a soluções diluídas. Tal comportamento se deve à sua capacidade de comunicar a fome aos trabalhadores. A taxa de consumo depende do tipo, concentração e estado do alimento de que se alimentam. As operárias tendem a recrutar mais companheiros de ninho para fontes de alimentos cheias de altos níveis de sacarose do que para proteínas.[187]
A distribuição de alimentos desempenha um papel importante numa colônia. Este comportamento varia nas colônias, com as operárias pequenas recebendo mais alimentos do que as operárias maiores se uma colónia pequena for gravemente privada de alimentos. Em colónias maiores, contudo, as operárias maiores recebem mais alimentos. As operárias podem doar água com açúcar de forma eficiente para outras companheiras de ninho, algumas atuando como doadoras. Estes “doadores” distribuem as suas fontes de alimentos aos destinatários, que também podem atuar como doadores. As operárias também podem compartilhar uma porção maior de sua comida com outras companheiras de ninho.[188] Nas colônias que não passam fome, a comida ainda é distribuída entre as operárias e as larvas. Um estudo mostra que mel e óleo de soja foram dados às larvas após 12 a 24 horas após serem retidos pelas operárias. A distribuição proporcional destas fontes de alimento foi de 40% para as larvas e 60% para o trabalhador para o mel, e para o óleo de soja este valor foi de cerca de 30 e 70%, respectivamente.[189] As formigas-de-fogo-vermelhas também armazenam fontes específicas de alimentos, como pedaços de insetos, em vez de consumi-los imediatamente. Essas peças são geralmente transportadas abaixo da superfície do monte e nos locais mais secos e quentes.[190]
Esta espécie se envolve em trofalaxia com as larvas.[191] Independentemente dos atributos e condições de cada larva, são alimentadas aproximadamente com a mesma quantidade de alimento líquido. A taxa de trofalaxia pode aumentar com a privação alimentar das larvas, mas esse aumento depende do tamanho de cada larva. As larvas alimentadas regularmente tendem a receber pequenas quantidades. Para atingir a saciedade, todas as larvas, independentemente do seu tamanho, geralmente requerem o equivalente a oito horas de alimentação.[192]
Predadores
Diversos insetos, aracnídeos e aves se alimentam dessas formigas, especialmente quando as rainhas estão tentando estabelecer uma nova colônia.[193] Na ausência de operárias defensoras, as rainhas das formigas de fogo devem confiar em seu veneno para manter espécies competidoras afastadas.[4] Muitas espécies de libélula, incluindo Anax junius, Pachydiplax longipennis, Somatochlora provocans e Tramea carolina, capturam as rainhas durante o voo; 16 espécies de aranhas, incluindo a aranha-lobo Lycosa timuga e a viúva-negra-do-sul (Latrodectus mactans), matam ativamente as formigas-de-fogo-vermelhas. L. mactans captura todas as castas da espécie (operárias, rainhas e machos) em sua teia. Essas formigas constituem 75% das presas capturadas pela aranha. Aranhas jovens de L. mactans também foram observadas capturando essas formigas.[193][194] Outros invertebrados que predam as formigas-de-fogo-vermelhas são os tatuzinhos-de-jardim (Labidura riparia) e os besouros-tigre (Cicindela punctulata).[193] Aves que comem essas formigas incluem o andorinhão-peregrino (Chaetura pelagica), o suiriri-valente (Tyrannus tyrannus) e o codorniz-da-virgínia (Colinus virginianus virginianus). O codorniz-da-virgínia ataca essas formigas cavando os montes à procura de jovens rainhas.[193] Formigas-de-fogo-vermelhas também foram encontradas no conteúdo estomacal de tatus.[195]
Muitas espécies de formigas foram observadas atacando rainhas e matando-as. Aparentemente, o veneno das rainhas das formigas de fogo é quimicamente adaptado para subjugar rapidamente formigas competidoras.[4] Formigas predadoras incluem: Ectatomma edentatum, Ephebomyrmex spp., Lasius neoniger, Pheidole spp., Pogonomyrmex badius, e Conomyrma insana, sendo esta última uma das mais significativas.[193][196][197] As formigas C. insana são conhecidas por serem predadoras eficazes das rainhas fundadoras em áreas estudadas no norte da Flórida. A pressão dos ataques iniciados por C. insana aumenta com o tempo, fazendo com que as rainhas exibam diferentes reações, incluindo fuga, ocultação ou defesa. A maioria das rainhas atacadas por essas formigas é finalmente morta.[196] Rainhas em grupos têm maior chance de sobrevivência do que rainhas solitárias quando atacadas por S. geminata.[198] As formigas podem atacar rainhas no chão e invadir ninhos picando e desmembrando-as. Outras formigas, como P. porcula, tentam levar a cabeça e o gáster, e C. clara invadem em grupos. Certas formigas tentam arrastar as rainhas para fora de seus ninhos puxando antenas ou pernas. Formigas pequenas e monomórficas dependem de reforço de outras para matar as rainhas, não atacando até que cheguem reforços. Além de matar a rainha, algumas formigas podem roubar ovos para consumo ou emitir repelente eficaz contra formigas-de-fogo-vermelhas.[197] Certas espécies podem atacar colônias e destruí-las.[199]
Parasitas, patógenos e vírus

Moscas do gênero Pseudacteon (moscas-forídeas) são conhecidas por serem parasitas de formigas. Algumas espécies dentro desse gênero, como Pseudacteon tricuspis, foram introduzidas no ambiente com o propósito de controlar a formiga-de-fogo-vermelha. Essas moscas são parasitoides da formiga-de-fogo-vermelha em sua área de distribuição nativa na América do Sul, e podem ser atraídas pelos alcaloides do veneno das formigas.[200] Uma espécie, Pseudacteon obtusus, ataca a formiga pousando na parte posterior da cabeça e colocando um ovo. A localização do ovo torna impossível que a formiga o remova com sucesso. As larvas migram para a cabeça e então se desenvolvem alimentando-se da hemolinfa, do tecido muscular e do tecido nervoso. Após cerca de duas semanas, elas fazem a cabeça da formiga cair liberando uma enzima que dissolve a membrana que conecta a cabeça ao corpo. A mosca pupa dentro da cápsula da cabeça destacada, emergindo duas semanas depois.[201][202] P. tricuspis é outra mosca forídea que é parasitoide dessa espécie. Embora a pressão de parasitismo exercida por essas moscas não afete a densidade populacional e a atividade das formigas, ela tem um pequeno efeito na população da colônia.[203] O inseto estrepsíptero Caenocholax fenyesi é conhecido por infectar formigas machos dessa espécie e atacar os ovos,[204][205] e o ácaro Pyemotes tritici tem sido considerado um possível agente biológico contra a formiga-de-fogo-vermelha, sendo capaz de parasitar todas as castas dentro da colônia.[206] Bactérias, como Wolbachia, foram encontradas na formiga-de-fogo-vermelha; três variantes diferentes da bactéria são conhecidas por infectar essa formiga. Contudo, seu efeito sobre a formiga é desconhecido.[207][208] Solenopsis daguerrei é um parasita reprodutivo de colônias da formiga-de-fogo-vermelha.[209]
Uma grande variedade de patógenos e nemátodas também infecta as formigas-de-fogo-vermelhas. Os patógenos incluem Myrmecomyces annellisae, Mattesia spp., Steinernema spp.,[210] um nemátoda mermitídeo,[211] Vairimorpha invictae, que pode ser transmitida por meio de larvas e pupas vivas e adultos mortos[212][213] e Tetradonema solenopsis, que pode ser fatal para uma grande parte de uma colônia.[214] Indivíduos infectados por Metarhizium anisopliae tendem a realizar trofalaxia com mais frequência e apresentam uma preferência aumentada por quinina, uma substância alcaloide.[215] Moscas forídeas com Kneallhazia solenopsae podem atuar como vetores na transmissão da doença às formigas.[216] Enfraquecendo a colônia, infecções dessa doença são localizadas no tecido adiposo, com esporos ocorrendo apenas em indivíduos adultos.[217][218] A mortalidade de uma colônia infectada tende a ser maior em contraste com as que estão saudáveis.[211] Essas formigas são hospedeiras de Conidiobolus,[219] Myrmicinosporidium durum e Beauveria bassiana, cada um dos quais são fungos parasitas. Indivíduos infectados apresentam esporos por todo o corpo e aparentam estar mais escuros do que o normal.[220][221][222] A toxicidade da propriedade antimicrobiana de compostos voláteis produzidos pelas formigas pode reduzir significativamente a taxa de germinação de B. bassiana dentro da colônia.[223]
Aproximadamente 20% dos formigueiros de formigas-de-fogo-vermelhas apresentam infecção por um vírus, o S. invicta 1 (SINV-1), que parece causar a morte lenta das colônias infectadas. Ele mostrou ser autossustentável e transmissível. Uma vez introduzido, pode eliminar uma colônia em três meses. Pesquisadores acreditam que o vírus tem potencial como um biopesticida viável para controlar as formigas-de-fogo-vermelhas.[224][225][226] Também foram descobertos mais dois vírus: S. invicta 2 (SINV-2) e S. invicta 3 (SINV-3). Colônias poligínicas tendem a enfrentar infecções maiores em contraste com colônias monogínicas. Múltiplas infecções virais também podem ocorrer.[227][228]
Ciclo de vida e reprodução

Voo nupcial nas formigas-de-fogo-vermelhas começa durante as estações mais quentes do ano (primavera e verão), geralmente dois dias após a chuva. O horário em que os alados emergem e acasalam é entre o meio-dia e as 15h.[229][230] Voos nupciais registrados no norte da Flórida contam, em média, com 690 alados fêmeas e machos participando de um único voo.[231] Os machos são os primeiros a deixar o ninho, e ambos os sexos realizam voo prontamente, com pouca ou nenhuma atividade pré-voo. Contudo, as operárias aglomeram-se no monte de maneira excitada, estimuladas por glândulas mandibulares presentes na cabeça dos alados.[232][233] Como os montes não possuem aberturas, as operárias formam buracos durante o voo nupcial como forma de permitir a saída dos alados. Esse comportamento das operárias, provocado pelos feromônios, inclui corrida rápida com movimentos de vaivém e aumento de agressividade. As operárias também se agrupam ao redor dos alados enquanto estes sobem na vegetação e, em alguns casos, tentam puxá-los de volta antes que decolem. Sinais químicos de machos e fêmeas durante o voo nupcial atraem operárias, mas sinais químicos liberados por operárias não atraem outras companheiras de ninho. Esses sinais também induzem comportamento de alarme-recrutamento nas operárias, o que resulta em maior taxa de recuperação de alados.[232][234]
Os machos voam a altitudes maiores do que as fêmeas: machos capturados geralmente estão a 100 a 300 metros (330 a 980 pés) acima da superfície, enquanto as fêmeas estão apenas a 60 a 120 metros (200 a 390 pés). Um voo nupcial ocorre por aproximadamente meia hora e as fêmeas geralmente voam por menos de 1,6 quilômetros (0,99 milha) antes de pousar. Cerca de 95% das rainhas acasalam com sucesso e acasalam apenas uma vez; alguns machos podem ser inférteis devido à falha no desenvolvimento dos lóbulos testiculares.[229][235][236][237][238][239] Em colônias poligínicas, os machos não desempenham papel significativo e a maioria é, portanto, estéril; uma das razões é evitar o acasalamento com outras espécies de formigas. Isso também torna a mortalidade dos machos seletiva, o que pode afetar o sistema reprodutivo, o sucesso de acasalamento e o fluxo gênico.[240][241] As condições ideais para o início de um voo nupcial são níveis de umidade acima de 80% e quando a temperatura do solo está acima de 18 °C (64 °F). Os voos nupciais só ocorrem quando a temperatura ambiente está entre 24–32 °C (75–90 °F).[229]
As rainhas são frequentemente encontradas entre 1 e 2,3 milhas do ninho de onde voaram. A fundação da colônia pode ser feita individualmente ou em grupos, conhecidos como pleometrose.[242] Esse esforço conjunto das cofundadoras contribui para o crescimento e sobrevivência da colônia incipiente; ninhos fundados por múltiplas rainhas iniciam o período de crescimento com três vezes mais operárias em comparação às colônias fundadas por uma única rainha. Apesar disso, tais associações nem sempre são estáveis.[243][244][245][246] A emergência das primeiras operárias desencadeia lutas entre rainhas e entre rainhas e operárias. Em condições pleometróticas, apenas uma rainha emerge vitoriosa, enquanto as perdedoras são subsequentemente mortas pelas operárias.[247] Os dois fatores que podem afetar a sobrevivência de rainhas individuais são sua capacidade relativa de combate e sua contribuição relativa para a produção de operárias. Tamanho, um indicador de capacidade de luta, correlaciona-se positivamente com as taxas de sobrevivência. No entanto, a manipulação da contribuição relativa da rainha para a produção de operárias não apresentou correlação com a taxa de sobrevivência.[248]
Uma única rainha põe cerca de 10 a 15 ovos 24 horas após o acasalamento.[100] Em ninhos estabelecidos, a rainha aplica veneno em cada ovo que talvez contenha um sinal que convoca as operárias a movê-lo.[249] Esses ovos permanecem inalterados em tamanho por uma semana até que eclodam em larvas. Nesse momento, a rainha já terá posto cerca de 75 a 125 ovos adicionais. As larvas que eclodem geralmente permanecem cobertas pelas membranas de suas cascas por vários dias. As larvas conseguem liberar suas peças bucais das cascas usando movimentos corporais, mas ainda precisam de assistência das operárias na eclosão. O estágio larval divide-se em quatro ínstares, conforme observado através dos estágios de muda. Ao final de cada muda, um pedaço de material desconhecido é visto conectado às exúvias se elas estiverem isoladas das operárias. O estágio larval dura entre seis e doze dias antes que seus corpos aumentem significativamente de tamanho e se tornem pupas; o estágio pupal dura entre nove e 16 dias.[50][100]
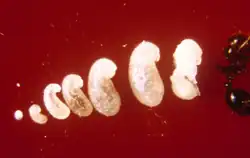

Assim que os primeiros indivíduos atingem o estágio de pupa, a rainha interrompe a produção de ovos até que as primeiras operárias amadureçam. Esse processo leva de duas semanas a um mês. As jovens larvas são alimentadas com óleos regurgitados de seu papo, bem como com ovo tróficos ou secreções. Ela também alimenta as jovens com seus músculos das asas, fornecendo os nutrientes necessários. A primeira geração de operárias é sempre pequena devido ao limite de nutrientes necessários para o desenvolvimento. Essas operárias são conhecidas como minims ou naníticas, que escavam para fora da câmara da rainha e começam a forragear por alimentos necessários para a colônia. A construção do monte também ocorre nesse período. Dentro de um mês após o nascimento da primeira geração, operárias maiores (operárias maiores) começam a se desenvolver, e dentro de seis meses, o monte será perceptível, quando observado, e abrigará vários milhares de residentes. Uma rainha madura é capaz de pôr 1 500 ovos por dia; todas as operárias são estéreis, portanto não podem se reproduzir.[100][250][251][252]
Uma colônia pode crescer excepcionalmente rápido. Colônias que abrigavam 15–20 operárias em maio cresceram para mais de sete mil em setembro. Essas colônias começaram a produzir formigas reprodutivas quando tinham um ano, e quando tinham dois anos possuíam mais de 25 mil operárias. A população dobrou para 50 mil quando essas colônias tinham três anos.[253] Quando maduras, uma colônia pode abrigar de 100 a 250 mil indivíduos, mas outros relatos sugerem que colônias podem conter mais de 400 mil.[d][254][255][256] Colônias políginas têm potencial para crescer muito mais do que colônias monóginas.[257]
Vários fatores contribuem para o crescimento da colônia. A temperatura desempenha um papel importante no crescimento e desenvolvimento; o crescimento cessa abaixo de 24 °C e o tempo de desenvolvimento diminui de 55 dias a 24 °C para 23 dias a 35 °C. O crescimento em colônias estabelecidas só ocorre entre 24 e 36 °C. A cria nanítica também se desenvolve muito mais rapidamente do que a cria de operárias menores (cerca de 35% mais rápido), o que é benéfico para colônias fundadoras.[258] Colônias que têm acesso ilimitado a presas de insetos apresentam crescimento substancial, mas esse crescimento é ainda mais acelerado se elas conseguirem acessar recursos vegetais colonizados por insetos hemípteros.[259] Em colônias monóginas incipientes onde machos diploides são produzidos, as taxas de mortalidade da colônia são significativamente altas e o crescimento é lento. Em alguns casos, colônias monóginas experimentam taxas de mortalidade de 100% nos estágios iniciais de desenvolvimento.[260]
A expectativa de vida de uma operária depende de seu tamanho, embora a média geral seja em torno de 62 dias.[261] Operárias menores vivem cerca de 30 a 60 dias, enquanto as maiores vivem muito mais. Operárias maiores, cuja expectativa de vida é de 60 a 180 dias, vivem de 50% a 140% mais do que suas contrapartes menores, mas isso depende da temperatura.[262] Porém, operárias mantidas em condições laboratoriais podem viver entre 10 e 70 semanas (70 dias a 490 dias); a maior longevidade já registrada para uma operária é de 97 semanas (ou 679 dias).[263] As rainhas vivem muito mais do que as operárias, com uma vida útil que varia de dois anos a quase sete anos.[100][263] Nas colônias, as rainhas são as únicas formigas capazes de alterar proporções sexuais, que podem ser previstas. Por exemplo, rainhas provenientes de colônias produtoras de machos tendem a produzir predominantemente machos, enquanto rainhas oriundas de colônias com proporção sexual voltada para fêmeas tendem a produzir fêmeas.[264][265] As rainhas também exercem controle sobre a produção de formas sexuais por meio de feromônios que influenciam o comportamento das operárias em relação tanto às larvas machos quanto às fêmeas.[266]
Monoginia e poliginia
Existem duas formas de organização social na formiga-de-fogo-vermelha: colônias poligínicas e colônias monogínicas.[267][268][267] As colônias poligínicas diferem substancialmente das monogínicas em insetos sociais. As primeiras apresentam reduções na fecundidade da rainha, dispersão, longevidade e grau de parentesco entre companheiras de ninho.[269][270][271][272] As rainhas poligínicas também são menos fisogástricas que as rainhas monogínicas, e as operárias são menores.[273][274] Entender os mecanismos por trás do recrutamento de rainhas é essencial para compreender como essas diferenças em aptidão são formadas. É incomum que o número de rainhas mais velhas em uma colônia não influencie o recrutamento de novas rainhas. Níveis de feromônio da rainha, que parecem estar relacionados ao número de rainhas, desempenham papéis importantes na regulação da reprodução. Seria de se esperar que as operárias rejeitassem novas rainhas quando expostas a grandes quantidades desse feromônio. Além disso, há evidências que apoiam a afirmação de que rainhas de ambas as populações entram em ninhos aleatoriamente, sem qualquer consideração pelo número de rainhas mais velhas presentes.[275] Não há correlação entre o número de rainhas mais velhas e o número de rainhas recém-recrutadas. Três hipóteses foram propostas para explicar a aceitação de múltiplas rainhas em colônias estabelecidas: mutualismo, seleção de parentesco e parasitismo.[276] A hipótese do mutualismo afirma que a cooperação leva a um aumento na aptidão pessoal das rainhas mais velhas. No entanto, essa hipótese não é consistente com o fato de que o aumento no número de rainhas reduz tanto a produção de rainhas quanto a longevidade das rainhas.[277] A seleção de parentesco também parece improvável, dado que se observou rainhas cooperando em circunstâncias nas quais são estatisticamente não aparentadas. Portanto, as rainhas não obtêm ganho de aptidão pessoal ao permitir que novas rainhas ingressem na colônia. O parasitismo de ninhos preexistentes parece ser a melhor explicação para a poliginia. Uma teoria é que tantas rainhas tentam entrar na colônia que as operárias ficam confusas e inadvertidamente permitem que várias rainhas se juntem.[278]
As operárias monogínicas matam rainhas estrangeiras e defendem agressivamente seu território. No entanto, nem todos os comportamentos são universais, principalmente porque os comportamentos das operárias dependem do contexto ecológico em que se desenvolvem, e a manipulação de genótipos de operárias pode provocar mudanças comportamentais. Portanto, comportamentos de populações nativas podem diferir daqueles de populações introduzidas.[279] Em um estudo destinado a avaliar o comportamento agressivo de operárias monogínicas e poligínicas da formiga-de-fogo-vermelha, observando interações em arenas neutras, e a desenvolver um etograma confiável para distinguir prontamente entre colônias monogínicas e poligínicas de formigas-de-fogo-vermelhas em campo,[280] operárias monogínicas e poligínicas discriminaram entre companheiras de ninho e estrangeiras, como indicado por diferentes comportamentos que variaram de tolerância a agressão. As formigas monogínicas sempre atacaram formigas estrangeiras, independentemente de serem provenientes de colônias monogínicas ou poligínicas, enquanto as formigas poligínicas reconheceram, mas não atacaram formigas poligínicas estrangeiras, exibindo principalmente posturas semelhantes a comportamentos assumidos após ataques por fóridos Pseudacteon. Comportamentos hostis versus comportamentos de advertência dependeram fortemente da estrutura social das operárias. Portanto, o comportamento em relação a operárias estrangeiras era um método de caracterização de colônias monogínicas e poligínicas.[281] A maioria das colônias no sudeste e centro-sul dos EUA tende a ser monogínica.[246]
A área territorial da colônia monogínica de formiga-de-fogo-vermelha e o tamanho do monte estão positivamente correlacionados, o que, por sua vez, é regulado pelo tamanho da colônia (número e biomassa de operárias), distância de colônias vizinhas, densidade de presas e pela capacidade competitiva coletiva da colônia. Em contraste, a discriminação entre companheiras de ninho em colônias poligínicas é mais relaxada, à medida que as operárias toleram formigas coespecíficas alheias à colônia, aceitam outras rainhas heterozigotas e não protegem agressivamente seu território contra coespecíficas poligínicas.[282] Essas colônias podem aumentar sua produção reprodutiva como resultado de possuir muitas rainhas e da possibilidade de explorar territórios maiores por meio de recrutamento cooperativo e montes interconectados.[283]
Relação com outros animais
Competição
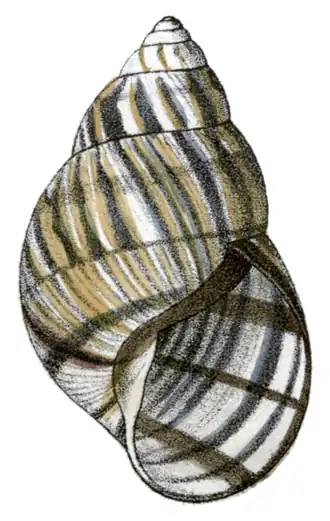
Quando formas políginas invadem áreas onde colônias ainda não foram estabelecidas, a diversidade de artrópodes e vertebrados nativos diminui significativamente.[284] Isso é evidente à medida que as populações de isópodes, ácaros e besouros-rola-bostas da família dos esracabeídeos diminuem significativamente. Elas também podem alterar de forma substancial as populações de muitas famílias de moscas e besouros, incluindo: califorídeos, histerídeos, muscídeos, sarcofagídeos, silfídeos e estafilinídeos. Apesar disso, uma revisão constatou que certos insetos podem não ser afetados pelas formigas-de-fogo-vermelhas; por exemplo, a densidade de isópodes diminui em áreas infestadas, mas grilos do gênero Gryllus não são afetados. Há alguns casos em que a diversidade de certas espécies de insetos e artrópodes aumenta em áreas onde as formigas-de-fogo-vermelhas estão presentes.[285][286][287] As formigas-de-fogo-vermelhas são predadoras importantes de invertebrados cavernícolas, alguns dos quais são espécies ameaçadas. Isso inclui opiliões, pseudoscorpiões, aranhas, besouros-de-solo e besouros pselafíneos. A maior preocupação não é a formiga em si, mas o isco usado no controle, pois ele pode ser fatal. Os caracóis Orthalicus reses estão extintos na natureza; acredita-se que a predação pelas formigas-de-fogo-vermelhas seja o principal fator de sua extinção.[285] De modo geral, elas preferem determinados artrópodes a outros, embora ataquem e matem qualquer invertebrado que não consiga se defender ou escapar.[288] A biodiversidade de artrópodes aumenta quando as populações de formigas-de-fogo-vermelhas são reduzidas ou erradicadas.[118][289]
As interações entre as formigas-de-fogo-vermelhas e mamíferos raramente foram documentadas. Entretanto, já foram observadas mortes de animais capturados vivos causadas por essas formigas.[285][290][291] As taxas de mortalidade de filhotes de Sylvilagus floridanus variam de 33 a 75% devido às formigas-de-fogo-vermelhas.[292] Acredita-se que as formigas-de-fogo-vermelhas tenham forte impacto sobre muitas espécies de herpetofauna; cientistas observaram declínios populacionais em Lampropeltis getula floridana, e ovos e adultos de Sceloporus undulatus e de Aspidoscelis sexlineata servem como fonte de alimento.[293][294][295] Por causa disso, Sceloporus undulatus desenvolveu adaptações como pernas mais longas e novos comportamentos para escapar das formigas-de-fogo-vermelhas.[296][297] Além disso, outra espécie de lagarto, Sphaerodactylus macrolepis, também é alvo das formigas-de-fogo-vermelhas e desenvolveu táticas para afastá-las, como sacudidelas da cauda.[298] Adultos de Terrapene carolina triunguis, juvenis do Houston toad (Anaxyrus houstonensis) e filhotes de aligátor-americano (Alligator mississippiensis) também são atacados e mortos por essas formigas.[285][299][300][301] Apesar dessa associação majoritariamente negativa, um estudo mostra que as formigas-de-fogo-vermelhas podem afetar a transmissão de doenças vetoriais ao regular populações de carrapatos e alterar a dinâmica entre vetores e hospedeiros, reduzindo assim as taxas de transmissão não apenas para animais, mas também para humanos.[302]
As taxas de mortalidade têm sido bem observadas em aves; houve casos em que nenhum filhote sobreviveu até a idade adulta em áreas com alta densidade de formigas-de-fogo-vermelhas. Muitas aves, incluindo andorinhas que nidificam em penhascos, patos, garças, codornas e gaivinas, têm sido afetadas pelas formigas-de-fogo-vermelhas.[303] Aves que nidificam no solo, particularmente a trinta-réis-miúdo (Sterna antillarum), são vulneráveis aos ataques das formigas-de-fogo-vermelhas.[304][301] O impacto das formigas-de-fogo-vermelhas em aves coloniais que se reproduzem em grupos é especialmente severo; aves aquáticas podem sofrer uma taxa de mortalidade de 100%, embora esse fator seja menor em aves que nidificam cedo. A sobrevivência das ninhadas diminui em andorinhas-de-dorso-acanelado (Petrochelidon pyrrhonota) quando elas são expostas a operárias forrageando.[305] A sobrevivência de ninhos de pássaros canoros diminui em áreas onde as formigas-de-fogo-vermelhas estão presentes, mas as taxas de sobrevivência nos ninhos de juruviara-de-olhos-brancos (Vireo griseus) e juruviara-de-cabeça-preta (Vireo atricapilla) aumentam de 10% para 31% e de 7% para 13% sempre que as formigas-de-fogo não estão presentes ou quando não conseguem atacá-los.[306] As formigas-de-fogo-vermelhas podem contribuir indiretamente para a baixa sobrevivência das ninhadas do galo-das-pradarias-grande-de-attwater (Tympanuchus cupido attwateri).[307] Inicialmente acreditava-se que as formigas estavam associadas ao declínio de aves invernantes, como o picanço-americano (Lanius ludovicianus), mas um estudo posterior mostrou que os esforços de erradicação das formigas usando o pesticida Mirex, conhecido por seus efeitos tóxicos colaterais, eram em grande parte responsáveis.[308][309]
Formigas-de-fogo-vermelhas são fortes competidoras em relação a muitas espécies de formigas. Elas conseguiram deslocar várias formigas nativas, o que levou a diversos impactos ecológicos.[310] No entanto, estudos mostram que essas formigas nem sempre são competidoras superiores capazes de suprimir as espécies nativas. A perturbação do habitat antes de sua chegada e limitações de recrutamento são razões mais plausíveis para explicar por que as formigas nativas são suprimidas.[311] Entre Tapinoma melanocephalum e Pheidole fervida, a formiga-de-fogo-vermelha é mais forte que ambas as espécies, mas demonstra níveis distintos de agressividade. Por exemplo, elas são menos hostis a T. melanocephalum em contraste com P. fervida. As taxas de mortalidade em T. melanocephalum e P. fervida quando enfrentam formigas-de-fogo-vermelhas são altas, sendo 31,8% e 49,9%, respectivamente. A taxa de mortalidade das operárias da formiga-de-fogo-vermelha, entretanto, é de apenas 0,2% a 12%.[312] A Nylanderia fulva apresenta maior dominância que a formiga-de-fogo-vermelha e é conhecida por deslocá-la em habitats onde ambas ocorrem.[313] Colônias maiores de Tetramorium caespitum podem destruir colônias de formigas-de-fogo-vermelhas, levando entomólogos a concluir que esse conflito entre as duas espécies pode ajudar a impedir a expansão da formiga-de-fogo-vermelha.[314][315] Indivíduos infectados por SINV-1 podem ser mortos mais rapidamente do que indivíduos saudáveis por Monomorium chinense. Isso significa que as formigas infectadas com SINV-1 são mais fracas que suas contrapartes saudáveis e muito provavelmente serão eliminadas por M. chinense. No entanto, operárias maiores, estejam infectadas ou não, raramente são mortas.[316]
Nas áreas onde é nativa, a formiga-de-fogo-vermelha ainda é uma espécie dominante e coexiste com 28 espécies de formigas em clareiras de florestas de galeria e com dez espécies em pastagens de florestas xerofíticas, vencendo a maioria das interações agressivas com outras formigas. No entanto, algumas formigas podem ser codominantes em áreas onde coexistem, como a formiga-argentina, com a qual competem de maneira simétrica.[317][318] As operárias envolvem-se regularmente em competição alimentar com outras formigas e podem suprimir a exploração de recursos alimentares provenientes de hemípteros produtores de melada (especificamente de Phenacoccus solenopsis) por formigas nativas; no entanto, as formigas-de-fogo vermelhas não conseguem eliminar completamente T. melanocephalum, embora consumam uma proporção maior do alimento. Em vez disso, as duas espécies podem coexistir pacificamente e compartilhar a melada.[319][320] Ao encontrar formigas-de-fogo-vermelhas vizinhas, as operárias podem adotar comportamentos de simulação de morte para evitá-las com sucesso. No entanto, esse comportamento é observado apenas em operárias jovens, pois as mais velhas ou fogem ou revidam quando ameaçadas.[321]
Como mencionado, as formigas-de-fogo-vermelhas e as formigas-argentinas competem entre si. As taxas de mortalidade variam em diferentes cenários (isto é, as taxas de mortalidade em confrontos entre colônias são menores do que aquelas nas quais se confrontam no campo). As operárias maiores também conseguem suportar mais ferimentos em seus corpos, aumentando assim a taxa de mortalidade das formigas-argentinas. Para que uma colônia de formigas-argentinas consiga eliminar com sucesso uma colônia monógina de 160 mil operárias, ela precisaria de 396.800 operárias. Uma colônia que tenha sido reduzida em tamanho devido a um tratamento com iscas bem-sucedido torna-se suscetível à predação por formigas-argentinas. As formigas podem desempenhar um papel vital na remoção de colônias enfraquecidas de formigas-de-fogo e também podem ser importantes para desacelerar a disseminação dessas formigas, especialmente em áreas fortemente infestadas por formigas-argentinas.[322] Apesar disso, as populações de formigas-argentinas no sudeste dos Estados Unidos diminuíram após a introdução da formiga-de-fogo-vermelha.[323] As formigas-de-fogo-vermelhas podem reduzir o número de borboletas devido à predação de ovos e lagartas[324][325][326] e têm sido associadas ao declínio de espécies de borboletas, incluindo a borboleta Schaus swallowtail (Papilio aristodemus).[327]
Mutualismo
As formigas-de-fogo-vermelhas estabeleceram uma relação com a cochonilha invasora Phenacoccus solenopsis. Sabe-se que o crescimento das colônias aumenta quando as formigas têm acesso aos recursos produzidos por P. solenopsis, e a densidade populacional dessas cochonilhas é significativamente maior em áreas onde as formigas-de-fogo-vermelhas estão presentes (a expansão de P. solenopsis em regiões onde não é nativa é atribuída à presença dessas formigas). Além disso, tanto a expectativa de vida quanto a taxa reprodutiva de P. solenopsis aumentam. Essas cochonilhas podem até ser transportadas por operárias de volta ao ninho. A predação de P. solenopsis diminui devido à interferência das operárias no ataque e no parasitismo por inimigos naturais. As cochonilhas são predadas pela joaninha Menochilus sexmaculatus e são hospedeiras de dois parasitas (Aenasius bambawalei e Acerophagus coccois) quando não há formigas presentes; porém, isso muda quando as formigas estão no local. Joaninhas são vistas com muito menos frequência em plantas com formigas-de-fogo-vermelhas, e a taxa de ninfas “mumificadas” é significativamente menor.[328] Isso é claramente evidente, pois cientistas observaram que as populações de pulgão-do-algodão (Aphis gossypii) e a predação de ovos sentinela da lagarta-do-algodoeiro aumentaram em áreas com presença de formigas-de-fogo-vermelhas.[329][330][331] As formigas-de-fogo-vermelhas também desenvolveram uma relação mutualística com outra cochonilha, Dysmicoccus morrisoni. As formigas promovem o crescimento da colônia de D. morrisoni por meio de proteção, cobrindo as colônias com detritos e coletando o honeydew que elas secretam.[332]
Toxicologia
A toxicologia do veneno da formiga-de-fogo-vermelho é relativamente bem estudada. O veneno é importante para a formiga, permitindo-lhe capturar presas e se defender. Cerca de 14 milhões de pessoas são picadas anualmente nos Estados Unidos,[333] podendo sofrer reações que variam de leve eczema a choque anafilático.[334] As reações mais comuns às picadas incluem sensação de queimação no local, seguida de urticária e formação de pústulas.[335] Algumas vítimas podem desenvolver uma reação alérgica mais séria e potencialmente fatal.[336][337] O veneno é composto principalmente de alcaloides insolúveis, com uma fase aquosa minoritária[338] que contém cerca de 46 proteínas,[339] das quais quatro são consideradas alérgenos.[340][341] Existe imunoterapia eficaz.[342]
Relação com os humanos
Pragas
.jpg)
Por causa de sua notoriedade e comportamento invasivo, as formigas-de-fogo-vermelhas são consideradas pragas. Nos Estados Unidos, a Food and Drug Administration estima que mais de US$ 5 bilhões sejam gastos anualmente em tratamento médico, danos e controle em áreas infestadas.[343][344] Só no Texas, as formigas-de-fogo-vermelhas causaram US$ 300 milhões em danos ao gado, à vida selvagem e à saúde pública.[345] Aproximadamente US$ 36 por domicílio americano, e mais de US$ 250 milhões foram gastos para controlar e erradicar as formigas-de-fogo-vermelhas. Agências privadas gastam de US$ 25 a 40 milhões anualmente em pesticidas.[100] A erradicação malsucedida na Austrália pode custar bilhões em danos anuais e, com base em um estudo do governo de Queensland, o custo estimado pode chegar a US$ 43 bilhões em 30 anos.[346]
As formigas-de-fogo-vermelhas prosperam em áreas urbanas, especialmente em quintais, campos de golfe, parques, áreas recreativas, terrenos escolares e canteiros de rua, onde sua presença pode desestimular atividades ao ar livre. Se entrarem em casas ou propriedades, podem ferir animais de estimação que estejam enjaulados, presos, amarrados ou incapazes de fugir.[344][347] Os ninhos podem ser construídos sob calçadas ou até sob estradas, bem como sob entradas de garagem, fundações, gramados, bordas de calçadas, sob lajes de pátios, em caixas elétricas ou perto de linhas de energia. Uma colônia pode escavar grandes quantidades de solo, resultando em problemas estruturais em entradas de garagem, pavimentos e paredes, e também pode causar a formação de buracos em estradas.[344][348][349][350] Danos adicionais causados pelos montes podem afetar árvores, plantas de jardim e tubulações; algumas estruturas também podem colapsar. As colônias podem migrar para casas humanas após chuvas fortes para se refugiarem do solo encharcado.[53][100]
Além de prosperarem em áreas urbanas, as formigas-de-fogo-vermelhas podem danificar equipamentos e infraestrutura e impactar negócios, terras e valores de propriedades.[347] Elas também são atraídas pela eletricidade; operárias estimuladas eletricamente liberam alcaloides de veneno, feromônios de alarme e feromônios de recrutamento, o que, por sua vez, atrai mais operárias ao local.[351] Como resultado, as formigas-de-fogo-vermelhas podem destruir equipamentos elétricos.[352] Isso é conhecido como magnetismo, no qual cientistas identificaram materiais magnéticos internos que podem desempenhar um papel nos comportamentos de orientação.[353][354] Sabe-se que mastigam o isolamento elétrico, causando danos a motores elétricos, linhas de irrigação, bombas, caixas de sinalização, transformadores, centrais telefônicas e outros equipamentos.[344] As colônias agregam-se perto de campos elétricos e são capazes de causar curtos-circuitos ou interferir com interruptores e equipamentos como aparelhos de ar-condicionado, computadores e bombas d'água. Também se sabe que infestam áreas de pouso de aeroportos e semáforos.[355]
Em 2002, o valor da produção agrícola de viveiros ornamentais nos condados de Orange, Los Angeles e San Diego foi de US$ 1,3 bilhão. Segundo o autor Les Greenberg, do Center for Invasive Species Research, aproximadamente 40% das culturas são produzidas nesses três condados, tornando-se um dos principais produtos dessas áreas. “O valor de todo o setor de viveiros da Califórnia em 2002 foi estimado em US$ 2,6 bilhões” (Greenberg, 1). Esse setor já sente os efeitos das leis de quarentena que exigem imersão em pesticidas antes que as importações possam começar. Os custos imediatos incluem a pulverização de inseticidas em todas as plantas em zonas restritas.[356]
Na agricultura

A formiga-de-fogo-vermelha é uma praga agrícola significativa em áreas onde não é nativa. Elas são capazes de danificar plantações e ameaçam pastagens e pomares.[347] Os próprios montes podem destruir equipamentos agrícolas, como sistemas de irrigação, e danificar máquinas durante a colheita.[357] Sabe-se que as formigas invadem plantações de soja, causando rendimentos mais baixos, e podem causar perdas de US$ 156 milhões nessas lavouras no sudeste dos Estados Unidos.[100][358][359] Relatórios da Geórgia e da Carolina do Norte afirmam que entre 16,8 e 49,1 kg/ha de soja não puderam ser colhidos devido à interferência dos montes de formigas-de-fogo; colheitadeiras desviavam dos montes, impedindo a colheita das plantas, e os agricultores elevavam as barras de corte das máquinas para evitar impacto com os montes.[360][361][362] O comportamento alimentar da formiga-de-fogo-vermelha pode causar danos significativos a muitas outras culturas, incluindo: feijão, repolho, citros, milho, pepino, berinjela, quiabo, amendoim, batata, sorgo, girassol e batata-doce. As formigas também interferem nos sistemas radiculares das plantas e se alimentam de brotações jovens.[100][363] Às vezes, as colônias constroem montes ao redor ou perto da base de árvores cítricas, roem novos brotos e se alimentam de flores ou frutos em desenvolvimento. Árvores cítricas frequentemente são anuladas ou mortas.[364]
Apesar de sua condição de praga e notoriedade, a formiga-de-fogo-vermelha pode ser benéfica. Ela é uma predadora eficaz de insetos e pode servir como agente biológico contra outras espécies de pragas, especialmente em plantações de cana-de-açúcar.[365] Insetos-praga que a formiga mata incluem: bicudo-do-algodoeiro (Anthonomus grandis) em culturas de algodão,[366][367][368] Diatraea saccharalis em campos de cana-de-açúcar,[369][370][371] mosca-dos-chifres (Haematobia irritans) em esterco,[372] lagarta-da-soja (Anticarsia gemmatalis) em lavouras de soja, e mosca-branca em estufas.[373][374] Vários estudos indicam que a formiga-de-fogo-vermelha não interfere nem ataca insetos de importância econômica em plantações de algodão, o que fez com que muitos agricultores do sudeste dos Estados Unidos a vejam como benéfica.[375] Contudo, alguns cientistas sugerem que o status benéfico da formiga-de-fogo-vermelha é difícil de prever quando fatores como geografia, tamanho das plantas, estação, umidade do solo e o uso de inseticidas não são considerados. Esses fatores podem reduzir a eficácia da formiga como agente de controle de pragas. Outro fator é que as operárias são indiscriminadas e matam insetos benéficos, como predadores de moscas-dos-chifres e outras pragas em pastagens, e predadores de pulgões e cochonilhas.[376][377] Elas também reduzem a eficácia de vespas parasitoides contra espécies de pragas ao comerem suas larvas e pupas.[375][378]
Controle
Em comparação com outras espécies de formigas como Anoplolepis gracilipes, que rapidamente dominam áreas nas quais foram contidas, as formigas-de-fogo-vermelhas vermelhas são relativamente fáceis de controlar.[379] As primeiras propostas para controlar a espécie ocorreram em 1957, quando o Congresso dos Estados Unidos autorizou um programa de erradicação com financiamento federal e estadual. A pesquisa sobre a formiga e sua biologia continuou após o estabelecimento do programa, e muitos produtos químicos foram usados para eliminá-las. No entanto, cientistas descobriram que esses inseticidas estavam matando a fauna nativa, e a Agência de Proteção Ambiental posteriormente os proibiu. Alguns cientistas até questionaram se as formigas eram realmente pragas.[380][381] Hoje, é improvável que a formiga-de-fogo-vermelha seja erradicada em áreas como os Estados Unidos. As populações podem ser manejadas adequadamente se for usada uma abordagem integrada.[382] Alguns cientistas consideraram usar os inimigos naturais da espécie como agentes de controle biológico; isso inclui Kneallhazia solenopsae e B. bassiana. Moscas fórides também têm sido vistas como potenciais agentes biológicos, pois podem reduzir a atividade de forrageamento e afetar os níveis populacionais das formigas-de-fogo-vermelhas vermelhas. No entanto, elas não conseguem afetar a taxa de crescimento da colônia.[383] Além disso, formigas parasitas, vespas parasitas, ácaros, outros patógenos, nematoides e fungos têm sido considerados potenciais agentes biológicos.[384] Outros sugerem que as populações podem ser mantidas ou reduzidas manipulando-se vários fatores ecológicos.[385]

Várias iscas têm sido usadas para controlar populações. Os montes são destruídos em poucas semanas se as iscas forem aplicadas sobre eles. Em comparação com métodos como encharcamento, pulverização ou fumigação, as iscas são consideradas eficazes e simples de usar contra as formigas-de-fogo-vermelhas vermelhas. Elas são espalhadas sobre o monte e então coletadas e consumidas pelas formigas.[386][387] Certas iscas, como reguladores de crescimento e soluções de ácido bórico com sacarose, beneficiam a fauna nativa e normalmente exigem baixas concentrações para eliminar uma colônia.[388][389] Outras iscas usadas incluem Amdro, Ascend, hidrametilnona, indoxacarbe e Maxforce.[390]
Pesquisadores também vêm testando outros métodos, como fumigação, injeção do monte, encharcamento e pulverização superficial. O encharcamento do monte consiste em despejar grandes volumes de líquido tóxico dentro dele. Embora isso possa afetar grande parte do monte, é possível que não chegue até a rainha, impedindo a destruição da colônia. A pulverização superficial é similar ao encharcamento, exceto que os inseticidas são aplicados sobre o monte e penetram no solo quando molhados. Injeções no monte usam pressurização e injeção de inseticidas, mas a rainha pode não ser afetada. Os montes podem ser eliminados com eficácia por fumigação. O tratamento em área pode ser usado pulverizando regiões infestadas com equipamentos agrícolas. Por fim, o tratamento localizado com inseticidas pode ser feito perfurando o monte e injetando inseticida residual.[100][386]
Além do controle químico, outros métodos que podem ser usados incluem dispositivos mecânicos e elétricos. No entanto, não se sabe se esses dispositivos são eficazes. A vedação de frestas pode ser eficiente contra colônias dentro de edificações, bloqueando rachaduras e selando aberturas, o que suprime a população fora das paredes. Moradores às vezes usam seus próprios métodos, como despejar água fervente nos montes ou incendiá-los com líquidos inflamáveis. Embora esses métodos possam funcionar, não são recomendados porque podem ser perigosos para humanos e para o meio ambiente.[100][386]
Notas
- [a] ^ Embora S. geminata aparece no cladograma, não é um membro do grupo de espécies. É incluído apenas para servir como "ponto de fixação"; para ser preciso, está mostrando onde o cladograma sob investigação se conecta com a árvore da vida.[35]
- [c] ^ As formigas-de-fogo-vermelhas provavelmente também chegaram a Nova Orleães, na Luisiana, mas a presença de formigas-argentinas (Linepithema humile) impediu que as formigas se estabelecessem e se espalhassem.[392]
Referências
- ↑ Johnson, N. F. (19 de dezembro de 2007). «Solenopsis invicta Buren». Hymenoptera Name Server version 1.5. Columbus, Ohio, USA: Ohio State University. Consultado em 1 de abril de 2015. Arquivado do original em 20 de setembro de 2016
- ↑ Infopédia. «formiga-de-fogo | Definição ou significado de formiga-de-fogo no Dicionário Infopédia da Língua Portuguesa». Infopédia - Dicionários Porto Editora. Consultado em 24 de junho de 2021. Cópia arquivada em 21 de setembro de 2022
- ↑ Infopédia. «formiga-de-fogo-vermelha | Definição ou significado de formiga-de-fogo-vermelha no Dicionário Infopédia da Língua Portuguesa». Infopédia - Dicionários Porto Editora. Consultado em 24 de junho de 2021. Cópia arquivada em 21 de setembro de 2022
- ↑ a b c Fox, Eduardo G.P.; Wu, Xiaoqing; Wang, Lei; Chen, Li; Lu, Yong-Yue; Xu, Yijuan (fevereiro de 2019). «Queen venom isosolenopsin A delivers rapid incapacitation of fire ant competitors» (PDF). Toxicon. 158: 77–83. PMID 30529381. doi:10.1016/j.toxicon.2018.11.428. Cópia arquivada (PDF) em 11 de julho de 2020
- ↑ «Red Imported Fire Ant | National Invasive Species Information Center» (em inglês). Centro Nacional de Informações sobre Espécies Invasoras. Consultado em 21 de novembro de 2022. Cópia arquivada em 6 de abril de 2022
- ↑ Tschinkel 2006, p. vii.
- ↑ Taber 2000, p. 12.
- ↑ France Presse (1 de fevereiro de 2011). «Genoma possibilita controlar proliferação de formiga argentina». Folha de S.Paulo. Cópia arquivada em 4 de março de 2016
- ↑ a b Wurm, Y.; Wang, J.; Riba-Grognuz, O.; Corona, M.; Nygaard, S.; Hunt, B.G.; Ingram, K.K.; Falquet, L.; Nipitwattanaphon, M.; Gotzek, D.; Dijkstra, M.B.; Oettler, J.; Comtesse, F.; Shih, C.-J.; Wu, W.-J.; Yang, C.-C.; Thomas, J.; Beaudoing, E.; Pradervand, S.; Flegel, V.; Cook, E.D.; Fabbretti, R.; Stockinger, H.; Long, L.; Farmerie, W.G.; Oakey, J.; Boomsma, J.J.; Pamilo, P.; Yi, S.V.; Heinze, J.; Goodisman, M. A.D.; Farinelli, L.; Harshman, K.; Hulo, N.; Cerutti, L.; Xenarios, I.; Shoemaker, D.; Keller, L. (2011). «The genome of the fire ant Solenopsis invicta» (PDF). Proceedings of the National Academy of Sciences. 108 (14): 5679–5684. Bibcode:2011PNAS..108.5679W. PMC 3078418
 . PMID 21282665. doi:10.1073/pnas.1009690108
. PMID 21282665. doi:10.1073/pnas.1009690108 . Cópia arquivada (PDF) em 15 de novembro de 2018
. Cópia arquivada (PDF) em 15 de novembro de 2018
- ↑ a b Lowe, S.; Browne, M.; Boudjelas, S.; Poorter, M. (2004) [2000]. «100 of the World's Worst Invasive Alien Species: A selection from the Global Invasive Species Database» (PDF). Auclanda: O Grupo de Especialistas em Espécies Invasoras (ISSG), um grupo de especialistas da Comissão de Sobrevivência de Espécies (SSC) da União Mundial de Conservação (IUCN). Consultado em 25 de outubro de 2022. Cópia arquivada (PDF) em 16 de março de 2017
- ↑ Bowersock, G.W.; Brown, P. (1999). Late Antiquity: a Guide to the Postclassical World 2.ª ed. Cambrígia: Belknap Press of Harvard University Press. p. 284. ISBN 978-0-674-51173-6
- ↑ Starr, C.; Evers, C.; Starr, L. (2010). Biology: Concepts and Applications without Physiology 8th ed. Belmont, California: Cengage Learning. p. 431. ISBN 978-0-538-73925-2
- ↑ Lewis, P.H. (24 de julho de 1990). «Mighty Fire Ants March Out of the South». The New York Times. Consultado em 2 de novembro de 2016. Cópia arquivada em 4 de abril de 2022
- ↑ Departamento do Ambiente, Água, Património e Artes. «Species Bank: Solenopsis invicta (Family Formicidae)». Australian Biological Resources Study: Australian Faunal Directory. Camberra: Government of Australia. Consultado em 8 de abril de 2014. Cópia arquivada em 21 de setembro de 2016
- ↑ Tschinkel 2006, pp. 13–14.
- ↑ Drees, B.M. (2002). «Medical problems and treatment considerations for the red imported fire ant» (PDF). Texas Imported Fire Ant Research and Management Project. Texas A&M University. Consultado em 23 de agosto de 2016. Cópia arquivada (PDF) em 22 de julho de 2022
- ↑ Booth, K.; Dhami, M. (2008). Red Imported Fire Ant (Solenopsis invicta): A review of the literature regarding the determination of colony age (PDF). Centre for Biodiversity and Biosecurity (Relatório). Ministry for Primary Industries: Biosecurity New Zealand. p. 2. Consultado em 29 de novembro de 2018. Arquivado do original (PDF) em 9 de outubro de 2016
- ↑ Masterson, J. (2007). «Species Name: Solenopsis invicta». Smithsonian Marine Station. Consultado em 2 de abril de 2016. Cópia arquivada em 20 de setembro de 2016
- ↑ Carmichael, A. (2005). «Red imported fire ant Solenopsis invicta Buren (Hymenoptera: Formicidae: Myrmicinae)». PaDIL (Australian Biosecurity). Consultado em 2 de abril de 2016. Cópia arquivada em 20 de novembro de 2020
- ↑ Buhs 2005, p. 13.
- ↑ a b Santschi, F. (1916). «Formicides sudaméricains nouveaux ou peu connus». Physis. 2: 365–399. doi:10.5281/ZENODO.14374
- ↑ Taber 2000, p. 25.
- ↑ a b Shattuck, S.O.; Porter, S.D.; W., D. P. (1999). «Case 3069. Solenopsis invicta Buren, 1972 (Insecta, Hymenoptera): proposed conservation of the specific name». Bulletin of Zoological Nomenclature. 56 (1): 27–30. ISSN 0007-5167. doi:10.5962/bhl.part.23022
- ↑ Creighton, W.S. (1930). «The new world species of the genus Solenopsis (Hymenop. Formicidae)» (PDF). Proceedings of the American Academy of Arts and Sciences. 66 (2): 39–152. JSTOR 20026320. doi:10.2307/20026320. Arquivado do original (PDF) em 4 de março de 2016
- ↑ Wilson, E.O. (1952). «O complexo Solenopsis saevissima na América do Sul (Hymenoptera: Formicidae) / The Solenopsis saevissima complex in South America (Hymenoptera: Formicidae)». Memórias do Instituto Oswaldo Cruz. 50: 60–68. ISSN 0074-0276. PMID 13012835. doi:10.1590/S0074-02761952000100003. Cópia arquivada em 20 de janeiro de 2022
- ↑ Ettershank, G. (1966). «A generic revision of the world Myrmicinae related to Solenopsis and Pheidologeton (Hymenoptera : Formicidae)». Australian Journal of Zoology. 14 (1): 73–171. doi:10.1071/ZO9660073
- ↑ Kempf, W.W. (1972). «Catalogo abreviado das formigas da Regiao Neotropical». Studia Entomologica. New Series. 15: 3–344
- ↑ a b c d e f g h Buren, W.F. (1972). «Revisionary studies on the taxonomy of the imported fire ants». Journal of the Georgia Entomological Society. 7: 1–26. doi:10.5281/zenodo.27055
- ↑ a b c Trager, J.C. (1991). «A revision of the fire ants, Solenopsis geminata group (Hymenoptera: Formicidae: Myrmicinae)». Journal of the New York Entomological Society. 99 (2): 141–198. JSTOR 25009890. doi:10.5281/zenodo.24912
- ↑ Pitts, James P.; Camacho, Gabriela P.; Gotzek, Dietrich; Mchugh, Joseph V.; Ross, Kenneth G. (abril de 2018). «Revision of the Fire Ants of the Solenopsis saevissima Species-Group (Hymenoptera: Formicidae)». Proceedings of the Entomological Society of Washington (em inglês). 120 (2): 308–411. ISSN 0013-8797. doi:10.4289/0013-8797.120.2.308
- ↑ a b Bolton, B. (1995). A New General Catalogue of the Ants of the World. Cambrígia: Harvard University Press. pp. 388–391. ISBN 978-0-674-61514-4
- ↑ Taber 2000, p. 26.
- ↑ International Commission on Zoological Nomenclature (2001). «Opinion 1976 Solenopsis invicta Buren, 1972 (Insecta, Hymenoptera): specific name conserved». Bulletin of Zoological Nomenclature. 58 (2): 156–157. ISSN 0007-5167
- ↑ Bolton, B. (2016). «Solenopsis invicta». AntCat. Consultado em 19 de agosto de 2016
- ↑ a b Tschinkel 2006, p. 14.
- ↑ a b Ross, K.G.; Meer, R.K.V.; Fletcher, D.J.C.; Vargo, E.L. (1987). «Biochemical phenotypic and genetic studies of two introduced fire ants and their hybrid (Hymenoptera: Formicidae)». Evolution. 41 (2): 280–293. JSTOR 2409138. PMID 28568766. doi:10.2307/2409138
- ↑ Tschinkel 2006, p. 15–16.
- ↑ Ross, K.G.; Fletcher, D.J.C. (1986). «Diploid male production — a significant colony mortality factor in the fire ant Solenopsis invicta (Hymenoptera: Formicidae)». Behavioral Ecology and Sociobiology. 19 (4): 283–291. Bibcode:1986BEcoS..19..283R. doi:10.1007/BF00300643
- ↑ a b Pitts, J.P.; McHugh, J.V.; Ross, K.G. (2005). «Cladistic analysis of the fire ants of the Solenopsis saevissima species-group (Hymenoptera: Formicidae)». Zoologica Scripta. 34 (5): 493–505. doi:10.1111/j.1463-6409.2005.00203.x
- ↑ Tschinkel 2006, p. 503.
- ↑ Pitts, J.P. (2002). A cladistic analysis of the Solenopsis saevissima species-group (Hymenoptera: Formicidae) (PDF) (Ph.D.). University of Georgia, Athens. pp. 42–43
- ↑ Taber 2000, p. 43.
- ↑ Ross, K. G.; Shoemaker, D. D. (1997). «Nuclear and mitochondrial genetic structure in two social forms of the fire ant Solenopsis invicta: insights into transitions to an alternate social organization». Heredity. 78 (6): 590–602. doi:10.1038/hdy.1997.98
- ↑ Krieger, M. J. B.; Ross, K.G.; Chang, C. W. Y.; Keller, L. (1999). «Frequency and origin of triploidy in the fire ant Solenopsis invicta». Heredity. 82 (2): 142–150. doi:10.1038/sj.hdy.6884600
- ↑ Keller, L.; Ross, K.G. (1998). «Selfish genes: a green beard in the red fire ant» (PDF). Nature. 394 (6693): 573–575. Bibcode:1998Natur.394..573K. doi:10.1038/29064. Cópia arquivada (PDF) em 25 de maio de 2019
- ↑ Grafen, A. (1998). «Evolutionary biology: Green beard as death warrant». Nature. 394 (6693): 521–522. Bibcode:1998Natur.394..521G
- ↑ Hedges, S.A. (1997). Moreland, D., ed. Handbook of Pest Control 8th ed. Richfield, Ohio: Mallis Handbook and Technical Training Company. pp. 531–535
- ↑ Tschinkel 2006, p. 24.
- ↑ Buhs 2005, p. 11.
- ↑ a b c Petralia, R. S.; Vinson, S. B. (1979). «Developmental morphology of larvae and eggs of the Imported fire ant, Solenopsis invicta». Annals of the Entomological Society of America. 72 (4): 472–484. doi:10.1093/aesa/72.4.472
- ↑ Wheeler, G.C.; Wheeler, J. (1977). «Supplementary studies on ant larvae: Myrmicinae». Transactions of the American Entomological Society. 103: 581–602. doi:10.5281/zenodo.25100
- ↑ Petralia, R.S.; Sorensen, A.A.; Vinson, S.B. (1980). «The labial gland system of larvae of the imported fire ant, Solenopsis invicta Buren». Cell and Tissue Research. 206 (1): 145–156. PMID 6153574. doi:10.1007/BF00233615
- ↑ a b Greenberg, L.; Kabashima, J.N. (2014). «Pest Notes: Red Imported Fire Ant». Statewide Integrated Pest Management Program. Agriculture and Natural Resources, University of California. Consultado em 4 de abril de 2016
- ↑ O'Neal, J.; Markin, G.P. (1975). «The larval instars of the imported fire ant, Solenopsis invicta Buren (Hymenoptera: Formicidae)». Journal of the Kansas Entomological Society. 48 (2): 141–151. JSTOR 25082731
- ↑ Fox, Eduardo G P; Solis, Daniel Russ; Rossi, Mônica Lanzoni; Delabie, Jacques Hubert Charles; de Souza, Rodrigo Fernando; Bueno, Odair Correa (2012). «Comparative Immature Morphology of Brazilian Fire Ants (Hymenoptera: Formicidae: Solenopsis)». Psyche: A Journal of Entomology. 2012: 1–10. doi:10.1155/2012/183284

- ↑ Mirenda, J.T.; Vinson, S.B. (1981). «Division of labour and specification of castes in the red imported fire ant Solenopsis invicta Buren». Animal Behaviour. 29 (2): 410–420. doi:10.1016/S0003-3472(81)80100-5
- ↑ Schmid-Hempel 1998, p. 144.
- ↑ Hölldobler & Wilson 1990, p. 311.
- ↑ Hölldobler & Wilson 1990, p. 318.
- ↑ a b Tschinkel, W. R.; Mikheyev, A. S.; Storz, S. R. (2003). «Allometry of workers of the fire ant, Solenopsis invicta». Journal of Insect Science. 3 (2). 2 páginas. PMC 524642
 . PMID 15841219. doi:10.1673/031.003.0201
. PMID 15841219. doi:10.1673/031.003.0201
- ↑ Tschinkel, W.R. (1988). «Colony growth and the ontogeny of worker polymorphism in the fire ant, Solenopsis invicta». Behavioral Ecology and Sociobiology. 22 (2): 103–115. doi:10.1007/BF00303545
- ↑ Porter, S.D.; Tschinkel, W.R. (1985). «Fire ant polymorphism: the ergonomics of brood production». Behavioral Ecology and Sociobiology. 16 (4): 323–336. JSTOR 4599785. doi:10.1007/BF00295545
- ↑ a b Vogt, J.T.; Appel, A.G. (2000). «Discontinuous gas exchange in the fire ant, Solenopsis invicta Buren: Caste differences and temperature effects». Journal of Insect Physiology. 46 (4): 403–416. PMID 12770204. doi:10.1016/S0022-1910(99)00123-7
- ↑ a b Klowden, M.J. (2007). Physiological Systems in Insects. Amsterdam; Boston: Elsevier/Academic Press. pp. 357–383, 433–449. ISBN 978-0-12-369493-5
- ↑ Hill, R.W.; Wyse, G.A.; Anderson, M. (2012). Animal Physiology 3rd ed. Sunderland, Massachusetts: Sinauer Associates. pp. 612–614. ISBN 978-0-87893-662-5
- ↑ a b c d e Vinson, S. B. (1983). «The physiology of the imported fire ant revisited». The Florida Entomologist. 66 (1): 126–139. JSTOR 3494559. doi:10.2307/3494559
- ↑ Petralia, R. S.; Williams, H. J.; Vinson, S. B. (1982). «The hindgut ultrastructure, and excretory products of larvae of the imported fire ant, Solenopsis invicta Buren». Insectes Sociaux. 29 (2): 332–345. doi:10.1007/BF02228760
- ↑ Fletcher, D. J. C.; Blum, M. S. (1981). «Pheromonal control of dealation and oogenesis in virgin queen fire ants». Science. 212 (4490): 73–75. Bibcode:1981Sci...212...73F. PMID 17747633. doi:10.1126/science.212.4490.73
- ↑ Barker, J.F. (1978). «Neuroendocrine regulation of oocyte maturation in the imported fire ant Solenopsis invicta». General and Comparative Endocrinology. 35 (3): 234–237. PMID 689357. doi:10.1016/0016-6480(78)90067-9
- ↑ Jones, R. G.; Davis, W. L.; Hung, A. C. F.; Vinson, S. B. (1978). «Insemination-induced histolysis of the flight musculature in fire ants (Solenopsis, spp.): An ultrastructural study». American Journal of Anatomy. 151 (4): 603–610. PMID 645619. doi:10.1002/aja.1001510411
- ↑ Toom, P. M.; Johnson, C. P.; Cupp, E. W. (1976). «Utilization of body reserves during preoviposition activity by Solenopsis invicta». Annals of the Entomological Society of America. 69 (1): 145–148. doi:10.1093/aesa/69.1.145. Cópia arquivada em 15 de fevereiro de 2020
- ↑ a b Vinson, S. B.; Phillips, S. A.; Williams, H. J. (1980). «The function of the post-pharyngeal glands of the red imported fire ant, Solenopsis invicta buren». Journal of Insect Physiology. 26 (9): 645–650. doi:10.1016/0022-1910(80)90035-9
- ↑ a b Vander Meer, R. K.; Glancey, B. M.; Lofgren, C.S.; Glover, A.; Tumlinson, J.H.; Rocca, J. (1980). «The poison sac of red imported fire ant queens: source of a pheromone attractant». Annals of the Entomological Society of America. 73 (5): 609–612. doi:10.1093/aesa/73.5.609
- ↑ Vander Meer, R.K.; Lofgren, C.S. (1989). «Biochemical and behavioral evidence foe hybridization between fire ants, Solenopsis invicta and Solenopsis richteri (Hymenoptera: Formicidae)». Journal of Chemical Ecology. 15 (6): 1757–1765. PMID 24272179. doi:10.1007/BF01012263
- ↑ Choi, M.Y.; Vander Meer, R.K.; Renou, M. (2012). «Ant trail pheromone biosynthesis is triggered by a neuropeptide hormone» (PDF). PLOS ONE. 7 (11): e50400. Bibcode:2012PLoSO...750400C. PMC 3511524
 . PMID 23226278. doi:10.1371/journal.pone.0050400
. PMID 23226278. doi:10.1371/journal.pone.0050400 . Cópia arquivada (PDF) em 3 de março de 2022
. Cópia arquivada (PDF) em 3 de março de 2022
- ↑ Elzen, G.W (1986). «Oxygen consumption and water loss in the imported fire ant Solenopsis invicta Buren». Comparative Biochemistry and Physiology A. 84 (1): 13–17. doi:10.1016/0300-9629(86)90035-6
- ↑ Chen, J.; Rashid, T.; Feng, G.; Hughes, W. (2014). «A comparative study between Solenopsis invicta and Solenopsis richteri on tolerance to heat and desiccation stresses». PLOS ONE. 9 (6): e96842. Bibcode:2014PLoSO...996842C. PMC 4051589
 . PMID 24915009. doi:10.1371/journal.pone.0096842
. PMID 24915009. doi:10.1371/journal.pone.0096842
- ↑ Boyles, J. G.; Aubrey, D. P.; Hickman, C. R.; Murray, K. L.; Timpone, J. C.; Ops, C.H. (2009). «Variation in physiological response of red imported fire ants (Solenopsis invicta) to small-scale thermal heterogeneity». Journal of Thermal Biology. 34 (2): 81–84. doi:10.1016/j.jtherbio.2008.10.005
- ↑ a b Porter, S. D.; Tschinkel, W. R. (1993). «Fire ant thermal preferences: behavioral control of growth and metabolism». Behavioral Ecology and Sociobiology. 32 (5). doi:10.1007/BF00183787
- ↑ Vogt, J.T.; Appel, A.G. (1999). «Standard metabolic rate of the fire ant, Solenopsis invicta Buren: effects of temperature, mass, and caste». Journal of Insect Physiology. 45 (7): 655–666. PMID 12770351. doi:10.1016/S0022-1910(99)00036-0
- ↑ a b c d e f g Wetterer, J.K. (2013). «Exotic spread of Solenopsis invicta (Hymenoptera: Formicidae) beyond North America». Sociobiology. 60: 50–55. doi:10.13102/sociobiology.v60i1.50-55
- ↑ a b Allen, G. E.; Buren, W. F.; Williams, R. N.; Menezes, M. D.; Whitcomb, W. H. (1974). «The red imported fire ant, Solenopsis invicta; distribution and habitat in Mato Grosso, Brazil». Annals of the Entomological Society of America. 67 (1): 43–46. doi:10.1093/aesa/67.1.43. Cópia arquivada em 26 de novembro de 2022
- ↑ a b Mescher, M.C.; Ross, K.G.; Shoemaker, D.D.; Keller, L.; Krieger, M.J. B. (2003). «Distribution of the two social forms of the fire ant Solenopsis invicta (Hymenoptera: Formicidae) in the native South American range» (PDF). Annals of the Entomological Society of America. 96 (6): 810–817. doi:10.1603/0013-8746(2003)096[0810:DOTTSF]2.0.CO;2. Arquivado do original (PDF) em 10 de fevereiro de 2017
- ↑ a b Noordijk, J. (2010). «A risk analysis for fire ants in the Netherlands». Leiden: Stichting European Invertebrate Survey. p. 15. Consultado em 5 de abril de 2016. Cópia arquivada em 27 de janeiro de 2021
- ↑ a b c d Buren, W. F.; Allen, G. E.; Whitcomb, W. H.; Lennartz, F. E.; Williams, R.N. (1974). «Zoogeography of the imported fire ants». Journal of the New York Entomological Society. 82 (2): 113–124. JSTOR 25008914
- ↑ Caldera, E. J.; Ross, K. G.; DeHeer, Ch. J.; Shoemaker, D. D. (2008). «Putative native source of the invasive fire ant Solenopsis invicta in the USA». Biological Invasions. 10 (8): 1457–1479. doi:10.1007/s10530-008-9219-0
- ↑ Pesquero, M. A.; Dias, A. M. P. M. (2011). «Geographical transition zone of Solenopsis fire ants (Hymenoptera: Formicidae) and Pseudacteon fly parasitoids (Diptera: Phoridae) in the state of São Paulo, Brazil». Neotropical Entomology. 40 (6): 647–652. PMID 23939270. doi:10.1590/S1519-566X2011000600003
- ↑ a b c d «Species: Solenopsis invicta Buren, 1972». AntWeb. The California Academy of Sciences. Consultado em 5 de abril de 2016
- ↑ Wild, A.L. (2007). «A catalogue of the ants of Paraguay (Hymenoptera: Formicidae)» (PDF). Zootaxa. 1622: 1–55. ISSN 1175-5334. doi:10.11646/zootaxa.1622.1.1. Cópia arquivada (PDF) em 22 de outubro de 2021
- ↑ Santschi, F. (1923). «Solenopsis et autres fourmis néotropicales» (PDF). Revue Suisse de Zoologie. 30 (8): 245–273. doi:10.5281/ZENODO.14217. Cópia arquivada (PDF) em 26 de novembro de 2022
- ↑ Ahrens, M.E.; Ross, K.G.; Shoemaker, D.D. (2005). «Phylogeographic structure of the fire ant Solenopsis invicta in its native South American range: roles of natural barriers and habitat connectivity» (PDF). Evolution. 59 (8): 1733–1743. PMID 16329243. doi:10.1111/j.0014-3820.2005.tb01822.x. Arquivado do original (PDF) em 18 de fevereiro de 2017
- ↑ a b c d e f «Solenopsis invicta (red imported fire ant)». Invasive Species Compendium. CABI. 2014. Consultado em 12 de abril de 2016. Cópia arquivada em 7 de outubro de 2022
- ↑ Taber 2000, p. 28.
- ↑ Cokendolpher, J.C.; Phillips, S.A. Jr. (1989). «Rate of spread of the red imported fire ant, Solenopsis invicta (Hymenoptera: Formicidae), in Texas». The Southwestern Naturalist. 34 (3): 443–449. JSTOR 3672182. doi:10.2307/3672182
- ↑ Fernandes, Elisa Furtado; Santos-Prezoto, Helba Helena; Prezoto, Fábio (27 de junho de 2016). «Formigas lava-pés em ambientes urbanos: Bioecologia e risco de acidentes». CES Revista. 30 (1): 25–42. ISSN 1983-1625. Cópia arquivada em 6 de fevereiro de 2021
- ↑ «Solenopsis invicta (insect)». Global Invasive Species Database. Invasive Species Specialist Group. 2010. Consultado em 2 de abril de 2016. Cópia arquivada em 31 de janeiro de 2022
- ↑ Buhs 2005, p. 12.
- ↑ a b c Kemp, S. F.; deShazo, R. D.; Moffitt, J. E.; Williams, D. F.; Buhner, W. A. (2000). «Expanding habitat of the imported fire ant (Solenopsis invicta): a public health concern». The Journal of Allergy and Clinical Immunology. 105 (4): 683–691. PMID 10756216. doi:10.1067/mai.2000.105707. Cópia arquivada em 4 de abril de 2022
- ↑ Desforges, J. F.; deShazo, R. D.; Butcher, B. T.; Banks, W. A. (1990). «Reactions to the stings of the imported fire ant». New England Journal of Medicine. 323 (7): 462–466. PMID 2197555. doi:10.1056/NEJM199008163230707. Cópia arquivada em 13 de março de 2022
- ↑ a b c d e f g h i j k l m Collins, L.; Scheffrahn, R.H. (2001). «Red imported fire ant, Solenopsis invicta Buren». UF/IFAS Featured Creatures. University of Florida. Consultado em 13 de abril de 2016. Cópia arquivada em 21 de setembro de 2016
- ↑ «Ant Colonies and Social Structure | Terminix». www.terminix.com (em inglês). Consultado em 19 de novembro de 2019. Cópia arquivada em 19 de abril de 2021
- ↑ Hubbard, M.D.; Cunningham, W.G. (1977). «Orientation of mounds in the ant Solenopsis invicta (Hymenoptera, Formicidae, Myrmicinae)». Insectes Sociaux. 24 (1): 3–7. doi:10.1007/BF02223276
- ↑ Penick, C. A.; Tschinkel, W. R. (2008). «Thermoregulatory brood transport in the fire ant, Solenopsis invicta». Insectes Sociaux. 55 (2): 176–182. doi:10.1007/s00040-008-0987-4
- ↑ Cassill, D.; Tschinkel, W. R.; Vinson, S. B. (2002). «Nest complexity, group size and brood rearing in the fire ant, Solenopsis invicta». Insectes Sociaux. 49 (2): 158–163. doi:10.1007/s00040-002-8296-9. hdl:10806/3290
- ↑ Taber 2000, p. 29.
- ↑ Taber 2000, p. 31.
- ↑ Mooallem, J. (5 de dezembro de 2013). «There's a Reason They Call Them 'Crazy Ants'». The New York Times. Consultado em 23 de agosto de 2016. Cópia arquivada em 10 de novembro de 2022
- ↑ Fountain, H. (8 de dezembro de 2008). «Fire Ants Win Out Through Land Changes, Not a Better Build». The New York Times. Consultado em 31 de outubro de 2016. Cópia arquivada em 26 de novembro de 2022
- ↑ King, J. R.; Tschinkel, W. R. (2008). «Experimental evidence that human impacts drive fire ant invasions and ecological change». Proceedings of the National Academy of Sciences. 105 (51): 20339–20343. Bibcode:2008PNAS..10520339K. PMC 2629336
 . PMID 19064909. doi:10.1073/pnas.0809423105
. PMID 19064909. doi:10.1073/pnas.0809423105
- ↑ Tschinkel 2006, p. 28.
- ↑ Buhs 2005, p. 9.
- ↑ Wilcove, D.S.; Rothstein, D.; Dubow, J.; Phillips, A.; Losos, E. (1998). «Quantifying threats to imperiled species in the United States» (PDF). BioScience. 48 (8): 607–615. JSTOR 1313420. doi:10.2307/1313420. Arquivado do original (PDF) em 12 de agosto de 2011
- ↑ Fountain, H. (8 de julho de 2008). «Tracing an Ant Invasion to a Handful of Queens». The New York Times. Consultado em 2 de novembro de 2016. Cópia arquivada em 26 de novembro de 2022
- ↑ Ross, K. G.; Shoemaker, D. D. (2008). «Estimation of the number of founders of an invasive pest insect population: the fire ant Solenopsis invicta in the USA». Proceedings of the Royal Society B: Biological Sciences. 275 (1648): 2231–2240. PMC 2603238
 . PMID 18577505. doi:10.1098/rspb.2008.0412
. PMID 18577505. doi:10.1098/rspb.2008.0412
- ↑ Tschinkel 2006, p. 25.
- ↑ Buhs 2005, p. 23.
- ↑ Adkins, H.G. (1970). «The imported fire ant in the Southern United States». Annals of the Association of American Geographers. 60 (3): 578–592. doi:10.1111/j.1467-8306.1970.tb00742.x
- ↑ a b Epperson, D.M.; Allen, C.R. (2010). «Red imported fire ant impacts on upland arthropods in southern Mississippi». The American Midland Naturalist. 163 (1): 54–63. doi:10.1674/0003-0031-163.1.54. Cópia arquivada em 19 de maio de 2022
- ↑ Callcott, A.-M.; Collins, H.L. (1996). «Invasion and range expansion of imported fire ants (Hymenoptera: Formicidae) in North America from 1918–1995». The Florida Entomologist. 79 (2): 240–251. JSTOR 3495821. doi:10.2307/3495821
- ↑ Korzukhin, M. D.; Porter, S. D.; Thompson, L. C.; Wiley, S. (2001). «Modeling temperature-dependent range limits for the fire ant Solenopsis invicta (Hymenoptera: Formicidae) in the United States» (PDF). Environmental Entomology. 30 (4): 645–655. doi:10.1603/0046-225X-30.4.645. Cópia arquivada (PDF) em 7 de janeiro de 2019
- ↑ Capinera 2008, pp. 2034–2035.
- ↑ Callcott, A.-M.; Oi, D. H.; Collins, H. L.; Williams, D. F.; Lockley, T. C. (2000). «Seasonal studies of an isolated red imported fire ant (Hymenoptera: Formicidae) population in eastern Tennessee» (PDF). Environmental Entomology. 29 (4): 788–794. doi:10.1603/0046-225X-29.4.788. Cópia arquivada (PDF) em 6 de janeiro de 2019
- ↑ Pimm, S. L.; Bartell, D. P. (1980). «Statistical model for predicting range expansion of the red imported fire ant, Solenopsis invicta, in Texas». Environmental Entomology. 9 (5): 653–658. doi:10.1093/ee/9.5.653. Cópia arquivada em 23 de julho de 2020
- ↑ Morrison, L.W.; Korzukhin, M.D.; Porter, S.D. (2005). «Predicted range expansion of the invasive fire ant, Solenopsis invicta, in the eastern United States based on the VEMAP global warming scenario». Diversity and Distributions. 11 (3): 199–204. doi:10.1111/j.1366-9516.2005.00142.x. Cópia arquivada em 29 de novembro de 2021
- ↑ Buhs 2005, p. 5.
- ↑ a b Morrison, L.W.; Porter, S.D.; Daniels, E.; Korzukhin, M. D. (2004). «Potential global range expansion of the invasive fire ant, Solenopsis invicta» (PDF). Biological Invasions. 6 (2): 183–191. doi:10.1023/B:BINV.0000022135.96042.90. Arquivado do original (PDF) em 28 de abril de 2016
- ↑ Wilder, Shawn M.; Holway, David A.; Suarez, Andrew V.; LeBrun, Edward G.; Eubanks, Micky D. (20 de dezembro de 2011). «Intercontinental differences in resource use reveal the importance of mutualisms in fire ant invasions». National Academy of Sciences. Proceedings of the National Academy of Sciences. 108 (51): 20639–20644. Bibcode:2011PNAS..10820639W. ISSN 0027-8424. PMC 3251143
 . PMID 22143788. doi:10.1073/pnas.1115263108
. PMID 22143788. doi:10.1073/pnas.1115263108
- ↑ «Red imported fire ant - Solenopsis invicta». Department of the Environment. Government of Australia. Consultado em 21 de março de 2015. Cópia arquivada em 21 de setembro de 2016
- ↑ McCubbin, K. I.; Weiner, J. M. (2002). «Fire ants in Australia: a new medical and ecological hazard.». The Medical Journal of Australia. 176 (11): 518–519. PMID 12064981. doi:10.5694/j.1326-5377.2002.tb04547.x
- ↑ Henshaw, Michael T.; Kunzmann, N.; Vanderwoude, C.; Sanetra, M.; Crozier, R. H. (2005). «Population genetics and history of the introduced fire ant, Solenopsis invicta Buren (Hymenoptera: Formicidae), in Australia». Australian Journal of Entomology. 44 (1): 37–44. doi:10.1111/j.1440-6055.2005.00421.x
- ↑ Condon, M. (27 de julho de 2013). «Queensland launched a war against the fire ant invasion, but 12 years later, they're still on the march». The Courier Mail. Consultado em 30 de dezembro de 2014
- ↑ Willis, P. (22 de fevereiro de 2007). «Fire ant update». ABC News. Consultado em 4 de maio de 2015. Cópia arquivada em 21 de setembro de 2016
- ↑ «National fire ant eradication program». Department of Primary Industries. Government of Queensland. 2007. Cópia arquivada em 21 de outubro de 2009
- ↑ «Importation of Red Imported Fire Ants Solenopsis invicta Buren 1972 - profile». Office of Environment and Heritage. Government of NSW. 2014. Consultado em 5 de maio de 2015. Cópia arquivada em 21 de setembro de 2016
- ↑ Creedon, K. (4 de dezembro de 2014). «Race against time to quarantine Sydney outbreak of red fire ants». 9 News. Sydney, Australia. Consultado em 6 de dezembro de 2014. Cópia arquivada em 21 de setembro de 2016
- ↑ Australian Associated Press (25 de fevereiro de 2016). «US fire ants found at Brisbane airport». SBS News. Consultado em 23 de agosto de 2016. Cópia arquivada em 21 de setembro de 2016
- ↑ Moloney, S.; Vanderwoude, C. (2002). «Red imported fire ants: A threat to eastern Australia's wildlife?». Ecological Management and Restoration. 3 (3): 167–175. doi:10.1046/j.1442-8903.2002.t01-1-00109.x. Cópia arquivada em 15 de outubro de 2021
- ↑ Rajagopal, T.; Sevarkodiyone, S.P.; Sekar, M. (2005). «Ant species richness, diversity and similarity index at five selected localities of Sattur Taluk». Indian Journal of Environmental Education. 5: 7–12
- ↑ Na, J.P.S.; Lee, C.Y. (2001). «Identification key to common urban pest ants in Malaysia» (PDF). Tropical Biomedicine. 18 (1): 1–17. Cópia arquivada (PDF) em 31 de março de 2022
- ↑ Kuo, K.C. (2008). Management of Red Invasive Fire Ants and Fruit Flies: The Taiwan Experience (PDF). Taipé, Taiuã: Food & Fertilizer Technology Center (FFTC). p. 1. Cópia arquivada (PDF) em 6 de janeiro de 2019
- ↑ Bharti, H.; Guénard, B.; Bharti, M.; Economo, E. P. (2016). «An updated checklist of the ants of India with their specific distributions in Indian states (Hymenoptera, Formicidae)». ZooKeys (551): 1–83. PMC 4741291
 . PMID 26877665. doi:10.3897/zookeys.551.6767
. PMID 26877665. doi:10.3897/zookeys.551.6767 . Cópia arquivada em 8 de agosto de 2022
. Cópia arquivada em 8 de agosto de 2022
- ↑ Tschinkel 2006, p. 72.
- ↑ Wang, L.; Yongyue, L.; Yijuan, X.; Ling, Z. (2013). «The current status of research on Solenopsis invicta Buren (Hymenoptera: Formicidae) in mainland China» (PDF). Asian Myrmecology. 5: 125–137. ISSN 1985-1944. Cópia arquivada (PDF) em 27 de fevereiro de 2022
- ↑ Zeng, L.; Lu, Y. Y.; He, X. F.; Zhang, W. Q.; Liang, G. W. (2005). «Identification of red imported fire ant Solenopsis invicta to invade mainland China and infestation in Wuchuan, Guangdong». Chinese Bulletin of Entomology. 42 (2): 144–148. ISSN 0452-8255. Cópia arquivada em 7 de janeiro de 2021
- ↑ Zhang, R.; Li, Y.; Liu, N.; Porter, S.D. (2007). «An overview of the red imported fire ant (Hymenoptera: Formicidae) in Mainland China». The Florida Entomologist. 90 (4): 723–731. doi:10.1653/0015-4040(2007)90[723:aootri]2.0.co;2. Consultado em 12 de abril de 2016. Cópia arquivada em 6 de janeiro de 2019
- ↑ Sutherst, R.W.; Maywald, G. (2005). «A climate model of the red imported fire ant, Solenopsis invicta Buren (Hymenoptera: Formicidae): implications for invasion of new regions, particularly Oceania». Environmental Entomology. 34 (2): 317–335. doi:10.1603/0046-225X-34.2.317
- ↑ Buren, W.F. (1982). «Scientific Notes: Red Imported Fire Ant now in Puerto Rico». The Florida Entomologist. 65 (1): 188–189. JSTOR 3494163. doi:10.2307/3494163. Cópia arquivada em 29 de outubro de 2019
- ↑ Wetterer, J.K.; Snelling, R.R. (2006). «The red imported fire ant, Solenopsis invicta, in the Virgin Islands (Hymenoptera: Formicidae)» (PDF). The Florida Entomologist. 89 (4): 431–434. doi:10.1653/0015-4040(2006)89[431:TRIFAS]2.0.CO;2. Cópia arquivada (PDF) em 6 de janeiro de 2019
- ↑ Deyrup, M.; Davis, L.; Buckner, S. (1998). Composition of the Ant Fauna of Three Bahamian Islands (PDF). São Salvador: Proceedings of the 7th Symposium on the Natural History of the Bahamas. p. 27. ISBN 978-0-935909-66-1. Cópia arquivada (PDF) em 12 de setembro de 2021
- ↑ Davis, L.R.; Vander Meer, R.K.; Porter, S.D. (2001). «Red imported fire ants expand their range across the West Indies» (PDF). The Florida Entomologist. 84 (4). 735 páginas. JSTOR 3496416. doi:10.2307/3496416. Cópia arquivada em 16 de agosto de 2020
- ↑ Ascunce, M. S.; Yang, C.-C.; Oakey, J.; Calcaterra, L.; Wu, W.-J.; Shih, C. -J.; Goudet, J.; Ross, K. G.; Shoemaker, D. (2011). «Global invasion history of the fire ant Solenopsis invicta». Science. 331 (6020): 1066–1068. Bibcode:2011Sci...331.1066A. PMID 21350177. doi:10.1126/science.1198734. Cópia arquivada em 13 de março de 2022
- ↑ Mlot, N.J.; Craig, A.T.; Hu, D.L. (2011). «Fire ants self-assemble into waterproof rafts to survive floods». Proceedings of the National Academy of Sciences. 108 (19): 7669–7673. Bibcode:2011PNAS..108.7669M. PMC 3093451
 . PMID 21518911. doi:10.1073/pnas.1016658108
. PMID 21518911. doi:10.1073/pnas.1016658108
- ↑ Morrill, W.L. (1974). «Dispersal of red imported fire ants by water». The Florida Entomologist. 57 (1): 39–42. JSTOR 3493830. doi:10.2307/3493830
- ↑ Hölldobler & Wilson 1990, p. 171.
- ↑ Adams, B.J.; Hooper-Bùi, L.M.; Strecker, R.M.; O'Brien, D.M. (2011). «Raft formation by the red imported fire ant, Solenopsis invicta». Journal of Insect Science. 11 (171). 171 páginas. PMC 3462402
 . PMID 22950473. doi:10.1673/031.011.17101
. PMID 22950473. doi:10.1673/031.011.17101
- ↑ Haight, K.L. (2006). «Defensiveness of the fire ant, Solenopsis invicta, is increased during colony rafting». Insectes Sociaux. 53 (1): 32–36. doi:10.1007/s00040-005-0832-y
- ↑ Howard, D.F.; Tschinkel, W.R. (1976). «Aspects of necrophoric behavior in the red imported fire ant, Solenopsis invicta» (PDF). Behaviour. 56 (1): 157–178. ISSN 0005-7959. doi:10.1163/156853976x00334
- ↑ Qiu, H.-L.; Lu, L.-H.; Shi, Q.-X.; Tu, C.-C.; Lin, T.; He, Y.-R. (2015). «Differential necrophoric behaviour of the ant Solenopsis invicta towards fungal-infected corpses of workers and pupae». Bulletin of Entomological Research. 105 (5): 607–614. PMID 26082426. doi:10.1017/S0007485315000528
- ↑ Smith, C.W.; Frederiksen, R.A. (2000). Sorghum: Origin, History, Technology, and Production. Nova Iorque: John Wiley & Sons. p. 456. ISBN 978-0-471-24237-6
- ↑ Zettler, J.A.; Spira, T.P.; Allen, C.R. (2001). «Ant–seed mutualisms: can red imported fire ants sour the relationship?». Biological Conservation. 101 (2): 249–253. doi:10.1016/S0006-3207(01)00074-X
- ↑ Cumberland, M.S.; Kirkman, L.K. (2013). «The effects of the red imported fire ant on seed fate in the longleaf pine ecosystem». Plant Ecology. 214 (5): 717–724. doi:10.1007/s11258-013-0201-2
- ↑ a b Porter, S.D.; Tschinkel, W.R. (1987). «Foraging in Solenopsis invicta (Hymenoptera: Formicidae): effects of weather and season». Environmental Entomology. 16 (3): 802–808. doi:10.1093/ee/16.3.802
- ↑ Markin, G.P.; O'Neal, J.; Dillier, J. (1975). «Foraging tunnels of the red imported fire ant, Solenopsis invicta (Hymenoptera: Formicidae)». Journal of the Kansas Entomological Society. 48 (1): 83–89. JSTOR 25082717
- ↑ Showler, A.T.; Knaus, R.M.; Reagan, T.E. (1989). «Foraging territoriality of the imported fire ant, Solenopsis invicta Buren, in surgarcane as determined by neutron activation analysis». Insectes Sociaux. 36 (3): 235–239. doi:10.1007/BF02226306
- ↑ Gravish, N.; Monaenkova, D.; Goodisman, M.A.D.; Goldman, D.I. (2013). «Climbing, falling, and jamming during ant locomotion in confined environments». Proceedings of the National Academy of Sciences. 110 (24): 9746–9751. Bibcode:2013PNAS..110.9746G. PMC 3683784
 . PMID 23690589. arXiv:1305.5860
. PMID 23690589. arXiv:1305.5860 . doi:10.1073/pnas.1302428110
. doi:10.1073/pnas.1302428110
- ↑ Yijuan, X.; Yongyue, L.; Ling, Z.; Guangwen, L. (2007). «Foraging behavior and recruitment of red imported fire ant Solenopsis invicta Buren in typical habitats of South China». Acta Ecologica Sinica. 27 (3): 855–860. doi:10.1016/S1872-2032(07)60022-5
- ↑ Tschinkel, W.R. (2011). «The organization of foraging in the fire ant, Solenopsis invicta». Journal of Insect Science. 11 (26). 26 páginas. PMC 3391925
 . PMID 21529150. doi:10.1673/031.011.0126
. PMID 21529150. doi:10.1673/031.011.0126
- ↑ a b c Vander Meer, R.K. (1983). «Semiochemicals and the red imported fire ant (Solenopsis invicta Buren) (Hymenoptera: Formicidae)». The Florida Entomologist. 66 (1): 139–161. JSTOR 3494560. doi:10.2307/3494560
- ↑ Williams, H.J.; Strand, M.R.; Vinson, S.B. (1981). «Trail pheromone of the red imported fire ant Solenopsis invicta (Buren)». Experientia. 37 (11): 1159–1160. doi:10.1007/BF01989893
- ↑ Vander Meer, R.K.; Alvarez, F.; Lofgren, C.S. (1988). «Isolation of the trail recruitment pheromone of Solenopsis invicta». Journal of Chemical Ecology. 14 (3): 825–838. PMID 24276134. doi:10.1007/BF01018776
- ↑ Barlin, M.R.; Blum, M.S.; Brand, M.M. (1976). «Fire ant trail pheromones: Analysis of species specificity after gas chromatographic fractionation». Journal of Insect Physiology. 22 (6): 839–844. doi:10.1016/0022-1910(76)90253-5
- ↑ Capinera 2008, p. 3445.
- ↑ Taber 2000, p. 41.
- ↑ Vander Meer, R.K.; Preston, C.A.; Choi, M.-Y. (2010). «Isolation of a pyrazine alarm pheromone component from the fire ant, Solenopsis invicta». Journal of Chemical Ecology. 36 (2): 163–170. PMID 20145982. doi:10.1007/s10886-010-9743-0
- ↑ Hubbard, M.D. (1974). «Influence of nest material and colony odor on digging in the ant Solenopsis invicta (Hymenoptera: Formicidae)». Georgia Entomological Society. 9: 127–132
- ↑ Obin, Martin S. (1986). «Nestmate recognition cues in laboratory and field colonies of Solenopsis invicta Buren (Hymenoptera: Formicidae)». Journal of Chemical Ecology. 12 (9): 1965–1975. PMID 24305971. doi:10.1007/BF01041858
- ↑ Obin, M.S.; Vander Meer, R.K. (1989). «Nestmate recognition in fire ants (Solenopsis invicta Buren). Do queens label workers?». Ethology. 80 (1–4): 255–264. doi:10.1111/j.1439-0310.1989.tb00744.x
- ↑ Vander Meer, R.K.; Preston, C.A.; Hefetz, A. (2008). «Queen regulates biogenic amine level and nestmate recognition in workers of the fire ant, Solenopsis invicta». Naturwissenschaften. 95 (12): 1155–1158. Bibcode:2008NW.....95.1155V. PMID 18704354. doi:10.1007/s00114-008-0432-6
- ↑ Obin, M.S.; Vander Meer, R.K. (1988). «Sources of nestmate recognition cues in the imported fire ant Solenopsis invicta Buren (Hymenoptera: Formicidae)». Animal Behaviour. 36 (5): 1361–1370. doi:10.1016/S0003-3472(88)80205-7
- ↑ Taber 2000, p. 38.
- ↑ Taber 2000, p. 37.
- ↑ Tennant, L.E.; Porter, S.D. (1991). «Comparison of diets of two fire ant species (Hymenoptera: Formicidae): solid and liquid components». Journal of Entomological Science. 26 (4): 450–465. ISSN 0749-8004. doi:10.18474/0749-8004-26.4.450
- ↑ a b Porter, S.D. (1989). «Effects of diet on the growth of laboratory fire ant colonies (Hymenoptera: Formicidae)». Journal of the Kansas Entomological Society. 62 (2): 288–291. JSTOR 25085088
- ↑ Lanza, J.; Vargo, E. L.; Pulim, S.; Chang, Y. Z. (1993). «Preferences of the fire ants Solenopsis invicta and S. geminata (Hymenoptera: Formicidae) for amino acid and sugar components of extrafloral nectars». Environmental Entomology. 22 (2): 411–417. doi:10.1093/ee/22.2.411
- ↑ Lanza, J. (1991). «Response of fire ants (Formicidae: Solenopsis invicta and S.gerninata) to artificial nectars with amino acids». Ecological Entomology. 16 (2): 203–210. Bibcode:1991EcoEn..16..203L. doi:10.1111/j.1365-2311.1991.tb00210.x
- ↑ Vogt, J.T.; Grantham, R.A.; Corbett, E.; Rice, S.A.; Wright, R.E. (2002). «Dietary habits of Solenopsis invicta (Hymenoptera: Formicidae) in four Oklahoma habitats». Environmental Entomology. 31 (1): 47–53. doi:10.1603/0046-225X-31.1.47
- ↑ Cassill, D.L.; Tschinkel, W.R. (1999). «Regulation of diet in the fire ant, Solenopsis invicta» (PDF). Journal of Insect Behavior. 12 (3): 307–328. doi:10.1023/A:1020835304713
- ↑ Howard, D.F.; Tschinkel, W.R. (1980). «The effect of colony size and starvation on food flow in the fire ant, Solenopsis invicta (Hymenoptera: Formicidae)». Behavioral Ecology and Sociobiology. 7 (4): 293–300. JSTOR 4599344. doi:10.1007/BF00300670
- ↑ Sorensen, A.A.; Vinson, S.B. (1981). «Quantitative food distribution studies within laboratory colonies of the imported fire ant, Solenopsis invicta Buren». Insectes Sociaux. 28 (2): 129–160. doi:10.1007/BF02223701
- ↑ Gayahan, G.G.; Tschinkel, W.R. (2008). «Fire ants, Solenopsis invicta, dry and store insect pieces for later use». Journal of Insect Science. 8 (39). 39 páginas. PMC 3127378
 . doi:10.1673/031.008.3901
. doi:10.1673/031.008.3901
- ↑ Taber 2000, p. 39.
- ↑ Cassill, D.L.; Tschinkel, W.R. (1995). «Allocation of liquid food to larvae via trophallaxis in colonies of the fire ant, Solenopsis invicta». Animal Behaviour. 50 (3): 801–813. doi:10.1016/0003-3472(95)80140-5
- ↑ a b c d e Whitcomb, W.H.; Bhatkar, A.; Nickerson, J.C. (1973). «Predators of Solenopsis invicta queens prior to successful colony establishment». Environmental Entomology. 2 (6): 1101–1103. doi:10.1093/ee/2.6.1101
- ↑ Nyffeler, M.; Dean, D.A.; Sterling, W.L. (1988). «The southern black widow spider, Latrodectus mactans (Araneae, Theridiidae), as a predator of the red imported fire ant, Solenopsis invicta (Hymenoptera, Formicidae), in Texas cotton fields». Journal of Applied Entomology. 106 (1–5): 52–57. doi:10.1111/j.1439-0418.1988.tb00563.x
- ↑ Deyrup, M.; Trager, J. (1986). «Ants of the Archbold Biological Station, Highlands County, Florida (Hymenoptera: Formicidae)». The Florida Entomologist. 69 (1): 206–228. JSTOR 3494763. doi:10.2307/3494763
- ↑ a b Nickerson, J.C.; Whitcomb, W.H.; Bhatkar, A.P.; Naves, M.A. (1975). «Predation on founding queens of Solenopsis invicta by workers of Conomyrma insana». The Florida Entomologist. 58 (2): 75–82. JSTOR 3493384. doi:10.2307/3493384
- ↑ a b Nichols, B.J.; Sites, R.W. (1991). «Ant predators of founder queens of Solenopsis invicta (Hymenoptera: Formicidae) in central Texas». Environmental Entomology. 20 (4): 1024–1029. doi:10.1093/ee/20.4.1024
- ↑ Jerome, C.A.; McInnes, D.A.; Adams, E.S. (1998). «Group defense by colony-founding queens in the fire ant Solenopsis invicta». Behavioral Ecology. 9 (3): 301–308. doi:10.1093/beheco/9.3.301

- ↑ Rao, Asha; Vinson, S. B. (2004). «Ability of resident ants to destruct small colonies of Solenopsis invicta (Hymenoptera: Formicidae)». Environmental Entomology. 33 (3): 587–598. doi:10.1603/0046-225X-33.3.587

- ↑ Chen, Li; Sharma, K.R.; Fadamiro, H.Y. (2009). «Fire ant venom alkaloids act as key attractants for the parasitic phorid fly, Pseudacteon tricuspis (Diptera: Phoridae)». Naturwissenschaften. 96 (12): 1421–1429. Bibcode:2009NW.....96.1421C. PMID 19714317. doi:10.1007/s00114-009-0598-6
- ↑ Williams, D.F.; Banks, W.A. (1987). «Pseudacteon obtusus (Diptera: Phoridae) attacking Solenopsis invicta (Hymenoptera: Formicidae) in Brazil». Psyche: A Journal of Entomology. 94 (1–2): 9–13. doi:10.1155/1987/85157

- ↑ Ehrenberg, R. (18 de setembro de 2009). «Venom attracts decapitating flies». Science News. Consultado em 30 de dezembro de 2014. Cópia arquivada em 22 de setembro de 2016
- ↑ Morrison, L.W.; Porter, S.D. (2005). «Testing for population-level impacts of introduced Pseudacteon tricuspis flies, phorid parasitoids of Solenopsis invicta fire ants». Biological Control. 33 (1): 9–19. Bibcode:2005BiolC..33....9M. CiteSeerX 10.1.1.542.4377
 . doi:10.1016/j.biocontrol.2005.01.004
. doi:10.1016/j.biocontrol.2005.01.004
- ↑ Schmid-Hempel 1998, p. 94.
- ↑ Kathirithamby, J.; Johnston, J.S. (1992). «Stylopization of Solenopsis invicta (Hymenoptera: Formicidae) by Caenocholax fenyesi (Strepsiptera: Myrmecolacidae) in Texas». Annals of the Entomological Society of America. 85 (3): 293–297. doi:10.1093/aesa/85.3.293
- ↑ Bruce, W.A.; LeCato, G.L. (1980). «Pyemotes tritici: A potential new agent for biological control of the red imported fire ant, Solenopsis invicta (Acari: Pyemotidae)». International Journal of Acarology. 6 (4): 271–274. Bibcode:1980IJAca...6..271B. doi:10.1080/01647958008683230
- ↑ Ahrens, M.E.; Shoemaker, D. (2005). «Evolutionary history of Wolbachia infections in the fire ant Solenopsis invicta». BMC Evolutionary Biology. 5 (1): 35. Bibcode:2005BMCEE...5...35A. PMC 1175846
 . PMID 15927071. doi:10.1186/1471-2148-5-35
. PMID 15927071. doi:10.1186/1471-2148-5-35
- ↑ Schmid-Hempel 1998, p. 34.
- ↑ Capinera 2008, p. 188.
- ↑ Schmid-Hempel 1998, p. 59.
- ↑ a b Briano, J.; Calcaterra, L.; Varone, L. (2012). «Fire ants (Solenopsis spp.) and their natural enemies in southern South America». Psyche: A Journal of Entomology. 2012: 1–19. doi:10.1155/2012/198084

- ↑ Jouvenaz, D.P.; Ellis, E.A. (1986). «Vairimorpha invictae N. Sp. (Microspora: Microsporida), a parasite of the red imported fire ant, Solenopsis invicta Buren (Hymenoptera: Formicidae)». The Journal of Protozoology. 33 (4): 457–461. doi:10.1111/j.1550-7408.1986.tb05641.x
- ↑ Oi, D.H.; Briano, J. A.; Valles, S.M.; Williams, D.F. (2005). «Transmission of Vairimorpha invictae (Microsporidia: Burenellidae) infections between red imported fire ant (Hymenoptera: Formicidae) colonies». Journal of Invertebrate Pathology. 88 (2): 108–115. Bibcode:2005JInvP..88..108O. PMID 15766927. doi:10.1016/j.jip.2004.11.006
- ↑ Nickle, W.R.; Jouvenaz, D.P. (1987). «Tetradonema solenopsis n. sp. (Nematoda: Tetradonematidae) parasitic on the red imported fire ant Solenopsis invicta Buren from Brazil». Journal of Nematology. 19 (3): 311–313. PMC 2618658
 . PMID 19290149
. PMID 19290149
- ↑ Qiu, H.-L.; Lu, L.-H.; Zalucki, M.-P.; He, Y.-R. (2016). «Metarhizium anisopliae infection alters feeding and trophallactic behavior in the ant Solenopsis invicta» (PDF). Journal of Invertebrate Pathology. 138: 24–29. Bibcode:2016JInvP.138...24Q. PMID 27234423. doi:10.1016/j.jip.2016.05.005
- ↑ Durham, S. (2010). «ARS Parasite Collections Assist Research and Diagnoses». Agricultural Research Service. United States Department of Agriculture. Consultado em 25 de agosto de 2014
- ↑ Knell, J.D.; Allen, G.E.; Hazard, E.I. (1977). «Light and electron microscope study of Thelohania solenopsae n. sp. (Microsporida: Protozoa) in the red imported fire ant, Solenopsis invicta». Journal of Invertebrate Pathology. 29 (2): 192–200. Bibcode:1977JInvP..29..192K. PMID 850074. doi:10.1016/0022-2011(77)90193-8
- ↑ «South fights fire ants with pathogen». CNN. 1 de junho de 1998. Consultado em 1 de novembro de 2016. Cópia arquivada em 21 de março de 2004
- ↑ Schmid-Hempel 1998, p. 295.
- ↑ Pereira, R.M. (2004). «Occurrence of Myrmicinosporidium durum in red imported fire ant, Solenopsis invicta, and other new host ants in eastern United States». Journal of Invertebrate Pathology. 86 (1–2): 38–44. Bibcode:2004JInvP..86...38P. PMID 15145249. doi:10.1016/j.jip.2004.03.005
- ↑ Schmid-Hempel 1998, p. 44.
- ↑ Tschinkel 2006, p. 632.
- ↑ Wang, L.; Elliott, B.; Jin, X.; Zeng, L.; Chen, J. (2015). «Antimicrobial properties of nest volatiles in red imported fire ants, Solenopsis invicta (hymenoptera: formicidae)». Naturwissenschaften. 102 (11–12): 66. Bibcode:2015SciNa.102...66W. PMID 26467352. doi:10.1007/s00114-015-1316-1
- ↑ Valles, S.M.; Strong, C.A.; Dang, P.M.; Hunter, W.B.; Pereira, R.M.; Oi, D.H.; Shapiro, A.M.; Williams, D.F. (2004). «A picorna-like virus from the red imported fire ant, Solenopsis invicta: initial discovery, genome sequence, and characterization» (PDF). Virology. 328 (1): 151–157. PMID 15380366. doi:10.1016/j.virol.2004.07.016
- ↑ Valles, S.M.; Strong, C.A.; Oi, D.H.; Porter, S.D.; Pereira, R.M.; Vander Meer, R.K.; Hashimoto, Y.; Hooper-Bùi, L.M.; Sánchez-Arroyo, H.; Davis, T.; Karpakakunjaram, V.; Vail, K.M.; Fudd Graham, L.C.; Briano, J.A.; Calcaterra, L.A.; Gilbert, L.E.; Ward, R.; Ward, K.; Oliver, J.B.; Taniguchi, G.; Thompson, D.C. (2007). «Phenology, distribution, and host specificity of Solenopsis invicta virus-1». Journal of Invertebrate Pathology. 96 (1): 18–27. Bibcode:2007JInvP..96...18V. PMID 17412359. doi:10.1016/j.jip.2007.02.006
- ↑ «Fire ants may have met their match». CNN. Associated Press. 7 de maio de 2007. Cópia arquivada em 13 de maio de 2007
- ↑ Valles, S.M.; Hashimoto, Y. (2009). «Isolation and characterization of Solenopsis invicta virus 3, a new positive-strand RNA virus infecting the red imported fire ant, Solenopsis invicta». Virology. 388 (2): 354–61. PMID 19403154. doi:10.1016/j.virol.2009.03.028
- ↑ Allen, C.; Valles, S.M.; Strong, C.A. (2011). «Multiple virus infections occur in individual polygyne and monogyne Solenopsis invicta ants». Journal of Invertebrate Pathology. 107 (2): 107–111. Bibcode:2011JInvP.107..107A. PMID 21439294. doi:10.1016/j.jip.2011.03.005
- ↑ a b c Trager 1988, p. 419.
- ↑ Buhs 2005, p. 21.
- ↑ Morrill, W.L. (1974). «Production and flight of alate red imported fire ants». Environmental Entomology. 3 (2): 265–271. doi:10.1093/ee/3.2.265
- ↑ a b Alonso, L.E.; Vander Meer, R.K. (1997). «Source of alate excitant pheromones in the red imported fire ant Solenopsis invicta (Hymenoptera: Formicidae)». Journal of Insect Behavior. 10 (4): 541–555. Bibcode:1997JIBeh..10..541A. doi:10.1007/BF02765376
- ↑ Markin, G.P.; Dillier, J.H.; Hill, S.O.; Blum, M.S.; Hermann, H.R. (1971). «Nuptial flight and flight ranges of the imported fire ant, Solenopsis saevissima richteri (Hymenoptera: Formicidae)». Journal of the Georgia Entomological Society. 6 (3): 145–156
- ↑ Obin, M.S.; Vander Meer, R.K. (1994). «Alate semiochemicals release worker behavior during fire ant nuptial flights» (PDF). Journal of Entomological Science. 29 (1): 143–151. doi:10.18474/0749-8004-29.1.143
- ↑ Hung, A.C.F.; Vinson, S. B.; Summerlin, J. W. (1974). «Male sterility in the red imported fire ant, Solenopsis invicta». Annals of the Entomological Society of America. 67 (6): 909–912. doi:10.1093/aesa/67.6.909
- ↑ Trager 1988, p. 422.
- ↑ Capinera 2008, p. 3444.
- ↑ Capinera 2008, p. 3112.
- ↑ Hölldobler & Wilson 1990, p. 156.
- ↑ Fritz, G.N.; Vander Meer, R.K.; Preston, C.A. (2006). «Selective male mortality in the red imported fire ant, Solenopsis invicta». Genetics. 173 (1): 207–213. PMC 1461442
 . PMID 16489215. doi:10.1534/genetics.106.056358
. PMID 16489215. doi:10.1534/genetics.106.056358
- ↑ Hölldobler & Wilson 1990, p. 145.
- ↑ Tschinkel, W. (1992). «Brood raiding and the population dynamics of founding and incipient colonies of the fire ant, Solenopsis invicta». Ecological Entomology. 17 (2): 179–188. Bibcode:1992EcoEn..17..179T. doi:10.1111/j.1365-2311.1992.tb01176.x
- ↑ Goodisman, M.; Ross, K. (1999). «Queen recruitment in a multiple-queen population of the fire ant Solenopsis invicta». Behavioral Ecology. 10 (4): 428–435. doi:10.1093/beheco/10.4.428
- ↑ Tschinkel, W.R.; Howard, D.F. (1983). «Colony founding by pleometrosis in the fire ant, Solenopsis invicta» (PDF). Behavioral Ecology and Sociobiology. 12 (2): 103–113. Bibcode:1983BEcoS..12..103T. doi:10.1007/BF00343200
- ↑ Trager 1988, p. 217.
- ↑ a b Trager 1988, p. 218.
- ↑ Manfredini, F.; Riba-Grognuz, O.; Wurm, Y.; Keller, L.; Shoemaker, D.; Grozinger, C.M.; Tsutsui, N.D. (2013). «Sociogenomics of cooperation and conflict during colony founding in the fire ant Solenopsis invicta». PLOS Genetics. 9 (8). PMC 3738511
 . PMID 23950725. doi:10.1371/journal.pgen.1003633
. PMID 23950725. doi:10.1371/journal.pgen.1003633
- ↑ Bernasconi, G.; Keller, L. (1996). «Reproductive conflicts in cooperative associations of fire ant queens (Solenopsis invicta)» (PDF). Proceedings of the Royal Society B: Biological Sciences. 263 (1369): 509–513. Bibcode:1996RSPSB.263..509B. doi:10.1098/rspb.1996.0077
- ↑ Taber 2000, p. 42.
- ↑ Doebeli, Mi.; Abouheif, E. (2016). «Modeling evolutionary transitions in social insects». eLife. 5. PMC 4744194
 . PMID 26780668. doi:10.7554/eLife.12721
. PMID 26780668. doi:10.7554/eLife.12721
- ↑ Hölldobler & Wilson 1990, p. 157.
- ↑ Hölldobler & Wilson 1990, p. 168.
- ↑ Markin, G. P.; Dillier, J. H.; Collins, H. L. (1973). «Growth and development of colonies of the red imported fire ant, Solenopsis invicta». Annals of the Entomological Society of America. 66 (4): 803–808. doi:10.1093/aesa/66.4.803
- ↑ a b Hölldobler & Wilson 1990, p. 163.
- ↑ Schmid-Hempel 1998, p. 10.
- ↑ Schmid-Hempel 1998, p. 16.
- ↑ Taber 2000, p. 32.
- ↑ Porter, S.D. (1988). «Impact of temperature on colony growth and developmental rates of the ant, Solenopsis invicta». Journal of Insect Physiology. 34 (12): 1127–1133. Bibcode:1988JInsP..34.1127P. doi:10.1016/0022-1910(88)90215-6
- ↑ Helms, K.R.; Vinson, S.B. (2008). «Plant resources and colony growth in an invasive ant: the importance of honeydew-producing Hemiptera in carbohydrate transfer across trophic levels». Environmental Entomology. 37 (2): 487–493. PMID 18419921. doi:10.1093/ee/37.2.487

- ↑ Ross, K. G.; Vargo, E. L.; Fletcher, David J.C. (1987). «Comparative biochemical genetics of three fire ant species in North America, with special reference to the two social forms of Solenopsis invicta (Hymenoptera: Formicidae)». Evolution. 41 (5): 979–990. JSTOR 2409186. PMID 28563420. doi:10.2307/2409186
- ↑ Wang, L.; Xu, Y.; Di, Z.; Roehner, B.M. (2013). «How does group interaction and its severance affect life expectancy?» (PDF). Cornell University Library: 1–28. Bibcode:2013arXiv1304.2935W. arXiv:1304.2935
 . Cópia arquivada (PDF) em 3 de novembro de 2016
. Cópia arquivada (PDF) em 3 de novembro de 2016
- ↑ Calabi, P.; Porter, S.D. (1989). «Worker longevity in the fire ant Solenopsis invicta: Ergonomic considerations of correlations between temperature, size and metabolic rates». Journal of Insect Physiology. 35 (8): 643–649. Bibcode:1989JInsP..35..643C. doi:10.1016/0022-1910(89)90127-3
- ↑ a b Hölldobler & Wilson 1990, p. 170.
- ↑ Davies, N.B.; Krebs, J.R.; West, S.A. (2012). An Introduction to Behavioural Ecology 4th ed. Chichester: Wiley-Blackwell. p. 385. ISBN 978-1-4051-1416-5
- ↑ Passera, L.; Aron, S.; Vargo, E.L.; Keller, L. (2001). «Queen control of sex Ratio in fire ants» (PDF). Science. 293 (5533): 1308–1310. Bibcode:2001Sci...293.1308P. PMID 11509728. doi:10.1126/science.1062076. hdl:2013/ULB-DIPOT:oai:dipot.ulb.ac.be:2013/19205
- ↑ Vargo, E.L.; Fletcher, D.J.C. (1986). «Evidence of pheromonal queen control over the production of male and female sexuals in the fire ant, Solenopsis invicta». Journal of Comparative Physiology A. 159 (6): 741–749. ISSN 1432-1351. doi:10.1007/BF00603727
- ↑ a b Tschinkel 2006, p. 95.
- ↑ Hölldobler & Wilson 1990, p. 187.
- ↑ Goodisman, Michael A. D.; Ross, K.G. (1998). «A test of queen recruitment models using nuclear and mitochondrial markers in the fire ant Solenopsis invicta» (PDF). Evolution. 52 (5): 1416–1422. JSTOR 2411311. PMID 28565383. doi:10.2307/2411311. Consultado em 4 de maio de 2015. Cópia arquivada (PDF) em 5 de maio de 2015
- ↑ Morel, L.; Meer, R.K.V.; Lofgren, C.S. (1990). «Comparison of nestmate recognition between monogyne and polygyne populations of Solenopsis invicta (Hymenoptera: Formicidae)». Annals of the Entomological Society of America. 83 (3): 642–647. doi:10.1093/aesa/83.3.642
- ↑ Schmid-Hempel 1998, p. 191.
- ↑ Trager 1988, p. 204.
- ↑ Fletcher, D.J.C.; Blum, M.S.; Whitt, T.V.; Temple, N. (1980). «Monogyny and polygyny in the fire ant, Solenopsis invicta». Annals of the Entomological Society of America. 73 (6): 658–661. doi:10.1093/aesa/73.6.658
- ↑ Greenberg, L.; Fletcher, D.J.C.; Vinson, S.B. (1985). «Differences in worker size and mound distribution in monogynous and polygynous colonies of the fire ant Solenopsis invicta Buren». Journal of the Kansas Entomological Society. 58 (1): 9–18. JSTOR 25084596
- ↑ Harrison, R.G. (1980). «Dispersal polymorphisms in insects». Annual Review of Ecology and Systematics. 11 (1): 95–118. Bibcode:1980AnRES..11...95H. JSTOR 2096904. doi:10.1146/annurev.es.11.110180.000523
- ↑ DeHeer, C.J.; Goodisman, M.A.D.; Ross, K.G. (1999). «Queen dispersal strategies in the multiple-queen form of the fire ant Solenopsis invicta» (PDF). The American Naturalist. 153 (6): 660–675. Bibcode:1999ANat..153..660D. ISSN 0003-0147. JSTOR 303205. doi:10.1086/303205. hdl:1853/31356. Consultado em 4 de maio de 2015. Cópia arquivada (PDF) em 24 de setembro de 2015
- ↑ Keller, L. (1995). «Social life: the paradox of multiple-queen colonies». Trends in Ecology & Evolution. 10 (9): 355–360. Bibcode:1995TEcoE..10..355K. PMID 21237068. doi:10.1016/S0169-5347(00)89133-8
- ↑ Ross, Kenneth G. (1993). «The breeding system of the fire ant Solenopsis invicta: Effects on colony genetic structure». The American Naturalist. 141 (4): 554–76. Bibcode:1993ANat..141..554R. JSTOR 2462750. PMID 19425999. doi:10.1086/285491
- ↑ Goodisman, M.A.D.; Sankovich, K.A.; Kovacs, J.L. (2006). «Genetic and morphological variation over space and time in the invasive fire ant Solenopsis invicta» (PDF). Biological Invasions. 9 (5): 571–584. doi:10.1007/s10530-006-9059-8. Consultado em 4 de maio de 2015. Cópia arquivada (PDF) em 24 de setembro de 2015
- ↑ Adams, E.S.; Balas, M.T. (1999). «Worker discrimination among queens in newly founded colonies of the fire ant Solenopsis invicta». Behavioral Ecology and Sociobiology. 45 (5): 330–338. Bibcode:1999BEcoS..45..330A. doi:10.1007/s002650050568
- ↑ Chirino, M.G.; Gilbert, L.E.; Folgarait, P.J. (2012). «Behavioral discrimination between monogyne and polygyne red fire ants (Hymenoptera: Formicidae) in their native range». Annals of the Entomological Society of America. 105 (5): 740–745. doi:10.1603/AN11073

- ↑ Goodisman, M.; Ross, K.G. (1997). «Relationship of queen number and queen relatedness in multiple-queen colonies of the fire ant Solenopsis invicta». Ecological Entomology. 22 (2): 150–157. Bibcode:1997EcoEn..22..150G. doi:10.1046/j.1365-2311.1997.t01-1-00052.x
- ↑ Adams, E.S.; Tschinkel, W.R. (2001). «Mechanisms of population regulation in the fire ant Solenopsis invicta: an experimental study». Journal of Animal Ecology. 70 (3): 355–369. doi:10.1046/j.1365-2656
- ↑ «The reduction in the biodiversity of Australian native fauna and flora due to the red imported fire ant, Solenopsis invicta (fire ant)». Department of the Environment and Energy. Government of Australia. Consultado em 10 de agosto de 2016. Cópia arquivada em 22 de setembro de 2016
- ↑ a b c d Wojcik, D.; Allen, C.R.; Brenner, R.J.; Forys, E.A.; Jouvenaz, D.P.; Lutz, R.S. (2001). «Red imported fire ants: impact on biodiversity» (PDF). American Entomologist. 47 (1): 16–23. doi:10.1093/ae/47.1.16. Cópia arquivada (PDF) em 16 de dezembro de 2010
- ↑ Porter, S.D.; Savignano, D.A. (1990). «Invasion of polygyne fire ants decimates native ants and disrupts arthropod community». Ecology. 71 (6): 2095–2106. Bibcode:1990Ecol...71.2095P. JSTOR 1938623. doi:10.2307/1938623
- ↑ Stoker, R.L.; Grant, W.E.; Bradleigh Vinson, S. (1995). «Solenopsis invicta (Hymenoptera: Formicidae) effect on invertebrate decomposers of carrion in central Texas». Environmental Entomology. 24 (4): 817–822. doi:10.1093/ee/24.4.817
- ↑ Ricks, B.L.; Vinson, B.S. (1970). «Feeding acceptability of certain insects and various water-soluble compounds to two varieties of the imported fire ant». Journal of Economic Entomology. 63 (1): 145–148. doi:10.1093/jee/63.1.145
- ↑ Cook, J.L. (2003). «Conservation of biodiversity in an area impacted by the red imported fire ant, Solenopsis invicta (Hymenoptera: Formicidae)». Biodiversity and Conservation. 12 (2): 187–195. Bibcode:2003BiCon..12..187C. doi:10.1023/A:1021986927560
- ↑ Masser, M.P.; Grant, W.E. (1986). «Fire ant-Induced trap mortality of small mammals in east-central Texas». The Southwestern Naturalist. 31 (4): 540–542. Bibcode:1986SWNat..31..540M. JSTOR 3671712. doi:10.2307/3671712
- ↑ Flickinger, E.L. (1989). «Observations of predation by red imported fire ants on live-trapped wild cotton rats». Texas Journal of Science. 41 (2): 223–224
- ↑ Hill, E.P. (1970). «Observations of imported fire ant predation on nestling cottontails». Proceedings of the Annual Conference, Southeastern Association of Game and Fish Commissioners. 23: 171–181
- ↑ Thawley, C.J.; Langkilde, T. (2016). «Invasive fire ant (Solenopsis invicta) predation of eastern fence lizard (Sceloporus undulatus) eggs». Journal of Herpetology. 50 (2): 284–288. doi:10.1670/15-017
- ↑ Mount, R.H.; Trauth, S.E.; Mason, W.H. (1981). «Predation by the red imported fire ant, Solenopsis invicta (Hymenoptera: Formicidae), on eggs of the lizard Cnemidophorus sexlineatus (Squamata: Teiidae)». Journal of the Alabama Academy of Science. 52: 66–70
- ↑ Bartlett, D. (1997). «40 years of thoughts on Paynes Prairie». Reptiles. 5 (7): 68, 70–73
- ↑ Langkilde, T. (2009). «Invasive fire ants alter behavior and morphology of native lizards». Ecology. 90 (1): 208–217. Bibcode:2009Ecol...90..208L. PMID 19294926. doi:10.1890/08-0355.1
- ↑ Bryner, J. (26 de janeiro de 2009). «Lizards' Dance Avoids Deadly Ants». LiveScience. Consultado em 20 de agosto de 2016
- ↑ Kelehear, Crystal; Graham, Sean P.; Langkilde, Tracy (março de 2017). «Defensive Strategies of Puerto Rican Dwarf Geckos (Sphaerodactylus macrolepis) Against Invasive Fire Ants». Herpetologica. 73 (1): 48–54. ISSN 0018-0831. doi:10.1655/HERPETOLOGICA-D-16-00042
- ↑ Freed, P.S.; Neitman, K. (1988). «Notes on predation on the endangered Houston toad, Bufo houstonensis». Texas Journal of Science. 40: 454–456
- ↑ Allen, C.R.; Rice, K.G.; Wojcik, D.P.; Percival, H.F. (1997). «Effect of red imported fire ant envenomization on neonatal American alligators». Journal of Herpetology. 31 (2): 318–321. JSTOR 1565408. doi:10.2307/1565408
- ↑ a b Capinera 2008, p. 1080.
- ↑ Castellanos, Adrian A.; Medeiros, Matthew C. I.; Hamer, Gabriel L.; Morrow, Michael E.; Eubanks, Micky D.; Teel, Pete D.; Hamer, Sarah A.; Light, Jessica E. (2016). «Decreased small mammal and on-host tick abundance in association with invasive red imported fire ants (Solenopsis invicta)». Biology Letters. 12 (9). PMC 5046925
 . PMID 27651533. doi:10.1098/rsbl.2016.0463
. PMID 27651533. doi:10.1098/rsbl.2016.0463
- ↑ Moloney, S.D.; Vanderwoude, C. (2003). «Potential ecological impacts of red imported fire ants in eastern Australia» (PDF). Journal of Agricultural and Urban Entomology. 20 (3): 131–142. Consultado em 20 de agosto de 2016. Cópia arquivada (PDF) em 9 de outubro de 2016
- ↑ Lockley, T.C. (1995). «Effect of imported fire ant predation on a population of the least tern: an endangered species». Southwestern Entomologist. 20: 517–519
- ↑ Sikes, P.J.; Arnold, K.A. (1986). «Red imported fire ant (Solenopsis invicta) predation on cliff swallow (Hirundo pyrrhonota) nestlings in east central Texas». Southwestern Naturalist. 31 (1): 105–106. Bibcode:1986SWNat..31..105S. JSTOR 3670967. doi:10.2307/3670967
- ↑ Campomizzi, A.J.; Morrison, M.L.; Farrell, S.L.; Wilkins, R..N.; Drees, B.M.; Packard, J.M. (2009). «Red imported fire ants can decrease songbird nest survival». The Condor. 111 (3): 534–537. doi:10.1525/cond.2009.090066

- ↑ Morrow, M.E.; Chester, R.E.; Lehnen, S.E.; Drees, B.M.; Toepfer, J.E. (2015). «Indirect effects of red imported fire ants on Attwater's prairie-chicken brood survival». The Journal of Wildlife Management. 79 (6): 898–906. Bibcode:2015JWMan..79..898M. PMC 4745021
 . PMID 26900176. doi:10.1002/jwmg.915
. PMID 26900176. doi:10.1002/jwmg.915
- ↑ Yosef, R.; Lohrer, F.E. (1995). «Loggerhead shrikes, red fire ants and red herrings?» (PDF). The Condor. 97 (4): 1053–1056. JSTOR 1369544. doi:10.2307/1369544
- ↑ «Environment: Fighting the Fire Ant». Time. 2 de novembro de 1970. Consultado em 28 de agosto de 2016. Cópia arquivada em 22 de setembro de 2016
- ↑ Capinera 2008, p. 1771.
- ↑ King, J.R.; Tschinkel, W.R. (2006). «Experimental evidence that the introduced fire ant, Solenopsis invicta, does not competitively suppress co-occurring ants in a disturbed habitat». Journal of Animal Ecology. 75 (6): 1370–1378. Bibcode:2006JAnEc..75.1370K. JSTOR 4125078. PMID 17032369. doi:10.1111/j.1365-2656.2006.01161.x
- ↑ Gao, Y.; Lu, L-H.; He, Y-R.; Qi, G-J.; Zhang, J-Q. (2011). «Interference competition between the red imported fire ant (Solenopsis invicta Buren) and two native ant species (Hymenoptera: Formicidae)». Acta Entomologica Sinica. 54 (5): 602–608
- ↑ LeBrun, E.G.; Abbott, J.; Gilbert, L.E. (2013). «Imported crazy ant displaces imported fire ant, reduces and homogenizes grassland ant and arthropod assemblages». Biological Invasions. 15 (11): 2429–2442. Bibcode:2013BiInv..15.2429L. doi:10.1007/s10530-013-0463-6
- ↑ Vitone, T.; Lucky, A. (2014). «Pavement ant - Tetramorium caespitum». UF/IFAS Featured Creatures. University of Florida. Consultado em 4 de abril de 2016. Cópia arquivada em 19 de abril de 2016
- ↑ King, T.G.; Phillips, S.A. (1992). «Destruction of young colonies of the red imported fire ant by the pavement ant». Entomological News. 103 (3): 72–77. ISSN 0013-872X
- ↑ Chen, Y.C.; Kafle, L.; Shih, C.J. (2011). «Interspecific competition between Solenopsis invicta and two native ant species, Pheidole fervens and Monomorium chinense». Journal of Economic Entomology. 104 (2): 614–621. PMID 21510213. doi:10.1603/ec10240

- ↑ Calcaterra, L.A.; Livore, J.P.; Delgado, A.; Briano, J.A. (2008). «Ecological dominance of the red imported fire ant, Solenopsis invicta, in its native range». Oecologia. 156 (2): 411–421. Bibcode:2008Oecol.156..411C. PMID 18305962. doi:10.1007/s00442-008-0997-y
- ↑ LeBrun, E.G.; Tillberg, C.V.; Suarez, A.V.; Folgarait, P.J.; Smith, C.R.; Holway, D.A. (2007). «An experimental study of competition between fire ants and Argentine ants in their native range.» (PDF). Ecology. 88 (1): 63–75. PMID 17489455. doi:10.1890/0012-9658(2007)88[63:AESOCB]2.0.CO;2
- ↑ Zhou, A.; Liang, G.; Lu, Y.; Zeng, L.; Xu, Y. (2014). «Interspecific competition between the red imported fire ant, Solenopsis invicta Buren and ghost ant, Tapinoma melanocephalum Fabricius for honeydew resources produced by an invasive mealybug, Phenacoccus solenopsis Tinsiley». Arthropod-Plant Interactions. 8 (5): 469–474. Bibcode:2014APInt...8..469Z. doi:10.1007/s11829-014-9324-1
- ↑ Wu, B.; Wang, L.; Liang, G.; Lu, Y.; Zeng, L. (2014). «Food competition mechanism between Solenopsis invicta Buren and Tapinoma melanocephalum Fabricius». Sociobiology. 61 (3): 265–273. doi:10.13102/sociobiology.v61i3.265-273
 . Cópia arquivada em 22 de setembro de 2016
. Cópia arquivada em 22 de setembro de 2016
- ↑ Cassill, D.L.; Vo, K.; Becker, B. (2008). «Young fire ant workers feign death and survive aggressive neighbors». Naturwissenschaften. 95 (7): 617–624. Bibcode:2008NW.....95..617C. PMID 18392601. doi:10.1007/s00114-008-0362-3
- ↑ Kabashima, J.N.; Greenberg, L.; Rust, M.K.; Paine, T.D. (2007). «Aggressive interactions between Solenopsis invicta and Linepithema humile (Hymenoptera: Formicidae) under laboratory conditions.» (PDF). Journal of Economic Entomology. 100 (1): 148–154. PMID 17370822. Consultado em 11 de agosto de 2016. Cópia arquivada (PDF) em 9 de outubro de 2016
- ↑ Capinera 2008, p. 290.
- ↑ Epperson, Deborah M.; Allen, Craig R.; Hogan, Katharine F. E. (janeiro de 2021). «Red Imported Fire Ants Reduce Invertebrate Abundance, Richness, and Diversity in Gopher Tortoise Burrows». Diversity (em inglês). 13 (1): 7. Bibcode:2021Diver...1....7E. ISSN 1424-2818. doi:10.3390/d13010007

- ↑ Hermann, Sara L.; Blackledge, Carissa; Haan, Nathan L.; Myers, Andrew T.; Landis, Douglas A. (4 de outubro de 2019). «Predators of monarch butterfly eggs and neonate larvae are more diverse than previously recognised». Scientific Reports (em inglês). 9 (1): 14304. Bibcode:2019NatSR...914304H. ISSN 2045-2322. PMC 6778129
 . PMID 31586127. doi:10.1038/s41598-019-50737-5
. PMID 31586127. doi:10.1038/s41598-019-50737-5
- ↑ Geest, Emily A.; Berman, David D.; Baum, Kristen A. (novembro de 2023). «Butterfly abundance is higher in areas treated for fire ants». The Journal of Wildlife Management (em inglês). 87 (8). Bibcode:2023JWMan..87E2483G. ISSN 0022-541X. doi:10.1002/jwmg.22483
- ↑ Forys, Elizabeth A.; Quistorff, Anna; Allen, Craig R. (2001). «Potential Fire Ant (Hymenoptera: Formicidae) Impact on the Endangered Schaus Swallowtail (Lepidoptera: Papilionidae)». The Florida Entomologist. 84 (2): 254–258. ISSN 0015-4040. JSTOR 3496176. doi:10.2307/3496176

- ↑ Zhou, A.; Lu, Y.; Zeng, L.; Xu, Y.; Liang, G. (2012). «Does mutualism drive the invasion of two alien species? The case of Solenopsis invicta and Phenacoccus solenopsis». PLOS ONE. 7 (7). Bibcode:2012PLoSO...741856Z. PMC 3402455
 . PMID 22911859. doi:10.1371/journal.pone.0041856
. PMID 22911859. doi:10.1371/journal.pone.0041856
- ↑ Kaplan, I.; Eubanks, M.D. (2002). «Disruption of cotton aphid (Homoptera: Aphididae)—natural enemy dynamics by red imported fire ants (Hymenoptera: Formicidae)». Environmental Entomology. 31 (6): 1175–1183. doi:10.1603/0046-225X-31.6.1175

- ↑ Coppler, L.B.; Murphy, J.F.; Eubanks, M.D. (2007). «Red imported fire ants (Hymenoptera: Formicidae) increase the abundance of aphids in tomato». The Florida Entomologist. 90 (3): 419–425. doi:10.1653/0015-4040(2007)90[419:RIFAHF]2.0.CO;2
 . hdl:10919/95478
. hdl:10919/95478
- ↑ Diaz, R.; Knutson, A.; Bernal, J.S. (2004). «Effect of the red imported fire ant on cotton aphid population density and predation of bollworm and beet armyworm eggs.». Journal of Economic Entomology. 97 (2): 222–229. PMID 15154439. doi:10.1603/0022-0493-97.2.222

- ↑ Tedders, W.L.; Reilly, C.C.; Wood, B.W.; Morrison, R.K.; Lofgren, C.S. (1990). «Behavior of Solenopsis invicta (Hymenoptera: Formicidae) in pecan orchards». Environmental Entomology. 19 (1): 44–53. doi:10.1093/ee/19.1.44
- ↑ Taber 2000, p. 308.
- ↑ More, Daniel R.; Kohlmeier, R E.; Hoffman, Donald R. (março de 2008). «Fatal Anaphylaxis to Indoor Native Fire Ant Stings in an Infant». The American Journal of Forensic Medicine and Pathology. 29 (1): 62–63. PMID 19749619. doi:10.1097/PAF.0b013e3181651b53
- ↑ Fitzgerald, Kevin T.; Flood, Aryn A. (novembro de 2006). «Hymenoptera Stings». Clinical Techniques in Small Animal Practice. 21 (4): 194–204. PMID 17265905. doi:10.1053/j.ctsap.2006.10.002
- ↑ Rhoades, Robert B.; Stafford, Chester T.; James, Frank K. (agosto de 1989). «Survey of fatal anaphylactic reactions to imported fire ant stings». Journal of Allergy and Clinical Immunology. 84 (2): 159–162. PMID 2760357. doi:10.1016/0091-6749(89)90319-9
- ↑ Zamith-Miranda, Daniel; Fox, Eduardo G. P.; Monteiro, Ana Paula; Gama, Diogo; Poublan, Luiz E.; de Araujo, Almair Ferreira; Araujo, Maria F. C.; Atella, Georgia C.; Machado, Ednildo A.; Diaz, Bruno L. (26 de setembro de 2018). «The allergic response mediated by fire ant venom proteins». Scientific Reports. 8 (1): 14427. Bibcode:2018NatSR...814427Z. PMC 6158280
 . PMID 30258210. doi:10.1038/s41598-018-32327-z
. PMID 30258210. doi:10.1038/s41598-018-32327-z
- ↑ Fox, E. G. P. (2016). «Venom Toxins of Fire Ants». In: Gopalakrishnakone P.; Calvete J. Venom Genomics and Proteomics. Dordrecht: Springer
- ↑ dos Santos Pinto, José R. A.; Fox, Eduardo G. P.; Saidemberg, Daniel M.; Santos, Lucilene D.; da Silva Menegasso, Anally R.; Costa-Manso, Eliúde; Machado, Ednildo A.; Bueno, Odair C.; Palma, Mario S. (22 de agosto de 2012). «Proteomic View of the Venom from the Fire Ant Buren». Journal of Proteome Research. 11 (9): 4643–4653. PMID 22881118. doi:10.1021/pr300451g
- ↑ Baer, H.; Liu, T.-Y.; Anderson, M.C.; Blum, M.; Schmid, W.H.; James, F.J. (1979). «Protein components of fire ant venom (Solenopsis invicta)». Toxicon. 17 (4): 397–405. Bibcode:1979Txcn...17..397B. PMID 494321. doi:10.1016/0041-0101(79)90267-8
- ↑ Hoffman, DR; Dove, DE; Jacobson, RS (novembro de 1988). «Allergens in Hymenoptera venom. XX. Isolation of four allergens from imported fire ant (Solenopsis invicta) venom.». The Journal of Allergy and Clinical Immunology. 82 (5 Pt 1): 818–27. PMID 3192865. doi:10.1016/0091-6749(88)90084-X
- ↑ FREEMAN, T; HYLANDER, R; ORTIZ, A; MARTIN, M (1992). «Imported fire ant immunotherapy: Effectiveness of whole body extracts». Elsevier BV. Journal of Allergy and Clinical Immunology. 90 (2): 210–215. ISSN 0091-6749. PMID 1500625. doi:10.1016/0091-6749(92)90073-b
- ↑ McDonald, M. (2006). «Reds under your feet». New Scientist. 189 (2538): 50. Cópia arquivada em 25 de abril de 2016
- ↑ a b c d «Red imported fire ant: declared pest in Western Australia». Department of Agriculture and Food. Government of Western Australia. 2014. Consultado em 21 de agosto de 2016. Cópia arquivada em 22 de setembro de 2016
- ↑ Pimentel, D.; Lach, L.; Zuniga, R.; Morrison, D. (2000). «Environmental and economic costs of nonindigenous species in the United States». BioScience. 50 (1): 53–65. doi:10.1641/0006-3568(2000)050[0053:EAECON]2.3.CO;2

- ↑ Dye, J. (8 de dezembro de 2014). «Red fire ant outbreak in Sydney could cost economy billions». Sydney Morning Herald. Consultado em 8 de dezembro de 2014
- ↑ a b c «Fire Ants». Agriculture Victoria. Government of Victoria. 2004. Consultado em 20 de agosto de 2016. Cópia arquivada em 22 de setembro de 2016
- ↑ Smith, M.R. (1965). House-infesting Ants of the Eastern United States: Their Recognition, Biology, and Economic Importance (PDF). Washington, D.C.: United States Department of Agriculture. p. 43. OCLC 6078460
- ↑ Stiles, J.H.; Jones, R.H. (1998). «Distribution of the red imported fire ant, shape Solenopsis invicta, in road and powerline habitats». Landscape Ecology. 13 (6): 335–346. Bibcode:1998LaEco..13..335S. doi:10.1023/A:1008073813734
- ↑ «U.S. imports fire ant enemies». CNN. 30 de novembro de 1999. Consultado em 1 de novembro de 2016. Cópia arquivada em 3 de novembro de 2016
- ↑ Vander Meer, R. K. Vander; Slowik, T. J.; Thorvilson, H. G. (2002). «Semiochemicals released by electrically stimulated red imported fire ants, Solenopsis invicta». Journal of Chemical Ecology. 28 (12): 2585–2600. Bibcode:2002JCEco..28.2585M. PMID 12564802. doi:10.1023/A:1021448522147
- ↑ Mackay, W.P.; Vinson, S.B.; Irving, J.; Majdi, S.; Messer, C. (1992). «Effect of electrical fields on the red imported fire ant (Hymenoptera: Formicidae)». Environmental Entomology. 21 (4): 866–870. doi:10.1093/ee/21.4.866
- ↑ Slowik, T.J.; Green, B.L.; Thorvilson, H.G. (1997). «Detection of magnetism in the red imported fire ant (Solenopsis invicta) using magnetic resonance imaging». Bioelectromagnetics. 18 (5): 396–399. PMID 9209721. doi:10.1002/(SICI)1521-186X(1997)18:5<396::AID-BEM7>3.0.CO;2-Y
- ↑ Anderson, J.B.; Vander Meer, R.K. (1993). «Magnetic orientation in the fire ant, Solenopsis invicta». Naturwissenschaften. 80 (12): 568–570. Bibcode:1993NW.....80..568A. doi:10.1007/BF01149274
- ↑ Jetter, K.M.; Hamilton, J.; Klotz, J.H. (2002). «Eradication costs calculated: Red imported fire ants threaten agriculture, wildlife and homes» (PDF). California Agriculture. 56 (1): 26–34. doi:10.3733/ca.v056n01p26
- ↑ Greenberg, Les (2018). «The Red Imported Fire Ant, Solenopsis invicta». UC Riverside: 1–2
- ↑ «Fire ant impacts - why they are a problem». Department of Agriculture and Fisheries. Government of Queensland. 2016. Consultado em 20 de agosto de 2016. Cópia arquivada em 22 de setembro de 2016
- ↑ Lofgren, C.S.; Adams, C.T. (1981). «Reduced yield of soybeans in fields infested with the red imported fire ant, Solenopsis invicta». The Florida Entomologist. 64 (1): 199–202. JSTOR 3494619. doi:10.2307/3494619
- ↑ Banks, W.A.; Adams, C.T.; Lofgren, C.S.; Wojcik, D.P. (1990). «Imported fire ant infestation of soybean fields in the southern United States». The Florida Entomologist. 73 (3): 503–504. JSTOR 3495467. doi:10.2307/3495467
- ↑ Adams, C.T.; Plumley, J.K.; Lofgren, C.S.; Banks, W.A. (1976). «Economic Importance of the red imported fire ant, Solenopsis invicta Buren. I. Preliminary investigations of impact on soybean harvest». Journal of the Georgia Entomological Society. 11: 165–169
- ↑ Adams, C.T.; Plumley, J.K.; Banks, W.A.; Lofgren, C.S. (1977). «Impact of red imported fire ant, Solenopsis invicta Buren (Hymenoptera: Formicidae) on harvest of soybean in North Carolina». Journal of the Elisha Mitchell Society. 93: 150–153
- ↑ Apperson, C.S.; Adams, C.T. (1983). «Medical and agricultural importance of red imported fire ant». The Florida Entomologist. 66 (1): 121–126. JSTOR 3494558. doi:10.2307/3494558
- ↑ Capinera 2008, p. 903.
- ↑ Banks, W.A.; Adams, C.T.; Lofgren, C.S. (1991). «Damage to young citrus trees by the red imported fire ant (Hymenoptera: Formicidae)». Journal of Economic Entomology. 84 (1): 241–246. doi:10.1093/jee/84.1.241
- ↑ Capinera 2008, p. 1084.
- ↑ Sterling, W.L. (1978). «Fortuitous biological suppression of the boll weevil by the red imported fire ant». Environmental Entomology. 7 (4): 564–568. doi:10.1093/ee/7.4.564
- ↑ Fillman, D.A.; Sterling, W.L. (1983). «Killing power of the red imported fire ant [Hym.: Formicidae]: a key predator of the boll weevil [Col.: Curculionidae]». Entomophaga. 28 (4): 339–344. Bibcode:1983BioCo..28..339F. doi:10.1007/BF02372186
- ↑ Sterling, W.L.; Dean, D.A.; Fillman, D.A.; Jones, D. (1984). «Naturally-occurring biological control of the boll weevil [Col.: Curculionidae]». Entomophaga. 29 (1): 1–9. Bibcode:1984BioCo..29....1S. doi:10.1007/BF02372203
- ↑ Negm, A.A.; Hensley, S.D. (1967). «The relationship of arthropod predators to crop damage inflicted by the sugarcane borer». Journal of Economic Entomology. 60 (6): 1503–1506. doi:10.1093/jee/60.6.1503
- ↑ Reagan, T.E.; Coburn, G.; Hensley, S.D. (1972). «Effects of mirex on the arthropod fauna of a Louisiana sugarcane field». Environmental Entomology. 1 (5): 588–591. doi:10.1093/ee/1.5.588

- ↑ Capinera 2008, p. 4173.
- ↑ Lemke, L.A.; Kissam, J.B. (1988). «Impact of red imported fire ant (Hymenoptera: Formicidae) predation on horn flies (Diptera: Muscidae) in a cattle pasture treated with pro-drone». Journal of Economic Entomology. 81 (3): 855–858. PMID 3403766. doi:10.1093/jee/81.3.855
- ↑ Lee, J.-H.; Johnson, S.J.; Wright, V.L. (1990). «Quantitative survivorship analysis of the velvetbean caterpillar (Lepidoptera: Noctuidae) pupae in soybean fields in Louisiana». Environmental Entomology. 19 (4): 978–986. doi:10.1093/ee/19.4.978
- ↑ Morrill, W.L. (1977). «Red imported fire ant foraging in a greenhouse». Environmental Entomology. 6 (3): 416–418. doi:10.1093/ee/6.3.416
- ↑ a b Eubanks, M.D. (2001). «Estimates of the direct and indirect effects of red imported fire ants on biological control in field crops». Biological Control. 21 (1): 35–43. Bibcode:2001BiolC..21...35E. doi:10.1006/bcon.2001.0923
- ↑ Wilson, N.L.; Olive, A.D. (1969). «Food habits of the imported fire ant in pasture and pine forest areas in southeastern Louisiana». Journal of Economic Entomology. 62 (6): 1268–1271. doi:10.1093/jee/62.6.1268
- ↑ Hu, G.Y.; Frank, J.H. (1996). «Effect of the red imported fire ant (Hymenoptera: Formicidae) on dung-inhabiting arthropods in Florida». Environmental Entomology. 25 (6): 1290–1296. doi:10.1093/ee/25.6.1290
- ↑ Lopez, J.D. (1982). «Emergence pattern of an overwintering population of Cardiochiles nigriceps in central Texas». Environmental Entomology. 11 (4): 838–842. doi:10.1093/ee/11.4.838
- ↑ Elliot, D. (1 de julho de 2013). «"Crazy Ants" swarming in southeastern states». CBS News. Consultado em 22 de novembro de 2016
- ↑ Lofgren, C.S.; Banks, W.A.; Glancey, B.M. (1975). «Biology and control of imported fire ants». Annual Review of Entomology. 20 (1): 1–30. PMID 1090234. doi:10.1146/annurev.en.20.010175.000245
- ↑ Buhs 2005, pp. 1–2.
- ↑ Williams, D.F.; deShazo, R.D. (2004). «Biological control of fire ants: an update on new techniques». Annals of Allergy, Asthma & Immunology. 93 (1): 15–22. PMID 15281467. doi:10.1016/S1081-1206(10)61442-1
- ↑ Mottern, J.L; Heinz, K.M; Ode, P.J (2004). «Evaluating biological control of fire ants using phorid flies: effects on competitive interactions». Biological Control. 30 (3): 566–583. Bibcode:2004BiolC..30..566M. doi:10.1016/j.biocontrol.2004.02.006
- ↑ Drees, B.M.; Puckett, R. «Potential Biological Control Agents for the Red Imported Fire Ant» (PDF). Texas Imported Fire Ant Research and Management Project. Texas A&M University. Consultado em 21 de agosto de 2016. Cópia arquivada (PDF) em 9 de outubro de 2016
- ↑ Buren, W.F.; Allen, G.E.; Williams, R.N. (1978). «Approaches toward possible pest management of the imported fire ants». Bulletin of the Entomological Society of America. 24 (4): 418–421. doi:10.1093/besa/24.4.418

- ↑ a b c «Integrated Pest Management Manual: Fireants». National Park Service. United States Department of the Interior. 2010. Consultado em 21 de agosto de 2016. Cópia arquivada em 22 de setembro de 2016
- ↑ Bonnefoy, X.; Kampen, H.; Sweeney, K. (2008). Public Health Significance of Urban Pests. Copenhague: World Health Organization, Regional Office for Europe. p. 193. ISBN 978-92-890-7188-8
- ↑ Calixto, A.A.; Harris, M.K.; Knutson, A.; Barr, C.L. (2007). «Native ant responses to Solenopsis invicta Buren reduction using broadcast baits». Environmental Entomology. 36 (5): 1112–1123. PMID 18284735. doi:10.1603/0046-225X(2007)36[1112:NARTSI]2.0.CO;2

- ↑ Klotz, J.H.; Vail, K.M.; Willams, D.F. (1997). «Toxicity of a boric acid-sucrose water bait to Solenopsis invicta (Hymenoptera: Formicidae)». Journal of Economic Entomology. 90 (2): 488–491. doi:10.1093/jee/90.2.488

- ↑ Benson, E.P.; Zungoli, P.A.; Riley, M.B. (2003). «Effects of contaminants on bait acceptance by Solenopsis invicta (Hymenoptera: Formicidae)». Journal of Economic Entomology. 96 (1): 94–97. PMID 12650350. doi:10.1093/jee/96.1.94
- ↑ Capinera 2008, p. 3116.
- ↑ Buhs 2005, p. 20.
Bibliografia
- Buhs, J.B. (2005). The Fire Ant Wars: Nature, Science and Public Policy in Twentieth Century America. Chicago, Ilinóis: Imprensa da Universidade de Chicago. ISBN 978-0-226-07981-3
- Capinera, J. L. (2008). Encyclopedia of Entomology 2.ª ed. Dordrecht, Netherlands: Springer. ISBN 978-1-4020-6242-1
- Hölldobler, B.; Wilson, E.O. (1990). The Ants 🔗. Cambrígia, Massachussetes: Belknap Press of Harvard University Press. ISBN 978-0-674-04075-5
- Schmid-Hempel, P. (1998). Parasites in Social Insects. Princeton, New Jersey: Princeton University Press. ISBN 978-0-691-05924-2
- Taber, S.W. (2000). Fire Ants. College Station, Texas: Texas A&M University Press. ISBN 978-1-60344-711-9
- Trager, J.C. (1988). Advances in Myrmecology 1.ª ed. Leida, Países Baixos: E. J. Brill. ISBN 978-0-916846-38-1
- Tschinkel, W. (2006). The Fire Ants. Cambrígia, Massachussetes: Belknap Press of Harvard University Press. ISBN 978-0-674-02207-2