Citocalasina B
Citocalasina B
| |||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||
| Nomes | |||||||||||||||||||||||
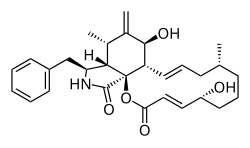
| Nome IUPAC | (1S,4E,6R,10R,12E,14S,15S,17S,18S,19S)-19-bencil-6,15-dihidroxi-10,17-dimetil-16-metilideno-2-oxa-20-azatriciclo[12.7.0.01,18]henicosa-4,12-dieno-3,21-diona | ||||||||||||||||||||||
| Outros nomes | Fomina, phomin | ||||||||||||||||||||||
| |||||||||||||||||||||||
| |||||||||||||||||||||||
| |||||||||||||||||||||||
| Página de dados suplementares | |||||||||||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||||||||||
Citocalasina B (CB), cujo nome provém do grego cytos ('célula') e chalasis ('relaxamento'),[1] é uma micotoxina que pode permear células. Concentrações subestequiométricas de citocalasina B inibem fortemente a formação de redes de filamentos de actina. Devido a isso, é frequentemente utilizada em investigações biológicas. Inibe a divisão do citoplasma (citocinese) bloqueando a formação de microfilamentos contráteis. Inibe o movimento celular e induz a extrusão nuclear. A citocalasina B encurta os filamentos de actina bloqueando a adição de monómeros na extremidade de crescimento rápido dos polímeros.[2] A citocalasina B inibe o transporte de glicose[3] e a agregação de plaquetas. Bloqueia a formação de corpos apoptóticos induzida pela adenosina sem afetar a ativação endógena da ADP-ribosilação em células HL-60 leucemia.[4] É também utilizado na clonagem por transferência nuclear, em que as células recetoras enucleadas são tratadas com citocalasina B. A citocalasina B torna o citoplasma do oócito mais fluido e possibilita a aspiração do genoma nuclear do oócito para uma pequena vesícula de membrana com uma microagulha. Assim, o genoma do ovócito é removido da célula, evitando a rutura da membrana plasmática.
Este alcalóide está isolado do fungo Helminthosporium dematioideum.
História
Anos 60
A citocalasina B (CB) foi descrita pela primeira vez em 1967, quando o Dr. W.B. Turner a isolou dos fungos.[5] Smith et al. descobriram que o CB causa multinucleação nas células e afeta significativamente a motilidade celular. As células multinucleadas surgem provavelmente da falha do controlo mitótico, o que provoca variações no tamanho e na forma dos núcleos na interfase.[6]
Anos 70
Na década de 1970, foram realizadas pesquisas sobre a mitose das células polinucleadas. Aparentemente, estas células eram criadas pela adição progressiva de núcleos, e não pela divisão nuclear.[7] O processo pelo qual isto ocorre é designado por pseudomitose, que é uma mitose síncrona resultante da divisão de um único núcleo.[7] Os núcleos separados são unidos por uma ponte nuclear e, nas células binucleadas, os centríolos são duplicados. Além disso, verificou-se que o CB provoca a desorganização dos microfilamentos de 50 Å das células epiteliais do ratinho, fazendo com que as células percam a sua forma.[8] Afeta também o aparecimento de novas glândulas nas células e a formação de novas glândulas.[9] noutras células. Outro grupo descobriu que o CB inibe a capacidade das células HeLa de realizar citocinese ao quebrar o seu anel contrátil.[10] Pesquisas conduzidas em 1971 mostraram que o CB interfere com a libertação de iodo da tiroglobulina e bloqueia a endocitose do colóide da tiroide.[11] Além disso, o CB teve um efeito inibitório na captação de (3H) sacarose tritiada em células hepáticas humanas da estirpe Chang, e foram observadas alterações na aparência e localização dos microfilamentos nas células tratadas com CB.[12] Além disso, o CB inibiu reversivelmente o movimento dos grânulos de melanina nos melanócitos.[13] Um ano depois, foram realizadas pesquisas sobre a influência do CB nos cloroplastos. Verificou-se que o movimento dos cloroplastos, impulsionado pela luz, é reversivelmente inibido pela citocalasina B.[14] Em 1973, descobriu-se que a citocalasina B era um potente inibidor não competitivo do transporte de glicose. Uma das principais proteínas da membrana eritrocitária identificáveis eletroforeticamente pode ser o sítio de ligação da citocalasina B dos eritrócitos.[15]
Desde 1980
Nos anos seguintes, o conhecimento sobre a citocalasina B aumentou. À medida que se foi adquirindo uma compreensão geral da molécula, foram realizadas análises mais detalhadas, como a do mecanismo de ação.
Produção
As Citocalasinas podem ser isoladas de fungos nos quais ocorrem naturalmente. Originalmente, foram isoladas de Helminthosporium dematioideum. Outros produtores são fungos dos géneros Phoma e Hormiscium e os da espécie Curvularia lunata.[16] Além disso, podem ser sintetizados em laboratório. Existem diversas estratégias que podem ser seguidas. Em primeiro lugar, é possível formar o anel de seis membros do núcleo de isoindolona e o anel macrocíclico maior simultaneamente numa ciclização intramolecular de Diels-Adler numa fase tardia. Em segundo lugar, é possível formar primeiro o núcleo de isoindolona numa reação intermolecular de Diels-Alder e, numa segunda etapa, adicionar o macrociclo em várias etapas.[17]
Propriedades
A citocalasina B contém vários grupos ceto e hidroxilo altamente polares e uma unidade periférica lipofílica benzila.
Mecanismo
O mecanismo predominante da citocalasina B (CB) foi sugerido como sendo a inibição da polimerização dos filamentos de actina pela ligação à extremidade de crescimento rápido ("farpada") dos filamentos de F-actina.[18][19] Uma alternativa poderá ser a intervenção da proteínas cap. Ao fazê-lo, o CB não só inibe a polimerização da actina, mas também processos subsequentes, como a construção da rede filamentosa. Esta inibição pode afetar as três principais etapas da polimerização da actina, que são:
- Nucleação: Forma-se um núcleo inicial de pelo menos 3 monómeros de actina.
- Alongamento: Este núcleo é utilizado para o alongamento pela adição de mais monómeros de actina.
- Estado estacionário/anelamento: É atingido um equilíbrio entre a polimerização e a despolimerização (estado estacionário). O filamento de actina F deixa de crescer e as duas extremidades de crescimento rápido fundem-se para criar um filamento.
A Nucleação é essencial para a montagem do filamento.[20] A Oligomerização é a etapa limitante da velocidade na formação de todo o filamento de actina. A chamada fase retardada da polimerização da actina tem origem nesta etapa. A polimerização demora muito tempo a começar, mas uma vez iniciada, o processo é autocatalítico até que a taxa máxima de polimerização fisiológica seja atingida.
O alongamento é favorecido na extremidade de crescimento rápido do filamento em crescimento.[21] Aqui, a influência da citocalasina B depende fortemente das condições gerais de alongamento. Se estiverem presentes condições fisiológicas ideais, a influência inibitória da citocalasina B é ínfima. Se as condições forem inferiores às ideais, o alongamento pode ser inibido até 90%.[17]
O recozimento é a etapa final da polimerização. As experiências indicam que, nesta fase, as células tratadas com citocalasina B e as células controlo são indistinguíveis, indicando que o CB não tem um efeito significativo nesta fase.
O CB contém um éster beta-insaturado que pode sofrer conjugação do tipo Michael com nucleófilos.[22] Se for esse o caso, o aduto de ADN poderá ser uma reação subsequente plausível. Uma reação mais adequada parece ser entre grupos tiol de várias biomoléculas.[23] Os grupos tiol deixariam de estar disponíveis para criar pontes dissulfeto para posterior polimerização da actina.[24] e, assim, uma etapa crucial na polimerização da actina é inibida, uma vez que as extremidades de crescimento rápido dos filamentos são bloqueadas. Um princípio análogo é utilizado pelas proteínas de encapsulação bem estudadas, que constituem um fator natural limitante da velocidade de polimerização da actina. A primeira etapa da polimerização da actina, uma vez iniciada a polimerização, é a desprotonação do grupo tiol da actina G. Isto deixa o átomo de enxofre carregado disponível para a polimerização da actina. Se a citocalasina B estiver presente na célula, a desprotonação do tiol estará completa. O grupo éster beta-insaturado reativo da citocalasina B reage com o grupo tiol da actina através do ataque nucleofílico do enxofre carregado no átomo de carbono beta. Isto obriga a ligação π a deslocar-se para o lado esquerdo do carbono beta. Consequentemente, ocorre a mesomeria, deslocando a carga negativa entre o carbono alfa e o átomo de oxigénio. Esta etapa é seguida por uma etapa de protonação para contrariar a carga negativa. O ião hidrónio necessário para tal foi produzido durante a ativação do átomo de enxofre numa etapa anterior.
Metabolismo
Existem dez possíveis locais comprovados para a degradação in vitro da citocalasina B. Ainda não existem evidências de que estes mesmos locais sejam utilizados para a degradação in vivo.[25] A degradação por clivagem periodática do composto,[26] que ocorre nos carbonos 14 e 21. Como resultado, são libertados ácido carbónico, formaldeído, 5-metilhexano-1,1,6-triol e uma grande molécula restante. O 5-metilhexano-1,1,6-triol e a grande molécula restante são então oxidados através da reação de Kuhn Roth, levando à formação de 7-hidroxiheptanal, ácido acético e [[ácido benzoico]. Mais uma vez, permanece uma molécula maior. Por outro lado, o 7-hidroxiheptanal, o ácido acético e o ácido benzoico podem sofrer a reação de Schmidt, se não forem degradados por via da degradação ácida pela álcool desidrogenase (ADH) em metilamina e dióxido de carbono. O 7-hidroxiheptano é oxidado a ácido 3-metilheptanodioico. As reações metabólicas subsequentes levam à formação de várias moléculas orgânicas mais pequenas, como aminas, dióxido de carbono e ácido acético. Este último é metabolizado pelo ADH em metilamina e dióxido de carbono. A molécula grande restante é clivada para produzir vários compostos mais pequenos, como o ácido acético, a metilamina e o dióxido de carbono, bem como vários compostos metilados mais pequenos.
Eficácia e efeitos adversos
Interações
Quando a citocalasina B (CB) e o agonista beta-adrenérgico (-)-isoproterenol, prostaglandina E1 ou toxina colérica são adicionados a células de linfoma S49 selvagem, ocorre a acumulação de adenosina monofosfato cíclico (AMPc).[27] O CB não consegue transformar as células tumorais de forma semelhante ao 3T3, mas aumenta a frequência de transformação celular ao multiplicá-la entre 8 e 40.[28] Além disso, o CB pode intensificar a pinocitose, que é induzida pela concanavalina A em Amoeba proteus.[29] O CB pode também interagir com o ácido indol-3-acético do grupo auxinas, que ocorre nos segmentos coleóptilo das raízes do trigo e do milho. Isto resulta na inibição do transporte de vesículas e da secreção de componentes da parede celular, bloqueando assim o alongamento e o crescimento.[30]
Eficácia
Estudos in vitro demonstraram que uma concentração de 30 μM de citocalasina B reduziu significativamente a viscosidade relativa de uma solução normal de filamentos de actina de 20 μM, bem como diminuiu em 20 μM a da solução de filamentos de actina-glutationa.[31] A concentração efetiva in vivo é ainda mais baixa. Parece que uma concentração de 2 μM é suficiente nas células vivas para ter uma influência mensurável na polimerização da actina. A fase de nucleação demorou 2 a 4 vezes mais tempo nos grupos controlo. No alongamento, os efeitos foram mínimos; na anulação, foram insignificantes. Isto pode ocorrer porque existe uma diferença real nas interações moleculares do CB durante estas três etapas ou simplesmente porque a fase retardada é a etapa limitante da velocidade na polimerização global.
Aplicações
Estudos sobre a polimerização da actina
Uma vez que a citocalasina B inibe a polimerização dos filamentos de actina, muitos processos celulares que dependem do funcionamento dos filamentos de actina são afetados. A citocinese é inibida, embora a mitose não seja afetada. Devido aos seus efeitos em várias funções celulares, mas à ausência de toxicidade geral, o CB é aplicado em estudos de polimerização da actina, métodos de imagem celular, estudos de ciclo celular e possivelmente como um medicamento anticancerígeno.[1][32]
Inibe a divisão celular
A citocalasina B é utilizada para testar a genotoxicidade de substâncias. Para tal, o ensaio de micronúcleos de bloqueio da citocinese (ensaio CBMN) é aplicado com linfócitos humanos.[33] Isto funciona in vitro. Os micronúcleos podem ser detetados durante a anáfase da mitose e da meiose.[34] São pequenos núcleos que contêm um cromossoma ou parte de um cromossoma que não atinge um dos polos da célula durante a divisão celular.[35] O test CBMN está baseado en que só as células en división poden expresar micronúcleos, o cal significa que só nesas células se poden detectar os danos cromosómicos.[33] Como a genotoxicidade causa anomalias na célula em divisão, os micronúcleos podem ser detetados nas células binucleadas. A citocinese, a etapa seguinte, é inibida pela citocalasina B. Uma vantagem fundamental deste método é que permite a deteção simultânea de múltiplos eventos moleculares que levam a danos cromossómicos e instabilidade cromossómica. O ensaio CBMN foi aplicado com sucesso em linfócitos humanos normais, linfócitos de baço de ratinho, fibroblastos de ratinho e fibroblastos de hamster chinês.[36]
Inibe o movimento celular
A citocalasina B pode diminuir o número de células móveis quando adicionada às células do sarcoma de Yoshida. Pode também diminuir a motilidade celular e inibir o seu crescimento, dependendo da dose.[37] Como a citocalasina B penetra de forma irregular nas células, promove contrações focais da rede rompida dos filamentos de actina corticais por ação da miosina. Isto causa uma superprecipitação, que requer contrações ativas e, portanto, um metabolismo energético ativo. As contracções corticais desorganizadas distorcem a montagem dos pseudópodes envolvidos no movimento celular.[38]
Induz a extrusão nuclear
A extrusão nuclear induzida pela citocalasina B inicia-se com o movimento do núcleo em direção à membrana plasmática, seguido pela formação de uma protuberância na membrana. O núcleo move-se então para fora da membrana, mas permanece ligado à célula por uma ponte citoplasmática em forma de fio. Se a célula for mantida num meio contendo citocalasina B durante várias horas, o processo torna-se irreversível. A extrusão pode ser auxiliada pelo enfraquecimento da membrana plasmática induzido pela citocalasina B.[39]
Inibe o transporte de glicose
A citocalasina B liga-se covalentemente a proteínas transportadoras de glicose de mamíferos quando irradiada com luz UV.[40] Liga-se mais fortemente à AraE e à GalP do que aos seus substratos habituais.[41] A citocalasina B inibe o GLUT1, 2, 3 e 4.[42] A ligação ao GLUT1 ocorre internamente, uma vez que a citocalasina B atua como um inibidor competitivo do efluxo de glicose.[43] Evidências adicionais provêm de estudos de fotomarcação em que o Trp388 e o Trp412 da proteína purificada são marcados após exposição à citocalasina B marcada. Uma vez que o Trp388 e o Trp412 mutados não reduzem completamente a inibição do GLUT1, presume-se que existam locais adicionais envolvidos na ligação da citocalasina B.[44]
Usos terapêuticos
A citocalasina B tem também sido investigada para fins terapêuticos. Por exemplo, foram examinados os efeitos da citocalasina B nas células tumorais causados por macrófagos ativados por BCG (Bacillus Calmette-Guerin). Observou-se que a citocalasina B aumenta a lise e a estase das células tumorais devido à ação dos macrófagos ativados a uma concentração de 10−7M. A citocalasina B não atua diretamente nos macrófagos, mas exerce o seu efeito predominantemente na célula tumoral. Uma das razões pode ser o facto de a citocalasina B inibir a formação de filamentos de actina, que podem ser importantes para a destruição das células tumorais pelos macrófagos ativados.[45]
Outros efeitos
A citocalasina B tem efeito sobre a secreção de hormona tiroideia e hormona do crescimento.[1] A biossíntese da fosfatidilcolina e da fosfatidiletanolamina é inibida pela citocalasina B, como demonstrado por George et al.[46] Isto ocorre através da inibição da conversão de fosfoetanolamina em CDP-etanolamina. Foi proposto que o mecanismo está associado a alterações nos iões de cálcio intracelulares. A citocalasina B tem também efeitos sobre os microrganismos. Por exemplo, o crescimento e a diferenciação de Entamoeba histolytica são inibidos. Além disso, a citocalasina B tem um efeito inibitório sobre o crescimento celular sem provocar efeitos imunossupressores prolongados ou profundos.[47]
Contexto natural
Na natureza, a citocalasina B está envolvida na virulência fúngica, na deterioração dos alimentos e na manutenção da simbiose entre o hospedeiro e o simbionte.[37]
Notas
Referências
- ↑ a b c Scherlach, K; et al. (2010). «The chemistry and biology of cytochalasins». Natural Product Reports. 27 (6): 869–86. PMID 20411198. doi:10.1039/b903913a
- ↑ Theodoropoulos, PA; Gravanis, A; Tsapara, A; Margioris, AN; Papadogiorgaki, E; Galanopoulos, V; Stournaras, C (1994). «Cytochalasin B may shorten actin filaments by a mechanism independent of barbed end capping». Biochemical Pharmacology. 47 (10): 1875–81. PMID 8204105. doi:10.1016/0006-2952(94)90318-2
- ↑ Jung, C. Y.; Rampal, A. L. (1977). «Cytochalasin B binding sites and glucose transport carrier in human erythrocyte ghosts». The Journal of Biological Chemistry. 252 (15): 5456–5463. PMID 885863. doi:10.1016/S0021-9258(19)63372-7
- ↑ Tanaka, Y.; Yoshihara, K.; Tsuyuki, M.; Kamiya, T. (1994). «Apoptosis Induced by Adenosine in Human Leukemia HL-60 Cells». Experimental Cell Research. 213 (1): 242–559. PMID 8020596. doi:10.1006/excr.1994.1196
- ↑ Smith, GF; Ridler, MA; Faunch, JA (16 de dezembro de 1967). «Action of Cytochalasin B on Cultured Human Lymphocytes». Nature. 216 (5120): 1134–1135. Bibcode:1967Natur.216.1134S. PMID 6075266. doi:10.1038/2161134a0
- ↑ Ridler, MA; Smith, GA (1968). «The Response of Human Cultured Lymphocytes to Cytochalasin B». Journal of Cell Science. 3 (4): 595–602. PMID 5751143. doi:10.1242/jcs.3.4.595
- ↑ a b Smith, G; O'Hara, P; Ridler, M (1970). «The Production of Multinucleated Lymphocytes by Cytochalasin B. An Electron Microscopic Study». Pediatric Research. 4 (5). 441 páginas. doi:10.1203/00006450-197009000-00032
- ↑ Spooner, BS; Wessells, NK (junho de 1970). «Effects of Cytochalasin B upon Microfilaments Involved in Morphogenesis of Salivary Epithelium». Proceedings of the National Academy of Sciences of the United States of America. 66 (2): 360–364. Bibcode:1970PNAS...66..360S. PMC 283052
 . PMID 5271169. doi:10.1073/pnas.66.2.360
. PMID 5271169. doi:10.1073/pnas.66.2.360
- ↑ Wrenn, JT; Wessells, NK (1 de julho de 1970). «Cytochalasin B: Effects upon Microfilaments Involved in Morphogenesis of Estrogen-Induced Glands of Oviduct». PNAS. 66 (3): 904–908. Bibcode:1970PNAS...66..904W. PMC 283136
 . PMID 5269252. doi:10.1073/pnas.66.3.904
. PMID 5269252. doi:10.1073/pnas.66.3.904
- ↑ Schroeder, TE (1970). «Contractile Ring 1. Fine Structure of Dividing Mammalian (HeLa) Cells and Effects of Cytochalasin B». Zeitschrift für Zellforschung und Mikroskopische Anatomie. 109 (4): 431–449. PMC 2108733
 . PMID 5063470. doi:10.1007/bf00343960
. PMID 5063470. doi:10.1007/bf00343960
- ↑ Williams, J; Wollf, J (1971). «Cytochalasin B Inhibits Thyroid Secretion». Biochemical and Biophysical Research Communications. 44 (2): 422–5. PMID 4334139. doi:10.1016/0006-291x(71)90617-6
- ↑ Wagner, R; Rosenber, M; Estensen, R (1971). «Endocytosis in Chang Liver Cells. Quantitation by Sucrose-3H uptake and Inhibition by Cytochalasin B». Journal of Cell Biology. 50 (3): 804–17. PMC 2108291
 . PMID 4329157. doi:10.1083/jcb.50.3.804
. PMID 4329157. doi:10.1083/jcb.50.3.804
- ↑ Malawist, S (1971). «Cytochalasin B Reversibly Inhibits Melanin Granule Movement in Melanocytes». Nature. 234 (5328): 354–5. Bibcode:1971Natur.234..354M. PMID 4944488. doi:10.1038/234354a0
- ↑ Wagner, G; Haupt, W; Laux, A (1972). «Reversible Inhibition of Chloroplast Movement by Cytochalasin B in the Green Alga Maugeofia». Science. 176 (4036): 808–9. Bibcode:1972Sci...176..808W. PMID 17795409. doi:10.1126/science.176.4036.808
- ↑ Taverna, RD; Langdon, RG (1973). «Reversible Association of Cytochalasin B with the Human Erythrocyte Membrane. Inhibition of Glucose Transport and the Stoichiometry of Cytochalasin Binding». Biochimica et Biophysica Acta (BBA) - Biomembranes. 323 (2): 207–219. PMID 4752283. doi:10.1016/0005-2736(73)90145-4
- ↑ Wells, JM; et al. (1981). «Curvularia-Lunata: A New Source of Cytochalasin B». Applied and Environmental Microbiology. 41 (4): 967–971. Bibcode:1981ApEnM..41..967W. PMC 243842
 . PMID 16345760. doi:10.1128/AEM.41.4.967-971.1981
. PMID 16345760. doi:10.1128/AEM.41.4.967-971.1981
- ↑ a b Haidle, AM; Myers, AG (2004). «An Enantioselective, Modular, and General Route to the Cytochalasins: Synthesis of L-696,474 and Cytochalasin B». Proceedings of the National Academy of Sciences of the United States of America. 101 (33): 12048–12053. Bibcode:2004PNAS..10112048H. PMC 514432
 . PMID 15208404. doi:10.1073/pnas.0402111101
. PMID 15208404. doi:10.1073/pnas.0402111101
- ↑ MacLean-Fletcher, S; Pollard, T. D. (1980). «Mechanism of Action of Cytochalasin B on Actin». Cell. 20 (2): 329–341. PMID 6893016. doi:10.1016/0092-8674(80)90619-4
- ↑ A, P; Gravanis, Achille; Tsapara, Anna; Margioris, Andrew N.; Papadogiorgaki, Eva; Galanopoulos, Vassilis; Stournaras, Christos (1994). «Cytochalasin B may Shorten Filaments by a Mechanism Independent of Barbed End Capping». Biochemical Pharmacology. 47 (10): 1875–1881. PMID 8204105. doi:10.1016/0006-2952(94)90318-2
- ↑ Hausman, RE (2007). The Cell: A Molecular Approach. Washington, DC: Sinauer Associates
- ↑ Woodrum, DT; Rich, S. A.; Pollard, T. D. (1975). «Evidence for the Biased Bidirectional Polymerization of Actin Using Heavy Mecromyosin Produced by an Improved Method». Journal of Cell Biology. 67 (1): 231–237. PMC 2109590
 . PMID 240859. doi:10.1083/jcb.67.1.231
. PMID 240859. doi:10.1083/jcb.67.1.231
- ↑ Little, RD (2004). «The Intramolecular Michael Reaction». Organic Reactions: 315–552. ISBN 0471264180. doi:10.1002/0471264180.or047.02
- ↑ Derek, N. «Cytochalasin B run in all species and on all endpoints: Alert 361». Derek Nexus
- ↑ Tang, JX; Janmey, Paul A.; Stossel, Thomas P.; Ito, Tadanao (1999). «Thiol Oxidation of Actin Produces Dimers That Enhance the Elasticity of the F-Actin Network». Biophysical Journal. 76 (4): 2208–2215. Bibcode:1999BpJ....76.2208T. PMC 1300193
 . PMID 10096915. doi:10.1016/S0006-3495(99)77376-5
. PMID 10096915. doi:10.1016/S0006-3495(99)77376-5
- ↑ Bruice, PY (2011). Organic Chemistry. [S.l.]: Prentice Hall
- ↑ Binder, M; Tamm, C (1973). «The Cytochalasans: A New Class of Biologically Active Microbial Metabolites». Angewandte Chemie International Edition. 12 (5): 370–380. PMID 4200278. doi:10.1002/anie.197303701
- ↑ Insel, PA; Koachman, AM (1982). «Cytochalasin B Enhances Hormone and Cholera Toxin-Stimulated Cyclic AMP Accumulation in S49 Lymphoma Cells». Journal of Biological Chemistry. 257 (16): 9717–23. PMID 6286631. doi:10.1016/S0021-9258(18)34132-2
- ↑ Seif, R (1980). «Factors which Disorganize Microtubules or Microfilaments Increase the Frequency of Cell Transformation by Polyoma Virus». Journal of Virology. 36 (2): 421–8. PMC 353658
 . PMID 6253667. doi:10.1128/JVI.36.2.421-428.1980
. PMID 6253667. doi:10.1128/JVI.36.2.421-428.1980
- ↑ Prusch, RD (1981). «A influência da concanavalina A e da citocalasina B na atividade pinocitótica em Amoeba Proteus». Protoplasma. 106 (3–4): 223–230. doi:10.1007/bf01275554
- ↑ Pope, DG; et al. (1979). «The Effect of Cytochalasin B on the Rate of Growth and Ultrastructure of Wheat Coleoptile and Maize Roots». Planta. 144 (4): 373–383. Bibcode:1979Plant.144..373P. PMID 24407327. doi:10.1007/bf00391581
- ↑ Panayotis (1994). «A citocalasina B pode encurtar os filamentos de actina por mecanismos independentes do revestimento da extremidade farpada». Biochemical Pharmacology. 47 (10): 1875–1881. PMID 8204105. doi:10.1016/0006-2952(94)90318-2
- ↑ Carter, SB (1967). «Effects of Cytochalasin B on Mammalian Cells». Nature. 213 (5073): 261–264. Bibcode:1967Natur.213..261C. PMID 6067685. doi:10.1038/213261a0
- ↑ a b Speit, G; Linsenmeyer, R; Schutz, P; Kuehner, S (2012). «Insensitivity of the In Vitro Cytokinesis-Block Micronucleus Assay with Human Lymphocytes for the Detection of DNA Damage Present at the Start of the Cell Culture». Mutagenesis. 27 (6): 743–747. PMID 22869611. doi:10.1093/mutage/ges041
- ↑ «Genotoxicity: The Micronucleus Test». Crios. Consultado em 19 de março de 2013. Cópia arquivada em 28 de agosto de 2012
- ↑ Fenech, M; Kirsch-Volders, M; Nararajan, AT; et al. (2010). «Molecular Mechanisms of Micronucleus, Nucleoplasmic Bridge and Nuclear Bud Formation in Mammalian and Human Cells». Mutagenesis. 26 (1): 125–132. PMID 21164193. doi:10.1093/mutage/geq052
- ↑ Umegaki, K; Fenech, M (2000). «Cytokinesis-Block Micronucleus Assay in WIL2-NS Cells: A Sensitive System to Detect Chromosomal Damage Induced by Reactive Oxygen Species and Activated Human Neutrophils». Mutagenesis. 15 (3): 261–269. PMID 10792021. doi:10.1093/mutage/15.3.261
- ↑ a b Hosaka, S; et al. (1980). «Efeito da Citocalasina B e da Colchicina na Motilidade e no Crescimento de Células do Sarcoma de Yoshida In Vitro». Sci Rep Res Inst Tohoku Univ Ser C: 27
- ↑ Stossel, TP (1981). Chapter 14 Actin Filaments and Secretion: The Macrophage Model. Methods of Cell Biology. Col: Methods in Cell Biology. 23. [S.l.: s.n.] pp. 215–230. ISBN 9780125641234. PMID 7035803. doi:10.1016/s0091-679x(08)61500-9
- ↑ Copeland, M (1974). «Cellular Response to Cytochalasin B - Critical Overview». Cytologia. 39 (4): 709–727. PMID 4448103. doi:10.1508/cytologia.39.709
- ↑ Baly, DL; Horuk, R (1988). «The Biology and Biochemistry of the Glucose Transporter». Biochimica et Biophysica Acta (BBA) - Reviews on Biomembranes. 947 (3): 571–590. PMID 3048404. doi:10.1016/0304-4157(88)90008-1
- ↑ Henderson, PJF (1992). «Sugar—Cation Symport Systems in Bacteria». Molecular Biology of Receptors and Transporters - Bacterial and Glucose Transporters. International Review of Cytology - A Survey of Cell Biology. Col: International Review of Cytology. 137. [S.l.: s.n.] pp. 149–208. ISBN 9780123645371. PMID 1428670. doi:10.1016/s0074-7696(08)62676-5
- ↑ Bernhardt, I (2003). Red Cell Membrane Transport in Health and Disease. [S.l.]: Springer
- ↑ Basketter, DA; Widdas, WF (1978). «Asymmetry of Hexose Transfer System in Human Erythrocytes - Comparison of Effects of Cytochalasin B, Phloretin and Maltose as Competitive Inhibitors». Journal of Physiology. 278 (1): 389–401. PMC 1282356
 . PMID 671319. doi:10.1113/jphysiol.1978.sp012311
. PMID 671319. doi:10.1113/jphysiol.1978.sp012311
- ↑ Inukai, K; et al. (1994). «Replacement of Bath Tryptophan Residues at 388 and 412 Completely Abolish Cytochalasin B Photolabeling of the GLUT1 Glucose Transporter». Biochemical Journal. 302 (2): 355–361. PMC 1137236
 . PMID 8092986. doi:10.1042/bj3020355
. PMID 8092986. doi:10.1042/bj3020355
- ↑ Martin, F; et al. (1981). «Effects of Four Agents that Modify Microtubules and Microfilaments (Vinblastine, Colchicine, Lidocaine, and Cytochalasin B) on Macrophage-Mediated Cytotoxicity on Tumor Cells». Cancer Immunology, Immunotherapy. 10-10 (2–3). 113 páginas. doi:10.1007/bf00205882
- ↑ George, TP; et al. (1991). «Inhibition of Phosphatidylcholine and Phosphatidylethanoamine Biosynthesis by Cytochalasin B in Cultured Glioma Cells: Potential Regulation of Biosynthesis by Ca2+-Dependent Mechanisms». Biochimica et Biophysica Acta (BBA) - Lipids and Lipid Metabolism. 1084 (2): 185–193. PMID 1854804. doi:10.1016/0005-2760(91)90219-8
- ↑ Bogyo, D; et al. (1990). «Cytochalasin-B-Induced Immunosuppression of Murein Allogeneic Anti-Tumor Response and the Effect of Recombinant Human Interleukin-2». Cancer Immunology, Immunotherapy. 32 (6): 400–405. PMC 11038590
 . PMID 1901032. doi:10.1007/bf01741335
. PMID 1901032. doi:10.1007/bf01741335
Ver também
Outros artigos
- Merck Index 13, 2819.
- Benya, P.; Padilla, S. (1993). «Dihydrocytochalasin B Enhances Transforming Growth Factor-β-Induced Reexpression of the Differentiated Chondrocyte Phenotype without Stimulation of Collagen Synthesis». Experimental Cell Research. 204 (2): 268–277. PMID 8440324. doi:10.1006/excr.1993.1033