Ativador do plasminogênio tecidual
| Ativador do t-plasmidogênio | |||||||
|---|---|---|---|---|---|---|---|
 | |||||||
| Indicadores | |||||||
| Número EC | 3.4.21.68 | ||||||
| Número CAS | 139639-23-9-- | ||||||
| Bases de dados | |||||||
| IntEnz | IntEnz | ||||||
| BRENDA | BRENDA | ||||||
| ExPASy | NiceZyme | ||||||
| KEGG | KEGG | ||||||
| MetaCyc | via metabólica | ||||||
| PRIAM | PRIAM | ||||||
| Estruturas PDB | RCSB PDB PDBe PDBj PDBsum | ||||||
| |||||||
Ativador do plasminogênio tecidual (abreviado como t-PA, AP-t ou PLAT) é uma protease sérica secretada que converte a proenzima plasminogênio em plasmina, que é uma enzima fibrinolítica. O plasminogênio é sintetizado como uma cadeia única que é clivada pela t-PA na plasmina de duas cadeias ligadas por dissulfato.
O tPA pode ser obtido usando técnicas biotecnológicas recombinantes; o tPA produzido dessa maneira denomina-se ativador do plasminogénio tecidual recombinante (rtPA). rtPAs específicos são a alteplase, reteplase e tenecteplase. São utilizados em medicina interna para tratar acidentes vasculares cerebrais embólicos ou trombóticos. O uso desta proteína está contraindicado nos acidentes cardiovasculares hemorrágicos e traumas cranioencefálicos. O antídoto para o tPA em caso de toxicidade é o ácido aminocaproico.
Função
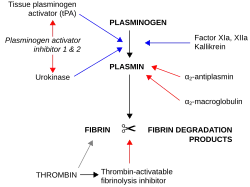
O tPA e a plasmina são as enzimas essenciais da via fibrinolítica na qual ocorre a geração de plasmina mediada por tPA. Concretamente, o tPA cliva o zimogénio plasminogénio no seu ligação peptídica Arg561-Val562, formando a serina protease plasmina.[1]
O aumento desta atividade enzimática causa hiperfibrinólise, que se manifesta como um excesso de hemorragia ou um aumento da permeabilidade vascular.[2] O decréscimo da atividade origina hipofibrinólise, que pode dar lugar a trombose ou embolismo.
Em pacientes de acidentes vascular cerebral isquémicos, a diminuição da atividade do tPA está associada a um aumento da concentração plasmática de P-selectina.[3]
O tPA também desempenha um papel na migração celular e na remodelação de tecidos.[4]
Fisiologia e regulação
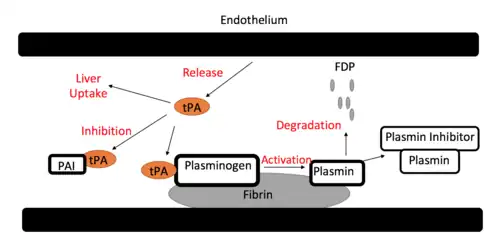
Uma vez no corpo, o tPA administrado pode seguir três rotas; uma delas resulta na atividade trombolítica (ver figura). Após a administração e libertação, o tPA pode ser absorvido pelo fígado e depurado (eliminado) através de recetores desse órgão. Um dos recetores específicos responsável por estes processos é a proteína LRP1.[6] Além disso, o tPA pode ligar-se a um inibidor do ativador do plasminogénio (PAI), o que resulta na inativação da sua atividade, e isto é seguido da sua depuração do corpo pelo fígado. Finalmente, o tPA pode ligar-se ao plasminogénio clivando e separando dele a plasmina. A plasmina, outro tipo de protease, pode ligar-se depois ao inibidor do plasminogénio ou funcionar degradando os coágulos de fibrina, que é a via mais utilizada e desejada no uso clínico.[5]
Genética
O ativador do plasminogénio tecidual é uma proteína codificada no gene PLAT humano, situado no cromossoma 8, que contém 14 exões.[7] O transcrito primário produzido por este gene sofre empalme alternativo, originando vários transcritos, um dos quais codifica uma isoforma que é processada proteoliticamente.[8]
Usos médicos
O tPA é utilizado nalguns casos de doenças que produzem coágulos sanguíneos, como a embolia pulmonar, enfarte do miocárdio e acidente vascular cerebral, num tratamento médico chamado trombólise. O seu uso mais comum é nos AVC (Acidentes Vasculares Cerebrais) isquémicos. Pode ser administrado de forma sistémica, no caso de enfarte do miocárdio, AVC isquémico e na maioria dos casos de embolia pulmonar maciça aguda ou ser administrado através de um cateter arterial diretamente no local da oclusão no caso de trombos arteriais periféricos e trombos nas veias profundas proximais da perna.[9]
AVC isquémico
Estatísticas
Foram realizados doze ensaios de alta qualidade em larga escala sobre o rtPA no AVC isquémico agudo. Uma metanálise desses ensaios concluiu que o rtPA administrado nas primeiras 6 horas após um AVC aumenta significativamente as possibilidades de sobreviver e não ser uma pessoa dependente no seguimento final, especialmente em pacientes tratados nas 3 primeiras horas. No entanto, detetou-se também uma significativa mortalidade, principalmente devido a hemorragias intracranianas aos 7 dias, mas posteriormente a mortalidade não era significativa entre os pacientes tratados e não tratados.[10]
Sugeriu-se que para que o tPA seja efetivo no AVC isquémico, deve ser administrado o mais rapidamente possível após o início dos sintomas do AVC, supondo que os pacientes se apresentem nas Urgências a tempo.[10][11] Muitas diretrizes como a da AHA interpretaram este conjunto de estudos sugerindo que existem subgrupos específicos que podem beneficiar do tPA e recomendam o seu uso numa janela de tempo limitada após o início do AVC. As diretrizes dos protocolos indicam o seu uso intravenoso dentro das primeiras três horas após o evento, depois das quais as suas desvantagens podem ser maiores que os seus benefícios.
Por exemplo, as diretrizes da Canadian Stroke Network assinalam que "Todos os pacientes com AVC isquémico agudo discapacitante que possam ser tratados dentro das 4,5 horas do início dos sintomas deveriam ser avaliados sem demora para determinar a sua elegibilidade para o tratamento" com tPA.[12] Apresentar-se tarde nas Urgências causa uma diminuição na elegibilidade para este tratamento; apenas 3% das pessoas são adequadas para este tratamento.[13] Igualmente, nos Estados Unidos, a janela de administração costuma ser de 3 horas desde o início dos sintomas, mas as diretrizes mais recentes também recomendam o seu uso até às 4,5 horas após o início dos sintomas, dependendo do estado do paciente, história médica, comorbilidade atual e uso de medicação.[14] O tPA parece ser benéfico não só nas obstruções de grandes artérias, mas também no infarto lacunar cerebral. Como o tPA dissolve os coágulos, o seu uso supõe um risco de sofrer hemorragias.
Referências
- ↑ Diapharma Tissue plasminogen activator (tPA)
- ↑ Marcos-Contreras OA, Martinez de Lizarrondo S, Bardou I, Orset C, Pruvost M, Anfray A, Frigout Y, Hommet Y, Lebouvier L, Montaner J, Vivien D, Gauberti M (novembro de 2016). «Hyperfibrinolysis increases blood-brain barrier permeability by a plasmin- and bradykinin-dependent mechanism». Blood. 128 (20): 2423–2434. PMID 27531677. doi:10.1182/blood-2016-03-705384
- ↑ Wang J, Li J, Liu Q (agosto de 2005). «Association between platelet activation and fibrinolysis in acute stroke patients». Neuroscience Letters. 384 (3): 305–9. PMID 15916851. doi:10.1016/j.neulet.2005.04.090
- ↑ Uniprot P00750
- ↑ a b «Tissue Plasminogen Activator (tPA) |». diapharma.com. Consultado em 10 de dezembro de 2017
- ↑ a b Gravanis I, Tsirka SE (fevereiro de 2008). «Tissue-type plasminogen activator as a therapeutic target in stroke». Expert Opinion on Therapeutic Targets. 12 (2): 159–70. PMC 3824365
 . PMID 18208365. doi:10.1517/14728222.12.2.159
. PMID 18208365. doi:10.1517/14728222.12.2.159
- ↑ OMIM 173370
- ↑ GeneCards PLAT
- ↑ Rivera-Bou WL, Cabanas JG, Villanueva SE (20 de novembro de 2008). «Thrombolytic Therapy». Medscape
- ↑ a b Wardlaw JM, Murray V, Berge E, del Zoppo G, Sandercock P, Lindley RL, Cohen G (junho de 2012). «Recombinant tissue plasminogen activator for acute ischaemic stroke: an updated systematic review and meta-analysis». Lancet. 379 (9834): 2364–72. PMC 3386494
 . PMID 22632907. doi:10.1016/S0140-6736(12)60738-7
. PMID 22632907. doi:10.1016/S0140-6736(12)60738-7
- ↑ DeMers G, Meurer WJ, Shih R, Rosenbaum S, Vilke GM (dezembro de 2012). «Tissue plasminogen activator and stroke: review of the literature for the clinician». The Journal of Emergency Medicine. 43 (6): 1149–54. PMID 22818644. doi:10.1016/j.jemermed.2012.05.005
- ↑ Lindsay, Gubitz G, Bayley M, Hill MD, Davies-Schinkel C, Singh S, Phillips S (8 de dezembro de 2010). «Hyperacute stroke management». Canadian best practice recommendations for stroke care. Ottawa, ON: Canadian Stroke Network. Canadian Stroke Strategy Best Practices and Standards Writing Group. pp. 55–84. Consultado em 13 de setembro de 2018. Arquivado do original em 3 de dezembro de 2013
- ↑ Hemmen T (abril de 2008). «Patient delay in acute stroke response». European Journal of Neurology. 15 (4): 315–6. PMC 2677077
 . PMID 18353121. doi:10.1111/j.1468-1331.2008.02083.x
. PMID 18353121. doi:10.1111/j.1468-1331.2008.02083.x
- ↑ Davis SM, Donnan GA (junho de 2009). «4.5 hours: the new time window for tissue plasminogen activator in stroke». Stroke. 40 (6): 2266–7. PMID 19407232. doi:10.1161/STROKEAHA.108.544171