Trombina
| Coagulation factor II, thrombin | |||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Identificadores | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Nomes alternativos | fibrinofermento | ||||||||||||||||||||||||||||||||||||||||||||||||||
| IDs externos | GeneCards: | ||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Wikidata | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
Trombina (fator II ativado) ou fibrinofermento é uma proteína do tipo das serinas protease¹ (EC 3.4.21.5)² e portanto age clivando proteínas em determinados sítios. A sua principal função é converter fibrinogênio em fibrina (proteína filamentar), desempenhando um papel fundamental no processo de coagulação. Serina protease: tipo de enzima chave nos processos de hemostase e trombose.
Geração
A trombina é produzida da protrombina, que é essencialmente o estado inativo desta proteína. A protrombina é produzida no fígado.
Fatores ativados de coagulação Xa e Va formam um complexo que é responsável pela conversão da protrombina em trombina. Deficiência de vitamina K ou administração de warfarin¹ afetam negativamente o funcionamento da trombina.
(¹Warfarin: 3-(alfa-acetonilbenzilo) 4– hidróxi cumarina: um anticoagulante sintético usado terapeuticamente em medicina clínica e como agente para roedor, em doses letais.
Genética
O gene da protrombina tem seu locus (localização) no décimo-primeiro cromossomo (11p11-q12).
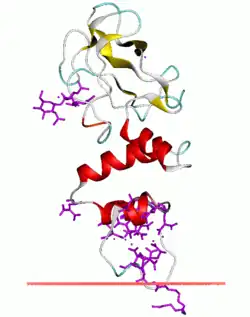
Estrutura
O peso molecular da protrombina é de aproximadamente 72 000 Da. O domínio catalítico é libertado do fragmento 1.2 da protrombina para criar a enzima ativa trombina, que tem um peso molecular de 36 000 Da. Estruturalmente, é um membro do grande clã PA [en] das proteases.
A protrombina é composta por quatro domínios: um domínio Gla [en] N-terminal, dois domínios kringle e um domínio serina protease C-terminal semelhante à tripsina. O fator Xa, com o fator V como cofator, leva à clivagem dos domínios Gla e dois Kringle (formando juntos um fragmento chamado fragmento 1.2) e deixa a trombina, composta exclusivamente pelo domínio serina protease.[2]
Tal como acontece com todas as serinas proteases, a protrombina é convertida em trombina ativa pela proteólise de uma ligação peptídica interna, expondo um novo N-terminal Ile-NH3. O modelo histórico de ativação das proteases de serina envolve a inserção deste N-terminal recém-formado da cadeia pesada no barril β, promovendo a conformação correta dos resíduos catalíticos.[3] Ao contrário das estruturas cristalinas da trombina ativa, estudos de espectrometria de massa de troca de hidrogénio-deutério indicam que este N-terminal Ile-NH3 não é inserido no barril β na forma apo da trombina. No entanto, a ligação do fragmento ativo da trombomodulina parece promover alostericamente a conformação ativa da trombina através da inserção desta região N-terminal.[4]
Ação
Coagulação
Em uma pessoa normal, o processo de coagulação inicia-se segundos após uma ferida atingir o vaso sanguíneo endotélio; quando plaquetas formam uma parede hemostática no lado da ferida. Isto é chamado hemostasia primária (não confundir com hematose). A hemostasia secundária segue quando os componentes do plasma chamados fatores de coagulação¹ respondem (em uma cascata complexa), para formar fibras de fibrina que fortalecem a tampa de plaquetas. Ao contrário do que a crença popular diz, a coagulação de um corte na pele não é iniciado pelo ar ou por secagem, mas porque as plaquetas aderem ao lado de fora dos vasos sanguíneos e pele, e são ativadas pelo colágeno. As plaquetas ativadas, então, liberam grânulos que contém proteínas pro-coagulantes, que realizam coagulação posterior.
O uso de produtos químicos adsorventes, como o Zeolite, e de outros agentes hemostáticos, está também sendo explorado para tampar ferimentos graves rapidamente. ¹A Trombina é o fator de coagulação II ativado.
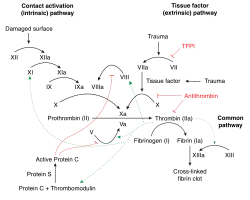
Cascata de Coagulação
A Cascata de Coagulação é um processo complexo no qual vários fatores de coagulação e substâncias atuam para obter uma tampa que fecha uma ferida em um vaso sanguíneo. Ocorre na hemostasia secundária.
A forma ativa do fator II, trombina, tem um número de efeitos em outras proteínas coagulantes. Seu efeito principal é a conversão de fibrinogênio em fibrina, mas também age sobre:
os fatores XI (plasma trombomplastina antecente) e VIII (uma glicoproteína produzida no fígado), aumentando o fluxo dentre os caminhos intrinseco da coagulação; ativa o fator V (proacelerina) o que aumenta a produção de protrombina; e ativa o fator XIII que liga moléculas de fibrina, estabilizando o coágulo.
Plaquetas
A trombina promove o agregamento das plaquetas.
Inibidores e fibrinólise
Interessantemente, a trombina ativa a proteína C, que inibe a coagulação. Isso acontece na superfície do endotélio, em uma proteína chamada trombomodulina. A formação da proteína C ativada é importante para a digestão dos fatores de coagulação Va e VIIIa. Portanto, a trombina além de transformar o fibrinogênio em fibrina, ele também retarda o processo de coagulação (provavelmente, de modo que este não ocorra descontroladamente). Fatores genéticos como o Fator V de Leiden podem interferir diretamente nesse sistema de autocontrole. Nesses casos a ineficiência desse autocontrole da coagulação (via proteína C) pode ocasionar uma hipercoabilidade do sangue, favorecendo a formação de trombos (coágulos) nas veias, cuja condição clínica é a trombose.
A trombina, também inicia a fibrinólise (junto com o fator XII).
Ver também
- Trombospondina 1
Bibliografia
- Poort SR, Rosendaal FR, Reitsma PH, Bertina RM. A common genetic variation in the 3' untranslated region of the prothrombin gene is associated with elevated plasma prothrombin levels and an increase in venous thrombosis. Blood 1996;88:3698-703. PMID 8916933.
- ²EC: Enzyme Commission numbers - número para identificar enzimas. O site expasy.org possui informações sobre esta enzima.)
- Este artigo foi traduzido e adaptado do artigo em inglês, Thrombin.
- Retirado do Dicionário Rossetti)
Referências
- ↑ PDB 1nl2; Huang M, Rigby AC, Morelli X, Grant MA, Huang G, Furie B, Seaton B, Furie BC (setembro de 2003). «Structural basis of membrane binding by Gla domains of vitamin K-dependent proteins». Nature Structural Biology. 10 (9): 751–6. PMID 12923575. doi:10.1038/nsb971
- ↑ Davie EW, Kulman JD (abril de 2006). «An overview of the structure and function of thrombin». Seminars in Thrombosis and Hemostasis. 32 (Suppl 1): 3–15. PMID 16673262. doi:10.1055/s-2006-939550
- ↑ Huber R, Bode W (1 de março de 1978). «Structural basis of the activation and action of trypsin». Accounts of Chemical Research. 11 (3): 114–122. ISSN 0001-4842. doi:10.1021/ar50123a006
- ↑ Handley LD, Treuheit NA, Venkatesh VJ, Komives EA (novembro de 2015). «Thrombomodulin Binding Selects the Catalytically Active Form of Thrombin». Biochemistry. 54 (43): 6650–8. PMC 4697735
 . PMID 26468766. doi:10.1021/acs.biochem.5b00825
. PMID 26468766. doi:10.1021/acs.biochem.5b00825