Túbulo-T
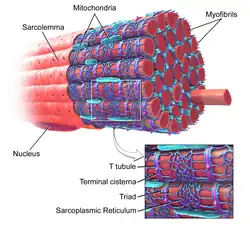
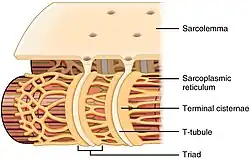
Os túbulos T (túbulos transversos) são extensões da membrana celular que penetram pelo centro das fibras musculares esqueléticas e cardíacas. Os túbulos T, com as suas membranas que contêm grandes concentrações de canais iónicos, transportadores e bombas, permitem a transmissão rápida do potencial de ação na célula, e também exercem uma função importante na regulação da concentração de cálcio celular.
Por meio desses mecanismos, os túbulos T permitem que as células musculares cardíacas (cardiomiócitos) se contraiam mais vigorosamente ao sincronizarem a libertação de cálcio do retículo sarcoplásmico na célula.[1] A estrutura e função do túbulo T são afetadas batimento a batimento pela contração do cardiomiócito,[2] assim como por doenças, contribuindo potencialmente para a insuficiência cardíaca e as arritmias. Embora estas estruturas tenham sido descobertas em 1897, continuam a ser um importante campo de investigação hoje.
Estrutura
Os túbulos T são túbulos formados a partir da mesma bicamada fosfolipídica da membrana da superfície ou sarcolema das células musculares esqueléticas ou cardíacas.[1] Ligam-se diretamente ao sarcolema numa das extremidades e depois introduzem-se profundamente dentro da célula, formando uma rede de túbulos com secções que decorrem tanto perpendicularmente (transversais) como em paralelo (axiais) ao sarcolema.[1] Devido a esta complexa orientação, alguns autores referem-se aos túbulos T como o sistema tubular transverso-axial.[3] O interior do lúmen do túbulo T está aberto na superfície celular, o que significa que o túbulo T está cheio de líquido que contém os mesmos constituintes que a solução que rodeia a célula (o fluido extracelular). Em vez de ser simplesmente um tubo passivo de ligação, a membrana que forma os túbulos T é muito ativa, e está repleta de proteínas como os canais de cálcio tipo L, os permutadores de sódio-cálcio, ATPases de cálcio e beta-adrenoceptores.[1]
Aínda que os túbulos T não se formem até depois do nascimento em cardiomiócitos de ratinhos, ratos, coelhos e gatos (por exemplo, aos 4-9 dias depois do nascimento dos ratos), estão já presentes durante a etapa fetal em espécies como vacas, porquinhos-da-índia, ovelhas e humanos.[4][5][6][7] Encontram-se em células musculares ventriculares na maioria das espécies, e tanto nas células cardíacas das aurículas como nas dos ventrículos nos mamíferos de grande porte.[8] Em células musculares cardíacas, em diferentes espécies, os túbulos T têm um diâmetro entre 20 e 450 nanómetros e costumam estar situados em regiões chamadas discos Z onde os miofilamentos de actina se ancoram na célula.[1] Os túbulos T das células do coração estão estreitamente associados com o armazém de cálcio intracelular, que é o retículo sarcoplásmico, em regiões específicas denominadas cisternas terminais. A associação dos túbulos T com as cisternas terminais chama-se díade.[9]
Nas células musculares esqueléticas, os túbulos T são três ou quatro vezes mais estreitos do que os das células musculares cardíacas, e têm um diâmetro de entre 20 e 40 nm.[1] Estão normalmente localizados em ambos os lados da banda de miosina, na junção de sobreposição (junção A-I) entre as bandas A e I do sarcómero.[10] Os túbulos T do músculo esquelético estão associados com duas cisternas terminais, o que se conhece como tríade.[1][11]
Reguladores
A forma do sistema de túbulos T origina-se e mantém-se pela ação de diversas proteínas. A proteína anfifisina-2 codificada pelo gene BIN1 é a responsável pela formação da estrutura do túbulo T e assegura que se localizem as proteínas apropriadas (especialmente os canais de cálcio tipo L) na membrana dos túbulos T.[12] A juncofilina-2 está codificada pelo gene JPH2 e contribui para a formação de uma união entre a membrana do túbulo T e o retículo sarcoplásmico, vital para o acoplamento excitação-contração.[9] A proteína tipo titina que cobre as extremidades conhecida como teletonina está codificada no gene TCAP e ajuda ao desenvolvimento do túbulo T e é potencialmente responsável pelo incremento do número de túbulos T que se observa quando o músculo cresce.[9]
Função
Acoplamento excitação-contração
Os túbulos T são um elo importante na cadeia que vai desde a excitação elétrica de uma célula até à sua consequente contração (acoplamento excitação-contração). Quando é necessária a contração de um músculo, a estimulação desde um nervo a uma célula muscular adjacente causa um característico fluxo de iões através da membrana celular conhecido como potencial de ação. Em repouso, há menos partículas carregadas positivamente (catiões) no lado interno da membrana do que no lado externo, e diz-se que a membrana está polarizada. Durante o potencial de ação, as partículas carregadas positivamente (maioritariamente iões sódio e cálcio) fluem através da membrana do exterior para o interior. Isto inverte o desequilíbrio normal de iões e denomina-se Despolarização. Uma região da membrana despolariza as regiões contíguas, e a onda resultante de despolarização espalha-se depois ao longo da membrana celular.[13] A polarização da membrana restaura-se à medida que os iões potássio fluem de volta através da membrana do interior para o exterior da célula.
Em células musculares cardíacas, à medida que o potencial de ação passa pelos túbulos T, vai ativando os canais de cálcio tipo L da membrana do túbulo T. A ativação de ditos canais permite que o cálcio passe para o interior da célula. Os túbulos T contêm uma maior concentração de canais de cálcio de tipo L do que o resto do sarcolema e, por tanto, a maioria do cálcio que entra na célula fá-lo através dos túbulos T.[14] Este cálcio une-se e ativa um recetor, conhecido como recetor de ryanodina, localizado no próprio armazém interno de cálcio da célula, o retículo sarcoplásmico. A ativação do recetor de ryanodina causa que o cálcio seja libertado do retículo sarcoplásmico, originando a contração da célula muscular.[15] No entanto, em células do músculo esquelético, o canal de cálcio tipo L está diretamente unido ao recetor de ryanodina do retículo sarcoplásmico permitindo a ativação do recetor de ryanodina diretamente sem necessidade de um influxo de cálcio.[16]
A importância dos túbulos T não se deve apenas à concentração que têm de canais de cálcio tipo L, mas depende também da sua capacidade de sincronizar a libertação de cálcio dentro da célula. O rápido espalhamento do potencial de ação ao longo da rede de túbulos T ativa todos os canais de cálcio tipo L quase simultaneamente. Como os túbulos T fazem com que a membrana do sarcolema chegue muito perto do retículo sarcoplásmico em todas as regiões da célula, o cálcio pode depois ser libertado do retículo sarcoplásmico por toda a célula ao mesmo tempo. Esta sincronização da libertação de cálcio possibilita que as células musculares se contraiam mais vigorosamente.[17] Em células que carecem de túbulos T como células do músculo liso, os cardiomiócitos alterados por uma doença, ou as células musculares nas quais os túbulos T foram eliminados artificialmente, o cálcio que entra pelo sarcolema tem de difundir-se gradualmente através da célula, ativando os recetores de ryanodina muito mais lentamente como uma onda de cálcio que dará lugar a uma contração menos vigorosa.[17]
Como os túbulos T são a localização primária do acoplamento excitação-contração, os canais iónicos e proteínas implicadas neste processo estão concentrados ali (há o triplo de canais de cálcio tipo L localizados dentro da membrana dos túbulos T comparados com o resto do sarcolema). Além disso, os beta-adrenoceptores estão também muito concentrados na membrana do túbulo T,[18] e a sua estimulação incrementa a libertação de cálcio do retículo sarcoplásmico.[19]
Controlo do cálcio
Como o espaço do lúmen do túbulo T é contínuo com o espaço que rodeia a célula (o espaço extracelular), as concentrações de iões em ambos são muito similares. Contudo, devido à importância dos iões dentro dos túbulos T (especialmente do cálcio no músculo cardíaco), é muito importante que estas concentrações permaneçam relativamente constantes. Como os túbulos T são muito delgados, essencialmente "aprisionam" os iões. Isto é importante porque, independentemente das concentrações de iões noutras partes da célula, os túbulos T ainda têm iões cálcio suficientes para permitir a contração muscular. Por tanto, mesmo no caso de baixar a concentração de cálcio fora da célula (Hipocalcemia), a concentração de cálcio dentro do túbulo T permanece relativamente constante, permitindo que a contração cardíaca continue.[9]
Igual que os túbulos T são um sítio de entrada de cálcio na célula, são também um sítio para a retirada do cálcio. Isto é importante já que significa que os níveis de cálcio dentro da célula podem ser estreitamente controlados numa pequena área (ou seja, entre o túbulo T e o retículo sarcoplásmico, o que se conhece como controlo local).[20] Proteínas como o permutador de sódio-cálcio e a ATPase do sarcolema estão localizadas principalmente na membrana do túbulo T.[9] O permutador de sódio-cálcio retira passivamente um ião cálcio da célula trocando-o por três iões sódio. Como é um processo passivo, pode permitir ao cálcio fluir para dentro ou fora da célula dependendo da combinação de concentrações relativas destes iões e a voltagem através da membrana celular (o gradiente eletroquímico).[13] A ATPase de cálcio retira cálcio da célula ativamente, usando energia derivada do adenosina trifosfato (ATP).[13]
Destubulação
Para estudar a função dos túbulos T, estes túbulos podem desacoplar-se artificialmente da membrana superficial usando uma técnica chamada destubulação ou detubulação. Compostos químicos como o glicerol[21] ou a formamida[17] (para o músculo esquelético e o cardíaco, respetivamente) podem ser adicionados à solução extracelular que rodeia as células. Estes agentes aumentam a osmolaridade da solução extracelular, causando que as células encolham (por perda de líquidos). Quando se retiram estes agentes, as células expandem-se rapidamente e tornam ao seu tamanho normal. Este encolhimento e reexpansão da célula causa que os túbulos T se desconectem da membrana superficial.[22] Alternativamente, pode fazer-se com que diminua a osmolaridade da solução extracelular, usando para isso, por exemplo, uma solução salina hipotónica, o que causa que a célula inche transitoriamente. Ao fazer voltar a solução extracelular a uma osmolaridade normal, as células tornam ao seu tamanho prévio, o que causa outra vez a destubulação.[23]
História
A ideia da existência de uma estrutura celular que posteriormente se conheceria como túbulo T foi proposta já em 1881. O tempo tão breve que decorre desde a estimulação da célula muscular estriada e a sua contração era demasiado pequeno para ser causado por uma sinalização química que cobrisse a distância entre o sarcolema e o retículo sarcoplásmico. Por tanto, sugeriu-se que haveria bolsas da membrana que chegariam ao interior da célula, o que poderia explicar o início tão rápido da contração observado.[24][25] No entanto, até 1897 não se observaram os primeiros túbulos T, usando microscópio ótico para estudar o músculo cardíaco injetado com tinta-da-china. Depois a tecnologia de imagens avançou, e com a chegada do microscópio eletrónico de transmissão a estrutura dos túbulos T tornou-se mais evidente,[26] o que levou à descrição do componente longitudinal da rede de túbulos T em 1971.[27] Nas décadas de 1990 e 2000 a microscopia confocal permitiu fazer a reconstrução tridimensional da rede de túbulos T e a quantificação do tamanho dos túbulos T e da sua distribuição,[28] e as relações importantes entre os túbulos T e a libertação de cálcio começaram a aclarar-se com a descoberta dos chamados faíscas de cálcio (calcium sparks).[29] Embora os primeiros trabalhos se focassem no estudo com o músculo cardíaco ventricular e do músculo esquelético, em 2009 observaram-se extensas redes de túbulos T nas células musculares cardíacas auriculares.[30] Investigações que estão agora em marcha centram-se na regulação da estrutura dos túbulos T e em como os túbulos T são afetados e contribuem para as doenças cardiovasculares.[31]
Importância clínica
A estrutura dos túbulos T pode alterar-se por causa de enfermidades, o que no coração pode contribuir para a debilidade do músculo cardíaco ou para ritmos cardíacos anormais. As alterações encontradas em doenças vão desde uma perda completa dos túbulos T a mudanças mais subtis na sua orientação ou padrões de ramificação.[32] Os túbulos T podem perder-se ou distorcer-se depois de um enfarte do miocárdio,[32] e estão também alterados nos ventrículos de doentes com insuficiência cardíaca, contribuindo para reduzir a força de contração e potencialmente diminuindo as probabilidades de recuperação.[33] A insuficiência cardíaca pode também causar a perda quase total dos túbulos T nos cardiomiócitos auriculares, reduzindo a contratilidade auricular e podendo contribuir para a fibrilhação auricular.[30]
As mudanças estruturais nos túbulos T podem originar que os canais de cálcio tipo L se separem dos recetores de ryanodina. Isto pode incrementar o tempo que os níveis de cálcio dentro da célula tardam a elevar-se, causando contrações mais fracas e arritmias.[9][30] No entanto, a estrutura desordenada dos túbulos T pode não ser permanente, como sugere o facto de que a remodelação dos túbulos T se possa reverter por meio do uso de treino intervalado (interval training, que alterna períodos de exercício intenso e de repouso).[9]
Referências
- 1 2 3 4 5 6 7 Hong, TingTing; Shaw, Robin M. (1 de janeiro de 2017). «Cardiac T-Tubule Microanatomy and Function». Physiological Reviews (em inglês). 97 (1): 227–252. ISSN 0031-9333. PMC 6151489
 . PMID 27881552. doi:10.1152/physrev.00037.2015
. PMID 27881552. doi:10.1152/physrev.00037.2015 - ↑ Rog-Zielinska EA, et al. (2021). «Beat-by-Beat Cardiomyocyte T-Tubule Deformation Drives Tubular Content Exchange». Circ. Res. 128 (2): 203–215. PMC 7834912
 . PMID 33228470. doi:10.1161/CIRCRESAHA.120.317266
. PMID 33228470. doi:10.1161/CIRCRESAHA.120.317266 - ↑ Ferrantini, Cecilia; Coppini, Raffaele; Sacconi, Leonardo; Tosi, Benedetta; Zhang, Mei Luo; Wang, Guo Liang; Vries, Ewout de; Hoppenbrouwers, Ernst; Pavone, Francesco (1 de junho de 2014). «Impact of detubulation on force and kinetics of cardiac muscle contraction». The Journal of General Physiology (em inglês). 143 (6): 783–797. PMC 4035744
 . PMID 24863933. doi:10.1085/jgp.201311125
. PMID 24863933. doi:10.1085/jgp.201311125 - ↑ Haddock, Peter S.; Coetzee, William A.; Cho, Emily; Porter, Lisa; Katoh, Hideki; Bers, Donald M.; Jafri, M. Saleet; Artman, Michael (3 de setembro de 1999). «Subcellular [Ca2+]i Gradients During Excitation-Contraction Coupling in Newborn Rabbit Ventricular Myocytes». Circulation Research (em inglês). 85 (5): 415–427. ISSN 0009-7330. PMID 10473671. doi:10.1161/01.RES.85.5.415
- ↑ Munro, Michelle L.; Soeller, Christian (1 de dezembro de 2016). «Early transverse tubule development begins in utero in the sheep heart». Journal of Muscle Research and Cell Motility (em inglês). 37 (6): 195–202. ISSN 1573-2657. PMID 28062939. doi:10.1007/s10974-016-9462-4
- ↑ Kim, Ho-dirk; Kim, Dae-joong; Lee, In-jae; Rah, Bong-jin; Sawa, Yoshiki; Schaper, Jutta (1 de setembro de 1992). «Human fetal heart development after mid-term: Morphometry and ultrastructural study». Journal of Molecular and Cellular Cardiology (em inglês). 24 (9): 949–965. ISSN 0022-2828. doi:10.1016/0022-2828(92)91862-Y
- ↑ Setterberg, Ingunn E.; Le, Christopher; Frisk, Michael; Li, Jia; Louch, William E. (2021). «The Physiology and Pathophysiology of T-Tubules in the Heart». Frontiers in Physiology. 12. ISSN 1664-042X. PMC 8458775
 . PMID 34566684. doi:10.3389/fphys.2021.718404
. PMID 34566684. doi:10.3389/fphys.2021.718404 - ↑ Richards, M. A.; Clarke, J. D.; Saravanan, P.; Voigt, N.; Dobrev, D.; Eisner, D. A.; Trafford, A. W.; Dibb, K. M. (novembro de 2011). «Transverse tubules are a common feature in large mammalian atrial myocytes including human». American Journal of Physiology. Heart and Circulatory Physiology. 301 (5): H1996–2005. ISSN 1522-1539. PMC 3213978
 . PMID 21841013. doi:10.1152/ajpheart.00284.2011
. PMID 21841013. doi:10.1152/ajpheart.00284.2011 - 1 2 3 4 5 6 7 Ibrahim, M.; Gorelik, J.; Yacoub, M. H.; Terracciano, C. M. (22 de setembro de 2011). «The structure and function of cardiac t-tubules in health and disease». Proceedings of the Royal Society B: Biological Sciences (em inglês). 278 (1719): 2714–2723. PMC 3145195
 . PMID 21697171. doi:10.1098/rspb.2011.0624
. PMID 21697171. doi:10.1098/rspb.2011.0624 - ↑ di Fiore, Mariano SH; Eroschenko, Victor P (2008). Di Fiore's Atlas of histology: with functional correlations. Philadelphia: Wolters Kluwer Health/Lippincott Williams & Wilkins. 124 páginas. ISBN 978-0-7817-7057-6
- ↑ «4. Calcium reuptake and relaxation.». www.bristol.ac.uk. Consultado em 21 de fevereiro de 2017
- ↑ Caldwell, Jessica L.; Smith, Charlotte E. R.; Taylor, Rebecca F.; Kitmitto, Ashraf; Eisner, David A.; Dibb, Katharine M.; Trafford, Andrew W. (5 de dezembro de 2014). «Dependence of cardiac transverse tubules on the BAR domain protein amphiphysin II (BIN-1)». Circulation Research. 115 (12): 986–996. ISSN 1524-4571. PMC 4274343
 . PMID 25332206. doi:10.1161/CIRCRESAHA.116.303448
. PMID 25332206. doi:10.1161/CIRCRESAHA.116.303448 - 1 2 3 M., Bers, D. (2001). Excitation-contraction coupling and cardiac contractile force 2ª ed. Dordrecht: Kluwer Academic Publishers. ISBN 9780792371588. OCLC 47659382
- ↑ Scriven, D. R.; Dan, P.; Moore, E. D. (novembro de 2000). «Distribution of proteins implicated in excitation-contraction coupling in rat ventricular myocytes». Biophysical Journal. 79 (5): 2682–2691. Bibcode:2000BpJ....79.2682S. ISSN 0006-3495. PMC 1301148
 . PMID 11053140. doi:10.1016/S0006-3495(00)76506-4
. PMID 11053140. doi:10.1016/S0006-3495(00)76506-4 - ↑ Bers, Donald M. (10 de janeiro de 2002). «Cardiac excitation-contraction coupling». Nature. 415 (6868): 198–205. Bibcode:2002Natur.415..198B. ISSN 0028-0836. PMID 11805843. doi:10.1038/415198a
- ↑ Rebbeck, Robyn T.; Karunasekara, Yamuna; Board, Philip G.; Beard, Nicole A.; Casarotto, Marco G.; Dulhunty, Angela F. (1 de março de 2014). «Skeletal muscle excitation-contraction coupling: who are the dancing partners?». The International Journal of Biochemistry & Cell Biology. 48: 28–38. ISSN 1878-5875. PMID 24374102. doi:10.1016/j.biocel.2013.12.001
- 1 2 3 Ferrantini, Cecilia; Coppini, Raffaele; Sacconi, Leonardo; Tosi, Benedetta; Zhang, Mei Luo; Wang, Guo Liang; de Vries, Ewout; Hoppenbrouwers, Ernst; Pavone, Francesco (1 de junho de 2014). «Impact of detubulation on force and kinetics of cardiac muscle contraction». The Journal of General Physiology. 143 (6): 783–797. ISSN 1540-7748. PMC 4035744
 . PMID 24863933. doi:10.1085/jgp.201311125
. PMID 24863933. doi:10.1085/jgp.201311125 - ↑ Laflamme, M. A.; Becker, P. L. (1 de novembro de 1999). «G(s) and adenylyl cyclase in transverse tubules of heart: implications for cAMP-dependent signaling». The American Journal of Physiology. 277 (5 Pt 2): H1841–1848. ISSN 0002-9513. PMID 10564138. doi:10.1152/ajpheart.1999.277.5.H1841
- ↑ Bers, Donald M. (15 de maio de 2006). «Cardiac ryanodine receptor phosphorylation: target sites and functional consequences». Biochemical Journal. 396 (Pt 1): e1–3. ISSN 0264-6021. PMC 1450001
 . PMID 16626281. doi:10.1042/BJ20060377
. PMID 16626281. doi:10.1042/BJ20060377 - ↑ Hinch, R., Greenstein, J.L., Tanskanen, A.J., Xu, L. and Winslow, R.L. (2004) ‘A simplified local control model of calcium-induced calcium release in cardiac ventricular Myocytes’, 87(6).
- ↑ Fraser, James A.; Skepper, Jeremy N.; Hockaday, Austin R.; Huang1, Christopher L.-H. (1 de agosto de 1998). «The tubular vacuolation process in amphibian skeletal muscle». Journal of Muscle Research & Cell Motility (em inglês). 19 (6): 613–629. ISSN 0142-4319. PMID 9742446. doi:10.1023/A:1005325013355
- ↑ Kawai M, Hussain M, Orchard CH (1999). «Excitation-contraction coupling in rat ventricular myocytes after formamide-induced detubulation». Am J Physiol. 277 (2): H603-9. PMID 10444485. doi:10.1152/ajpheart.1999.277.2.H603
- ↑ Moench, I.; Meekhof, K. E.; Cheng, L. F.; Lopatin, A. N. (julho de 2013). «Resolution of hyposmotic stress in isolated mouse ventricular myocytes causes sealing of t-tubules». Experimental Physiology. 98 (7): 1164–1177. ISSN 1469-445X. PMC 3746342
 . PMID 23585327. doi:10.1113/expphysiol.2013.072470
. PMID 23585327. doi:10.1113/expphysiol.2013.072470 - ↑ Huxley, A. F. (15 de junho de 1971). «The activation of striated muscle and its mechanical response». Proceedings of the Royal Society of London. Series B, Biological Sciences. 178 (1050): 1–27. ISSN 0950-1193. PMID 4397265. doi:10.1098/rspb.1971.0049
- ↑ Hill, A. V. (outubro de 1949). «The abrupt transition from rest to activity in muscle». Proceedings of the Royal Society of London. Series B, Biological Sciences. 136 (884): 399–420. Bibcode:1949RSPSB.136..399H. ISSN 0950-1193. PMID 18143369. doi:10.1098/rspb.1949.0033
- ↑ Lindner, E. (1957). «[Submicroscopic morphology of the cardiac muscle]». Zeitschrift für Zellforschung und Mikroskopische Anatomie. 45 (6): 702–746. ISSN 0340-0336. PMID 13456982
- ↑ Sperelakis, N.; Rubio, R. (agosto de 1971). «An orderly lattice of axial tubules which interconnect adjacent transverse tubules in guinea-pig ventricular myocardium». Journal of Molecular and Cellular Cardiology. 2 (3): 211–220. ISSN 0022-2828. PMID 5117216. doi:10.1016/0022-2828(71)90054-x
- ↑ Savio-Galimberti, Eleonora; Frank, Joy; Inoue, Masashi; Goldhaber, Joshua I.; Cannell, Mark B.; Bridge, John H. B.; Sachse, Frank B. (agosto de 2008). «Novel features of the rabbit transverse tubular system revealed by quantitative analysis of three-dimensional reconstructions from confocal images». Biophysical Journal. 95 (4): 2053–2062. Bibcode:2008BpJ....95.2053S. ISSN 1542-0086. PMC 2483780
 . PMID 18487298. doi:10.1529/biophysj.108.130617
. PMID 18487298. doi:10.1529/biophysj.108.130617 - ↑ Cheng, H.; Lederer, W. J.; Cannell, M. B. (29 de outubro de 1993). «Calcium sparks: elementary events underlying excitation-contraction coupling in heart muscle». Science. 262 (5134): 740–744. Bibcode:1993Sci...262..740C. ISSN 0036-8075. PMID 8235594. doi:10.1126/science.8235594
- 1 2 3 Dibb, Katharine M.; Clarke, Jessica D.; Horn, Margaux A.; Richards, Mark A.; Graham, Helen K.; Eisner, David A.; Trafford, Andrew W. (setembro de 2009). «Characterization of an extensive transverse tubular network in sheep atrial myocytes and its depletion in heart failure». Circulation: Heart Failure. 2 (5): 482–489. ISSN 1941-3297. PMID 19808379. doi:10.1161/CIRCHEARTFAILURE.109.852228
- ↑ Eisner, David A.; Caldwell, Jessica L.; Kistamás, Kornél; Trafford, Andrew W. (7 de julho de 2017). «Calcium and Excitation-Contraction Coupling in the Heart». Circulation Research. 121 (2): 181–195. ISSN 1524-4571. PMC 5497788
 . PMID 28684623. doi:10.1161/CIRCRESAHA.117.310230
. PMID 28684623. doi:10.1161/CIRCRESAHA.117.310230 - 1 2 Pinali, Christian; Malik, Nadim; Davenport, J. Bernard; Allan, Laurence J.; Murfitt, Lucy; Iqbal, Mohammad M.; Boyett, Mark R.; Wright, Elizabeth J.; Walker, Rachel (4 de maio de 2017). «Post-Myocardial Infarction T-tubules Form Enlarged Branched Structures With Dysregulation of Junctophilin-2 and Bridging Integrator 1 (BIN-1)». Journal of the American Heart Association. 6 (5 (número de artigo: e004834)). ISSN 2047-9980. PMC 5524063
 . PMID 28473402. doi:10.1161/JAHA.116.004834
. PMID 28473402. doi:10.1161/JAHA.116.004834 - ↑ Seidel, Thomas; Navankasattusas, Sutip; Ahmad, Azmi; Diakos, Nikolaos A.; Xu, Weining David; Tristani-Firouzi, Martin; Bonios, Michael J.; Taleb, Iosif; Li, Dean Y. (25 de abril de 2017). «Sheet-Like Remodeling of the Transverse Tubular System in Human Heart Failure Impairs Excitation-Contraction Coupling and Functional Recovery by Mechanical Unloading». Circulation. 135 (17): 1632–1645. ISSN 1524-4539. PMC 5404964
 . PMID 28073805. doi:10.1161/CIRCULATIONAHA.116.024470
. PMID 28073805. doi:10.1161/CIRCULATIONAHA.116.024470