Lindano
Lindano | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||
| Nomes | |||||||||||||||
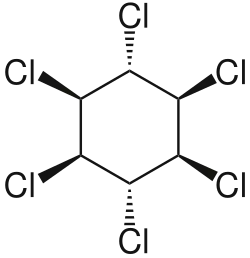
| Nome IUPAC | (1r,2R,3S,4r,5R,6S)-1,2,3,4,5,6-hexaclorocicloexano | ||||||||||||||
| |||||||||||||||
| |||||||||||||||
| |||||||||||||||
| Página de dados suplementares | |||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||
Lindano (γ-HCH), também conhecido como gama-hexaclorocicloexano, gammexano e hexacloreto de benzeno (BHC), é um composto organoclorado que foi amplamente utilizado como pesticida agrícola e como medicamento pediculicida e escabicida para uso tópico.[1] Trata-se do isômero gama do hexaclorocicloexano (HCH), único isômero com atividade inseticida significativa.
O lindano é um neurotóxico que interfere na função do GABA ao interagir com o complexo receptor GABAA–canal de cloreto no sítio de ligação da picrotoxina.[1] Em 2015, a Agência Internacional de Pesquisa sobre o Câncer (IARC) classificou o lindano como carcinógeno do Grupo 1 (cancerígeno humano confirmado), com evidências suficientes de associação ao linfoma não-Hodgkin.[2] Em 2009, sua produção e uso agrícola foram banidos pela Convenção de Estocolmo sobre poluentes orgânicos persistentes.[3] No Brasil, todos os usos do lindano foram proibidos pela ANVISA por meio da RDC n.º 165, de 18 de agosto de 2006.[4]
Histórico
O hexaclorocicloexano (HCH) foi sintetizado pela primeira vez em 1825 pelo cientista britânico Michael Faraday, por meio da reação do benzeno com cloro sob luz solar intensa.[1] Em 1912, o químico neerlandês Teunis van der Linden (1884–1965) isolou e descreveu o isômero gama (γ-HCH) puro, e o composto recebeu o nome de lindano em sua homenagem.[1]
As propriedades inseticidas do gama-HCH não foram reconhecidas até a década de 1940. Pesquisas realizadas nos laboratórios de Jealott's Hill da Imperial Chemical Industries (ICI), no Reino Unido, identificaram em 1942 que o isômero gama era o principal componente ativo da mistura de HCH com ação inseticida.[5] O desenvolvimento do lindano foi acelerado durante a Segunda Guerra Mundial, quando importações do inseticida rotenona foram restringidas, tornando urgente a busca por alternativas.[5] Estima-se que entre 1950 e 2000 foram produzidas cerca de 600 mil toneladas de lindano no mundo.[5]
A produção de lindano gerava grandes volumes de resíduos: para cada tonelada do produto, eram geradas de seis a dez toneladas de isômeros de HCH indesejados, depositados a céu aberto e contaminando solos e águas subterrâneas em diversos países.[5]
Síntese e propriedades físico-químicas
O lindano é produzido industrialmente pela fotocloração do benzeno sob luz ultravioleta, gerando uma mistura técnica de isômeros de HCH com composição aproximada de 65–70% de α-HCH, 7–10% de β-HCH, 14–15% de γ-HCH (lindano) e cerca de 7% de δ-HCH.[1] A Organização Mundial da Saúde (OMS) e a ISO reservam o nome "lindano" para o material contendo mais de 99% de γ-HCH.[1]
O composto se apresenta como pó cristalino branco, de baixa solubilidade em água, porém solúvel em solventes orgânicos apolares e polares apróticos.[1] A combinação entre baixa solubilidade em água e alta capacidade de adsorção em matéria orgânica favorece o acúmulo do composto ao longo da cadeia alimentar, especialmente em tecidos ricos em gordura dos organismos vivos.[6]
Mecanismo de ação
O lindano atua como neurotoxina ao se ligar ao complexo receptor GABAA–canal de cloreto no sítio de ligação da picrotoxina, bloqueando o fluxo de íons cloreto para o interior dos neurônios.[1] Esse bloqueio inibe a ação inibitória do GABA sobre o sistema nervoso central, resultando em hiperexcitabilidade neuronal, convulsões e, em doses elevadas, morte.[1] Nos insetos, o mesmo mecanismo provoca hiperexcitação e óbito.
Possíveis destinos no meio ambiente
Dependendo das propriedades do solo e do relevo da região, o lindano pode ser carreado até rios,[6] ficar retido no solo, ir para a atmosfera ou ainda ser transportado por grandes distâncias.[7] Os solos argilosos com alto teor de matéria orgânica tendem a reter resíduos por maior tempo, intensificando a persistência desse pesticida.
Quando utilizado na agricultura, estima-se que 12–30% da quantidade aplicada se volatiliza para a atmosfera, ficando sujeita ao transporte de longa distância e podendo ser depositada por precipitação.[1] O lindano no solo pode infiltrar-se até águas superficiais e subterrâneas e se bioacumular na cadeia alimentar.
Reações e biodegradação
Muitos compostos organoclorados são recalcitrantes e apresentam alta resistência à degradação química e biológica. Os isômeros de HCH apresentam baixa solubilidade em água e alta solubilidade em solventes orgânicos, especialmente os apolares e polares apróticos.[8] A combinação entre a baixa solubilidade em água e a alta capacidade de adsorção na matéria orgânica leva ao acúmulo desses compostos ao longo da cadeia alimentar, especialmente nos tecidos ricos em gorduras dos organismos vivos.[6]
No solo e na água, o HCH é normalmente biodegradado por algas, fungos e bactérias em moléculas cloradas eventualmente menos tóxicas. Condições tanto anaeróbicas quanto aeróbias favorecem a biodegradação ou metabolização do lindano.[8] A meia-vida para degradação ambiental do lindano, em condições naturais com umidade e submersão, varia de poucos dias a cerca de três anos, dependendo de fatores como tipo de solo, clima e profundidade de aplicação.[9]
Riscos à saúde
A Agência de Proteção Ambiental dos Estados Unidos (EPA) determina que o lindano pode causar efeitos no sistema nervoso a partir de exposições de curta duração em concentrações superiores a 0,0002 mg/L na água, além de temperatura corporal elevada e edema pulmonar em crianças expostas agudamente ao composto.[10]
Entre os riscos à saúde humana associados aos isômeros de HCH encontram-se irritações pulmonares, problemas cardíacos e sanguíneos, encefalias, convulsões e alteração dos níveis de hormônios sexuais.[7]
Em 2015, a IARC classificou o lindano como carcinógeno do Grupo 1 (cancerígeno humano confirmado), com base em evidências de associação ao linfoma não-Hodgkin em estudos epidemiológicos de trabalhadores agrícolas nos EUA e no Canadá.[2] Estudos em animais demonstraram aumento consistente na incidência de tumores hepáticos benignos e malignos.[2]
De acordo com os Valores Orientadores para Solos e Águas Subterrâneas no Estado de São Paulo (CETESB, Decisão de Diretoria 045/2014/E/C/I), o Valor de Intervenção (VI) do lindano para água subterrânea é de 0,002 mg/L.[11]
Regulamentação
Em 2009, a produção e o uso agrícola do lindano foram banidos internacionalmente pela Convenção de Estocolmo sobre Poluentes Orgânicos Persistentes.[3] Uma isenção específica permitiu por cinco anos adicionais o uso farmacêutico como tratamento de segunda linha para pediculose e escabiose.[3]
No Brasil, a ANVISA proibiu todos os usos do lindano por meio da RDC n.º 165, de 18 de agosto de 2006, com base na alta toxicidade, na provável carcinogenicidade e nos efeitos sobre o sistema nervoso central.[4] A comercialização ficou proibida a partir de 30 de março de 2007, e a utilização encerrou-se em 30 de junho de 2007.[4]
Referências
- 1 2 3 4 5 6 7 8 9 10 IARC Working Group on the Evaluation of Carcinogenic Risks to Humans. DDT, Lindane, and 2,4-D. Lyon: International Agency for Research on Cancer, 2018. (IARC Monographs on the Evaluation of Carcinogenic Risks to Humans, v. 113). Disponível em: https://www.ncbi.nlm.nih.gov/books/NBK507412/. Acessado em: 17 de janeiro de 2026.
- 1 2 3 International Agency for Research on Cancer. IARC Monographs evaluate DDT, lindane, and 2,4-D. IARC Press Release n.º 236. Lyon: IARC/OMS, 23 jun. 2015. Disponível em: https://www.iarc.who.int/wp-content/uploads/2018/07/pr236_E.pdf. Acessado em: 17 de janeiro de 2026.
- 1 2 3 Report of the Conference of the Parties of the Stockholm Convention on Persistent Organic Pollutants on the work of its fourth meeting. Genebra, 4–8 maio 2009. Disponível em: http://chm.pops.int/Portals/0/Repository/COP4/UNEP-POPS-COP.4-38.English.pdf. Acessado em: 17 de janeiro de 2026.
- 1 2 3 Brasil. Agência Nacional de Vigilância Sanitária. Resolução da Diretoria Colegiada – RDC n.º 165, de 18 de agosto de 2006. Proíbe todos os usos do Ingrediente Ativo Lindano no Brasil. Disponível em: https://anvisalegis.datalegis.net/action/ActionDatalegis.php?acao=abrirTextoAto&link=S&tipo=RDC&numeroAto=00000165&seqAto=002&valorAno=2006&orgao=RDC/DC/ANVISA/MS. Acessado em: 17 de janeiro de 2026.
- 1 2 3 4 Vijgen, J. The Legacy of Lindane HCH Isomer Production. Internacional HCH & Pesticides Forum. IPEN, jan. 2006. Disponível em: https://www.cluin.org/download/misc/Lindane_Main_Report_DEF20JAN06.pdf. Acessado em: 17 de janeiro de 2026.
- 1 2 3 FLORES, A. V. et al. Organoclorados: um problema de saúde pública. Ambiente & Sociedade, Campinas, v. 7, n. 2, jul./dez. 2004.
- 1 2 IPT – Instituto de Pesquisas Tecnológicas do Estado de São Paulo. Disponível em: http://www.ipt.br/projetos/3.htm. Acessado em: 17 de janeiro de 2026.
- 1 2 SILVA, Aline Ramos da. Biodegradação de hexaclorociclohexano utilizando microrganismos e enzimas desenhadas computacionalmente. 2014. Tese (Doutorado em Biotecnologia) – Universidade de São Paulo, São Paulo, 2014. Disponível em: http://www.teses.usp.br/teses/disponiveis/87/87131/tde-16052014-124535/pt-br.php. Acessado em: 17 de janeiro de 2026.
- ↑ MENDES, R. Hexaclorociclohexano (HCH) e a Saúde Humana: Síntese do Estágio Atual do Conhecimento e Identificação das Principais Questões Controversas. Relatório técnico. Departamento de Ciência e Tecnologia em Saúde/Secretaria de Políticas de Saúde/Ministério da Saúde, 2001.
- ↑ U.S. Environmental Protection Agency. National Primary Drinking Water Regulations – Lindane. Disponível em: http://www.epa.gov/ogwdw/pdfs/factsheets/soc/tech/lindane.pdf. Acessado em: 17 de janeiro de 2026.
- ↑ CETESB – Companhia Ambiental do Estado de São Paulo. Decisão de Diretoria n.º 045/2014/E/C/I, de 20 de fevereiro de 2014. Disponível em: https://web.archive.org/web/20140601055725/http://www.cetesb.sp.gov.br/userfiles/file/institucional/do/2014/DD-045-2014-P53.pdf. Acessado em: 17 de janeiro de 2026.