Fluoreto de potássio
Fluoreto de potássio | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||
| Nomes | |||||||||||||||||||
| Nome IUPAC | Potassium fluoride | ||||||||||||||||||
| |||||||||||||||||||
| |||||||||||||||||||
| |||||||||||||||||||
| |||||||||||||||||||
| Página de dados suplementares | |||||||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||||||
Fluoreto de potássio é o composto de fórmula química KF[1]É a segunda maior fonte do íon fluoreto na indústria e na química orgânica, ficando atrás apenas do fluoreto de hidrogênio. Por ser um sal de haleto de metal alcalino, ele ocorre naturalmente como o raro mineral carobbiita
Princípios Químicos e Mecanismos Estruturais
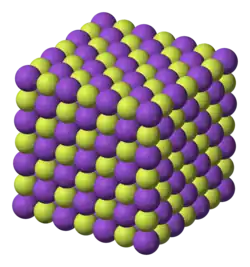
O fluoreto de potássio é um composto iônico que se cristaliza na estrutura cúbica de face centrada (Símbolo de Pearson cF8), a mesma estrutura do cloreto de sódio (NaCl). Essa configuração geométrica garante que cada íon de potássio ( ) seja cercado por seis íons de fluoreto ( ) e vice-versa, resultando em uma rede cristalina altamente estável.
Em condições padrão, o KF apresenta-se como um pó branco ou cristais incolores, sendo altamente higroscópico (absorve umidade do ar com facilidade), o que frequentemente o leva a formar hidratos, como o KF·2H₂O. Sua solubilidade em água é elevada devido à forte interação entre os íons e as moléculas de água, resultando em soluções ligeiramente alcalinas devido à hidrólise do íon fluoreto.
Isomerismo e Configuração Molecular
Diferente das moléculas orgânicas, o fluoreto de potássio não apresenta isomerismo de cadeia ou óptico, pois é uma rede iônica infinita. No entanto, ele exibe variações em sua configuração estrutural dependendo da temperatura e pressão: Polimorfismo: Sob pressões extremamente elevadas, o KF pode sofrer uma transição de fase da estrutura tipo NaCl para uma estrutura tipo CsCl (cloreto de césio), onde a coordenação dos íons muda de 6 para 8. Complexos de Bifluoreto: Em presença de excesso de fluoreto de hidrogênio (HF), o KF reage para formar o bifluoreto de potássio ( ). Este sal contém o ânion , que possui a ligação de hidrogênio mais forte conhecida, sendo um isômero funcional importante no processamento industrial de flúor.
Ocorrência Natural e Síntese
Embora o mineral carobbiita seja a forma natural do KF, ele é extremamente escasso e encontrado principalmente em depósitos vulcânicos (como no Monte Vesúvio). Por isso, quase todo o fluoreto de potássio utilizado globalmente é sintetizado industrialmente. A produção ocorre tipicamente através da reação de neutralização entre o carbonato de potássio (K2CO3)
ou a potassa cáustica (KOH) com o ácido fluorídrico (HF)
O produto é então purificado através de processos de evaporação e secagem controlada para evitar a formação excessiva de hidratos.
Aplicações Industriais e Laboratoriais
O KF é um reagente versátil com aplicações que vão da metalurgia à síntese fina: Química Orgânica (Fluoração): É amplamente utilizado para converter clorocarbonetos em fluorocarbonetos através da Reação de Finkelstein. É a escolha preferida para introduzir flúor em moléculas orgânicas devido à sua alta solubilidade em solventes polares aprotic (como o DMF ou DMSO). Metalurgia: Atua como um fluxo de soldagem, ajudando a remover óxidos da superfície dos metais durante processos de brasagem e solda. Gravação de Vidro: Devido à reatividade do íon fluoreto com silicatos, o KF é utilizado em formulações para foscar ou gravar superfícies de vidro de maneira controlada. Saúde: Em alguns países, o fluoreto de potássio é adicionado ao sal de cozinha (sal fluorado) como uma medida de saúde pública para a prevenção da cárie dentária, de forma análoga à fluoretação da água.
=Vantagens e Desafios de Manuseio
A principal vantagem do KF em relação a outros fluoretos (como o NaF) é sua maior solubilidade, o que acelera as reações químicas. Contudo, ele apresenta desafios significativos: Toxicidade: Como todos os fluoretos solúveis, o KF é tóxico se ingerido ou inalado em grandes quantidades, podendo causar fluorose ou hipocalcemia aguda. Corrosividade: Em presença de umidade, pode liberar traços de ácido fluorídrico, que é altamente corrosivo para tecidos vivos e equipamentos de vidro. O armazenamento deve ser feito em recipientes de polietileno ou metais resistentes à corrosão.
Referências
- ↑ «Potassium fluoride». National Institute of Standards and Technology (NIST). Consultado em 9 de julho de 2019
