Vias dopaminérgicas
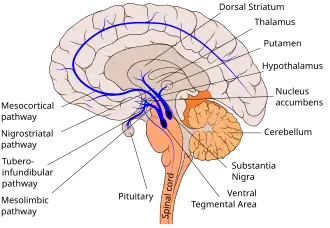
Vias dopaminérgicas (vias da dopamina, projeções dopaminérgicas) no cérebro humano estão envolvidas em processos tanto fisiológicos quanto comportamentais, incluindo movimento, cognição, funções executivas, recompensa, motivação e controle neuroendócrino.[1] Cada via consiste em um conjunto de neurônios de projeção, formados por neurônios dopaminérgicos individuais.
As quatro principais vias dopaminérgicas são a via mesolímbica, a via mesocortical, a via nigrostriatal e a via tuberoinfundibular. A via mesolímbica e a via mesocortical formam o sistema mesocorticolímbico. Outras duas vias dopaminérgicas a serem consideradas são o Trato hipotálamo-espinal e a Via incerto-hipotalâmica.
A doença de Parkinson, o TDAH, os transtornos por uso de substâncias (dependência) e a síndrome das pernas inquietas podem ser atribuídos a disfunções em vias dopaminérgicas específicas.
Os neurônios dopaminérgicos dessas vias sintetizam e liberam o neurotransmissor dopamina.[2][3] As enzimas tirosina hidroxilase e dopa descarboxilase são necessárias para a síntese de dopamina.[4] Essas enzimas são produzidas nos corpos celulares dos neurônios dopaminérgicos. A dopamina é armazenada no citoplasma e em vesículas nos terminais axonais. A liberação de dopamina das vesículas é desencadeada pela despolarização da membrana induzida pela propagação do potencial de ação.[4] Os axônios dos neurônios dopaminérgicos se estendem por todo o comprimento de sua via designada.
Vias
Principais
Seis das vias dopaminérgicas são listadas abaixo.[5][6][7]
| Nome da via | Descrição | Processos associados | Transtornos associados | |
|---|---|---|---|---|
| Sistema mesocorticolímbico | A via mesolímbica transmite dopamina da Área tegmental ventral (ATV), localizada no mesencéfalo, para o estriado ventral, que inclui tanto o Núcleo accumbens quanto o Tubérculo olfatório.[5] | Recompensa relacionada à cognição (saliência de incentivo ("querer"), resposta de prazer ("gostar") a certos estímulos, reforço positivo) e cognição relacionada à aversão | TDAH, dependência, esquizofrenia | |
| A via mesocortical transmite dopamina da ATV para o Córtex pré-frontal. | Funções executivas (atenção, memória de trabalho, controle inibitório, planejamento) | TDAH, dependência, esquizofrenia | ||
| Via nigrostriatal | A via nigrostriatal transmite dopamina da zona compacta da Substância negra para o Núcleo caudado e o Putâmen. | Função motora, cognição relacionada à recompensa, aprendizagem associativa | Dependência, coreia, Doença de Huntington, esquizofrenia, TDAH, Síndrome de Tourette, Doença de Parkinson | |
| Via tuberoinfundibular | A via tuberoinfundibular transmite dopamina do Hipotálamo para a Glândula pituitária. Controla a secreção de hormônios, incluindo a prolactina.[8] | Regulação da secreção de prolactina | Hiperprolactinemia | |
| Trato hipotálamo-espinal | O trato hipotálamo-espinal não apenas regula o equilíbrio hormonal, mas também influencia redes locomotoras no tronco encefálico e na medula espinhal, modulando o controle e a coordenação motores. | Função motora | Síndrome das pernas inquietas | |
| Via incerto-hipotalâmica | Esta via, originada na Zona incerta, influencia o hipotálamo e centros locomotores no tronco encefálico. | Atividades viscerais e sensório-motoras | Tremor | |
Menores
- Trato hipotálamo-espinal
- Via incerto-hipotalâmica
- Zona incerta → Hipotálamo
- Zona incerta → Tronco encefálico VTA → Amígdala (via mesoamigdalóide)[6]
- VTA → Hipocampo[6]
- VTA → Córtex do cíngulo[6]
- VTA → Bulbo olfatório[6]
- SNc → Núcleo subtalâmico[9]
Função
Sistema mesocorticolímbico
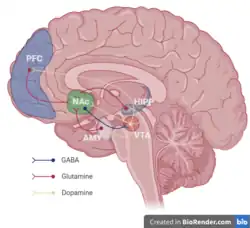
O sistema mesocorticolímbico refere-se às vias mesocortical e mesolímbica, ambas originadas na Área tegmental ventral (ATV) no mesencéfalo. Por meio de conexões separadas com o córtex pré-frontal (via mesocortical) e com o estriado ventral (via mesolímbica), essa projeção desempenha papel fundamental na aprendizagem, motivação, recompensa, memória e movimento.[3][10] Subtipos de receptores de dopamina, D1 e D2, têm funções complementares nessa via, facilitando a aprendizagem em resposta a feedback positivo e negativo.[11] Ambas as vias do sistema mesocorticolímbico estão associadas a TDAH, esquizofrenia e dependência.[12][13][14][15]
Via mesocortical
A via mesocortical projeta-se da ATV para o córtex pré-frontal, estando envolvida em processos cognitivos e regulação de funções executivas, como atenção, memória de trabalho e controle inibitório.[16][17] A disfunção nessa via tem sido relacionada ao TDAH.[13]
Via mesolímbica
Conhecida como via da recompensa, projeta-se da ATV para o estriado ventral (núcleo accumbens e tubérculo olfatório).[14] Quando uma recompensa é antecipada, a taxa de disparo dos neurônios dopaminérgicos nessa via aumenta.[18] Essa via está envolvida em saliência de incentivo, motivação, aprendizagem por reforço, medo e outros processos cognitivos.[6][13][19] Estudos em animais mostram que a depleção de dopamina nessa via reduz o empenho para obter recompensas.[18] Pesquisas buscam esclarecer o papel dessa via na percepção de prazer.[20]
Via nigrostriatal
A via nigrostriatal está envolvida em comportamentos relacionados ao movimento e à motivação. A transmissão de dopamina para o Estriado dorsal desempenha papel na recompensa e motivação, enquanto o movimento é influenciado pela transmissão para a substância negra.[21][22] Esta via está associada a Doença de Huntington, Doença de Parkinson, TDAH, esquizofrenia e Síndrome de Tourette, e também regula aprendizagem associativa.[23]
Via tuberoinfundibular
A via tuberoinfundibular transmite dopamina do hipotálamo para a glândula pituitária, desempenhando papel na regulação do equilíbrio hormonal e na modulação da secreção de prolactina, responsável pela produção de leite materno em fêmeas. A hiperprolactinemia, comum em gestantes, é uma condição associada ao excesso de prolactina.[24] Após o parto, a queda dos níveis de estrogênio contribui para a restauração da inibição dopaminérgica, prevenindo hiperprolactinemia sustentada em indivíduos não gestantes e não lactantes.[25]
Circuito córtico-gânglio basal-tálamo-cortical
As vias dopaminérgicas que projetam da Substância negra pars compacta (SNc) e da Área tegmental ventral (ATV) para o Estriado (vias nigrostriatal e mesolímbica, respectivamente) integram um componente do circuito córtico-gânglio basal-tálamo-cortical.[26] A porção nigrostriatal desse circuito consiste na SNc, que origina vias inibitórias e excitatórias do estriado para o Globo pálido e para o Núcleo subtalâmico, antes de projetar ao tálamo. Os neurônios dopaminérgicos nesse circuito aumentam a frequência de disparo fásico em resposta a erro de recompensa positiva, mas não diminuem o disparo em eventos de recompensa negativa, sugerindo que neurônios serotoninérgicos codifiquem perdas de recompensa.[27] Modelos propõem um "crítico" que codifica valor e um "ator" que seleciona ações, ou que as ações se originam no córtex sendo moduladas pelos gânglios basais, com a via direta facilitando comportamentos apropriados e a via indireta inibindo ações inadequadas. Em tais modelos, a atividade dopaminérgica tônica favorece a via direta, acelerando a execução de ações.[28]
Esses modelos são relevantes para o estudo de TOC,[29][30] TDAH, Síndrome de Tourette, Doença de Parkinson, esquizofrenia e dependência.[28]
Notas
Referências
- ↑ Alcaro A, Huber R, Panksepp J (dezembro 2007). «Behavioral functions of the mesolimbic dopaminergic system: an affective neuroethological perspective». Brain Research Reviews. 56 (2): 283–321. PMC 2238694
 . PMID 17905440. doi:10.1016/j.brainresrev.2007.07.014
. PMID 17905440. doi:10.1016/j.brainresrev.2007.07.014
- ↑ «Beyond the Reward Pathway». Learn Genetics. University of Utah. Consultado em 23 de outubro de 2009. Arquivado do original em 9 de fevereiro de 2010
- ↑ a b Le Moal M (1995). «Mesocorticolimbic Dopaminergic Neurons: Functional and Regulatory Roles». In: Bloom FE, Kupfer DJ. Psychopharmacology: the fourth generation of progress. New York: Raven Press. ISBN 978-0-7817-0166-2. Arquivado do original em 5 de fevereiro de 2018
- ↑ a b Harsing LG (2008). «Dopamine and the Dopaminergic Systems of the Brain». In: Lajtha A, Vizi ES. Handbook of Neurochemistry and Molecular Neurobiology. Boston, MA: Springer US. pp. 149–170. ISBN 978-0-387-30351-2. doi:10.1007/978-0-387-30382-6_7
- ↑ a b Ikemoto S (novembro 2010). «Circuito de recompensa cerebral além do sistema de dopamina mesolímbico: uma teoria neurobiológica». Neuroscience and Biobehavioral Reviews. 35 (2): 129–50. PMC 2894302
 . PMID 20149820. doi:10.1016/j.neubiorev.2010.02.001.
. PMID 20149820. doi:10.1016/j.neubiorev.2010.02.001. Estudos recentes sobre auto-administração intracraniana de neuroquímicos (drogas) mostraram que ratos aprendem a auto-administrar diversas drogas nas estruturas dopaminérgicas mesolímbicas – a área tegmental ventral posterior, a concha medial do núcleo accumbens e o tubérculo olfatório medial. … Na década de 1970, reconheceu-se que o tubérculo olfatório contém um componente estriatal, preenchido por neurônios espinhosos médios gabaérgicos que recebem entradas glutamatérgicas de regiões corticais e entradas dopaminérgicas da ATV, projetando-se ao pálido ventral assim como o núcleo accumbens.
- ↑ a b c d e f Malenka RC, Nestler EJ, Hyman SE (2009). «Capítulo 6: Sistemas de Projeção Ampla: Monoaminas, Acetilcolina e Orexina». In: Sydor A, Brown RY. Neurofarmacologia Molecular: Uma Base para a Neurociência Clínica 2ª ed. Nova Iorque: McGraw-Hill Medical. pp. 147–148, 154–157. ISBN 9780071481274.
Neurônios da SNc inervam densamente o estriado dorsal, onde desempenham papel crítico na aprendizagem e execução de programas motores. Neurônios da ATV inervam o estriado ventral (núcleo accumbens), bulbo olfatório, amígdala, hipocampo, córtex pré-frontal orbital e medial e córtex do cíngulo. Neurônios dopaminérgicos da ATV desempenham papel essencial na motivação, comportamento relacionado à recompensa, atenção e múltiplas formas de memória… Assim, atuando em diversos campos terminais, a dopamina confere saliência motivacional (“querer”) à própria recompensa ou a pistas associadas (região da casca do núcleo accumbens), atualiza o valor atribuído a diferentes metas à luz dessa nova experiência (córtex pré-frontal orbital), ajuda a consolidar múltiplas formas de memória (amígdala e hipocampo) e codifica novos programas motores que facilitarão a obtenção dessa recompensa no futuro (região central do núcleo accumbens e estriado dorsal)… A dopamina tem múltiplas ações no córtex pré-frontal. Promove o “controle cognitivo” do comportamento: seleção e monitoramento eficazes das ações para facilitar o alcance dos objetivos escolhidos. Aspectos do controle cognitivo em que a dopamina atua incluem memória de trabalho, capacidade de manter informação “online” para orientar ações, supressão de comportamentos prepotentes que competem com ações direcionadas a metas e controle de atenção, permitindo assim superar distrações… Projeções noradrenérgicas do LC interagem com projeções dopaminérgicas da ATV para regular o controle cognitivo.
- ↑ Malenka RC, Nestler EJ, Hyman SE (2009). «Chapter 10: Neural and Neuroendocrine Control of the Internal Milieu». In: Sydor A, Brown RY. Molecular Neuropharmacology: A Foundation for Clinical Neuroscience 2nd ed. New York: McGraw-Hill Medical. p. 249. ISBN 9780071481274.
Relationship of the hypothalamus and the pituitary gland. The anterior pituitary, or adenohypophysis, receives rich blood flow from the capillaries of the portal hypophyseal system. This system delivers factors released by hypothalamic neurons into portal capillaries at the median eminence. The figure shows one such projection, from the tuberal (arcuate) nuclei via the tuberoinfundibular tract to the median eminence.
- ↑ Habibi M (2017). «Acetylcholine ☆». Reference Module in Neuroscience and Biobehavioral Psychology. [S.l.]: Elsevier. ISBN 9780128093245. doi:10.1016/b978-0-12-809324-5.00464-8
- ↑ Cragg SJ, Baufreton J, Xue Y, Bolam JP, Bevan MD (outubro 2004). «Synaptic release of dopamine in the subthalamic nucleus». The European Journal of Neuroscience. 20 (7): 1788–802. PMID 15380000. doi:10.1111/j.1460-9568.2004.03629.x

- ↑ Doyon WM, Thomas AM, Ostroumov A, Dong Y, Dani JA (outubro 2013). «Potential substrates for nicotine and alcohol interactions: a focus on the mesocorticolimbic dopamine system». Biochemical Pharmacology. 86 (8): 1181–93. PMC 3800178
 . PMID 23876345. doi:10.1016/j.bcp.2013.07.007
. PMID 23876345. doi:10.1016/j.bcp.2013.07.007
- ↑ Verharen JP, Adan RA, Vanderschuren LJ (dezembro 2019). «Differential contributions of striatal dopamine D1 and D2 receptors to component processes of value-based decision making». Neuropsychopharmacology. 44 (13): 2195–2204. PMC 6897916
 . PMID 31254972. doi:10.1038/s41386-019-0454-0
. PMID 31254972. doi:10.1038/s41386-019-0454-0
- ↑ Malenka RC, Nestler EJ, Hyman SE (2009). «Capítulo 13: Função Cognitiva Superior e Controle Comportamental». In: Sydor A, Brown RY. Neurofarmacologia Molecular: Uma Base para a Neurociência Clínica 2ª ed. Nova Iorque: McGraw-Hill Medical. pp. 313–321. ISBN 9780071481274.
• A função executiva, o controle cognitivo do comportamento, depende do córtex pré-frontal, altamente desenvolvido em primatas superiores e especialmente em humanos.
• A memória de trabalho é um buffer cognitivo de curto prazo e capacidade limitada que armazena informações e permite sua manipulação para orientar a tomada de decisões e o comportamento. …
Essas diversas entradas e projeções de retorno para estruturas corticais e subcorticais colocam o córtex pré-frontal em posição de exercer o chamado controle “top-down” ou controle cognitivo do comportamento. … O córtex pré-frontal recebe entradas não apenas de outras regiões corticais, incluindo o córtex de associação, mas também, via tálamo, de estruturas subcorticais ligadas à emoção e motivação, como a amígdala (Capítulo 14) e o estriado ventral (ou núcleo accumbens; Capítulo 15). …
Em condições nas quais respostas prepotentes tendem a dominar o comportamento, como no vício em drogas, em que pistas relacionadas a substâncias podem induzir a busca pela droga (Capítulo 15), ou no transtorno de déficit de atenção e hiperatividade (TDAH; descrito a seguir), consequências negativas significativas podem ocorrer. … O TDAH pode ser concebido como um distúrbio da função executiva; especificamente, caracteriza-se pela capacidade reduzida de exercer e manter o controle cognitivo do comportamento. Em comparação com indivíduos saudáveis, portadores de TDAH têm menor habilidade para suprimir respostas prepotentes inadequadas a estímulos (inibição de resposta prejudicada) e menor capacidade para inibir respostas a estímulos irrelevantes (supressão de interferência prejudicada). …</quote> - ↑ a b c Engert V, Pruessner JC (dezembro 2008). «Contribuições dopaminérgicas e noradrenérgicas para a funcionalidade no TDAH: o papel do metilfenidato». Current Neuropharmacology. 6 (4): 322–8. PMC 2701285
 . PMID 19587853. doi:10.2174/157015908787386069
. PMID 19587853. doi:10.2174/157015908787386069
- ↑ a b Dreyer JL (dezembro 2010). «Novas perspectivas sobre o papel dos microRNAs no vício em drogas e na neuroplasticidade». Genome Medicine. 2 (12). 92 páginas. PMC 3025434
 . PMID 21205279. doi:10.1186/gm213
. PMID 21205279. doi:10.1186/gm213
- ↑ Robison AJ, Nestler EJ (outubro 2011). «Mecanismos transcricionais e epigenéticos da dependência». Nature Reviews Neuroscience. 12 (11): 623–37. PMC 3272277
 . PMID 21989194. doi:10.1038/nrn3111
. PMID 21989194. doi:10.1038/nrn3111
- ↑ Keyser, J. De (1990). «The mesoneocortical dopamine neuron system». Neurology. 40 (11): 1660–1662. PMID 2234421. doi:10.1212/WNL.40.11.1660
- ↑ Floresco, Stan B.; Magyar, Orsolya (2006). «Mesocortical dopamine modulation of executive functions: beyond working memory». Psychopharmacology. 188 (4): 567–585. PMID 16670842. doi:10.1007/s00213-006-0404-5 – via SpringerLink
- ↑ a b Salamone JD, Correa M (novembro 2012). «The mysterious motivational functions of mesolimbic dopamine». Neuron. 76 (3): 470–85. PMC 4450094
 . PMID 23141060. doi:10.1016/j.neuron.2012.10.021
. PMID 23141060. doi:10.1016/j.neuron.2012.10.021
- ↑ Pezze MA, Feldon J (dezembro 2004). «Mesolimbic dopaminergic pathways in fear conditioning». Progress in Neurobiology. 74 (5): 301–20. PMID 15582224. doi:10.1016/j.pneurobio.2004.09.004
- ↑ Berridge KC, Kringelbach ML (maio 2015). «Pleasure systems in the brain». Neuron. 86 (3): 646–64. PMC 4425246
 . PMID 25950633. doi:10.1016/j.neuron.2015.02.018.
. PMID 25950633. doi:10.1016/j.neuron.2015.02.018. To summarize: the emerging realization that many diverse pleasures share overlapping brain substrates; better neuroimaging maps for encoding human pleasure in orbitofrontal cortex; identification of hotspots and separable brain mechanisms for generating ‘liking’ and ‘wanting’ for the same reward; identification of larger keyboard patterns of generators for desire and dread within NAc, with multiple modes of function; and the realization that dopamine and most ‘pleasure electrode’ candidates for brain hedonic generators probably did not cause much pleasure after all.
- ↑ Balleine BW, Delgado MR, Hikosaka O (agosto 2007). «The role of the dorsal striatum in reward and decision-making». The Journal of Neuroscience. 27 (31): 8161–8165. PMC 6673072
 . PMID 17670959. doi:10.1523/JNEUROSCI.1554-07.2007
. PMID 17670959. doi:10.1523/JNEUROSCI.1554-07.2007
- ↑ Mishra A, Singh S, Shukla S (2018). «Physiological and Functional Basis of Dopamine Receptors and Their Role in Neurogenesis: Possible Implication for Parkinson's disease». Journal of Experimental Neuroscience. 12. 1179069518779829 páginas. PMC 5985548
 . PMID 29899667. doi:10.1177/1179069518779829
. PMID 29899667. doi:10.1177/1179069518779829
- ↑ Carmack SA, Koob GF, Anagnostaras SG (2017). «Learning and Memory in Addiction». Learning and Memory: A Comprehensive Reference. [S.l.]: Elsevier. pp. 523–538. ISBN 9780128052914. doi:10.1016/b978-0-12-809324-5.21101-2
- ↑ Attaar A, Curran M, Meyenburg L, Bottner R, Johnston C, Roberts Mason K (1 de agosto de 2021). «Perioperative pain management and outcomes in patients who -discontinued or continued pre-existing buprenorphine therapy». Journal of Opioid Management. 17 (7): 33–41. PMID 34520024. doi:10.5055/jom.2021.0640
- ↑ Russell, John A.; Douglas, Alison J.; Ingram, Colin D. (2001). «Chapter 1 Brain preparations for maternity — adaptive changes in behavioral and neuroendocrine systems during pregnancy and lactation. An overview». The Maternal Brain. Col: Progress in Brain Research. 133. [S.l.: s.n.] pp. 1–38. ISBN 978-0-444-50548-4. PMID 11589124. doi:10.1016/S0079-6123(01)33002-9 – via Elsevier
- ↑ Taylor SB, Lewis CR, Olive MF (2013). «O neurocircuito da dependência de psicostimulantes ilícitos: efeitos agudos e crônicos em humanos». Substance Abuse and Rehabilitation. 4: 29–43. PMC 3931688
 . PMID 24648786. doi:10.2147/SAR.S39684
. PMID 24648786. doi:10.2147/SAR.S39684 .
. Regiões dos gânglios da base, que incluem o estriado dorsal e ventral, segmentos interno e externo do globo pálido, núcleo subtalâmico e corpos celulares dopaminérgicos na substância negra, estão fortemente implicadas não apenas no controle motor fino, mas também na função do córtex pré-frontal.43 Dentre essas regiões, o NAc (descrita acima) e o DS (descrita abaixo) são as mais frequentemente examinadas em relação à dependência. Assim, apenas uma breve descrição do papel modulador dos gânglios da base em circuitos relevantes para a dependência será mencionada aqui. A saída geral dos gânglios da base ocorre predominantemente via tálamo, que projeta de volta ao córtex pré-frontal para formar loops córtico-estriato-tálamo-corticais (CSTC). Proõem-se três loops CSTC para modular a função executiva, a seleção de ações e a inibição comportamental. No circuito pré-frontal dorsolateral, os gânglios da base modulam principalmente a identificação e seleção de metas, incluindo recompensas.44 O circuito do córtex orbitofrontal modula a tomada de decisões e a impulsividade, e o circuito do cingulado anterior modula a avaliação de consequências.44 Esses circuitos são modulados por entradas dopaminérgicas da ATV para guiar, em última instância, comportamentos relacionados à dependência, incluindo a persistência e o estreitamento do repertório comportamental em direção à busca de drogas, e o uso continuado, apesar das consequências negativas.43–45
- ↑ Roberts, Angela C. (junho de 2011). «The Importance of Serotonin for Orbitofrontal Function». Biological Psychiatry. 69 (12): 1185–1191. ISSN 0006-3223. doi:10.1016/j.biopsych.2010.12.037
- ↑ a b Maia TV, Frank MJ (February 2011). «From reinforcement learning models to psychiatric and neurological disorders». Nature Neuroscience. 14 (2): 154–62. PMC 4408000
 . PMID 21270784. doi:10.1038/nn.2723 Verifique data em:
. PMID 21270784. doi:10.1038/nn.2723 Verifique data em: |data=(ajuda) - ↑ Beucke JC, Sepulcre J, Talukdar T, Linnman C, Zschenderlein K, Endrass T, et al. (junho–falhou de undefined). «Abnormally high degree connectivity of the orbitofrontal cortex in obsessive-compulsive disorder». JAMA Psychiatry. 70 (6): 619–29. PMID 23740050. doi:10.1001/jamapsychiatry.2013.173
 Verifique data em:
Verifique data em: |data=(ajuda) - ↑ Maia TV, Cooney RE, Peterson BS (1 de janeiro de 2008). «The neural bases of obsessive-compulsive disorder in children and adults». Development and Psychopathology. 20 (4): 1251–83. PMC 3079445
 . PMID 18838041. doi:10.1017/S0954579408000606
. PMID 18838041. doi:10.1017/S0954579408000606