Apneia obstrutiva do sono
| Apneia obstrutiva do sono | |
|---|---|
| Sinônimos | Apneia do sono obstrutiva |
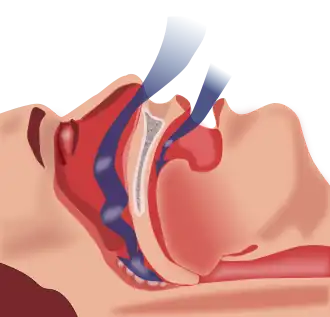 | |
| Apneia obstrutiva do sono: quando o tecido mole cai na parte posterior da garganta, impede a passagem de ar (setas azuis) pela traqueia. | |
| Especialidade | Medicina do sono |
| Classificação e recursos externos | |
| CID-11 | 7A41 |
| CID-10 | G47.33 |
| CID-9 | 327.23 |
| OMIM | 107650 |
| MeSH | D020181 |
Apneia obstrutiva do sono (AOS) é o distúrbio respiratório do sono mais comum e é caracterizado por episódios recorrentes de obstrução completa ou parcial das vias aéreas superiores, levando à redução ou ausência da respiração durante o sono. Esses episódios são denominados "apneias" quando ocorre cessação completa ou quase completa da respiração, ou "hipopneias" quando a redução da respiração é parcial. Em ambas as situações, pode haver queda na saturação de oxigênio no sangue, interrupção do sono ou ambos. A alta frequência de apneias ou hipopneias durante o sono pode interferir na qualidade do sono, o que – em combinação com distúrbios na oxigenação sanguínea – acredita-se contribuir para consequências negativas à saúde e à qualidade de vida.[1] Os termos síndrome da apneia obstrutiva do sono (SAOS) ou síndrome da apneia-hipopneia obstrutiva do sono (SAHOS) podem ser usados para referir-se à AOS quando esta está associada a sintomas diurnos (por exemplo, sonolência diurna excessiva, diminuição da função cognitiva).[2][3]
A maioria dos indivíduos com apneia obstrutiva do sono desconhece as perturbações respiratórias durante o sono, mesmo após despertar. Um parceiro de cama ou membro da família pode observar roncos ou aparentes pausas na respiração, engasgos ou engolições sonoras durante o sono. Pessoas que vivem ou dormem sozinhas costumam não estar cientes da condição. Os sintomas podem estar presentes por anos ou até décadas sem diagnóstico, período durante o qual o indivíduo pode se habituar à sonolência diurna, às cefaleias e à fadiga associadas a níveis significativos de distúrbio do sono. A apneia obstrutiva do sono tem sido associada a morbilidade neurocognitiva e existe uma relação entre ronco e distúrbios neurocognitivos.[4]
Classificação
Na terceira edição da International Classification of Sleep Disorders (ICSD-3), a apneia obstrutiva do sono é classificada entre os distúrbios respiratórios do sono e é dividida em duas categorias: AOS em adultos e AOS pediátrica.[5] A apneia obstrutiva do sono diferencia-se da apneia central do sono (ACS), caracterizada por episódios de redução ou cessação da respiração atribuíveis à diminuição do esforço respiratório, em vez de obstrução das vias aéreas superiores.[6] O esforço respiratório deve então ser avaliado para classificar corretamente a apneia como obstrutiva, dada a especificidade da atividade diafragmática nessa condição:[7] o esforço inspiratório é mantido ou aumentado durante todo o episódio de ausência de fluxo aéreo.[8]
Quando hipopneias estão presentes juntamente com apneias, usa-se o termo apneia-hipopneia obstrutiva do sono e, quando associada a sonolência diurna e outros sintomas, denomina-se síndrome da apneia-hipopneia obstrutiva do sono.[9] Para ser categorizada como obstrutiva, a hipopneia deve atender a um ou mais dos seguintes critérios: (1) ronco durante o evento, (2) achatamento do fluxo oronasal, ou (3) respiração paradoxal toracoabdominal durante o evento.[8] Se nenhum deles estiver presente, a hipopneia é categorizada como central.[8]
Sinais e sintomas
Os sintomas comuns da síndrome do distúrbio respiratório obstrutivo do sono incluem sonolência diurna inexplicada, sono agitado, despertares frequentes e ronco alto (com períodos de silêncio seguidos por ofegos).[10] Sintomas menos comuns são cefaleias matinais; insônia; dificuldade de concentração; alterações de humor como irritabilidade, ansiedade e depressão; bruxismo; perda de memória; aumento da frequência cardíaca ou da pressão arterial; disfunção erétil; ganho de peso inexplicado; aumento da frequência urinária ou noctúria; azia frequente ou refluxo gastroesofágico; e sudorese noturna intensa.[11][12][13]
Muitas pessoas apresentam episódios transitórios de AOS, por um curto período, devido a infecções respiratórias superiores que causam congestão nasal e edema da faringe, ou tonsilite que provoca hipertrofia das tonsilas.[14][15] O vírus Epstein-Barr pode aumentar dramaticamente o tamanho do tecido linfóide durante a infecção aguda, e a AOS é relativamente comum em casos graves de mononucleose infecciosa. Episódios temporários de SAOS também podem ocorrer em pessoas sob efeito de substâncias (por exemplo, álcool) que relaxam excessivamente o tônus corporal e interferem nos mecanismos normais de despertar.[16]
Adultos
O sintoma característico da SAOS em adultos é a sonolência diurna excessiva. Normalmente, um adulto ou adolescente com AOS grave de longa duração adormece por períodos breves durante atividades cotidianas, se tiver oportunidade de sentar ou descansar.[17] Esse comportamento pode ser bastante marcante, ocorrendo até durante conversas em eventos sociais.
A hipóxia associada à AOS pode causar alterações em neurônios do hipocampo e do córtex frontal direito. Estudos de neuroimagem apontaram atrofia hipocampal em pessoas com AOS, além de prejuízos na manipulação mental de informações não verbais, em funções executivas e na memória de trabalho.[18][carece de fontes] A AOS também pode estar associada a maior risco de desenvolvimento de doença de Alzheimer.[18][19]
A obesidade é um fator de risco significativo para AOS. Em indivíduos com obesidade severa, o risco de apneia pode variar entre 55% e 90%.[20] No entanto, entre 20% e 25% dos pacientes com apneia do sono não apresentam sobrepeso.[21] Muitas vezes não reconhecido na atenção primária, é extremamente importante identificar esses pacientes, pois eles têm quatro vezes mais probabilidade de desenvolver hipertensão do que indivíduos obesos sem AOS.[22] Pacientes não obesos apresentam risco maior de aterosclerose precoce, aproximadamente 2,7 vezes mais do que pacientes obesos sem AOS, e esse risco aumenta com a gravidade da síndrome.[23] Fatores nesse grupo incluem características anatômicas herdadas, instabilidade do controle ventilatório, ineficiência neuromuscular dos músculos dilatadores das vias aéreas superiores ou limiar mais baixo para despertar em resposta a estímulos respiratórios.[24]
O diagnóstico de AOS é significativamente mais comum entre pessoas em relacionamento, que são alertadas por seus parceiros, uma vez que os indivíduos com AOS muitas vezes ignoram a condição. Existe um estigma associado ao ronco alto, e não é considerado um traço feminino, fazendo com que mulheres sejam menos propensas a serem informadas ou a admitir o sintoma a si mesmas ou a médicos. Além disso, máquinas de CPAP (pressão positiva contínua nas vias aéreas) também são percebidas negativamente por mulheres, sendo menos utilizadas nesse grupo.[25]
Crianças
Embora essa chamada "hipersônia" (sonolência excessiva) também possa ocorrer em crianças, ela não é típica em crianças pequenas com apneia do sono. Crianças pequenas com AOS grave geralmente se comportam como se estivessem "excessivamente cansadas" ou "hiperativas"; e costumam apresentar problemas comportamentais como irritabilidade e déficit de atenção.[26][27][28]
Adultos e crianças com AOS muito grave também diferem no hábitus corporal. Adultos geralmente são obesos, com pescoços particularmente curtos e espessos. Crianças pequenas, por outro lado, apresentam-se magras ou podem ter "falha de crescimento", caracterizada por crescimento reduzido. O baixo ganho de peso ocorre por dois motivos: o esforço respiratório é tão intenso que calorias são queimadas em altas taxas mesmo em repouso, e a obstrução nasal e faríngea torna a alimentação desconfortável. A AOS em crianças, ao contrário dos adultos, é frequentemente causada pela hipertrofia de tonsilas e adenoides e pode ser, às vezes, curada com amigdalectomia e adenoidectomia.
Esse problema também pode ser causado por excesso de peso em crianças. Nesse caso, os sintomas se assemelham aos dos adultos, como inquietação e exaustão. Embora a hipertrofia adenotonsilar continue sendo a causa mais comum de AOS em crianças,[29][30] a obesidade também pode desempenhar um papel na obstrução das vias aéreas superiores durante o sono, tornando crianças obesas mais suscetíveis à AOS.[31] O aumento recente na prevalência de obesidade contribuiu para alterações na prevalência e nas características da AOS pediátrica,[32] sendo a gravidade proporcional ao grau de obesidade.[33][34]
Diagnóstico
O diagnóstico da SAOS é feito quando o paciente apresenta episódios recorrentes de colapso parcial ou completo das vias aéreas superiores durante o sono, resultando em apneias ou hipopneias, respectivamente.[35] Os critérios que definem apneia ou hipopneia variam. A American Academy of Sleep Medicine define apneia como redução do fluxo aéreo ≥ 90% por pelo menos 10 segundos. Hipopneia é definida como redução do fluxo aéreo ≥ 30% por pelo menos 10 segundos e associada a redução de ≥ 4% na oximetria de pulso, ou redução ≥ 30% no fluxo por pelo menos 10 segundos associada a redução de ≥ 3% na oximetria ou a um despertar.[36]
Para definir a gravidade, utilizam-se o Índice de Apneia-Hipopneia (IAH) ou o Índice de Distúrbio Respiratório (IDR). Enquanto o IAH mede a média de apneias e hipopneias por hora de sono, o IDR adiciona a esse valor os despertares relacionados ao esforço respiratório (RERAs).[37] A SAOS é diagnosticada se o IAH for > 5 episódios por hora e resultar em sonolência diurna e fadiga, ou quando o IDR for ≥ 15 independentemente dos sintomas.[38] A sonolência diurna pode ser classificada como leve, moderada ou grave conforme seu impacto na vida social, e avaliada pela Escala de Sonolência de Epworth.[39] Ferramentas de triagem incluem os questionários STOP, Berlin e STOP-BANG, sendo este último altamente eficaz na detecção de AOS.[40][41]
Polissonografia
| Classificação | IAH (adultos) | IAH (pediatria) |
|---|---|---|
| Normal | < 5 | <1 |
| Leve | ≥5, <15 | ≥1, <5 |
| Moderada | ≥15, <30 | ≥5, <10 |
| Grave | ≥ 30 | ≥10 |
A polissonografia de nível 1 em laboratório é o padrão-ouro para diagnóstico. Os pacientes são monitorados com eletrodos de EEG, oximetria de pulso, sensores de temperatura ou pressão para fluxo aéreo nasal e oral, cintas de resistência torácica e abdominal para detectar movimento, eletrocardiograma e sensores de EMG para atividade muscular no queixo, tórax e membros.
Um "evento" pode ser uma apneia, caracterizada pela cessação completa do fluxo aéreo por pelo menos 10 segundos, ou uma hipopneia em que o fluxo aéreo diminui 50 % por 10 segundos, ou 30 % se houver redução na saturação de oxigênio ou despertar.[42] Para classificar a gravidade da apneia, contabiliza-se o número de eventos por hora de sono, relatado como Índice de Apneia-Hipopneia (IAH). Para adultos, IAH < 5 é normal; [5–15) leve; [15–30) moderado; ≥ 30, grave. Para crianças, IAH < 1 é normal; [1–5) leve; [5–10) moderado; ≥10, grave.
Teste domiciliar de sono (HST/HSAT)
A apneia do sono também pode ser diagnosticada com kit de monitoramento domiciliar.[43] A principal vantagem é registrar o sono em ambiente habitual, sendo mais representativo e acessível do que a polissonografia, além de ter menor custo e evitar longas esperas.[44]
Oximetria domiciliar
Em pacientes com alta probabilidade de AOS, a oximetria domiciliar (método não invasivo de monitorar oxigenação sanguínea) pode ser adequada para triagem antes da polissonografia.[45] Pacientes de alta probabilidade são identificados por escore ≥ 10 na Escala de Epworth e ≥ 15 no Sleep Apnea Clinical Score.[46] No entanto, a oximetria não mede eventos apneicos ou RERAs e não gera valor de IAH, exigindo testes adicionais antes da prescrição de CPAP ou terapia com aparelho oral.
Critérios
Segundo a International Classification of Sleep Disorders, há quatro tipos de critérios: (1) sono – sonolência excessiva, sono não restaurador, fadiga ou insônia; (2) respiração – despertar com parada respiratória, engasgo ou sufocamento; (3) ronco ou interrupção da respiração durante o sono; (4) comorbidades – hipertensão, doença arterial coronariana, AVC, insuficiência cardíaca, fibrilação atrial, diabetes tipo 2, transtorno do humor ou comprometimento cognitivo. Dois níveis de gravidade são distinguidos: o primeiro definido por polissonografia ou teste domiciliar demonstrando ≥ 5 eventos respiratórios predominantemente obstrutivos por hora; níveis mais altos por ≥ 15 eventos. Se < 5 eventos por hora, não é diagnosticada apneia obstrutiva do sono.[47]
Variabilidade de noite a noite complica o diagnóstico, podendo exigir testes múltiplos em casos duvidosos.[48]
Fisiopatologia
A transição da vigília para o sono (REM ou NREM) associa-se à redução do tônus muscular das vias aéreas superiores. Durante o sono REM, o tônus da faringe, do pescoço e da maioria dos músculos esqueléticos relaxa quase completamente, permitindo que a língua e o palato mole relaxem, reduzindo a permeabilidade das vias aéreas e potencialmente bloqueando o fluxo de ar aos pulmões na inspiração, resultando em ventilação reduzida. Se a ventilação reduzida for associada a níveis de oxigênio sanguíneo suficientemente baixos ou a esforços respiratórios altos contra via aérea obstruída, mecanismos neurológicos podem desencadear um despertar, chamado de "arousal". Esse despertar pode levar a ofegos e breves excitações do sono, sem despertar total, mas com efeito negativo na qualidade restauradora do sono. Em casos significativos de AOS, uma consequência é a privação de sono devido às repetidas interrupções e recuperações durante o sono, prejudicando o sono profundo (estágio 3 do sono NREM) e o sono REM, interferindo no crescimento, cicatrização e resposta imune, especialmente em crianças e jovens adultos.
A causa fundamental da AOS é a obstrução das vias aéreas superiores, geralmente atrás da língua e da epiglote, em que a via aérea, patente em posição ereta e vigília, colapsa quando o paciente está deitado de costas e perde o tônus muscular ao entrar no sono profundo.
No início do sono, em sono leve, não há perda de tônus muscular faringiano, o fluxo aéreo é laminar e silencioso. À medida que o colapso progride, a obstrução torna-se aparente pelo ruído crescente da respiração, seguido de roncos cada vez mais altos, até cessar os ruídos, indicando obstrução total que pode durar minutos. Então, o paciente desperta parcialmente, recupera o tônus muscular, o fluxo aéreo retoma e a saturação de oxigênio sobe. O paciente retorna ao sono profundo, perde novamente o tônus aéreo e o ciclo se repete.
Modelos fisiopatológicos
As causas do bloqueio espontâneo das vias aéreas superiores são debatidas. Algumas correntes acreditam que:
- Idade avançada, embora ocorra em todas as faixas etárias, inclusive neonatos em síndrome de Pierre Robin.
- Lesão cerebral, temporária ou permanente, embora 99% dos pacientes tenham cérebros normais.
- Diminuição do tônus muscular por drogas, álcool ou distúrbios neurológicos.
- Ronco crônico, que pode causar lesões nervosas em tecidos da faringe por vibrações traumáticas.[49]
- Aumento de tecido mole ao redor da via aérea, muitas vezes decorrente de obesidade, embora nem todos pacientes obesos tenham AOS.
Otorinolaringologistas atribuem a fatores estruturais que estreitam a via aérea, como tonsilas grandes, base da língua volumosa ou depósitos de gordura no pescoço. Outras causas incluem respiração nasal prejudicada, palato mole flácido ou epiglote colapsável.
Cirurgiões bucomaxilofaciais veem fatores primários de hipoplasia mandibular, que oferecem base anatômica para desenvolvimento da AOS via glosoptose. Eles defendem cirurgias ortognáticas como tratamento definitivo, alegando garantia de cura superior a outras abordagens.
Fatores de risco
Obesidade
É sabido que crianças, adolescentes e adultos com AOS frequentemente são obesos, apresentando aumento de tecido adiposo no pescoço que potencia a obstrução respiratória durante o sono.[50]
No entanto, indivíduos com IMC normal também podem apresentar AOS sem gordura subcutânea ou cervical significativa em exames de DEXA, possivelmente por maior massa muscular ou tendência à diminuição do tônus muscular, facilitando o colapso das vias aéreas durante o sono.[carece de fontes]
Idade
Idade avançada costuma acompanhar perda muscular e neurológica de tônus nas vias aéreas superiores. A diminuição temporária do tônus pode ser causada por depressivos químicos, como álcool e sedativos, enquanto perda permanente pode decorrer de traumas cranianos ou distúrbios neuromusculares.
Tônus muscular
Indivíduos com tônus muscular reduzido, tecido mole aumentado nas vias aéreas e características estruturais que estreitam o trajeto aéreo têm alto risco de AOS. Homens, cuja anatomia apresenta maior massa no tronco e pescoço, têm risco aumentado, especialmente na meia-idade e além. Mulheres, em geral, apresentam menor frequência e gravidade, possivelmente pela fisiologia e níveis de progesterona. A prevalência em mulheres pós-menopáusicas aproxima-se da dos homens na mesma faixa etária. Mulheres grávidas também têm maior risco.[51]
Medicação e estilo de vida
Fatores como tabagismo podem aumentar o risco de AOS, pois irritantes químicos inflamam tecidos moles das vias aéreas e promovem retenção de fluidos, estreitando o trajeto aéreo; além disso, a queda de nicotina no sangue altera a estabilidade do sono.[3] O risco diminui com cessação do tabagismo. Crianças expostas à fumaça podem desenvolver hipertrofia adenotonsilar.[32] Consumo de álcool, sedativos e outras substâncias que relaxam músculos também pode prejudicar a AOS.[52] Rinite alérgica e asma estão associadas ao aumento de hipertrofia adenotonsilar e AOS.[53][54]
Genética
A AOS parece ter componente genético; indivíduos com histórico familiar estão mais propensos, por fatores diretos de suscetibilidade ou indiretos via fenótipos como obesidade, estrutura craniofacial e controle neurológico dos músculos das vias aéreas e do sono.[55]
Vários genes associados à apneia foram identificados, incluindo DLEU1, DLEU7, CTSF, MSRB3, FTO e TRIM66.[56]
Síndromes craniofaciais
Recentemente, sugere-se que a tendência humana a mandíbulas inferiores curtas (neotenia) seja causa de AOS por meio da glosoptose, em que uma mandíbula pequena desloca a língua para trás. Maxila estreita também contribui ao reduzir volume nasal e faríngeo, explicando congestão nasal em decúbito.
Cirurgiões maxilofaciais tratam mandíbulas pequenas cirurgicamente (por exemplo, BIMAX, GenioPaully, IMDO) oferecendo opção médica que substitui CPAP, placa de avanço mandibular, amigdalectomia e uvulopalatofaringoplastia. Existem síndromes craniofaciais reconhecíveis, genéticas ou não, em que anormalidades no nariz, boca e mandíbula ou tônus muscular predispoem à SAOS.
Na síndrome de Down, anomalia cromossômica, características como baixo tônus muscular, nasofaringe estreita e língua grande predispõem à AOS. Obesidade, tonsilas e adenoides aumentadas, comuns na população ocidental, têm maior impacto em pessoas com Down. Mais de 50% dos indivíduos com síndrome de Down apresentam AOS,[57] e alguns médicos defendem testes de rotina nesse grupo.[58]
Em outras síndromes, correções que melhoram vias aéreas (ex. palato fendido) podem, após cirurgia, aumentar risco de AOS quando a anatomia é modificada.
Avanço esquelético para aumentar espaço faríngeo é opção em pacientes craniofaciais com mandíbulas pequenas (por exemplo, síndrome de Treacher Collins, seqüência de Pierre Robin), utilizando cirurgia de avanço mandibular, redução de língua, amigdalectomia ou uvulopalatoplastia modificada.
Complicação pós-operatória
A SAOS também pode ocorrer como uma complicação pós-operatória grave, que parece estar mais frequentemente associada à cirurgia de retalho faríngeo posterior em comparação com outros procedimentos para o tratamento da insuficiência velofaríngea (IVF).[59] Na SAOS, interrupções recorrentes da respiração durante o sono estão associadas à obstrução temporária das vias aéreas. Após a cirurgia de retalho faríngeo, dependendo do tamanho e da posição, o próprio retalho pode exercer um efeito “obturador” ou obstrutivo dentro da faringe durante o sono, bloqueando as vias de entrada de ar e dificultando a respiração efetiva.[60][61] Há relatos documentados de obstrução aérea grave, e as notificações de SAOS pós-operatória continuam a aumentar à medida que os profissionais de saúde (ou seja, médicos, fonoaudiólogos) se conscientizam cada vez mais dessa condição potencialmente perigosa.[62] Subsequentemente, na prática clínica, as preocupações com a SAOS equipararam-se ou até superaram o interesse pelos resultados de fala após a cirurgia de retalho faríngeo.[carece de fontes]
O tratamento cirúrgico para insuficiência velo-palatina pode causar a síndrome da apneia obstrutiva do sono. Quando a insuficiência velo-palatina está presente, o ar vaza para a nasofaringe mesmo quando o palato mole deveria fechar a passagem nasal. Um teste simples para essa condição pode ser feito colocando um pequeno espelho abaixo do nariz e pedindo-se ao indivíduo que pronuncie “P”. Esse som plosivo é normalmente produzido com a via nasal obstruída – todo o ar sai pelos lábios semicerrados e nenhum pelo nariz. Se for impossível emitir esse som sem embaçar o espelho, há um vazamento de ar – evidência razoável de fechamento palatal inadequado. A fala costuma ficar pouco inteligível devido à incapacidade de pronunciar certos fonemas. Um dos tratamentos cirúrgicos para insuficiência velo-palatina envolve modelar o tecido da parte posterior da garganta e usá-lo para causar propositalmente obstrução parcial da abertura da nasofaringe. Isso pode, de fato, causar a síndrome da SAOS em indivíduos suscetíveis, particularmente nos dias que se seguem à cirurgia, quando ocorre edema (ver abaixo: Situação especial: anestesia e cirurgia).
Por fim, pacientes com SAOS apresentam risco aumentado de várias complicações perioperatórias quando submetidos a cirurgia, mesmo que o procedimento planejado não envolva cabeça ou pescoço. Diretrizes destinadas a reduzir o risco de complicações perioperatórias foram publicadas.[63]
Consequências
Existem três níveis de consequências: fisiológicas, intermediárias e clínicas.[64] As consequências fisiológicas incluem hipóxia, fragmentação do sono, desregulação do sistema nervoso autônomo ou hiperóxia.[64] Os resultados intermediários englobam inflamação, vasoconstrição pulmonar, disfunção metabólica geral, oxidação de proteínas e lipídios ou aumento da adiposidade.[64] As repercussões clínicas compreendem hipertensão pulmonar, acidentes, obesidade, diabetes, diversas cardiopatias ou hipertensão.[64]
Em crianças
A síndrome da apneia obstrutiva do sono (SAOS) é o distúrbio respiratório do sono (DRS) mais comum e afeta até 11% das crianças nascidas a termo – sendo ainda mais prevalente (de 3 a 6 vezes mais) em crianças nascidas prematuras.[65] Como DRS, a SAOS na infância pode levar a várias consequências adversas, inclusive de longo prazo, persistindo na vida adulta.[29] As implicações da SAOS em crianças são complexas e abrangem um amplo espectro de consequências: quando não tratada, a SAOS pode resultar em morbidade que afeta diferentes domínios da vida (órgãos, sistemas corporais, distúrbios comportamentais, depressão, reduzida qualidade de vida, etc.).[32] Dessa forma, sintomas noturnos que indiquem a presença de SAOS (por exemplo, ronco, ofegância, sono agitado e gasto excessivo de energia para respirar durante o sono) estão associados a sinais diurnos como dificuldades de concentração e aprendizado e irritabilidade, comprometimento do desenvolvimento neurocognitivo, queda no desempenho escolar e dificuldades comportamentais.[29] Por exemplo, distúrbios respiratórios do sono, como a SAOS, contribuem para comportamentos hiperativos que podem levar ao diagnóstico e tratamento do TDAH. No entanto, uma vez tratado o distúrbio respiratório do sono, o comportamento hiperativo pode melhorar e o tratamento pode ser suspenso.[66] A obesidade também impacta as consequências da SAOS e leva a diferentes manifestações ou gravidade.[32] Estudos demonstraram que, ao contrário dos adultos, crianças com distúrbios respiratórios do sono conseguem manter a oxigenação cerebral. Contudo, a condição ainda afeta o cérebro e pode resultar em sequelas neurocognitivas e comportamentais adversas. É especialmente preocupante, pois essas consequências ocorrem enquanto o cérebro ainda está em desenvolvimento.[65] O grau em que o sono é perturbado e fragmentado tem sido significativamente associado à gravidade das consequências, que podem diminuir uma vez que o sono seja melhorado.[31] É mais a interrupção dos processos do sono do que a quantidade total de sono que gera as consequências adversas no funcionamento diurno da criança;[31] contribui, por exemplo, para a hiperatividade.[66]
Consequências neurocognitivas e comportamentais
A fragmentação do sono noturno tem sido associada a deficiências neurocognitivas; portanto, a identificação de distúrbios respiratórios do sono (DRS), como a SAOS, é crucial em crianças, pois essas deficiências podem ser reversíveis com o tratamento apropriado do distúrbio do sono.[67] As disfunções neurocognitivas e comportamentais comumente presentes em crianças com SAOS incluem: hiperatividade, impulsividade, comportamentos agressivos,[32][31] baixa habilidade social e de comunicação e redução das habilidades adaptativas.[29]
Crianças com SAOS frequentemente apresentam déficits cognitivos, resultando em dificuldades de atenção e concentração, assim como pior desempenho acadêmico e baixo QI.[29][31] Baixo desempenho escolar tem sido associado à SAOS e sugerido como decorrente de excitações corticais e simpáticas e hipoxemia, que afeta a consolidação da memória.[68] Um estudo com crianças indianas afetadas pela SAOS demonstrou notas escolares baixas, incluindo matemática, ciências, língua e educação física. Esse estudo permitiu observar o impacto geral da SAOS nas habilidades de aprendizagem associadas à linguagem ou ao raciocínio numérico e ao desenvolvimento físico.[68] Sugere-se que os déficits no desempenho acadêmico relacionados à SAOS possam ser mediados por funções executivas reduzidas ou habilidades linguísticas,[69] domínios que contribuem significativamente para as habilidades de aprendizagem e o comportamento. Os déficits no desempenho escolar podem, no entanto, ser melhorados se for realizada adenoamigdalectomia para tratar a SAOS em crianças.[69] Assim, é crucial identificar a SAOS em crianças com dificuldades escolares; muitos casos permanecem não diagnosticados.[69]
Como estudos demonstraram que habilidades de aprendizagem e comportamentos podem ser melhorados se a SAOS for tratada,[29][31] os déficits neurocognitivos e comportamentais são, portanto, pelo menos parcialmente reversíveis.[32] Essa dimensão reversível tem sido postulada como negativamente correlacionada com a duração dos sintomas, o que significaria que quanto mais tempo a SAOS permanecer sem tratamento, menos reversíveis serão as consequências.[31]
Consequências somáticas e metabólicas
Assim como em adultos, a SAOS em crianças está associada a maior risco de doenças cardiovasculares[32][31] devido ao aumento da atividade simpática e ao comprometimento do controle autonômico cardíaco.[65] Entre as disfunções cardiovasculares decorrentes da SAOS, podem ser observadas hipertensão sistêmica[31] e desregulação da pressão arterial[29]<[70] (por exemplo, pressão arterial elevada ou variabilidade da pressão arterial[65]). A variabilidade da pressão arterial demonstrou correlação com a gravidade dos sintomas, como a frequência de apneias e hipopneias.[70] A hipertensão pulmonar também é comum entre os problemas cardiovasculares decorrentes da SAOS.[29] Crianças com distúrbios respiratórios do sono também apresentam frequência cardíaca elevada durante a vigília e o sono.[70]
Enurese noturna
Crianças com SAOS também apresentam risco maior de enurese noturna[29][71] e supõe-se que seja causada por produção excessiva de urina,[68][72] desempenho prejudicado da bexiga e da uretra[73] ou incapacidade de suprimir a contração vesical noturna, devido a falha na excitação.[72][73] O risco de enurese noturna aumenta com a gravidade do distúrbio respiratório do sono: quanto mais eventos respiratórios por hora de sono, maior é o risco de enurese noturna.[73] A obesidade também pode exercer papel, pois está associada à SAOS e à diurese noturna (devido a dieta inadequada). A interação entre SAOS e obesidade pode, assim, resultar em enurese noturna.[72] Considerando a alta prevalência de enurese noturna entre crianças com distúrbios respiratórios do sono, é importante considerar estes distúrbios no diagnóstico diferencial da enurese noturna, já que o tratamento do distúrbio do sono pode ter efeito terapêutico favorável na enurese.[74][71][73] Por exemplo, uma adenoamigdalectomia realizada para reduzir a SAOS tem impacto positivo na enurese noturna.[74][68] Um estudo mostrou que essa cirurgia tem de 60 a 75% de chance de resolver completamente a enurese noturna e de 80 a 85% de chance de reduzir seus sintomas juntamente com outros sintomas da SAOS.[71]
Crescimento atrofiado
Quando não tratada, a SAOS em crianças também pode levar a atraso de crescimento. Quando o sono é interrompido em crianças que ainda estão em crescimento, podem ocorrer consequências significativas. O hormônio do crescimento (HGH) é secretado durante a noite, especialmente durante o sono profundo não REM. Se isso for interrompido, a secreção do hormônio de crescimento pode ser comprometida; assim, o crescimento pode não ocorrer normalmente e as crianças podem ficar mais baixas do que seus pares.[75]
Outras consequências
Em contraste com adultos, sonolência diurna excessiva (SDE) não é o sintoma mais comumente relatado em crianças com SAOS.[67] No entanto, ao utilizar questionários objetivos, é possível observar que a frequência de SDE em crianças é maior do que aquela relatada pelos pais ou responsáveis (40–50%).[31] E o risco de SDE aumenta ainda mais quando a SAOS está associada à obesidade.[31][32]
Em adultos
Embora existam algumas semelhanças entre adultos e crianças, a SAOS não ocasiona as mesmas consequências em ambas as populações.[76] Exemplos de semelhanças são o ronco – que é a queixa mais comum tanto na SAOS pediátrica quanto na SAOS em adultos[76] – variabilidade da pressão arterial e morbilidades cardiovasculares.[3] Uma grande diferença é a sonolência diurna excessiva (SDE), comumente relatada na SAOS em adultos,[77] enquanto não é muito comum na SAOS pediátrica.[76] Ainda assim, a SAOS em adultos também implica um amplo espectro de consequências adversas e graves,[78] as quais levam a maior mortalidade entre pacientes com SAOS.[79] Essas consequências são ainda agravadas por comorbidades comuns, como a obesidade.[80]
Consequências neurocognitivas
Assim como nas crianças, a SAOS afeta as funções cognitivas em adultos.[76] Meta-análises demonstraram que os déficits cognitivos mais comuns ocorrem nos domínios de atenção, memória verbal e visual retardada,[81] habilidades visuoespaciais e construtivas e funções executivas,[82] como flexibilidade mental.[81] O funcionamento executivo – principalmente mediado pelo córtex pré-frontal[83] – está significativamente prejudicado em pacientes com SAOS, acreditando-se que a região pré-frontal e sua conectividade sejam afetadas pelos distúrbios do sono.[84]
Quanto aos déficits de memória, a memória verbal é significativamente prejudicada, pois os pacientes apresentam dificuldades para recordar informações verbais imediatamente e após atraso. Embora meta-análises não tenham encontrado déficits na retenção de informações em pacientes com SAOS, essas deficiências na memória verbal podem estar relacionadas a problemas no processo de codificação de informações.[85] Esse déficit no processo de codificação também é observado na memória visuoespacial; contudo, a memória visual parece estar preservada em pacientes com SAOS.[85]
Sugere-se que os déficits cognitivos resultem da fragmentação do sono e da privação de sono, bem como da sonolência diurna excessiva associada a eles.[82] Mais precisamente, déficits de atenção e memória parecem resultar da fragmentação do sono, enquanto déficits na função cognitiva global (função executiva, psicomotricidade, habilidades de linguagem) estão mais relacionados à hipóxia ou hipercarbia que acompanham os eventos obstrutivos durante o sono.[82][86] Entretanto, não foi encontrada correlação consistente entre o grau de prejuízo cognitivo e a gravidade da perturbação do sono ou da hipóxia.[85][86]
Esses prejuízos podem melhorar com um tratamento eficaz para a SAOS, como a terapia com pressão positiva contínua nas vias aéreas (CPAP).[82] Dirigir um veículo é um exemplo de tarefa complexa que depende das capacidades cognitivas do condutor, como atenção, tempo de reação e vigilância.[87] Momentos muito breves de desatenção chamados eventos de microsone podem indicar comprometimento da vigilância diurna, embora nem todos os motoristas com apneia obstrutiva do sono apresentem esses eventos.[88]
Consequências comportamentais
A hiperatividade e as dificuldades na autorregulação emocional encontradas em pacientes pediátricos não são relatadas em adultos.[76] Entretanto, a SAOS em adultos está associada a alterações de personalidade e comportamento automático.[77] O maior impacto da SAOS é a sonolência diurna excessiva (SDE), relatada em aproximadamente 30% dos pacientes com SAOS.[89] A SDE pode ser causada pela perturbação na qualidade do sono, pela duração insuficiente de sono ou pela fragmentação do sono[90] e é responsável por complicações adicionais, pois pode levar a sintomas depressivos,[91] prejuízos na vida social e redução da eficácia no trabalho.[92][93] Estudos demonstraram que essas consequências da SDE podem ser melhoradas após tratamento com CPAP.[94]
Consequências fisiológicas e metabólicas
A SAOS em adultos está associada a maior risco de comorbidades cardiovasculares, diabetes mellitus, hipertensão, doença arterial coronariana e acidente vascular cerebral[76][77] – a SAOS pode ter um papel na etiologia dessas condições. Esses quadros podem levar a aumento da mortalidade[76][77] que um tratamento adequado da SAOS pode reduzir.[77] A SAOS está frequentemente associada à hipertensão, pois induz aumento da atividade simpática que pode levar à elevação da pressão arterial. A hipercapnia relacionada à SAOS tem sido sugerida como fator no desenvolvimento da hipertensão.[95] O tratamento da SAOS pode prevenir o desenvolvimento de hipertensão.[96] A relação entre SAOS e excesso de peso corporal é complexa, pois a obesidade é mais prevalente entre pacientes com SAOS, mas também pode ser um fator de risco para o desenvolvimento da SAOS[77] – ela representa 58% dos casos em adultos.[97] Assim, tanto a SAOS quanto a obesidade (quando presente) podem atuar sinergicamente e levar a hiperlipidemia, diabetes, resistência à insulina e outros sintomas da síndrome metabólica.[3][77] A própria síndrome metabólica está frequentemente associada à SAOS: de 74% a 85% dos pacientes com SAOS são diagnosticados com ela. A terapia com CPAP pode levar à melhoria de alguns componentes cardiovasculares da síndrome metabólica[96] enquanto a perda de peso também é recomendada pelos seus efeitos positivos nas consequências da SAOS e nas disfunções metabólicas.[97] Uma intervenção que combine exercício e dieta é, portanto, eficaz no tratamento da SAOS, pois impacta positivamente a gravidade tanto dos sintomas de obesidade quanto dos sintomas da SAOS.[98]
Indivíduos com diabetes tipo 2 frequentemente são co-diagnosticados com SAOS, com taxas de prevalência do diabetes tipo 2 variando entre 15% e 30% na população com SAOS.[99] A relação entre SAOS e diabetes tipo 2 pode ser explicada pelo fato de que o sono fragmentado e a hipoxemia irregular, característicos da SAOS, levam ao metabolismo de glicose no sangue desregulado.[99] Em particular, muitos estudos de polissonografia mostraram que a SAOS não tratada piora o controle glicêmico em indivíduos com diabetes tipo 2.[99] Contudo, é possível que a relação entre SAOS e diabetes tipo 2 seja bidirecional, uma vez que a disfunção nervosa relacionada ao diabetes pode afetar o sistema respiratório e induzir distúrbios da respiração durante o sono.[99]
Polissonografia
| Classificação | IAH (adultos) | IAH (pediatria) |
|---|---|---|
| Normal | < 5 | <1 |
| Leve | ≥5 e <15 | ≥1 e <5 |
| Moderada | ≥15 e <30 | ≥5 e <10 |
| Grave | ≥ 30 | ≥10 |
A polissonografia de nível 1 em laboratório, realizada durante a noite, é o exame padrão‑ouro para diagnóstico. Os pacientes são monitorados com eletrodos de EEG, oximetria de pulso, sensores de temperatura ou pressão para detectar o fluxo aéreo nasal e oral, plestimografia de impedância respiratória ou cintas de resistência ao redor do tórax e abdome para detectar movimento, um eletrodo de ECG e sensores de EMG para detectar contração muscular no queixo, no tórax e nas pernas.
Um “evento” pode ser uma apneia, caracterizada pela cessação completa do fluxo de ar por pelo menos 10 segundos, ou uma hipopneia, na qual o fluxo de ar diminui 50% por 10 segundos ou diminui 30% se houver diminuição associada na saturação de oxigênio ou um despertar do sono.[42] Para graduar a gravidade da apneia do sono, o número de eventos por hora é registrado como o IAH. Para adultos, IAH <5 é considerado normal, IAH [5–15) é leve, [15–30) é moderada e ≥30 eventos por hora caracteriza apneia do sono severa. Para pediatria, IAH <1 é normal, [1–5) é leve, [5–10) é moderada e ≥10 eventos por hora caracteriza apneia do sono severa.
Oximetria domiciliar
Em pessoas com alta probabilidade de ter SAOS, a oximetria domiciliar (método não invasivo de monitorar a oxigenação sanguínea) pode ser adequada e mais fácil de obter do que a polissonografia formal.[45] Pacientes de alta probabilidade podem ser identificados por escore ≥10 na Escala de Sonolência de Epworth (ESE) e escore ≥15 no Sleep Apnea Clinical Score (SACS).[46] Contudo, a oximetria domiciliar não mede eventos apneicos nem despertares relacionados a eventos respiratórios e, portanto, não gera um valor de IAH.
Manejo
Diversas opções de tratamento são usadas na apneia obstrutiva do sono.[100] Evitar álcool e tabagismo é recomendado,[101] assim como evitar medicamentos que relaxem o sistema nervoso central (por exemplo, sedativos e relaxantes musculares). Recomenda-se perda de peso em indivíduos com sobrepeso. A pressão positiva contínua nas vias aéreas (CPAP) e dispositivos de avanço mandibular são frequentemente usados e mostraram-se igualmente eficazes.[102][103] O treinamento físico, mesmo sem perda de peso, melhora a apneia do sono.[104] Há evidências insuficientes para apoiar o uso generalizado de medicamentos.[102] Em pacientes selecionados, por exemplo com hiperplasia de amígdalas, recomenda-se amigdalectomia. Em pacientes que falham no CPAP e aparelhos orais, recomenda-se tratamento cirúrgico com uvulopalatofaringoplastia (UPPP) conservadora como cirurgia de resgate. A UPPP tem efeito positivo na respiração noturna e na sonolência diurna excessiva,[105][106]
Intervenção física
A intervenção terapêutica mais amplamente utilizada é a pressão positiva nas vias aéreas, em que um aparelho respiratório bombeia um fluxo controlado de ar por meio de uma máscara usada sobre o nariz, a boca ou ambos. A pressão adicional mantém as vias aéreas abertas, evitando o colapso muscular. Existem várias variantes:
- Pressão positiva contínua nas vias aéreas (CPAP) é eficaz tanto em casos moderados quanto graves.[107] É o tratamento mais comum para apneia obstrutiva do sono.[108]
- Pressão positiva variável nas vias aéreas (VPAP) (também conhecido como bilevel (BiPAP ou BPAP)) utiliza um circuito eletrônico para monitorar a respiração do paciente e fornece duas pressões diferentes, uma maior durante a inspiração e uma menor durante a expiração. Esse sistema é mais caro e às vezes é utilizado em pacientes com outros problemas respiratórios coexistentes ou que acham desconfortável ou perturbador para o sono expirar contra uma pressão aumentada.
- Pressão expiratória positiva nasal (EPAP nasal) é um dispositivo semelhante a um curativo colocado sobre as narinas que utiliza a própria respiração da pessoa para criar pressão positiva nas vias aéreas e evitar a obstrução respiratória.[109]
- Pressão positiva automática nas vias aéreas, também conhecida como "Auto CPAP", incorpora sensores de pressão e monitora a respiração do paciente.[110][111]
- Uma redução de 5% no peso entre pessoas com AOS moderada a grave pode diminuir os sintomas de forma similar ao CPAP.[112]
Incentivar pessoas com AOS moderada a grave a usar dispositivos de CPAP pode ser desafiador, pois seu uso frequentemente requer mudança comportamental nos hábitos de sono.[108] 8% das pessoas que usam dispositivos de CPAP deixam de usá-los após a primeira noite;[108] e 50% das pessoas com AOS moderada a grave deixam de usar seus dispositivos no primeiro ano.[108] Iniciativas educativas e intervenções de apoio para melhorar a adesão à terapia com CPAP têm demonstrado aumentar o tempo de uso dos dispositivos por quem necessita desse tratamento.[108]
Muitas pessoas se beneficiam de dormir com a parte superior do corpo elevada em 30 graus[113] ou mais, como em uma Poltrona reclinável. Fazer isso ajuda a prevenir o colapso gravitacional das vias aéreas. Deitar-se de lado em vez de deitar-se de costas também é recomendado.[114][115][116]
Alguns estudos sugerem que tocar um Instrumento de sopro pode reduzir roncos e episódios de apneia.[117] Isso pode ser especialmente verdadeiro para instrumentos de palheta dupla.[118]
Medicamentos
Evidências são insuficientes para apoiar o uso de medicamentos no tratamento direto da apneia obstrutiva do sono.[102][119][120]
Isso inclui o uso de fluoxetina, paroxetina, acetazolamida e triptofano, entre outros.[102][121]
Estudos recentes estão investigando os canabinoides como tratamento para a SAOS, especialmente o dronabinol, que é uma forma sintética do THC (delta-9-tetraidrocanabinol). A cannabis é conhecida por influenciar o sono, por exemplo, pode reduzir a latência de início do sono, porém os resultados não são consistentes.[122] Estudos sobre o dronabinol mostraram impacto positivo na SAOS, observando redução no índice de apneia–hipopneia (IAH) e aumento na sonolência autorreferida (a sonolência objetiva permanece inalterada).[123] No entanto, são necessárias mais evidências, pois muitos efeitos dessas substâncias permanecem desconhecidos, especialmente os efeitos do uso a longo prazo.[124] O efeito na sonolência e no ganho de peso é particularmente preocupante.[125] Devido à incerteza sobre seus efeitos e à falta de evidências consistentes, o uso de cannabis medicinal não é recomendado para o tratamento da SAOS.[124][126]
Para adultos com obesidade e SAOS moderada a grave, a tirzepatida por 52 semanas reduz substancialmente eventos apneicos-hipopnicos, peso corporal, carga hipóxica, concentração de hsCRP e pressão arterial sistólica, e melhora desfechos relacionados ao sono autorreferidos pelos pacientes, tudo presumivelmente mediado pela perda de peso induzida de 18–20% em relação ao valor basal.[127]
Existem vários medicamentos aprovados para o manejo da sonolência diurna excessiva associada à SAOS, mas que não tratam a causa subjacente. Esses incluem solriamfetol, modafinil e armodafinil.[128][129][130]
A tirzepatida (marca Zepbound) é usada para controle de peso em adultos com IMC superior a 30, para o tratamento da SAOS. Em 2024, dois estudos financiados pela Eli Lilly and Company observaram que pessoas que utilizaram o Zepbound apresentaram maior melhora nos sintomas da apneia do sono, incluindo menos interrupções do sono.[131]
Aparelhos dentários
Placas de avanço mandibular (dispositivos de avanço mandibular) são projetadas para manter a mandíbula inferior ligeiramente para baixo e avançada em relação à posição natural e relaxada. Essa posição afasta a língua da parte posterior da via aérea e pode ser suficiente para aliviar a apneia ou melhorar a respiração. Esse dispositivo é um protetor bucal semelhante aos usados em esportes para proteger os dentes. As placas de avanço mandibular são usadas para o ronco e para a apneia obstrutiva do sono de leve a moderada.[132] São mais adequadas para pessoas com IAH < 25, IMC < 30 e boa dentição.[133]
Quando apropriado, são consideradas uma boa opção terapêutica, pois são não invasivas, facilmente reversíveis e não produzem ruído. Geralmente são bem toleradas, pois são menos desconfortáveis. No entanto, podem não ser tão eficazes quanto o CPAP.[107] Dispositivos orais têm demonstrado sucesso no tratamento da AOS. Isso inclui os índices polissonográficos de AOS, medidas subjetivas e objetivas de sonolência, pressão arterial, aspectos do funcionamento neuropsicológico e qualidade de vida.[134] O foco de melhoria no design desses aparelhos é reduzir o volume, permitir movimento livre da mandíbula (por exemplo, bocejar, falar e beber) e permitir que o usuário respire pela boca (os dispositivos iniciais tipo “protetor gengival soldado” impediam a respiração oral).
Dispositivos de reposicionamento (retenção) da língua são feitos de acrílico macio, cobrem os dentes superiores e inferiores e criam vedação com os lábios. Possuem um “bulbo” ou “bolha” que se projeta na frente da boca. Isso cria pressão de sucção negativa, mantendo a língua em posição avançada e aumentando o espaço aéreo atrás da língua.[132] Dispositivos híbridos combinam avanço mandibular com retenção da língua. Esses aparelhos têm sido utilizados para ronco e apneia obstrutiva do sono.[135] Dispositivos de retenção da língua não foram bem aceitos como terapia, pois são invasivos e o período de adaptação é longo. No entanto, esses aparelhos têm apresentado altas taxas de sucesso terapêutico.[136][137]
Elevadores de palato mole são dispositivos que elevam o palato mole. São úteis para pessoas com fraqueza muscular na região.[132]
As evidências para apoiar aparelhos orais/aparelhos ortopédicos funcionais em crianças são insuficientes, com evidência muito baixa de efeito. No entanto, esses aparelhos podem ser considerados em casos específicos como auxiliar no tratamento de crianças com anomalias craniofaciais que são fatores de risco para apneia.[138]
Expansão palatina rápida
Ver também Em crianças, o tratamento ortodôntico para ampliar o volume das vias aéreas nasais, como a expansão palatina rápida não cirúrgica, é comum.
Como a sutura palatina está fundida em adultos, a expansão palatina rápida convencional com expansores apoiados nos dentes não pode ser realizada. A expansão palatina rápida assistida por mini-implante (MARPE) foi desenvolvida recentemente como opção não cirúrgica para a expansão transversal da maxila em adultos. Esse método aumenta o volume da cavidade nasal e da nasofaringe, levando ao aumento do fluxo de ar e à redução dos despertares respiratórios durante o sono.[139][140] As alterações são permanentes, com complicações mínimas.
A Cirurgia do sono é um conjunto de tratamentos cirúrgicos para modificar a anatomia das vias aéreas. Esses procedimentos são variados e adaptados à localização e natureza específicas da obstrução em cada indivíduo. A cirurgia não é considerada tratamento de primeira linha para apneia obstrutiva do sono em adultos. Para pessoas com apneia obstrutiva do sono que são incapazes ou não desejam cumprir o tratamento de primeira linha, a intervenção cirúrgica é adaptada à anatomia e fisiologia individuais, preferência pessoal e gravidade da doença.[100] A Uvulopalatofaringoplastia (UPFP) com ou sem Amigdalectomia é o procedimento mais comum para AOS. É eficaz em pacientes selecionados que não responderam ao tratamento conservador.[141][106] Na Amigdalectomia, o benefício da cirurgia aumenta com o tamanho das amígdalas.[142] Contudo, há pouca evidência de ensaios clínicos randomizados para outros tipos de cirurgia do sono.[102] Existem vários procedimentos que podem ser realizados, incluindo:
- Septoplastia — procedimento corretivo para Desvio de septo nasal em que o Septo nasal é endireitado.
- Amigdalectomia[142] ou Adenoidectomia para aumentar o diâmetro das vias aéreas.
- Tonsilotomia
- Remoção ou redução de partes do Palato mole e de parte ou toda a úvula, como Uvulopalatofaringoplastia ou uvulopalatoplastia assistida por laser (LAUP); variantes modernas podem usar Radiofrequência para remover tecido.
- Turbinectomia — remoção total ou parcial das Concha nasal para aliviar obstrução nasal.
- Redução da base da língua, por excisão a laser ou Ablação por radiofrequência.
- Avanço genioglosso — deslocamento de parte da mandíbula inferior para avançar a língua e desobstruir a via aérea.
- Suspensão do osso hioide — tracionamento do osso hioide para frente, em direção à Laringe, para expandir a via aérea.
- Avanço maxilomandibular[143]
- Cirurgia bariátrica (para obesidade mórbida)
- Estimulação do nervo hipoglosso
- Ablação por radiofrequência
Prognóstico
O Acidente vascular cerebral e outras Doença cardiovascular estão relacionados à AOS, e pessoas com menos de 70 anos têm risco aumentado de morte precoce.[35] Indivíduos com apneia do sono têm 30% mais risco de Infarto do miocárdio ou morte do que pessoas não afetadas.[144] Em casos graves e prolongados, o aumento da pressão pulmonar é transmitido ao lado direito do coração, podendo resultar em insuficiência cardíaca congestiva grave conhecida como Cor pulmonale. A função diastólica cardíaca também é afetada.[145] A pressão arterial elevada (Hipertensão) pode ser consequência da AOS.[146] Quando a hipertensão é causada pela AOS, ela não apresenta queda significativa durante o sono (não dipper) ou até aumenta (dipper invertido).[147]
Sem tratamento, a Privação de sono e a falta de oxigênio causadas pela apneia do sono aumentam riscos como Doença cardiovascular, Aneurisma da aorta, Hipertensão, Acidente vascular cerebral, Diabetes, Depressão clínica, ganho de peso, Obesidade e até morte.
A AOS está associada a comprometimento cognitivo, incluindo déficits em raciocínio indutivo e dedutivo, atenção, vigilância, aprendizagem, funções executivas e memória episódica e de trabalho. Está ligada a maior risco de Comprometimento cognitivo leve e demência, e a alterações neuroanatômicas (redução do volume do hipocampo e da substância cinzenta dos lobos frontal e parietal), as quais podem ser parcial ou totalmente revertidas com CPAP.[148][149]
Epidemiologia
Até a década de 1990, pouco se sabia sobre a frequência da AOS.[150][151] Para ≥ 5 eventos de apneia por hora, a prevalência variou de 9% a 38% (13%–33% em homens; 6%–19% em mulheres); em pessoas com ≥ 65 anos, chegou a 84% (90% em homens; 78% em mulheres). Para ≥ 15 eventos/hora, variou de 6% a 17%, chegando a quase 49% em ≥ 65 anos.[151] Um aumento de 10% no peso corporal multiplicou em seis vezes o risco de AOS em obesos.[151]
A AOS é subdiagnosticada, pois nem sempre cursa com sonolência diurna, deixando a respiração alterada despercebida.[152] Estima-se que AOS com sonolência diurna afete 3%–7% dos homens e 2%–5% das mulheres, sendo comum em países desenvolvidos e em desenvolvimento.[150] A prevalência aumenta com a idade (22,1%–83,6% em ≥ 65 anos) e cresceu muito nas últimas décadas devido à obesidade.[96]
Homens são mais afetados que mulheres, mas a apresentação clínica difere: ronco e apneias testemunhadas são mais comuns em homens; insônia é mais frequente em mulheres. A frequência aumenta com a idade feminina e a mortalidade é maior entre elas.[64]
Em polissonografia, acredita-se que 1 em cada 5 adultos nos Estados Unidos tenha ao menos AOS leve.[153] Estudos indicam maior frequência em hispânicos e afro-americanos do que em brancos.[64]
Sociedade e cultura
Estados Unidos
Nos Estados Unidos, o teste domiciliar do sono tem sido preferido pelas seguradoras privadas, pois custo e coparticipações podem ser menores que na polissonografia convencional.[carece de fontes]
A ablação por radiofrequência foi reconhecida pela Academia Americana de Otorrinolaringologia e Cirurgia de Cabeça e Pescoço[154] como opção de somnoplastia em AOS leve a moderada, mas o Colégio Americano de Médicos considerou a evidência insuficiente para uso rotineiro.[102]
Pesquisa
A Neuroestimulação está sendo estudada como método de tratamento.[155] Um sistema implantável de estimulação do nervo hipoglosso recebeu a marca CE na Europa em março de 2012.[156] Também são estudados exercícios dos músculos ao redor da boca e da Faringe por meio de atividades como tocar Didgeridoo.[157][158]
Ver também
Referências
- ↑ Punjabi, Naresh M.; Caffo, Brian S.; Goodwin, James L.; Gottlieb, Daniel J.; Newman, Anne B.; O'Connor, George T.; Rapoport, David M.; Redline, Susan; Resnick, Helaine E.; Robbins, John A.; Shahar, Eyal; Unruh, Mark L.; Samet, Jonathan M. (18 de agosto de 2009). «Sleep-Disordered Breathing and Mortality: A Prospective Cohort Study». PLOS Medicine. 6 (8): e1000132. PMC 2722083
 . PMID 19688045. doi:10.1371/journal.pmed.1000132
. PMID 19688045. doi:10.1371/journal.pmed.1000132
- ↑ Barnes L, ed. (2009). Surgical pathology of the head and neck 3rd ed. New York: Informa healthcare. ISBN 978-1-4200-9163-2:226
- ↑ a b c d Young, Terry; Skatrud, J; Peppard, PE (28 de abril de 2004). «Risk Factors for Obstructive Sleep Apnea in Adults». JAMA. 291 (16): 2013–2016. PMID 15113821. doi:10.1001/jama.291.16.2013
- ↑ Berry, Richard B.; Budhiraja, Rohit; Gottlieb, Daniel J.; Gozal, David; Iber, Conrad; Kapur, Vishesh K.; Marcus, Carole L.; Mehra, Reena; Parthasarathy, Sairam; Quan, Stuart F.; Redline, Susan; Strohl, Kingman P.; Ward, Sally L. Davidson; Tangredi, Michelle M.; American Academy of Sleep Medicine (2012). «Rules for Scoring Respiratory Events in Sleep: Update of the 2007 AASM Manual for the Scoring of Sleep and Associated Events». Journal of Clinical Sleep Medicine. 08 (5): 597–619. PMC 3459210
 . PMID 23066376. doi:10.5664/jcsm.2172
. PMID 23066376. doi:10.5664/jcsm.2172
- ↑ American Academy of Sleep Medicine (2014). International Classification of Sleep Disorders, 3rd edition. Darien, IL: American Academy of Sleep Medicine
- ↑ Tung P, Levitzky YS, Wang R, Weng J, Quan SF, Gottlieb DJ, et al. (julho 2017). «Obstructive and Central Sleep Apnea and the Risk of Incident Atrial Fibrillation in a Community Cohort of Men and Women». Journal of the American Heart Association. 6 (7). PMC 5586257
 . PMID 28668820. doi:10.1161/jaha.116.004500
. PMID 28668820. doi:10.1161/jaha.116.004500
- ↑ Stoohs RA, Blum HC, Knaack L, Butsch-von-der-Heydt B, Guilleminault C (março 2005). «Comparison of pleural pressure and transcutaneous diaphragmatic electromyogram in obstructive sleep apnea syndrome». Sleep. 28 (3): 321–329. PMID 16173653
- ↑ a b c American Academy of Sleep Medicine. «AASM Practice Guidelines». AASM. Consultado em 19 de junho de 2019
- ↑ Mbata, GC; Chukwuka, JC (2012). «Obstructive Sleep Apnea Hypopnea Syndrome». Annals of Medical and Health Sciences Research. 2 (1): 74–77. PMC 3507119
 . PMID 23209996. doi:10.4103/2141-9248.96943 (inativo 12 de novembro de 2024)
. PMID 23209996. doi:10.4103/2141-9248.96943 (inativo 12 de novembro de 2024)
- ↑ Patel, Sanjay R. (3 de outubro de 2024). «Entering a New Era in Sleep-Apnea Treatment». New England Journal of Medicine (em inglês). 391 (13): 1248–1249. ISSN 0028-4793. PMID 38912659. doi:10.1056/NEJMe2407117
- ↑ Caporale, Mina; Palmeri, Rosanna; Corallo, Francesco; Muscarà, Nunzio; Romeo, Laura; Bramanti, Alessia; Marino, Silvia; Lo Buono, Viviana (23 de maio de 2020). «Cognitive impairment in obstructive sleep apnea syndrome: a descriptive review». Sleep and Breathing. 25 (1): 29–40. PMID 32447633. doi:10.1007/s11325-020-02084-3
- ↑ Li, Deshui; Kuang, Boyuan; Lobbezoo, Frank; de Vries, Nico; Hilgevoord, Antonius; Aarab, Ghizlane (março de 2023). «Sleep bruxism is highly prevalent in adults with obstructive sleep apnea: a large-scale polysomnographic study». Journal of Clinical Sleep Medicine (em inglês). 19 (3): 443–451. ISSN 1550-9389. PMC 9978428
 . PMID 36448332. doi:10.5664/jcsm.10348
. PMID 36448332. doi:10.5664/jcsm.10348
- ↑ Gu, Yiwei (26 de maio de 2022). «Erectile Dysfunction and Obstructive Sleep Apnea: A Review». Frontiers in Psychiatry. 13. PMC 9178074
 . PMID 35693968. doi:10.3389/fpsyt.2022.766639
. PMID 35693968. doi:10.3389/fpsyt.2022.766639
- ↑ Ezzeddini R, Darabi M, Ghasemi B, Jabbari Moghaddam Y, Abdollahi SH, Rashtchizadeh N, Gharahdaghi A, Darabi M, Ansarin M, Shaaker M, Samadi A, Karamravan J (Apr 2012). «Circulating phospholipase-A2 activity in obstructive sleep apnea and recurrent tonsillitis». Int J Pediatr Otorhinolaryngol. 76 (4): 741–744. PMID 22297210. doi:10.1016/j.ijporl.2011.12.026 Verifique data em:
|data=(ajuda) - ↑ Ezzedini R, Darabi M, Ghasemi B, Darabi M, Fayezi SH, Jabbari Moghaddam Y, Mehdizadeh A, Abdollahi SH, Gharahdaghi A (maio 2013). «Tissue fatty acid composition in obstructive sleep apnea and recurrent tonsillitis». Int J Pediatr Otorhinolaryngol. 77 (6): 1008–1012. PMID 23643333. doi:10.1016/j.ijporl.2013.03.033
- ↑ «Obstructive Sleep Apnea». The Lecturio Medical Concept Library. 7 de agosto de 2020. Consultado em 21 de agosto de 2021
- ↑ Lal, Chitra; Weaver, Terri E.; Bae, Charles J.; Strohl, Kingman P. (2021). «Excessive Daytime Sleepiness in Obstructive Sleep Apnea. Mechanisms and Clinical Management». Annals of the American Thoracic Society. 18 (5): 757–768. ISSN 2325-6621. PMC 8086534
 . PMID 33621163. doi:10.1513/AnnalsATS.202006-696FR
. PMID 33621163. doi:10.1513/AnnalsATS.202006-696FR
- ↑ a b Gale, Shawn D.; Hopkins, Ramona O. (janeiro de 2004). «Effects of hypoxia on the brain: Neuroimaging and neuropsychological findings following carbon monoxide poisoning and obstructive sleep apnea». Journal of the International Neuropsychological Society. 10 (1): 60–71. PMID 14751008. doi:10.1017/S1355617704101082 (inativo 12 de novembro de 2024)
- ↑ Andrade, Andreia; Bubu, Omonigho M.; Varga, Andrew W.; Osorio, Ricardo S. (2018). «The relationship between Obstructive Sleep Apnea and Alzheimer's Disease». Journal of Alzheimer's Disease (em inglês). 64 (Suppl 1): S255–S270. PMC 6542637
 . PMID 29782319. doi:10.3233/JAD-179936
. PMID 29782319. doi:10.3233/JAD-179936
- ↑ Frey, William (13 de outubro de 2003). «Obstructive sleep-related breathing disorders in patients evaluated for bariatric surgery». Obesity Surgery. 13 (5): 676–683. PMID 14627460. doi:10.1381/096089203322509228
- ↑ Gray, Emma (15 de janeiro de 2017). «Obstructive Sleep Apnea without Obesity Is Common and Difficult to Treat: Evidence for a Distinct Pathophysiological Phenotype». Journal of Clinical Sleep Medicine. 13 (1): 81–88. PMC 5181619
 . PMID 27655455. doi:10.5664/jcsm.6394
. PMID 27655455. doi:10.5664/jcsm.6394
- ↑ Bixler, E.O. (agosto de 2000). «Association of hypertension and sleep-disordered breathing». Archives of Internal Medicine. 160 (15): 2289–2295. PMID 10927725. doi:10.1001/archinte.160.15.2289
- ↑ Luyster, Faith (1 de dezembro de 2014). «Relation of obstructive sleep apnea to coronary artery calcium in non-obese versus obese men and women aged 45-75 years». American Journal of Cardiology. 114 (11): 1690–4. PMC 4252727
 . PMID 25307200. doi:10.1016/j.amjcard.2014.08.040
. PMID 25307200. doi:10.1016/j.amjcard.2014.08.040
- ↑ Eckert, DJ (15 de outubro de 2013). «efining phenotypic causes of obstructive sleep apnea. Identification of novel therapeutic targets». American Journal Respiratory and Critical Care Medicine. 188 (81996–2004): 996–1004. PMC 3826282
 . PMID 23721582. doi:10.1164/rccm.201303-0448OC
. PMID 23721582. doi:10.1164/rccm.201303-0448OC
- ↑ Henry, Doug; Rosenthal, Leon (fevereiro de 2013). «'Listening for his breath:' The significance of gender and partner reporting on the diagnosis, management, and treatment of obstructive sleep apnea». Social Science & Medicine. 79: 48–56. PMID 22770968. doi:10.1016/j.socscimed.2012.05.021
- ↑ O'Brien, Louise M.; Holbrook, Cheryl R.; Mervis, Carolyn B.; Klaus, Carrie J.; Bruner, Jennifer L.; Raffield, Troy J.; Rutherford, Jennifer; Mehl, Rochelle C.; Wang, Mei; Tuell, Andrew; Hume, Brittany C.; Gozal, David (março de 2003). «Sleep and Neurobehavioral Characteristics of 5- to 7-Year-Old Children With Parentally Reported Symptoms of Attention-Deficit/Hyperactivity Disorder». Pediatrics. 111 (3): 554–563. PMID 12612236. doi:10.1542/peds.111.3.554
- ↑ Schechter, Michael S. (abril de 2002). «Technical Report: Diagnosis and Management of Childhood Obstructive Sleep Apnea Syndrome». Pediatrics. 109 (4): e69. PMID 11927742. doi:10.1542/peds.109.4.e69
- ↑ Rosen, Carol L.; Storfer-Isser, Amy; Taylor, H. Gerry; Kirchner, H. Lester; Emancipator, Judith L.; Redline, Susan (dezembro de 2004). «Increased Behavioral Morbidity in School-Aged Children With Sleep-Disordered Breathing». Pediatrics. 114 (6): 1640–1648. PMID 15574628. doi:10.1542/peds.2004-0103
- ↑ a b c d e f g h i Dehlink E, Tan HL (February 2016). «Update on paediatric obstructive sleep apnoea». Journal of Thoracic Disease. 8 (2): 224–235. PMC 4739955
 . PMID 26904263. doi:10.3978/j.issn.2072-1439.2015.12.04 Verifique data em:
. PMID 26904263. doi:10.3978/j.issn.2072-1439.2015.12.04 Verifique data em: |data=(ajuda) - ↑ Jazi SM, Barati B, Kheradmand A (dezembro 2011). «Treatment of adenotonsillar hypertrophy: A prospective randomized trial comparing azithromycin vs. fluticasone». Journal of Research in Medical Sciences. 16 (12): 1590–1597. PMC 3434901
 . PMID 22973368
. PMID 22973368
- ↑ a b c d e f g h i j k Capdevila OS, Kheirandish-Gozal L, Dayyat E, Gozal D (February 2008). «Pediatric obstructive sleep apnea: complications, management, and long-term outcomes». Proceedings of the American Thoracic Society. 5 (2): 274–282. PMC 2645258
 . PMID 18250221. doi:10.1513/pats.200708-138MG Verifique data em:
. PMID 18250221. doi:10.1513/pats.200708-138MG Verifique data em: |data=(ajuda) - ↑ a b c d e f g h Dayyat E, Kheirandish-Gozal L, Gozal D (setembro 2007). «Childhood Obstructive Sleep Apnea: One or Two Distinct Disease Entities?». Sleep Medicine Clinics. 2 (3): 433–444. PMC 2084206
 . PMID 18769509. doi:10.1016/j.jsmc.2007.05.004
. PMID 18769509. doi:10.1016/j.jsmc.2007.05.004
- ↑ Kalra M, Inge T, Garcia V, Daniels S, Lawson L, Curti R, et al. (julho 2005). «Obstructive sleep apnea in extremely overweight adolescents undergoing bariatric surgery». Obesity Research. 13 (7): 1175–1179. PMID 16076986. doi:10.1038/oby.2005.139

- ↑ Verhulst SL, Franckx H, Van Gaal L, De Backer W, Desager K (junho–falhou de undefined). «The effect of weight loss on sleep-disordered breathing in obese teenagers». Obesity. 17 (6): 1178–1183. PMID 19265797. doi:10.1038/oby.2008.673
 Verifique data em:
Verifique data em: |data=(ajuda) - ↑ a b Franklin KA, Lindberg E (agosto de 2015). «Obstructive sleep apnea is a common disorder in the population-a review on the epidemiology of sleep apnea». Journal of Thoracic Disease. 7 (8): 1311–1322. PMC 4561280
 . PMID 26380759. doi:10.3978/j.issn.2072-1439.2015.06.11
. PMID 26380759. doi:10.3978/j.issn.2072-1439.2015.06.11
- ↑ Berry RB, Quan SF, Abrue AR, et al.; for the American Academy of Sleep Medicine. The AASM Manual for the Scoring of Sleep and Associated Events: Rules, Terminology and Technical Specifications. Version 2.6. Darien, IL: American Academy of Sleep Medicine; 2020.
- ↑ Kapur VK, Auckley DH, Chowdhuri S, Kuhlmann DC, Mehra R, Ramar K, Harrod CG (março de 2017). «Clinical Practice Guideline for Diagnostic Testing for Adult Obstructive Sleep Apnea: An American Academy of Sleep Medicine Clinical Practice Guideline». Journal of Clinical Sleep Medicine. 13 (3): 479–504. PMC 5337595
 . PMID 28162150. doi:10.5664/jcsm.6506
. PMID 28162150. doi:10.5664/jcsm.6506
- ↑ Thurnheer, R. (setembro de 2007). «Diagnosis of the obstructive sleep apnea syndrome». Minerva Pneumologica. 46 (3): 191–204
- ↑ Crook S, Sievi NA, Bloch KE, Stradling JR, Frei A, Puhan MA, Kohler M (abril de 2019). «Minimum important difference of the Epworth Sleepiness Scale in obstructive sleep apnoea: estimation from three randomised controlled trials». Thorax. 74 (4): 390–396. PMID 30100576. doi:10.1136/thoraxjnl-2018-211959

- ↑ Chiu HY, Chen PY, Chuang LP, Chen NH, Tu YK, Hsieh YJ, et al. (dezembro de 2017). «Diagnostic accuracy of the Berlin questionnaire, STOP-BANG, STOP, and Epworth sleepiness scale in detecting obstructive sleep apnea: A bivariate meta-analysis». Sleep Medicine Reviews. 36: 57–70. PMID 27919588. doi:10.1016/j.smrv.2016.10.004
- ↑ Amra B, Javani M, Soltaninejad F, Penzel T, Fietze I, Schoebel C, Farajzadegan Z (2018). «Comparison of Berlin Questionnaire, STOP-Bang, and Epworth Sleepiness Scale for Diagnosing Obstructive Sleep Apnea in Persian Patients». International Journal of Preventive Medicine. 9 (28): 28. PMC 5869953
 . PMID 29619152. doi:10.4103/ijpvm.IJPVM_131_17
. PMID 29619152. doi:10.4103/ijpvm.IJPVM_131_17
- ↑ a b «Sleep-related breathing disorders in adults: recommendations for syndrome definition and measurement techniques in clinical research. The Report of an American Academy of Sleep Medicine Task Force». Sleep. 22 (5): 667–689. Agosto 1999. PMID 10450601. doi:10.1093/sleep/22.5.667

- ↑ Lux, Linda; Boehlecke, Brian; Lohr, Kathleen N. (2004). Effectiveness of Portable Monitoring Devices for Diagnosing Obstructive Sleep Apnea: Update of a Systematic Review. Col: AHRQ Technology Assessments. Rockville (MD): Agency for Healthcare Research and Quality (US). PMID 26065047
- ↑ Lee, Janet J.; Sundar, Krishna M. (abril de 2021). «Evaluation and Management of Adults with Obstructive Sleep Apnea Syndrome». Lung. 199 (2): 87–101. ISSN 1432-1750. PMID 33713177. doi:10.1007/s00408-021-00426-w
- ↑ a b Mulgrew AT, Fox N, Ayas NT, Ryan CF (February 2007). «Diagnosis and initial management of obstructive sleep apnea without polysomnography: a randomized validation study». Annals of Internal Medicine. 146 (3): 157–166. PMID 17283346. doi:10.7326/0003-4819-146-3-200702060-00004 Verifique data em:
|data=(ajuda) - ↑ a b Flemons WW, Whitelaw WA, Brant R, Remmers JE (novembro 1994). «Likelihood ratios for a sleep apnea clinical prediction rule». American Journal of Respiratory and Critical Care Medicine. 150 (5 Pt 1): 1279–1285. PMID 7952553. doi:10.1164/ajrccm.150.5.7952553
- ↑ American Academy of Sleep Medicine. International classification of sleep disorders. 3rd ed. Darien, IL: American Academy of Sleep Medicine, 2014.
- ↑ Tschopp, Samuel; Wimmer, Wilhelm; Caversaccio, Marco; Borner, Urs; Tschopp, Kurt (30 de março de 2021). «Night-to-night variability in obstructive sleep apnea using peripheral arterial tonometry: a case for multiple night testing». Journal of Clinical Sleep Medicine (em inglês). 17 (9): 1751–1758. ISSN 1550-9389. PMC 8636340
 . PMID 33783347. doi:10.5664/jcsm.9300
. PMID 33783347. doi:10.5664/jcsm.9300
- ↑ Saboisky JP, Butler JE, Gandevia SC, Eckert DJ (15 de junho de 2012). «Functional role of neural injury in obstructive sleep apnea». Frontiers in Neurology. 3: 95. PMC 3375463
 . PMID 22715333. doi:10.3389/fneur.2012.00095
. PMID 22715333. doi:10.3389/fneur.2012.00095
- ↑ Schwab RJ, Kim C, Bagchi S, Keenan BT, Comyn FL, Wang S, et al. (junho–falhou de undefined). «Understanding the anatomic basis for obstructive sleep apnea syndrome in adolescents». American Journal of Respiratory and Critical Care Medicine. 191 (11): 1295–1309. PMC 4476519
 . PMID 25835282. doi:10.1164/rccm.201501-0169OC Verifique data em:
. PMID 25835282. doi:10.1164/rccm.201501-0169OC Verifique data em: |data=(ajuda) - ↑ Edwards N, Sullivan CE (2008). «Sleep-Disordered Breathing in Pregnancy». Sleep Medicine Clinics. 3 (6): 81–95. PMC 1746354
 . PMID 12037233. doi:10.1016/j.jsmc.2007.10.010
. PMID 12037233. doi:10.1016/j.jsmc.2007.10.010
- ↑ «Sleep apnea – Symptoms and causes». Mayo Clinic
- ↑ Lu LR, Peat JK, Sullivan CE (agosto 2003). «Snoring in preschool children: prevalence and association with nocturnal cough and asthma». Chest. 124 (2): 587–593. PMID 12907547. doi:10.1378/chest.124.2.587
- ↑ McColley, Susanna A.; Carroll, John L.; Curtis, Shelly; Loughlin, Gerald M.; Sampson, Hugh A. (janeiro de 1997). «High Prevalence of Allergic Sensitization in Children With Habitual Snoring and Obstructive Sleep Apnea». Chest. 111 (1): 170–173. PMID 8996012. doi:10.1378/chest.111.1.170

- ↑ Mukherjee, Sutapa; Saxena, Richa; Palmer, Lyle J. (janeiro de 2018). «The genetics of obstructive sleep apnoea». Respirology. 23 (1): 18–27. ISSN 1440-1843. PMC 7308164
 . PMID 29113020. doi:10.1111/resp.13212
. PMID 29113020. doi:10.1111/resp.13212
- ↑ Campos, AI; Ingold, N; Huang, Y; Mitchell, BL; Kho, PF; Han, X; García-Marín, LM; Ong, JS; 23andMe Research, Team; Law, MH; Yokoyama, JS; Martin, NG; Dong, X; Cuellar-Partida, G; MacGregor, S; Aslibekyan, S; Rentería, ME (9 de março de 2023). «Discovery of genomic loci associated with sleep apnea risk through multi-trait GWAS analysis with snoring.». Sleep. 46 (3). PMC 9995783
 . PMID 36525587. doi:10.1093/sleep/zsac308
. PMID 36525587. doi:10.1093/sleep/zsac308
- ↑ de Miguel-Díez J, Villa-Asensi JR, Alvarez-Sala JL (dezembro 2003). «Prevalence of sleep-disordered breathing in children with Down syndrome: polygraphic findings in 108 children». Sleep. 26 (8): 1006–1009. PMID 14746382. doi:10.1093/sleep/26.8.1006
- ↑ Shott SR, Amin R, Chini B, Heubi C, Hotze S, Akers R (abril 2006). «Obstructive sleep apnea: Should all children with Down syndrome be tested?». Archives of Otolaryngology–Head & Neck Surgery. 132 (4): 432–436. PMID 16618913. doi:10.1001/archotol.132.4.432
- ↑ Sloan, Gerald M. (março de 2000). «Posterior Pharyngeal Flap and Sphincter Pharyngoplasty: The State of the Art». The Cleft Palate-Craniofacial Journal. 37 (2): 112–122. PMID 10749049. doi:10.1597/1545-1569_2000_037_0112_ppfasp_2.3.co_2
- ↑ Pugh, M.B. et al. (2000). Apnea. Stedman's Medical Dictionary (27th ed.) Retrieved June 18, 2006 from STAT!Ref Online Medical Library database.
- ↑ Liao YF, Noordhoff MS, Huang CS, Chen PK, Chen NH, Yun C, Chuang ML (março 2004). «Comparison of obstructive sleep apnea syndrome in children with cleft palate following Furlow palatoplasty or pharyngeal flap for velopharyngeal insufficiency». The Cleft Palate-Craniofacial Journal. 41 (2): 152–156. PMID 14989690. doi:10.1597/02-162
- ↑ McWilliams BJ, Peterson-Falzone SJ, Hardin-Jones MA, Karnell MP (2001). Cleft palate speech
 3rd ed. St. Louis: Mosby. ISBN 978-0-8151-3153-3
3rd ed. St. Louis: Mosby. ISBN 978-0-8151-3153-3
- ↑ Gross JB, Bachenberg KL, Benumof JL, Caplan RA, Connis RT, Coté CJ, et al. (maio 2006). «Practice guidelines for the perioperative management of patients with obstructive sleep apnea: a report by the American Society of Anesthesiologists Task Force on Perioperative Management of patients with obstructive sleep apnea». Anesthesiology. 104 (5): 1081–1093; quiz 1117–1118. PMID 16645462. doi:10.1097/00000542-200605000-00026
- ↑ a b c d e f Foldvary-Schaefer, Nancy R.; Waters, Tina E. (agosto de 2017). «Sleep-Disordered Breathing». Continuum: Lifelong Learning in Neurology. 23 (4): 1093–1116. PMID 28777178. doi:10.1212/01.CON.0000522245.13784.f6
- ↑ a b c d Walter LM, Horne RS (2018). «Obstructive Sleep-Disordered Breathing in Children; impact on the Developing Brain». Pediatric Respirology and Critical Care Medicine. 2 (4): 58–64. doi:10.4103/prcm.prcm_16_18

- ↑ a b Chervin RD, Archbold KH (maio 2001). «Hyperactivity and polysomnographic findings in children evaluated for sleep-disordered breathing». Sleep. 24 (3): 313–320. PMID 11322714. doi:10.1093/sleep/24.3.313

- ↑ a b O'Brien LM, Mervis CB, Holbrook CR, Bruner JL, Smith NH, McNally N, et al. (junho–falhou de undefined). «Neurobehavioral correlates of sleep-disordered breathing in children». Journal of Sleep Research. 13 (2): 165–172. PMID 15175097. doi:10.1111/j.1365-2869.2004.00395.x Verifique data em:
|data=(ajuda) - ↑ a b c d Goyal A, Pakhare AP, Bhatt GC, Choudhary B, Patil R (2018). «Association of pediatric obstructive sleep apnea with poor academic performance: A school-based study from India». Lung India. 35 (2): 132–136. PMC 5846262
 . PMID 29487248. doi:10.4103/lungindia.lungindia_218_17
. PMID 29487248. doi:10.4103/lungindia.lungindia_218_17
- ↑ a b c Galland B, Spruyt K, Dawes P, McDowall PS, Elder D, Schaughency E (outubro 2015). «Sleep Disordered Breathing and Academic Performance: A Meta-analysis». Pediatrics. 136 (4): e934–946. PMID 26347434. doi:10.1542/peds.2015-1677

- ↑ a b c Amin R, Somers VK, McConnell K, Willging P, Myer C, Sherman M, et al. (janeiro 2008). «Activity-adjusted 24-hour ambulatory blood pressure and cardiac remodeling in children with sleep disordered breathing». Hypertension. 51 (1): 84–91. PMID 18071053. doi:10.1161/HYPERTENSIONAHA.107.099762

- ↑ a b c Basha, Suzanne; Bialowas, Christie; Ende, Kevin; Szeremeta, Wasyl (2005). «Effectiveness of Adenotonsillectomy in the Resolution of Nocturnal Enuresis Secondary to Obstructive Sleep Apnea». The Laryngoscope. 115 (6): 1101–1103. PMID 15933530. doi:10.1097/01.MLG.0000163762.13870.83
- ↑ a b c Barone JG, Hanson C, DaJusta DG, Gioia K, England SJ, Schneider D (julho 2009). «Nocturnal enuresis and overweight are associated with obstructive sleep apnea». Pediatrics. 124 (1): e53–59. PMID 19564269. doi:10.1542/peds.2008-2805
- ↑ a b c d Brooks, Lee J.; Topol, Howard I. (maio de 2003). «Enuresis in children with sleep apnea». The Journal of Pediatrics. 142 (5): 515–518. PMID 12756383. doi:10.1067/mpd.2003.158
- ↑ a b Weissbach A, Leiberman A, Tarasiuk A, Goldbart A, Tal A (agosto 2006). «Adenotonsilectomy improves enuresis in children with obstructive sleep apnea syndrome». International Journal of Pediatric Otorhinolaryngology. 70 (8): 1351–1356. PMID 16504310. doi:10.1016/j.ijporl.2006.01.011
- ↑ Nieminen P, Löppönen T, Tolonen U, Lanning P, Knip M, Löppönen H. Growth and biochemical markers of growth in children with snoring and obstructive sleep apnea. Pediatrics. 2002;109(4):e55. doi:10.1542/peds.109.4.e55
- ↑ a b c d e f g Alsubie HS, BaHammam AS (janeiro 2017). «Obstructive Sleep Apnoea: Children are not little Adults». Paediatric Respiratory Reviews. 21: 72–79. PMID 27262609. doi:10.1016/j.prrv.2016.02.003
- ↑ a b c d e f g McNicholas WT (February 2008). «Diagnosis of obstructive sleep apnea in adults». Proceedings of the American Thoracic Society. 5 (2): 154–160. PMID 18250207. doi:10.1513/pats.200708-118MG Verifique data em:
|data=(ajuda) - ↑ Stranks EK, Crowe SF (março 2016). «The Cognitive Effects of Obstructive Sleep Apnea: An Updated Meta-analysis». Archives of Clinical Neuropsychology. 31 (2): 186–193. PMID 26743325. doi:10.1093/arclin/acv087

- ↑ Robichaud-Hallé L, Beaudry M, Fortin M (setembro 2012). «Obstructive sleep apnea and multimorbidity». BMC Pulmonary Medicine. 12 (60): 60. PMC 3515504
 . PMID 23006602. doi:10.1186/1471-2466-12-60
. PMID 23006602. doi:10.1186/1471-2466-12-60
- ↑ Romero-Corral A, Caples SM, Lopez-Jimenez F, Somers VK (março 2010). «Interactions between obesity and obstructive sleep apnea: implications for treatment». Chest. 137 (3): 711–719. PMC 3021364
 . PMID 20202954. doi:10.1378/chest.09-0360
. PMID 20202954. doi:10.1378/chest.09-0360
- ↑ a b Fulda S, Schulz H (2003). «Cognitive Dysfunction in Sleep-Related Breathing Disorders: A Meta-Analysis». Sleep Research Online. 5 (1): 19–51
- ↑ a b c d Bucks RS, Olaithe M, Eastwood P (janeiro 2013). «Neurocognitive function in obstructive sleep apnoea: a meta-review». Respirology. 18 (1): 61–70. PMID 22913604. doi:10.1111/j.1440-1843.2012.02255.x
- ↑ Nejati V, Salehinejad MA, Nitsche MA (janeiro 2018). «Interaction of the Left Dorsolateral Prefrontal Cortex (l-DLPFC) and Right Orbitofrontal Cortex (OFC) in Hot and Cold Executive Functions: Evidence from Transcranial Direct Current Stimulation (tDCS)». Neuroscience. 369: 109–123. PMID 29113929. doi:10.1016/j.neuroscience.2017.10.042
- ↑ Beebe DW, Groesz L, Wells C, Nichols A, McGee K (maio 2003). «The neuropsychological effects of obstructive sleep apnea: a meta-analysis of norm-referenced and case-controlled data». Sleep. 26 (3): 298–307. PMID 12749549. doi:10.1093/sleep/26.3.298

- ↑ a b c Wallace A, Bucks RS (February 2013). «Memory and obstructive sleep apnea: a meta-analysis». Sleep. 36 (2): 203–220. PMC 3543053
 . PMID 23372268. doi:10.5665/sleep.2374 Verifique data em:
. PMID 23372268. doi:10.5665/sleep.2374 Verifique data em: |data=(ajuda) - ↑ a b Olaithe, Michelle; Bucks, Romola S.; Hillman, David R.; Eastwood, Peter R. (abril de 2018). «Cognitive deficits in obstructive sleep apnea: Insights from a meta-review and comparison with deficits observed in COPD, insomnia, and sleep deprivation» (PDF). Sleep Medicine Reviews. 38: 39–49. PMID 28760549. doi:10.1016/j.smrv.2017.03.005
- ↑ Rizzo D (agosto 2018). «Driving with obstructive sleep apnea policies, behaviors and screening measures»
- ↑ Morrone E, D'Artavilla Lupo N (2020). «Microsleep as a marker of sleepiness in obstructive sleep apnea patients». Journal of Sleep Research. 29 (2): e12882. PMID 31180173. doi:10.1111/jsr.12882
- ↑ Cori JM, Jackson ML, Barnes M, Westlake J, Emerson P, Lee J, et al. (junho–falhou de undefined). «The Differential Effects of Regular Shift Work and Obstructive Sleep Apnea on Sleepiness, Mood and Neurocognitive Function». Journal of Clinical Sleep Medicine. 14 (6): 941–951. PMC 5991942
 . PMID 29852909. doi:10.5664/jcsm.7156 Verifique data em:
. PMID 29852909. doi:10.5664/jcsm.7156 Verifique data em: |data=(ajuda) - ↑ Slater G, Steier J (dezembro 2012). «Excessive daytime sleepiness in sleep disorders». Journal of Thoracic Disease. 4 (6): 608–616. PMC 3506799
 . PMID 23205286. doi:10.3978/j.issn.2072-1439.2012.10.07
. PMID 23205286. doi:10.3978/j.issn.2072-1439.2012.10.07
- ↑ LaGrotte C, Fernandez-Mendoza J, Calhoun SL, Liao D, Bixler EO, Vgontzas AN (setembro 2016). «The relative association of obstructive sleep apnea, obesity and excessive daytime sleepiness with incident depression: a longitudinal, population-based study». International Journal of Obesity. 40 (9): 1397–1404. PMC 5014694
 . PMID 27143032. doi:10.1038/ijo.2016.87
. PMID 27143032. doi:10.1038/ijo.2016.87
- ↑ Mulgrew AT, Ryan CF, Fleetham JA, Cheema R, Fox N, Koehoorn M, et al. (dezembro 2007). «The impact of obstructive sleep apnea and daytime sleepiness on work limitation». Sleep Medicine. 9 (1): 42–53. PMID 17825611. doi:10.1016/j.sleep.2007.01.009
- ↑ Guilleminault C, Brooks SN (agosto 2001). «Excessive daytime sleepiness: a challenge for the practising neurologist». Brain. 124 (Pt 8): 1482–1491. PMID 11459741. doi:10.1093/brain/124.8.1482

- ↑ Jackson ML, McEvoy RD, Banks S, Barnes M (janeiro 2018). «Neurobehavioral Impairment and CPAP Treatment Response in Mild-Moderate Obstructive Sleep Apneas». Journal of Clinical Sleep Medicine. 14 (1): 47–56. PMC 5734892
 . PMID 29198304. doi:10.5664/jcsm.6878
. PMID 29198304. doi:10.5664/jcsm.6878
- ↑ Eskandari D, Zou D, Grote L, Schneider H, Penzel T, Hedner J (junho–falhou de undefined). «Independent associations between arterial bicarbonate, apnea severity and hypertension in obstructive sleep apnea». Respiratory Research. 18 (1): 130. PMC 5490198
 . PMID 28659192. doi:10.1186/s12931-017-0607-9
. PMID 28659192. doi:10.1186/s12931-017-0607-9 Verifique data em:
Verifique data em: |data=(ajuda) - ↑ a b c Drager LF, Togeiro SM, Polotsky VY, Lorenzi-Filho G (agosto 2013). «Obstructive sleep apnea: a cardiometabolic risk in obesity and the metabolic syndrome». Journal of the American College of Cardiology. 62 (7): 569–76. PMC 4461232
 . PMID 23770180. doi:10.1016/j.jacc.2013.05.045
. PMID 23770180. doi:10.1016/j.jacc.2013.05.045
- ↑ a b Ashrafian H, Toma T, Rowland SP, Harling L, Tan A, Efthimiou E, et al. (julho 2015). «Bariatric Surgery or Non-Surgical Weight Loss for Obstructive Sleep Apnoea? A Systematic Review and Comparison of Meta-analyses». Obesity Surgery. 25 (7): 1239–1250. PMID 25537297. doi:10.1007/s11695-014-1533-2. hdl:10044/1/54731

- ↑ Dobrosielski DA, Patil S, Schwartz AR, Bandeen-Roche K, Stewart KJ (janeiro 2015). «Effects of exercise and weight loss in older adults with obstructive sleep apnea». Medicine and Science in Sports and Exercise. 47 (1): 20–26. PMC 4246024
 . PMID 24870569. doi:10.1249/MSS.0000000000000387
. PMID 24870569. doi:10.1249/MSS.0000000000000387
- ↑ a b c d Reutrakul, Sirimon; Mokhlesi, Babak (novembro de 2017). «Obstructive Sleep Apnea and Diabetes». Chest. 152 (5): 1070–1086. PMC 5812754
 . PMID 28527878. doi:10.1016/j.chest.2017.05.009
. PMID 28527878. doi:10.1016/j.chest.2017.05.009
- ↑ a b Friedman: Sleep Apnea and Snoring, 1st ed. 2008
- ↑ Azagra-Calero E, Espinar-Escalona E, Barrera-Mora JM, Llamas-Carreras JM, Solano-Reina E (novembro 2012). «Obstructive sleep apnea syndrome (OSAS). Review of the literature». Medicina Oral, Patologia Oral y Cirurgia Bucal. 17 (6): e925–929. PMC 3505711
 . PMID 22549673. doi:10.4317/medoral.17706
. PMID 22549673. doi:10.4317/medoral.17706
- ↑ a b c d e f Qaseem, Amir; Holty, Jon-Erik C.; Owens, Douglas K.; Dallas, Paul; Starkey, Melissa; Shekelle, Paul; Clinical Guidelines Committee of the American College of, Physicians. (1 de outubro de 2013). «Management of Obstructive Sleep Apnea in Adults: A Clinical Practice Guideline From the American College of Physicians». Annals of Internal Medicine. 159 (7): 471–483. PMID 24061345. doi:10.7326/0003-4819-159-7-201310010-00704

- ↑ Bratton DJ, Gaisl T, Wons AM, Kohler M (dezembro 2015). «CPAP vs Mandibular Advancement Devices and Blood Pressure in Patients With Obstructive Sleep Apnea: A Systematic Review and Meta-analysis». JAMA. 314 (21): 2280–2293. PMID 26624827. doi:10.1001/jama.2015.16303

- ↑ Iftikhar IH, Kline CE, Youngstedt SD (February 2014). «Effects of exercise training on sleep apnea: a meta-analysis». Lung. 192 (1): 175–184. PMC 4216726
 . PMID 24077936. doi:10.1007/s00408-013-9511-3 Verifique data em:
. PMID 24077936. doi:10.1007/s00408-013-9511-3 Verifique data em: |data=(ajuda) - ↑ Browaldh N, Nerfeldt P, Lysdahl M, Bring J, Friberg D (setembro 2013). «SKUP3 randomised controlled trial: polysomnographic results after uvulopalatopharyngoplasty in selected patients with obstructive sleep apnoea». Thorax. 68 (9): 846–853. PMID 23644225. doi:10.1136/thoraxjnl-2012-202610

- ↑ a b Stuck, Boris A.; Ravesloot, Madeline J. L.; Eschenhagen, Till; de Vet, H. C. W.; Sommer, J. Ulrich (1 de outubro de 2018). «Uvulopalatopharyngoplasty with or without tonsillectomy in the treatment of adult obstructive sleep apnea – A systematic review». Sleep Medicine. 50: 152–165. PMID 30056286. doi:10.1016/j.sleep.2018.05.004 Erro de citação: Código
<ref>inválido; o nome "pmid30056286" é definido mais de uma vez com conteúdos diferentes - ↑ a b Giles TL, Lasserson TJ, Smith BH, White J, Wright J, Cates CJ (julho 2006). Giles T, ed. «Continuous positive airways pressure for obstructive sleep apnoea in adults». The Cochrane Database of Systematic Reviews (3): CD001106. PMID 16855960. doi:10.1002/14651858.CD001106.pub3
- ↑ a b c d e Askland, Kathleen; Wright, Lauren; Wozniak, Dariusz R; Emmanuel, Talia; Caston, Jessica; Smith, Ian (7 de abril de 2020). «Educational, supportive and behavioural interventions to improve usage of continuous positive airway pressure machines in adults with obstructive sleep apnoea». Cochrane Database of Systematic Reviews. 2020 (4): CD007736. PMC 7137251
 . PMID 32255210. doi:10.1002/14651858.CD007736.pub3
. PMID 32255210. doi:10.1002/14651858.CD007736.pub3
- ↑ Riaz M, Certal V, Nigam G, Abdullatif J, Zaghi S, Kushida CA, Camacho M (2015). «Nasal Expiratory Positive Airway Pressure Devices (Provent) for OSA: A Systematic Review and Meta-Analysis». Sleep Disorders. 2015: 734798. PMC 4699057
 . PMID 26798519. doi:10.1155/2015/734798
. PMID 26798519. doi:10.1155/2015/734798
- ↑ Whitelaw, William A.; Brant, Rollin F.; Flemons, W. Ward (15 de janeiro de 2005). «Clinical Usefulness of Home Oximetry Compared with Polysomnography for Assessment of Sleep Apnea». American Journal of Respiratory and Critical Care Medicine. 171 (2): 188–193. PMID 15486338. doi:10.1164/rccm.200310-1360OC Review in: Caples SM (2005). «The accuracy of physicians in predicting successful treatment response in suspected obstructive sleep apnea did not differ between home monitoring and polysomnography». ACP Journal Club. 143 (1): 21. PMID 15989309. doi:10.7326/ACPJC-2005-143-1-021
- ↑ Littner M, Hirshkowitz M, Davila D, Anderson WM, Kushida CA, Woodson BT, et al. (março 2002). «Practice parameters for the use of auto-titrating continuous positive airway pressure devices for titrating pressures and treating adult patients with obstructive sleep apnea syndrome. An American Academy of Sleep Medicine report». Sleep. 25 (2): 143–147. PMID 11902424. doi:10.1093/sleep/25.2.143
- ↑ McNicholas WT, Bonsignore MR, Lévy P, Ryan S (outubro 2016). «Mild obstructive sleep apnoea: clinical relevance and approaches to management». The Lancet. Respiratory Medicine. 4 (10): 826–834. PMID 27245915. doi:10.1016/S2213-2600(16)30146-1
- ↑ Neill AM, Angus SM, Sajkov D, McEvoy RD (janeiro 1997). «Effects of sleep posture on upper airway stability in patients with obstructive sleep apnea». American Journal of Respiratory and Critical Care Medicine. 155 (1): 199–204. PMID 9001312. doi:10.1164/ajrccm.155.1.9001312
- ↑ Nakano H, Ikeda T, Hayashi M, Ohshima E, Onizuka A (março 2003). «Effects of body position on snoring in apneic and nonapneic snorers». Sleep. 26 (2): 169–172. PMID 12683476. doi:10.1093/sleep/26.2.169

- ↑ Loord H, Hultcrantz E (agosto 2007). «Positioner--a method for preventing sleep apnea». Acta Oto-Laryngologica. 127 (8): 861–868. PMID 17762999. doi:10.1080/00016480601089390
- ↑ Szollosi I, Roebuck T, Thompson B, Naughton MT (agosto 2006). «Lateral sleeping position reduces severity of central sleep apnea / Cheyne-Stokes respiration». Sleep. 29 (8): 1045–1051. PMID 16944673. doi:10.1093/sleep/29.8.1045

- ↑ Caba, Justin (16 de abril de 2015). «How The Saxophone Could Solve Your Sleep Apnea». Medical Daily
- ↑ Ward, Christopher P.; York, Kaki M.; McCoy, John G. (15 de junho de 2012). «Risk of Obstructive Sleep Apnea Lower in Double Reed Wind Musicians». Journal of Clinical Sleep Medicine. 08 (3): 251–255. PMC 3365082
 . PMID 22701381. doi:10.5664/jcsm.1906
. PMID 22701381. doi:10.5664/jcsm.1906
- ↑ Gaisl, Thomas; Haile, Sarah R.; Thiel, Sira; Osswald, Martin; Kohler, Malcolm (agosto de 2019). «Efficacy of pharmacotherapy for OSA in adults: A systematic review and network meta-analysis». Sleep Medicine Reviews. 46: 74–86. PMID 31075665. doi:10.1016/j.smrv.2019.04.009
- ↑ Gottlieb, Daniel J.; Punjabi, Naresh M. (14 de abril de 2020). «Diagnosis and Management of Obstructive Sleep Apnea: A Review». JAMA. 323 (14): 1389–1400. PMID 32286648. doi:10.1001/jama.2020.3514
- ↑ Veasey, Sigrid C. (1 de fevereiro de 2003). «Serotonin Agonists and Antagonists in Obstructive Sleep Apnea». American Journal of Respiratory Medicine. 2 (1): 21–29. PMID 14720019. doi:10.1007/BF03256636
- ↑ Babson, Kimberly A.; Sottile, James; Morabito, Danielle (27 de março de 2017). «Cannabis, Cannabinoids, and Sleep: a Review of the Literature». Current Psychiatry Reports. 19 (4): 23. PMID 28349316. doi:10.1007/s11920-017-0775-9
- ↑ Carley, David W.; Prasad, Bharati; Reid, Kathryn J.; Malkani, Roneil; Attarian, Hryar; Abbott, Sabra M.; Vern, Boris; Xie, Hui; Yuan, Chengbo; Zee, Phyllis C. (1 de janeiro de 2018). «Pharmacotherapy of Apnea by Cannabimimetic Enhancement, the PACE Clinical Trial: Effects of Dronabinol in Obstructive Sleep Apnea». Sleep. 41 (1). PMC 5806568
 . PMID 29121334. doi:10.1093/sleep/zsx184
. PMID 29121334. doi:10.1093/sleep/zsx184
- ↑ a b Ramar, Kannan; Rosen, Ilene M.; Kirsch, Douglas B.; Chervin, Ronald D.; Carden, Kelly A.; Aurora, R. Nisha; Kristo, David A.; Malhotra, Raman K.; Martin, Jennifer L.; Olson, Eric J.; Rosen, Carol L.; Rowley, James A. (15 de abril de 2018). «Medical Cannabis and the Treatment of Obstructive Sleep Apnea: An American Academy of Sleep Medicine Position Statement». Journal of Clinical Sleep Medicine. 14 (4): 679–681. PMC 5886446
 . PMID 29609727. doi:10.5664/jcsm.7070
. PMID 29609727. doi:10.5664/jcsm.7070
- ↑ Kolla, Bhanu Prakash; Mansukhani, Meghna P.; Olson, Eric J.; St. Louis, Erik K.; Silber, Michael H.; Morgenthaler, Timothy I. (junho de 2018). «Medical Cannabis for Obstructive Sleep Apnea: Premature and Potentially Harmful». Mayo Clinic Proceedings. 93 (6): 689–692. PMID 29866280. doi:10.1016/j.mayocp.2018.04.011
- ↑ Ramar, Kannan; Kirsch, Douglas B.; Carden, Kelly A.; Rosen, Ilene M.; Malhotra, Raman K. (15 de outubro de 2018). «Medical Cannabis, Synthetic Marijuana Extracts, and Obstructive Sleep Apnea». Journal of Clinical Sleep Medicine. 14 (10): 1815–1816. PMC 6175803
 . PMID 30353829. doi:10.5664/jcsm.7412
. PMID 30353829. doi:10.5664/jcsm.7412
- ↑ Malhotra, Atul; Grunstein, Ronald R.; Fietze, Ingo; Weaver, Terri E.; Redline, Susan; Azarbarzin, Ali; Sands, Scott A.; Schwab, Richard J.; Dunn, Julia P.; Chakladar, Sujatro; Bunck, Mathijs C.; Bednarik, Josef (21 de junho de 2024). «Tirzepatide for the Treatment of Obstructive Sleep Apnea and Obesity». New England Journal of Medicine (em inglês). 391 (13): 1193–1205. ISSN 0028-4793. PMC 11598664
 . PMID 38912654. doi:10.1056/NEJMoa2404881
. PMID 38912654. doi:10.1056/NEJMoa2404881
- ↑ «Obstructive Sleep Apnea (OSA) Medication: CNS stimulants, Dopamine/Norepinephrine Reuptake Inhibitors». emedicine.medscape.com (em inglês). Consultado em 15 de agosto de 2024
- ↑ Greenblatt, Karl; Adams, Ninos (2024), «Modafinil», Treasure Island (FL): StatPearls Publishing, StatPearls, PMID 30285371, consultado em 15 de agosto de 2024
- ↑ «Sunosi: Side effects, alternatives, uses, dosage, and more». www.medicalnewstoday.com (em inglês). 23 de setembro de 2020. Consultado em 15 de agosto de 2024
- ↑ Blum, Dani (20 de dezembro de 2024). «F.D.A. Approves Weight Loss Drug to Treat Obstructive Sleep Apnea». The New York Times
- ↑ a b c Deenadayal, DS; Bommakanti, V (4 de janeiro de 2022). Management of Snoring and Obstructive Sleep Apnea: A Practical Guide (em inglês). [S.l.]: Springer Nature. pp. 1, 4, 14, 29, 34, 44, 50, 51, 55, 56, 64, 98. ISBN 978-981-16-6620-9
- ↑ Rose, E (2004). «Identifying the Ideal Oral Appliance Candidate». Journal of Orofacial Orthopedics. 65: 6
- ↑ Chan, A; Lee, R; Cistulli, PA (Aug 2007). «Oral Appliances for Obstructive Sleep Apnea». Chest. 132 (2): 693–9. PMID 17699143. doi:10.1378/chest.06-2038 Verifique data em:
|data=(ajuda) - ↑ Lazard DS, Blumen M, Levy P, Chauvin P, Fragny D, Buchet I, Chabolle F. The tongue-retaining device: efficacy and side effects in obstructive sleep apnea syndrome. Journal of Clinical Sleep Medicine. 2009 Oct 15;5(5):431-8.
- ↑ Cartwright, Rosalind; Stefoski, Dusan; Caldarelli, David; Kravitz, Howard; Knight, Sara; Lloyd, Stephen; Samelson, Charles (1988). «Toward a treatment logic for sleep apnea: The place of the tongue retaining device». Behaviour Research and Therapy. 26 (2): 121–126. PMID 3365202. doi:10.1016/0005-7967(88)90111-8
- ↑ Lazard, Diane S.; Blumen, Marc; Levy, Pierre; Chauvin, Pierre; Fragny, Dorothee; Buchet, Isabelle; Chabolle, Frederic (15 de outubro de 2009). «The Tongue-Retaining Device: Efficacy and Side Effects in Obstructive Sleep Apnea Syndrome». Journal of Clinical Sleep Medicine. 5 (5): 431–438. PMC 2762714
 . PMID 19961027. doi:10.5664/jcsm.27598
. PMID 19961027. doi:10.5664/jcsm.27598
- ↑ Carvalho, Fernando R; Lentini-Oliveira, Débora A; Prado, Lucila BF; Prado, Gilmar F; Carvalho, Luciane BC (4 de outubro de 2016). «Oral appliances and functional orthopaedic appliances for obstructive sleep apnoea in children». Cochrane Database of Systematic Reviews. 10 (11): CD005520. PMC 6458031
 . PMID 27701747. doi:10.1002/14651858.CD005520.pub3
. PMID 27701747. doi:10.1002/14651858.CD005520.pub3
- ↑ Li, Qiming; Tang, Hongyi; Liu, Xueye; Luo, Qing; Jiang, Zhe; Martin, Domingo; Guo, Jing (1 de maio de 2020). «Comparison of dimensions and volume of upper airway before and after mini-implant assisted rapid maxillary expansion». The Angle Orthodontist. 90 (3): 432–441. PMC 8032299
 . PMID 32045299. doi:10.2319/080919-522.1
. PMID 32045299. doi:10.2319/080919-522.1
- ↑ Abdullatif, Jose; Certal, Victor; Zaghi, Soroush; Song, Sungjin A.; Chang, Edward T.; Gillespie, M. Boyd; Camacho, Macario (1 de maio de 2016). «Maxillary expansion and maxillomandibular expansion for adult OSA: A systematic review and meta-analysis». Journal of Cranio-Maxillofacial Surgery. 44 (5): 574–578. PMID 26948172. doi:10.1016/j.jcms.2016.02.001
- ↑ Browaldh, Nanna; Nerfeldt, Pia; Lysdahl, Michael; Bring, Johan; Friberg, Danielle (1 de setembro de 2013). «SKUP3 randomised controlled trial: polysomnographic results after uvulopalatopharyngoplasty in selected patients with obstructive sleep apnoea». Thorax. 68 (9): 846–853. PMID 23644225. doi:10.1136/thoraxjnl-2012-202610
- ↑ a b Tschopp, Samuel; Tschopp, Kurt (2019). «Tonsil size and outcome of uvulopalatopharyngoplasty with tonsillectomy in obstructive sleep apnea». The Laryngoscope (em inglês). 129 (12): E449–E454. PMID 30848478. doi:10.1002/lary.27899
- ↑ «Sleep apnea». University of Maryland Medical Center. Cópia arquivada em 30 de abril de 2008
- ↑ Shah NA, Botros NA, Yaggi HK, Mohsenin V (20 de maio de 2007). «Sleep Apnea Increases Risk of Heart Attack or Death by 30%» (Nota de imprensa). New Haven, Connecticut: American Thoracic Society. Cópia arquivada em 24 de maio de 2009
- ↑ Sun, Yi; Yuan, Hai; Zhao, Miao-Qing; Wang, Yan; Xia, Ming; Li, Yan-Zhong (abril 2014). «Cardiac structural and functional changes in old elderly patients with obstructive sleep apnoea–hypopnoea syndrome». Journal of International Medical Research. 42 (2): 395–404. PMID 24445697. doi:10.1177/0300060513502890
- ↑ Silverberg DS, Iaina A, Oksenberg A (janeiro 2002). «Treating obstructive sleep apnea improves essential hypertension and quality of life». American Family Physician. 65 (2): 229–236. PMID 11820487
- ↑ Grigg-Damberger, Madeleine (February 2006). «Why a Polysomnogram Should Become Part of the Diagnostic Evaluation of Stroke and Transient Ischemic Attack». Journal of Clinical Neurophysiology. 23 (1): 21–38. PMID 16514349. doi:10.1097/01.wnp.0000201077.44102.80 Verifique data em:
|data=(ajuda) - ↑ Gagnon K, Baril AA, Gagnon JF, Fortin M, Décary A, Lafond C, et al. (outubro 2014). «Cognitive impairment in obstructive sleep apnea». Pathologie-Biologie. 62 (5): 233–240. PMID 25070768. doi:10.1016/j.patbio.2014.05.015
- ↑ Lal C, Strange C, Bachman D (junho–falhou de undefined). «Neurocognitive impairment in obstructive sleep apnea». Chest. 141 (6): 1601–1610. PMID 22670023. doi:10.1378/chest.11-2214 Verifique data em:
|data=(ajuda) - ↑ a b Punjabi NM (February 2008). «The epidemiology of adult obstructive sleep apnea». Proceedings of the American Thoracic Society. 5 (2): 136–43. PMC 2645248
 . PMID 18250205. doi:10.1513/pats.200709-155MG Verifique data em:
. PMID 18250205. doi:10.1513/pats.200709-155MG Verifique data em: |data=(ajuda) - ↑ a b c Senaratna CV, Perret JL, Lodge CJ, Lowe AJ, Campbell BE, Matheson MC, et al. (agosto 2017). «Prevalence of obstructive sleep apnea in the general population: A systematic review». Sleep Medicine Reviews. 34: 70–81. PMID 27568340. doi:10.1016/j.smrv.2016.07.002
- ↑ Olaithe M, Nanthakumar S, Eastwood PR, Bucks RS (2015). «Cognitive and Mood Dysfunction in Adult Obstructive Sleep Apnea (OSA): Implications for Psychological Research and Practice». Translational Issues in Psychological Science. 1 (1): 67–78. doi:10.1037/tps0000021
- ↑ Shamsuzzaman AS, Gersh BJ, Somers VK (outubro 2003). «Obstructive sleep apnea: implications for cardiac and vascular disease». JAMA. 290 (14): 1906–14. PMID 14532320. doi:10.1001/jama.290.14.1906
- ↑ Erro de citação: Etiqueta
<ref>inválida; não foi fornecido texto para as "refs" nomeadasAAO2013 - ↑ Kezirian EJ, Boudewyns A, Eisele DW, Schwartz AR, Smith PL, Van de Heyning PH, De Backer WA (outubro 2010). «Electrical stimulation of the hypoglossal nerve in the treatment of obstructive sleep apnea». Sleep Medicine Reviews. 14 (5): 299–305. PMID 20116305. doi:10.1016/j.smrv.2009.10.009
- ↑ «ImThera aura6000 System for Sleep Apnea Gets a Go in Europe». Medgadget. 15 de março de 2012. Cópia arquivada em 20 de janeiro de 2022
|arquivourl=requer|url=(ajuda) Parâmetro desconhecido|doi-status=ignorado (ajuda); - ↑ Puhan, Milo A.; Suarez, Alex; Cascio, Christian Lo; Zahn, Alfred; Heitz, Markus; Braendli, Otto (2 de fevereiro de 2006). «Didgeridoo playing as alternative treatment for obstructive sleep apnoea syndrome: randomised controlled trial». BMJ. 332 (7536): 266–270. PMC 1360393
 . PMID 16377643. doi:10.1136/bmj.38705.470590.55
. PMID 16377643. doi:10.1136/bmj.38705.470590.55
- ↑ Guimarães, Kátia C.; Drager, Luciano F.; Genta, Pedro R.; Marcondes, Bianca F.; Lorenzi-Filho, Geraldo (15 de maio de 2009). «Effects of Oropharyngeal Exercises on Patients with Moderate Obstructive Sleep Apnea Syndrome». American Journal of Respiratory and Critical Care Medicine. 179 (10): 962–966. PMID 19234106. doi:10.1164/rccm.200806-981OC