Tripanotiona
Tripanotiona
| |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
.svg.png) | |||||||||||||||
.svg.png) | |||||||||||||||
 | |||||||||||||||
| Nomes | |||||||||||||||
| Outros nomes | N1,N8-bis(glutathionyl)spermidine | ||||||||||||||
| |||||||||||||||
| |||||||||||||||
| Página de dados suplementares | |||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||
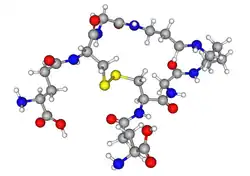
Tripanotiona (Mr = 721.86 g/mol) é uma forma não usual de glutationa contendo duas moléculas de glutationa conectadas por um espermidina (poliamina). É encontrada em protozoários parasitas como nas espécies dos gêneros Leishmania e Trypanosoma.[1] Estes parasitas são os agentes etiológicos das leishmanioses, doença do sono e doença de Chagas. A tripanotiona foi descoberta por Alan Fairlamb. A sua estrutura foi comprovada por síntese química,[2] e é exclusiva entre os Kinetoplastida, não sendo encontrada em outros protozoários.[3] Uma vez que este tiol está ausente nos seres humanos e é essencial para a sobrevivência dos parasitas, as enzimas que sintetizam e utilizam esta molécula são alvos para o desenvolvimento de novos medicamentos para tratar essas doenças.[4]
.svg.png)
.svg.png)
Os enzimas dependentes da Tripanotiona são redutases, peroxidases, glioxalases e transferases. A Tripanotiona-dissulfureto redutase (TryR) foi a primeira enzima dependente de Tripanotiona a ser descoberta (EC 1.8.1.12). É uma flavoenzima dependente do NADPH que reduz o dissulfureto de Tripanotiona. A TryR é essencial para a sobrevivência destes parasitas tanto in vitro como no hospedeiro humano.[5][6]
Uma importante função da Tripanotiona é a defesa contra o estresse oxidativo.[7] Aqui, as enzimas dependentes da Tripanotiona como a triparredoxina peroxidase (TryP) reduzem peróxidos usando eletrões doados diretamente da Tripanotiona ou através do intermediário redox triparredoxina (TryX). O metabolismo do peróxido de hidrogénio dependente de Tripanotiona é especialmente importante nestes organismos porque carecem de catalase. Como os tripanossomatídeos também carecem de um equivalente da tiorredoxina redutase, a Tripanotiona redutase é a única via que têm para que os eletrões possam passar do NADPH para estas enzimas antioxidantes.
Referências
- ↑ Fairlamb AH, Cerami A (1992). «Metabolism and functions of trypanothione in the Kinetoplastida». Annu. Rev. Microbiol. 46: 695–729. PMID 1444271. doi:10.1146/annurev.mi.46.100192.003403
- ↑ PMID 3883489 (PubMed)
- ↑ Ariyanayagam MR, Fairlamb AH (setembro de 1999). «Entamoeba histolytica lacks trypanothione metabolism». Mol. Biochem. Parasitol. 103 (1): 61–9. PMID 10514081. doi:10.1016/S0166-6851(99)00118-8
- ↑ Schmidt A, Krauth-Siegel RL (novembro de 2002). «Enzymes of the trypanothione metabolism as targets for antitrypanosomal drug development». Curr Top Med Chem. 2 (11): 1239–59. PMID 12171583. doi:10.2174/1568026023393048. Consultado em 27 de maio de 2019. Arquivado do original em 21 de julho de 2012
- ↑ Tovar J, Wilkinson S, Mottram JC, Fairlamb AH (julho de 1998). «Evidence that trypanothione reductase is an essential enzyme in Leishmania by targeted replacement of the tryA gene locus». Mol. Microbiol. 29 (2): 653–60. PMID 9720880. doi:10.1046/j.1365-2958.1998.00968.x
- ↑ Krieger S, Schwarz W, Ariyanayagam MR, Fairlamb AH, Krauth-Siegel RL, Clayton C (fevereiro de 2000). «Trypanosomes lacking trypanothione reductase are avirulent and show increased sensitivity to oxidative stress». Mol. Microbiol. 35 (3): 542–52. PMID 10672177. doi:10.1046/j.1365-2958.2000.01721.x
- ↑ Krauth-Siegel RL, Meiering SK, Schmidt H (abril de 2003). «The parasite-specific trypanothione metabolism of trypanosoma and leishmania». Biol. Chem. 384 (4): 539–49. PMID 12751784. doi:10.1515/BC.2003.062