Tiorredoxina redutase
As tiorredoxina redutases (TR, TrxR, ThxR, TXNRD) (EC 1.8.1.9) são enzimas que reduzem a tiorredoxina (Trx).[1] Identificaram-se duas classes de tiorredoxina redutases: uma classe em bactérias e alguns eucariotas, e outra em animais. Em bactérias, as TrxR também catalisam a redução das proteínas similares à glutarredoxina chamadas NrdH.[2][3][4] Ambas as classes são flavoproteínas que funcionam como homodímeros. Cada monómero contém um grupo prostético FAD, um domínio de ligação ao NADPH, e um sítio ativo que contém uma ligação dissulfureto com atividade redox.[5]
Função celular
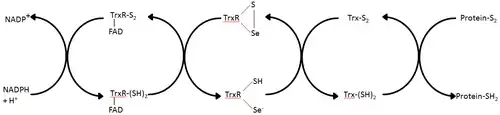
As tiorredoxina redutases (TrxR) são enzimas que catalisam a redução da tiorredoxina (Trx)[1] e, portanto, são um componente central do sistema da tiorredoxina. Juntamente com a tiorredoxina (Trx) e o NADPH, a descrição mais geral deste sistema é a de um sistema que reduz as ligações dissulfureto nas células. Eletrões são tomados do NADPH por meio da TrxR e transferidos para o sítio ativo da Trx, a qual reduz dissulfuretos em proteínas ou outros substratos.[6] O sistema Trx existe em todas as células vivas e tem uma história evolutiva ligada ao ADN como material genético, defesa contra danos oxidativos devido ao metabolismo do oxigénio, e sinalização redox usando moléculas como o peróxido de hidrogénio e o óxido nítrico.[7][8]
Diversidade
Duas classes de tiorredoxina redutases evoluíram independentemente:
Um tipo de alto peso molecular (MW ≈ 55.000) que contém um resíduo de selenocisteína no seu sítio ativo, identificado em eucariotas superiores, incluindo humanos. Esta TrxR está relacionada com a glutationa redutase, tripanotiona redutase, mercúrio(II) redutase e lipoamida desidrogenase.[5]
Um tipo de baixo peso molecular (MW ≈ 35.000) identificado em arqueas, bacterias e alguns eucariotas.[5]
Estas duas classes de TrxR têm apenas uma identidade de sequência de ≈ 20% na secção de sequência primária onde podem ser alinhadas confiavelmente.[5] A reação líquida de ambas as classes de TrxR é idêntica, mas o mecanismo de ação de cada uma é distinto.[9]
Os humanos expressam três isozimas tiorredoxina redutases, que são: tiorredoxina redutase 1 (TrxR1, citosólica), tiorredoxina redutase 2 (TrxR2, mitocondrial), tiorredoxina redutase 3 (TrxR3, específica do testículo).[10] Cada enzima é codificada por um gene separado, cada um num cromossoma distinto.
Estrutura
E. coli
Em Escherichia coli, a tiorredoxina redutase (ThxR) possui dois domínios de ligação, um para o FAD e outro para o NADPH. A conexão entre estes dois domínios é uma folha β de duas fitas antiparalelas.[11] Cada domínio individualmente é muito semelhante a domínios análogos da glutatião redutase e lipoamida desidrogenase, mas a orientação relativa destes domínios na ThxR está rodada em 66 graus.[11] Isto é significativo no mecanismo de ação da enzima, que é descrito mais abaixo. A ThxR homodimeriza-se com a interface entre os dois monómeros formada por três hélices α e dois loops.[11] Cada monómero pode ligar-se separadamente a uma molécula de tiorredoxina.
-
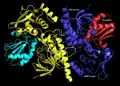 Estrutura da ThxR dímera de E. coli ligada à tiorredoxina.
Estrutura da ThxR dímera de E. coli ligada à tiorredoxina. -
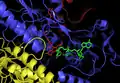 Estrutura da ThxR de E. coli com os grupos prostéticos FAD e NADPH rotulados.
Estrutura da ThxR de E. coli com os grupos prostéticos FAD e NADPH rotulados.
Mamíferos
A estrutura da tiorredoxina redutase de mamíferos é similar à de E. coli. Contém um domínio de ligação ao FAD e ao NADPH e uma interface entre duas subunidades monoméricas. Na tiorredoxina redutase de mamíferos existe uma inserção no domínio de ligação ao FAD entre duas hélices alpha que formam um pequeno par de fitas beta.[12] O dissulfureto ativo da enzima está localizado numa destas hélices e, portanto, a ligação dissulfureto ativa está localizada no domínio FAD e não no domínio NADPH, como em E. coli e noutros procariotas.[12]
-
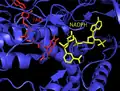 Estrutura dos grupos prostéticos FAD e NADPH da ThxR humana.
Estrutura dos grupos prostéticos FAD e NADPH da ThxR humana.
Mecanismo
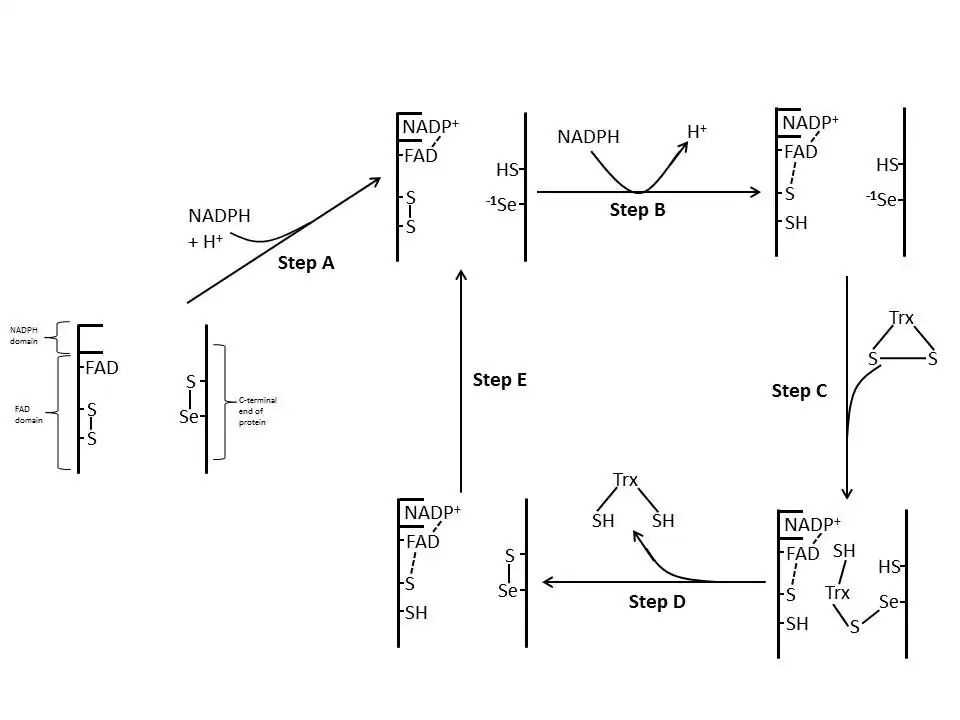
E. coli
Em E. coli, a orientação espacial da ThxR dos domínios FAD e NADPH faz com que os anéis com atividade redox do FAD e NADPH não estejam em estreita proximidade.[1] Quando o domínio FAD de E. coli é rodado 66 graus e o domínio NADPH permanece fixo, os dois grupos prostéticos entram em contacto próximo, permitindo que os eletrões passem do NADPH para o FAD e, em seguida, para a ligação dissulfureto do sítio ativo.[1][15] Os resíduos do sítio ativo conservados em E. coli são -Cys-Ala-Thr-Cys-.[1]
Mamíferos
As TrxRs de mamíferos têm uma homologia de sequências muito maior com a glutatião redutase do que E. coli.[1] Os resíduos de Cys do sítio ativo no domínio FAD e do domínio NADPH ligado estão em estreita proximidade, pelo que não há necessidade de uma rotação de 66 graus para a transferência de eletrões, como a encontrada em E. coli. Uma característica adicional do mecanismo dos mamíferos é a presença de um resíduo de selenocisteína no extremo C-terminal da proteína, que é necessário para a atividade catalítica. Os resíduos conservados no sítio ativo de mamíferos são -Cys-Val-Asn-Val-Gly-Cys-.[1]
Métodos de deteção
A tiorredoxina redutase pode ser quantificada por vários métodos, como o ensaio DTNB que usa o reactivo de Ellman. A série de sondas fluorescentes TRFS baseadas em dissulfuretos demonstraram ser capazes de fazer uma deteção seletiva da TrxR.[16] [17][18][19] Mafireyi sintetizou a primeira sonda disseleneto que foi aplicada na deteção da TrxR.[20] [21] Outros métodos de deteção são técnicas imunológicas e o ensaio de selenocistina-tiorredoxina (ensaio SC-TR).
Importância clínica
Tratamento do cancro
Como a atividade desta enzima é essencial para o crescimento e sobrevivência celular, é um bom alvo para a terapia antitumoral. Além disso, a enzima é regulada em alta em vários tipos de cancro, incluindo o mesotelioma maligno.[22][23] Por exemplo, o motexafim gadolínio (MGd) é um novo agente quimioterapêutico que atua seletivamente em células tumorais, originando a morte celular e a apoptose por inibição da tiorredoxina redutase e da ribonucleótido redutase.
Cardiomiopatia
A cardiomiopatia dilatada é um diagnóstico comum em casos de insuficiência cardíaca congestiva. As tiorredoxina redutases são proteínas essenciais para regular o balanço redox celular e mitigar o dano causado pelas espécies reativas do oxigénio geradas pela fosforilação oxidativa nas mitocôndrias. A inativação da TrxR2 mitocondrial em ratos resulta no adelgaçamento das paredes ventriculares do coração e na morte neonatal.[10] Além disso, encontram-se duas mutações no gene TrxR2 em pacientes diagnosticados com cardiomiopatia dilatada, mas não numa população de controlo. Hipotetiza-se que o impacto patológico destas mutações é uma capacidade alterada para controlar os danos oxidativos em miócitos cardíacos.[24]
Antibióticos
Recentemente, algumas investigações mostraram que o baixo peso molecular da tiorredoxina redutase poderia ser um alvo para novos antibióticos (como o auranofina ou o Ebselen).[25] Isto é especialmente verdadeiro em Mycobacterium haemophilum e poderia ser usado contra bactérias resistentes a antibióticos.[26]
Referências
- ↑ a b c d e f g Mustacich D, Powis G (fevereiro de 2000). «Thioredoxin reductase». The Biochemical Journal. 346 Pt 1 (1): 1–8. PMC 1220815
 . PMID 10657232. doi:10.1042/0264-6021:3460001
. PMID 10657232. doi:10.1042/0264-6021:3460001
- ↑ Jordan A, Aslund F, Pontis E, Reichard P, Holmgren A (julho de 1997). «Characterization of Escherichia coli NrdH. A glutaredoxin-like protein with a thioredoxin-like activity profile». The Journal of Biological Chemistry. 272 (29): 18044–50. PMID 9218434. doi:10.1074/jbc.272.29.18044
- ↑ Phulera S, Mande SC (junho de 2013). «The crystal structure of Mycobacterium tuberculosis NrdH at 0.87 Å suggests a possible mode of its activity». Biochemistry. 52 (23): 4056–65. PMID 23675692. doi:10.1021/bi400191z
- ↑ Phulera S, Akif M, Sardesai AA, Mande SC (1 de janeiro de 2014). «Redox Proteins of Mycobacterium tuberculosis». Journal of the Indian Institute of Science (em inglês). 94 (1): 127–138. ISSN 0970-4140
- ↑ a b c d Hirt RP, Müller S, Embley TM, Coombs GH (julho de 2002). «The diversity and evolution of thioredoxin reductase: new perspectives». Trends in Parasitology. 18 (7): 302–8. PMID 12379950. doi:10.1016/S1471-4922(02)02293-6
- ↑ a b Holmgren A, Lu J (maio de 2010). «Thioredoxin and thioredoxin reductase: current research with special reference to human disease». Biochemical and Biophysical Research Communications. 396 (1): 120–4. PMID 20494123. doi:10.1016/j.bbrc.2010.03.083
- ↑ Meyer Y, Buchanan BB, Vignols F, Reichheld JP (2009). «Thioredoxins and glutaredoxins: unifying elements in redox biology». Annual Review of Genetics. 43: 335–67. PMID 19691428. doi:10.1146/annurev-genet-102108-134201
- ↑ Lillig CH, Holmgren A (janeiro de 2007). «Thioredoxin and related molecules--from biology to health and disease». Antioxidants & Redox Signaling. 9 (1): 25–47. PMID 17115886. doi:10.1089/ars.2007.9.25
- ↑ Arscott LD, Gromer S, Schirmer RH, Becker K, Williams CH (abril de 1997). «The mechanism of thioredoxin reductase from human placenta is similar to the mechanisms of lipoamide dehydrogenase and glutathione reductase and is distinct from the mechanism of thioredoxin reductase from Escherichia coli». Proceedings of the National Academy of Sciences of the United States of America. 94 (8): 3621–6. Bibcode:1997PNAS...94.3621A. PMC 20490
 . PMID 9108027. doi:10.1073/pnas.94.8.3621
. PMID 9108027. doi:10.1073/pnas.94.8.3621
- ↑ a b Conrad M, Jakupoglu C, Moreno SG, Lippl S, Banjac A, Schneider M, Beck H, Hatzopoulos AK, Just U, Sinowatz F, Schmahl W, Chien KR, Wurst W, Bornkamm GW, Brielmeier M (novembro de 2004). «Essential role for mitochondrial thioredoxin reductase in hematopoiesis, heart development, and heart function». Molecular and Cellular Biology. 24 (21): 9414–23. PMC 522221
 . PMID 15485910. doi:10.1128/MCB.24.21.9414-9423.2004
. PMID 15485910. doi:10.1128/MCB.24.21.9414-9423.2004
- ↑ a b c Williams CH (outubro de 1995). «Mechanism and structure of thioredoxin reductase from Escherichia coli». FASEB Journal. 9 (13): 1267–76. PMID 7557016. doi:10.1096/fasebj.9.13.7557016. hdl:2027.42/154540
- ↑ a b Sandalova T, Zhong L, Lindqvist Y, Holmgren A, Schneider G (agosto de 2001). «Three-dimensional structure of a mammalian thioredoxin reductase: implications for mechanism and evolution of a selenocysteine-dependent enzyme». Proceedings of the National Academy of Sciences of the United States of America. 98 (17): 9533–8. Bibcode:2001PNAS...98.9533S. PMC 55487
 . PMID 11481439. doi:10.1073/pnas.171178698
. PMID 11481439. doi:10.1073/pnas.171178698
- ↑ Zhong L, Arnér ES, Holmgren A (maio de 2000). «Structure and mechanism of mammalian thioredoxin reductase: the active site is a redox-active selenolthiol/selenenylsulfide formed from the conserved cysteine-selenocysteine sequence». Proceedings of the National Academy of Sciences of the United States of America. 97 (11): 5854–9. Bibcode:2000PNAS...97.5854Z. PMC 18523
 . PMID 10801974. doi:10.1073/pnas.100114897
. PMID 10801974. doi:10.1073/pnas.100114897
- ↑ Becker K, Herold-Mende C, Park JJ, Lowe G, Schirmer RH (agosto de 2001). «Human thioredoxin reductase is efficiently inhibited by (2,2':6',2' '-terpyridine)platinum(II) complexes. Possible implications for a novel antitumor strategy». Journal of Medicinal Chemistry. 44 (17): 2784–92. PMID 11495589. doi:10.1021/jm001014i
- ↑ Lennon BW, Williams CH (agosto de 1997). «Reductive half-reaction of thioredoxin reductase from Escherichia coli». Biochemistry. 36 (31): 9464–77. PMID 9235991. doi:10.1021/bi970307j
- ↑ Li X, Zhang B, Yan C, Li J, Wang S, Wei X, et al. (junho de 2019). «A fast and specific fluorescent probe for thioredoxin reductase that works via disulphide bond cleavage». Nature Communications. 10 (1). 2745 páginas. Bibcode:2019NatCo..10.2745L. PMC 6588570
 . PMID 31227705. doi:10.1038/s41467-019-10807-8
. PMID 31227705. doi:10.1038/s41467-019-10807-8
- ↑ Ma H, Zhang J, Zhang Z, Liu Y, Fang J (outubro de 2016). «A fast response and red emission probe for mammalian thioredoxin reductase». Chemical Communications. 52 (81): 12060–12063. PMID 27709154. doi:10.1039/C6CC04984B
- ↑ Zhao J, Qu Y, Gao H, Zhong M, Li X, Zhang F, et al. (novembro de 2020). «Loss of thioredoxin reductase function in a mouse stroke model disclosed by a two-photon fluorescent probe». Chemical Communications. 56 (90): 14075–14078. PMID 33107534. doi:10.1039/D0CC05900E
- ↑ Liu Y, Ma H, Zhang L, Cui Y, Liu X, Fang J (fevereiro de 2016). «A small molecule probe reveals declined mitochondrial thioredoxin reductase activity in a Parkinson's disease model». Chemical Communications. 52 (11): 2296–9. PMID 26725656. doi:10.1039/c5cc09998f
- ↑ Mafireyi TJ, Laws M, Bassett JW, Cassidy PB, Escobedo JO, Strongin RM (agosto de 2020). «A Diselenide Turn-On Fluorescent Probe for the Detection of Thioredoxin Reductase». Angewandte Chemie. 59 (35): 15147–15151. PMC 9438933
 . PMID 32449244. doi:10.1002/ange.202004094
. PMID 32449244. doi:10.1002/ange.202004094
- ↑ Mafireyi TJ, Escobedo JO, Strongin RM (29 de março de 2021). «Fluorogenic probes for thioredoxin reductase activity». Results in Chemistry (em inglês). 3. 100127 páginas. ISSN 2211-7156. doi:10.1016/j.rechem.2021.100127
- ↑ Nilsonne G, Sun X, Nyström C, Rundlöf AK, Potamitou Fernandes A, Björnstedt M, Dobra K (setembro de 2006). «Selenite induces apoptosis in sarcomatoid malignant mesothelioma cells through oxidative stress». Free Radical Biology & Medicine. 41 (6): 874–85. PMID 16934670. doi:10.1016/j.freeradbiomed.2006.04.031. hdl:10616/47514
- ↑ Kahlos K, Soini Y, Säily M, Koistinen P, Kakko S, Pääkkö P, Holmgren A, Kinnula VL (maio de 2001). «Up-regulation of thioredoxin and thioredoxin reductase in human malignant pleural mesothelioma». International Journal of Cancer. 95 (3): 198–204. PMID 11307155. doi:10.1002/1097-0215(20010520)95:3<198::AID-IJC1034>3.0.CO;2-F
- ↑ Sibbing D, Pfeufer A, Perisic T, Mannes AM, Fritz-Wolf K, Unwin S, Sinner MF, Gieger C, Gloeckner CJ, Wichmann HE, Kremmer E, Schäfer Z, Walch A, Hinterseer M, Näbauer M, Kääb S, Kastrati A, Schömig A, Meitinger T, Bornkamm GW, Conrad M, von Beckerath N (maio de 2011). «Mutations in the mitochondrial thioredoxin reductase gene TXNRD2 cause dilated cardiomyopathy». European Heart Journal. 32 (9): 1121–33. PMID 21247928. doi:10.1093/eurheartj/ehq507
- ↑ Marshall AC, Kidd SE, Lamont-Friedrich SJ, Arentz G, Hoffmann P, Coad BR, Bruning JB (março de 2019). «Aspergillus fumigatus Thioredoxin Reductase». Antimicrobial Agents and Chemotherapy. 63 (3). PMC 6395915
 . PMID 30642940. doi:10.1128/AAC.02281-18
. PMID 30642940. doi:10.1128/AAC.02281-18
- ↑ Harbut MB, Vilchèze C, Luo X, Hensler ME, Guo H, Yang B, et al. (abril de 2015). «Auranofin exerts broad-spectrum bactericidal activities by targeting thiol-redox homeostasis». Proceedings of the National Academy of Sciences of the United States of America. 112 (14): 4453–8. Bibcode:2015PNAS..112.4453H. PMC 4394260
 . PMID 25831516. doi:10.1073/pnas.1504022112
. PMID 25831516. doi:10.1073/pnas.1504022112