Translocase da membrana externa
| subunidade recetora de importação mitocondrial TOM20 específica de plantas | |
|---|---|
| Indicadores | |
| Pfam | PF06552 |
| InterPro | IPR010547 |
| TCDB | 3.A.8 |
| Família OPM | 303 |
| Proteína OPM | 3awr |
| família TOM7 | |
|---|---|
| Indicadores | |
| Pfam | PF08038 |
| InterPro | IPR012621 |
A translocase da membrana externa mitocondrial, ou TOM (translocase da membrana externa), é um complexo proteico que se encontra na membrana externa mitocondrial que tem como função translocar as proteínas citosólicas para o outro lado da membrana externa, passando para o espaço intermembranar. Opera em conjunto com a TIM. A maioria das proteínas que actuam na mitocôndria estão codificadas no ADN do núcleo celular, sendo que a membrana mitocondrial é impermeável a moléculas com mais de 5000 daltons (unidades de massa molecular), dado que é necessário um sistema de transporte específico para as mesmas..[1] Muitas das proteínas do complexo TOM, como a TOMM22, foram identificadas pela primeira vez no fungos Neurospora crassa e Saccharomyces cerevisiae.[2]
O complexo de translocase de proteínas mitocondrial completo é constituído por pelo menos 19 proteínas: várias chaperonas, quatro proteínas recetoras de importação da translocase da membrana externa (Tom), cinco proteínas do complexo do canal Tom, cinco proteínas da translocase da membrana interna (Tim) e três proteínas "motoras".
Proteínas destinadas à mitocôndria
Existem diversas vias na mitocôndria para a importação de proteínas destinadas a esta organela. A chaperona Hsp90 liga-se às proteínas a transportar no citosol e ajuda a entregá-las ao complexo TOM num processo ATP-dependente.[3] Muitas proteínas precursoras (as que se destinam à matriz) contêm uma sequência sinal (ou pré-sequência) na terminal amino que indica que se destinam à matriz mitocondrial.[4] A sequência sinal consiste geralmente em cerca de 10 a 80 resíduos de aminoácidos que adotam uma conformação de hélice alfa anfipática.[5] e têm um lado positivo e um lado hidrofóbico. Assim que o precursor atinge a matriz, a sequência sinal é clivada por uma peptidase.[6] Algumas proteínas destinadas a outros subcompartimentos da mitocôndria, como o espaço intermembranar ou a membrana interna mitocondrial, contêm sinais internos (não localizados na extremidade amino-terminal); estas sequências são muito diversas. As proteínas destinadas à membrana externa também contêm sinais internos, e nem todos foram identificados, incluindo as proteínas que possuem uma estrutura em barril beta (β-barril).[7] como Tom40. Algumas proteínas, destinadas à membrana externa mitocondrial, possuem uma cauda hidrofóbica domínio que ancora a proteína à membrana.[8]
Componentes do complexo
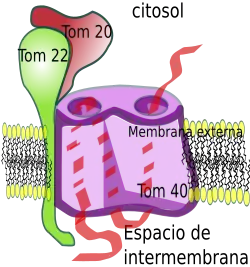
A translocase da membrana externa (TOM) forma um complexo constituído por Tom70, Tom22 e Tom20, juntamente com Tom40, Tom7, Tom6 e Tom5. O Tom20 e o Tom22 são recetores para a pré-proteína a transportar, responsáveis por reconhecer a sequência sinal nas proteínas destinadas às mitocôndrias.[9] O Tom70 é também um recetor para a pré-proteína a ser transportada e pode reconhecer algumas sequências sinalizadoras cliváveis em proteínas, mas é principalmente responsável pelo reconhecimento de pré-proteínas não cliváveis e atua como ponto de ligação para as chaperonas.[6][10] A proteína Tom22 está ancorada à membrana externa mitocondrial por um único segmento transmembranar e também desempenha um papel na estabilização do complexo TOM.[11] A Tom40 é o elemento central do complexo da translocase e forma um complexo com Tom22 com uma massa de aproximadamente 350kDa.[12] Forma o canal central por onde passa a proteína a transportar, com um diâmetro de aproximadamente 2,5 nm. [12] O Tom22 humano tem cerca de 15,5 kDa e está em complexo com o Tom20.[13] A extremidade amino-terminal do Tom22 estende-se na parte citosólica e está envolvida na ligação da pré-proteína a transportar. [13]
Proteínas humanas
TOMM22, TOMM40, TOM7, TOMM7
Referências
- ↑ Alberts, Bruce; Alexander Johnson, Julian Lewis, Martin Raff, Keith Roberts, Peter Walter (1994). Molecular Biology of the Cell. New York: Garland Publishing Inc. ISBN 0-8153-3218-1
- ↑ Seki N, Moczko M, Nagase T; et al. (1996). «A human homolog of the mitochondrial protein import receptor Mom19 can assemble with the yeast mitochondrial receptor complex». FEBS Lett. 375 (3): 307–10. PMID 7498524. doi:10.1016/0014-5793(95)01229-8
- ↑ Humphries AD, Streimann IC, Stojanovski D, Johnston AJ, Yano M, Hoogenraad NJ, Ryan MT (2005). «Dissection of the mitochondrial import and assembly pathway for human Tom40». J Biol Chem. 280 (12): 11535–43. PMID 15644312. doi:10.1074/jbc.M413816200
- ↑ Saitoh T, Igura M, Obita T, Ose T, Kojima R, Maenaka K, Endo T, Kohda D (2007). «Tom20 recognizes mitochondrial presequences through dynamic equilibrium among multiple bound states». EMBO J. 26 (22): 4777–87. PMC 2080804
 . PMID 17948058. doi:10.1038/sj.emboj.7601888
. PMID 17948058. doi:10.1038/sj.emboj.7601888
- ↑ Tokatlidis K, Vial S, Luciano P, Vergnolle M, Clémence S (2000). «Membrane protein import in yeast mitochondria». Biochem. Soc. Trans. 28 (4): 495–9. PMID 10961947. doi:10.1042/0300-5127:0280495
- ↑ a b Young JC, Hoogenraad NJ, Hartl FU (2003). «Molecular chaperones Hsp90 and Hsp70 deliver preproteins to the mitochondrial import receptor Tom70». Cell. 112 (1): 41–50. PMID 12526792. doi:10.1016/S0092-8674(02)01250-3
- ↑ Bolender N, Sickmann A, Wagner R, Meisinger C, Pfanner N (2008). «Multiple pathways for sorting mitochondrial precursor proteins». EMBO Rep. 9 (1): 42–9. PMC 2246611
 . PMID 18174896. doi:10.1038/sj.embor.7401126
. PMID 18174896. doi:10.1038/sj.embor.7401126
- ↑ Koehler CM, Merchant S, Schatz G (1999). «How membrane proteins travel across the mitochondrial intermembrane space». Trends Biochem. Sci. 24 (11): 428–32. PMID 10542408. doi:10.1016/S0968-0004(99)01462-0
- ↑ Ryan MT, Müller H, Pfanner N (1999). «Functional staging of ADP/ATP carrier translocation across the outer mitochondrial membrane». J. Biol. Chem. 274 (29): 20619–27. PMID 10400693. doi:10.1074/jbc.274.29.20619
- ↑ Asai T, Takahashi T, Esaki M, Nishikawa S, Ohtsuka K, Nakai M, Endo T (2004). «Reinvestigation of the requirement of cytosolic ATP for mitochondrial protein import». J. Biol. Chem. 279 (19): 19464–70. PMID 15001571. doi:10.1074/jbc.M401291200
- ↑ Endres M, Neupert W, Brunner M (1999). «Transport of the ADP/ATP carrier of mitochondria from the TOM complex to the TIM22.54 complex». EMBO J. 18 (12): 3214–21. PMC 1171402
 . PMID 10369662. doi:10.1093/emboj/18.12.3214
. PMID 10369662. doi:10.1093/emboj/18.12.3214
- ↑ a b Ahting U, Thieffry M, Engelhardt H, Hegerl R, Neupert W, Nussberger S (2001). «Tom40, the Pore-Forming Component of the Protein-Conducting Tom Channel in the Outer Membrane of Mitochondria». J. Cell Biol. 153 (6): 1151–60. PMC 2192023
 . PMID 11402060. doi:10.1083/jcb.153.6.1151
. PMID 11402060. doi:10.1083/jcb.153.6.1151
- ↑ a b Yano M, Hoogenraad N, Terada K, Mori M (2000). «Identification and Functional Analysis of Human Tom22 for Protein Import into Mitochondria». Mol Cell Biol. 20 (19): 7205–13. PMC 86274
 . PMID 10982837. doi:10.1128/MCB.20.19.7205-7213.2000
. PMID 10982837. doi:10.1128/MCB.20.19.7205-7213.2000