Tiopirílio
Tiopirílio
| |||||||||
|---|---|---|---|---|---|---|---|---|---|
 | |||||||||
| |||||||||
| |||||||||
| |||||||||
| Página de dados suplementares | |||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||
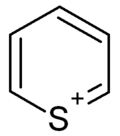
Tiopirílio é um cátion com a fórmula química C5H5S+. É um análogo ao cátion pirílio com o átomo de oxigênio substituído por um átomo de enxofre.
Sais de tiopirílio são menos reativos que os sais de pirílio análogos devido a menor eletronegatividade do átomo de enxofre.[1][2] Entre os 6 membros insaturados heterocíclicos calcogênicos, o tiopirílio é o mais aromático, devido ao enxofre ter a mesma eletronegatividade de Pauling que o carbono e apenas um pouco maior raio covalente.[1]
Os sais de tiopirílio podem ser sintetizados pela abstração de hidrogênio do tiopirano por um aceptor íon hidreto, tal como o perclorato de tritila.[3]
Os análogos tiopirílio de sais pirílio 2,4,6-trisubstituídos podem ser sintetizados pelo tratamento com sulfeto de sódio seguido por precipitação com ácido. Esta reação causa que o átomo de oxigênio no cátion pirílio seja substituído pelo enxofre.[2]
Referências
- ↑ a b Tadeusz Marek Krygowski, Michal Ksawery Cyranski, eds. (2009). Aromaticity in Heterocyclic Compounds. Volume 19 of Topics in Heterocyclic Chemistry. [S.l.]: Springer. pp. 219–220. ISBN 9783540683292
- ↑ a b K. Dimroth; K. H. Wolf (2012). Wilhelm Foerst, ed. Newer Methods of Preparative Organic Chemistry. 3. [S.l.]: Elsevier. p. 361. ISBN 9780323146104
- ↑ «Thiopyrans». Concise Encyclopedia Chemistry. Walter de Gruyter. 1994. p. 1101. ISBN 9783110854039