Tetrahidrocanabivarina
Tetrahidrocanabivarina
| |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||
 | |||||||||||
| Nomes | |||||||||||
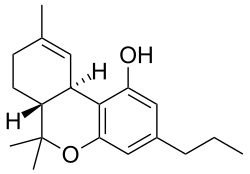
| Nome IUPAC | 6,6,9-Trimethyl-3-propyl-6a,7,8,10a-tetrahydro-6H-benzo[c]chromen-1-ol | ||||||||||
| Outros nomes | THCV | ||||||||||
| |||||||||||
| |||||||||||
| |||||||||||
| Página de dados suplementares | |||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||
Tetrahidrocanabivarina (THCV, THV, O-4394, GWP42004) é um homólogo do tetrahidrocanabinol (THC) que possui uma cadeia lateral propil (3 carbonos) em vez de pentil (5 carbonos), e por isso não é psicoativa em doses mais baixas. Foi demonstrado que apresenta atividade neuroprotetora, supressão do apetite, controle glicêmico e efeitos colaterais reduzidos em comparação ao THC, e é estudada como um tratamento em potencial para o controle da obesidade e diabetes.[1] Já em 1942, a THCV foi objeto de estudo do químico americano Roger Adams.[2]
Ocorrência natural
A THCV é predominante em algumas cepas de Cannabis da Ásia Central e do sul da África.[3][4]
Plantas com níveis elevados de canabinoides com cadeia lateral propil (incluindo a THCV) foram encontradas em populações de Cannabis sativa L. ssp. indica (= Cannabis indica Lam.) da China, Índia, Nepal, Tailândia, Afeganistão e Paquistão, bem como do sul e oeste da África. Foram relatados teores de THCV correspondentes a até 20% do total de canabinoides presentes.[5]
Química
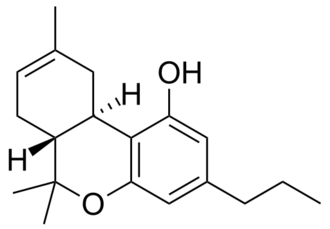
Assim como o THC, a THCV apresenta 7 possíveis isômeros de dupla ligação e 30 estereoisômeros (ver: Tetra-hidrocanabinol#Isomeria). O isômero alternativo Δ8-THCV é conhecido como um composto sintético identificado pelo código O-4395,[6] porém não há relatos de sua ocorrência natural em material vegetal da Cannabis.
Farmacologia
A THCV atua como antagonista do receptor canabinoide tipo 1 (CB1), podendo funcionar como agonista desse mesmo receptor e agonista parcial do receptor canabinóide tipo 2 [en] (CB2) quando administrada em doses mais elevadas.[8] O isômero Δ8-THCV também demonstrou atividade antagonista sobre o receptor CB1..[9] Ambos os estudos que descreveram as propriedades antagônicas da THCV foram conduzidos em camundongos. A THCV é um antagonista do THC nos receptores CB1 e diminui os efeitos psicoativos do THC.[10]
A THCV atua como agonista dos receptores GPR55 [en] e l-α-lisofosfatidilinositol [en] (LPI). Fora do sistema endocanabinoide, também ativa os receptores serotoninérgicos 5-HT1A, produzindo efeito antipsicótico com potencial para melhorar alguns dos sintomas cognitivos, negativos e positivos da esquizofrenia. Além disso, interage com diferentes canais da família dos receptores de potencial transitório (TRPs), incluindo o TRPV2, o que pode contribuir para seus efeitos analgésicos, anti-inflamatórios e anticancerígenos dos canabinoides e demais extratos de Cannabis. Ainda, a THCV apresenta propriedades antiepilépticas e anticonvulsivantes, indicando possível aplicação terapêutica no tratamento de estados de hiperexcitabilidade fisiopatológica, a exemplo da epilepsia refratária.[11]
A THCV também inibe a atividade da amida hidrolase de ácido graxo (FAAH) e da lipase de monoacilgli cerol [en] (MAGL), mesmo em concentrações micromolares. Por isso, é capaz de impedir a hidrólise dos endocanabinoides anandamida (AEA: C22H37NO2; 20:4, ω-6), bem como de outras N-aciletanolaminas e do 2-araquidonoilglicerol [en] (2-AG: C23H38O4; 20:4, ω-6), respectivamente. Por esse motivo, a THCV também atua como agonista indireto nos receptores canabinoides, promovendo o aumento da atividade do sistema endocanabinoide (ECS).[12][13]
Biossíntese
Ao contrário do THC, do canabidiol (CBD) e do canabicromeno (CBC), a THCV não se origina a partir do ácido canabigerólico (CBGA). Em vez de se combinar com o ácido olivetólico para criar CBGA, o pirofosfato de geranil se une ao ácido divarinólico, que tem dois átomos de carbono a menos, formando ácido canabigerovarínico [en] (CBGVA). Depois que o CBGVA é criado, o processo é similar ao da biossíntese de THC. Nesse ponto, a THCV é decomposta em ácido tetrahidrocanabivarina carboxílico (THCVA) pela THCV sintase (enzima responsável pela produção de tetrahidrocanabivarina). Em seguida, a THCVA pode ser descarboxilada por meio de calor ou exposição à luz ultravioleta, resultando na formação da THCV.[14]
Pesquisa médica
Redução do açúcar no sangue
A THCV é considerada um tratamento em potencial para a intolerância à glicose associada à obesidade, com farmacologia diferente dos agonistas/antagonistas inversos do CB1.[15] A GW Pharmaceuticals está estudando a tetrahidrocanabivarina de origem vegetal (código de desenvolvimento: GWP42004) para o tratamento do diabetes tipo 2, em combinação ou como alternativa à metformina.[16]
Controle do apetite
O THC é um agonista dos receptores CB1, de modo que estimula o apetite, efeito popularmente conhecido como "larica". Já a THCV, que atua como antagonista dos receptores CB1, demonstrou reduzir o apetite em um estudo com modelos murinos.[17]
Ver também
- Cannabis
- Canabinoide
- Canabivarina (CBV)
- Canabidivarina (CBDV)
- Cannabis medicinal
- Rimonabanto (antagonista sintético do CB1)
Referências
- ↑ Abioye A, Ayodele O, Marinkovic A, Patidar R, Akinwekomi A, Sanyaolu A (janeiro de 2020). «Δ9-Tetrahydrocannabivarin (THCV): a commentary on potential therapeutic benefit for the management of obesity and diabetes». Journal of Cannabis Research. 2 (1). 6 páginas. PMC 7819335
 . PMID 33526143. doi:10.1186/s42238-020-0016-7
. PMID 33526143. doi:10.1186/s42238-020-0016-7
- ↑ Adams R, Loewe S, Smith CM, McPhee WD (1942). «Tetrahydrocannabinol Homologs and Analogs with Marihuana Activity. XIII¹». Journal of the American Chemical Society. 64 (3): 694–697. doi:10.1021/ja01255a061 Verifique o valor de
|url-access=subscription(ajuda) - ↑ Baker PB, Gough TA, Taylor BJ (1980). «Illicitly imported Cannabis products: some physical and chemical features indicative of their origin». Bulletin on Narcotics. 32 (2): 31–40. PMID 6907024
- ↑ Hillig KW, Mahlberg PG (junho de 2004). «A chemotaxonomic analysis of cannabinoid variation in Cannabis (Cannabaceae)». American Journal of Botany. 91 (6): 966–75. PMID 21653452. doi:10.3732/ajb.91.6.966

- ↑ Lester, Black (22 de outubro de 2023). «Extremely rare pot discovered 50 years ago is finally available in California». www.sfgate.com (em inglês). Consultado em 23 de junho de 2025. Cópia arquivada em 21 de abril de 2024
- ↑ Brown NK, Harvey DJ (abril de 1988). «In vivo metabolism of the n-propyl homologues of delta-8- and delta-9-tetrahydrocannabinol in the mouse». Biomedical & Environmental Mass Spectrometry. 15 (7): 403–10. PMID 2839261. doi:10.1002/bms.1200150708
- ↑ PubChem. «Propyl-delta(8)-tetrahydrocannabinol». pubchem.ncbi.nlm.nih.gov (em inglês). Consultado em 23 de junho de 2025
- ↑ Pertwee RG (janeiro de 2008). «The diverse CB1 and CB2 receptor pharmacology of three plant cannabinoids: delta9-tetrahydrocannabinol, cannabidiol and delta9-tetrahydrocannabivarin». British Journal of Pharmacology. 153 (2): 199–215. PMC 2219532
 . PMID 17828291. doi:10.1038/sj.bjp.0707442
. PMID 17828291. doi:10.1038/sj.bjp.0707442
- ↑ Pertwee RG, Thomas A, Stevenson LA, Ross RA, Varvel SA, Lichtman AH, Martin BR, Razdan RK (março de 2007). «The psychoactive plant cannabinoid, Delta9-tetrahydrocannabinol, is antagonized by Delta8- and Delta9-tetrahydrocannabivarin in mice in vivo». British Journal of Pharmacology. 150 (5): 586–94. PMC 2189766
 . PMID 17245367. doi:10.1038/sj.bjp.0707124
. PMID 17245367. doi:10.1038/sj.bjp.0707124
- ↑ Thomas A, Stevenson LA, Wease KN, Price MR, Baillie G, Ross RA, Pertwee RG (dezembro de 2005). «Evidence that the plant cannabinoid Delta9-tetrahydrocannabivarin is a cannabinoid CB1 and CB2 receptor antagonist». British Journal of Pharmacology. 146 (7): 917–26. PMC 1751228
 . PMID 16205722. doi:10.1038/sj.bjp.0706414
. PMID 16205722. doi:10.1038/sj.bjp.0706414
- ↑ «Tetrahydrocannabivarin». PubChem (em inglês). U.S. National Library of Medicine. Consultado em 30 de junho de 2023
- ↑ McPartland JM, Duncan M, Di Marzo V, Pertwee RG (fevereiro de 2015). «Are cannabidiol and Δ(9) -tetrahydrocannabivarin negative modulators of the endocannabinoid system? A systematic review». British Journal of Pharmacology. 172 (3): 737–753. PMC 4301686
 . PMID 25257544. doi:10.1111/bph.12944
. PMID 25257544. doi:10.1111/bph.12944
- ↑ Jadoon KA (13 de setembro de 2013). «Efficacy and Safety of Cannabidiol and Tetrahydrocannabivarin on Glycemic and Lipid Parameters in Patients With Type 2 Diabetes: A Randomized, Double-Blind, Placebo-Controlled, Parallel Group Pilot Study». Diabetes Care. 39 (10)
- ↑ Walsh KB, McKinney AE, Holmes AE (29 de novembro de 2021). «Minor Cannabinoids: Biosynthesis, Molecular Pharmacology and Potential Therapeutic Uses». Frontiers in Pharmacology. 12. 777804 páginas. PMC 8669157
 . PMID 34916950. doi:10.3389/fphar.2021.777804
. PMID 34916950. doi:10.3389/fphar.2021.777804
- ↑ Wargent ET, Zaibi MS, Silvestri C, Hislop DC, Stocker CJ, Stott CG, Guy GW, Duncan M, Di Marzo V, Cawthorne MA (maio de 2013). «The cannabinoid Δ(9)-tetrahydrocannabivarin (THCV) ameliorates insulin sensitivity in two mouse models of obesity». Nutrition & Diabetes. 3 (5): e68. PMC 3671751
 . PMID 23712280. doi:10.1038/nutd.2013.9
. PMID 23712280. doi:10.1038/nutd.2013.9
- ↑ GW Pharmaceuticals plc (17 de março de 2014). «GW Pharmaceuticals Provides Update on Cannabinoid Pipeline». GlobeNewswire News Room (Nota de imprensa) (em inglês). Consultado em 7 de julho de 2022
- ↑ Riedel G, Fadda P, McKillop-Smith S, Pertwee RG, Platt B, Robinson L (2009). «Synthetic and plant-derived cannabinoid receptor antagonists show hypophagic properties in fasted and non-fasted mice». British Journal of Pharmacology. 156 (7): 1154–1166. PMC 2697695
 . PMID 19378378. doi:10.1111/j.1476-5381.2008.00107.x
. PMID 19378378. doi:10.1111/j.1476-5381.2008.00107.x