Termômetro de RNA
Um termômetro de RNA (ou termossensor de RNA) é uma molécula de RNA não codificante sensível à temperatura, que regula a expressão gênica.[1] Sua característica única é que não requer proteínas ou metabólitos para funcionar, respondendo apenas a mudanças de temperatura.[2] Frequentemente, termômetros de RNA regulam genes necessários durante respostas ao choque térmico ou ao choque frio [en], mas também estão implicados em outros papéis regulatórios, como em patogenicidade e inanição.[1]
De modo geral, os termômetros de RNA operam alterando sua estrutura secundária e estrutura terciária[3] em resposta a flutuações de temperatura. Essa transição estrutural pode expor ou ocultar regiões importantes do RNA, como o sítio de ligação ao ribossomo, afetando a taxa de tradução de um gene codificador de proteína próximo.
Termômetros de RNA, juntamente com riboswitches, são usados como exemplos em apoio à hipótese do mundo de RNA. Essa teoria propõe que o RNA foi, outrora, o único ácido nucleico presente nas células, sendo posteriormente substituído pelo atual sistema DNA → RNA → proteína.[4]
Exemplos de termômetros de RNA incluem o FourU [en],[5] o elemento cis-regulador Hsp90 [en],[6] o elemento ROSE [en],[7] o termômetro de RNA Lig [en],[8] e o termômetro Hsp17 [en].[9]
Descoberta
O primeiro elemento de RNA sensível à temperatura foi relatado em 1989.[10] Antes dessa pesquisa, mutações a montante do sítio de início de transcrição em um fago lambda (λ) [en] cIII mRNA foram encontradas afetando o nível de tradução da proteína cIII.[11] Essa proteína está envolvida na escolha entre um ciclo lítico ou lisogênico no fago λ, com altas concentrações de cIII promovendo a lisogenia.[11] Estudos adicionais dessa região de RNA a montante identificaram duas estruturas secundárias alternativas; estudos experimentais descobriram que as estruturas são intercambiáveis e dependem da concentração de íons de magnésio [en] e da temperatura.[10][12] Esse termômetro de RNA agora é considerado como incentivador da entrada em um ciclo lítico sob estresse térmico, permitindo que o bacteriófago se replique rapidamente e escape da célula hospedeira.[1]
O termo "termômetro de RNA" foi cunhado apenas em 1999,[13] quando foi aplicado ao elemento de RNA rpoH identificado em Escherichia coli.[14] Mais recentemente, buscas bioinformáticas foram empregadas para descobrir vários candidatos a termômetros de RNA.[15] No entanto, buscas baseadas em sequências tradicionais são ineficientes, pois a estrutura secundária do elemento é muito mais conservada do que a sequência de ácido nucleico.[15]
Reações biológicas e organismos são sensíveis à temperatura para o funcionamento celular. Termômetros de RNA são uma forma eficiente de responder à temperatura, pois permitem que as células monitorem e detectem mudanças para manter a célula viva e estável. Mecanismos induzidos por DNA, RNA ou proteínas evitam pequenas mudanças, pois detectam alterações externas.[16]
Bactérias utilizam termômetros de RNA para entrar e sobreviver em seus hospedeiros, fixando-se a eles e causando flutuações em sua temperatura. As bactérias podem responder rapidamente contra condições de choque térmico e frio, uma vez que os termômetros de RNA controlam a expressão gênica em nível traducional.[16]
O primeiro termômetro de RNA descoberto no cloroplasto de Chlamydomonas reinhardtii, encontrado na 5’-UTR do mRNA psaA, tem uma função distinta, especialmente por ser considerado ausente. Possui uma estrutura secundária do tipo grampo que protege a sequência Shine-Dalgarno em baixas temperaturas, mas, ao ocorrer uma mudança de temperatura, ela se desfaz, ativando a produção de proteínas.[2] A pesquisa sobre o termômetro de RNA de C. reinhardtii é uma porta de entrada para observar o cloroplasto de organismos fotossintéticos para a regulação gênica e como isso pode ser usado na agricultura no futuro, ajudando as plantas a se adaptarem a temperaturas externas.[2]
Distribuição
A maioria dos termômetros de RNA conhecidos está localizada na 5ª região não traduzida [en] (UTR) de RNAs mensageiros que codificam proteínas de choque térmico — embora tenha sido sugerido que esse fato pode ser devido, em parte, a viés de amostragem e às dificuldades inerentes de detectar sequências curtas e não conservadas de RNA em dados genômicos.[17][18]
Embora predominantemente encontrados em procariotos, um potencial termômetro de RNA foi identificado em mamíferos, incluindo humanos.[19] O candidato a termossensor, RNA de choque térmico-1 (HSR1), ativa o fator de transcrição de choque térmico 1 (HSF1) e induz proteínas protetoras quando a temperatura celular excede 37 °C (temperatura corporal [en]), prevenindo o superaquecimento das células.[19]
Os elementos ROSE, uma classe de termômetros de RNA bacterianos, regulam a ativação de genes que possuem pequenas proteínas de choque térmico. Eles derretem moderadamente conforme a temperatura do ambiente aumenta. Quando completamente derretidos a uma alta temperatura de cerca de 42 °C, liberam a sequência Shine-Dalgarno e o códon de início AUG. Termômetros de RNA também podem ser encontrados em alguns simbiontes ou patógenos de plantas, que utilizam esses termômetros para regular a expressão gênica das plantas.[3] Uma bactéria simbiótica bem estudada é da família Rhizobiaceae. Na maioria das espécies rizobiais, elementos ROSE (cis-atuantes) foram observados controlando genes de choque térmico.[3]
Estrutura
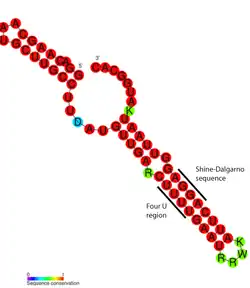
Os termômetros de RNA são estruturalmente simples e podem ser formados por sequências curtas de RNA; o menor possui apenas 44 nucleotídeos e é encontrado no mRNA de uma proteína de choque térmico, hsp17, em espécies de Synechocystis [en], PCC 6803 [en].[9] Geralmente, esses elementos de RNA variam de 60 a 110 nucleotídeos de comprimento[21] e tipicamente contêm um grampo com um pequeno número de pares de bases não correspondentes, o que reduz a estabilidade da estrutura, facilitando o desdobramento em resposta a um aumento de temperatura.[17]
A análise estrutural detalhada do termômetro de RNA ROSE revelou que as bases não correspondentes estão, na verdade, envolvidas em pareamentos não padrão que preservam a estrutura helicoidal do RNA (veja a figura). Os pareamentos incomuns consistem em pares G-G, U-U e UC-U. Como esses pares de bases não canônicos são relativamente instáveis, o aumento da temperatura causa o derretimento local da estrutura do RNA nessa região, expondo a sequência Shine-Dalgarno.[20]
Alguns termômetros de RNA são significativamente mais complexos do que um único grampo, como no caso de uma região encontrada no CspA mRNA [en], que se acredita conter um pseudonó [en], além de múltiplos grampos.[22][23]
Termômetros de RNA sintéticos foram projetados com uma estrutura simples de grampo único.[24] No entanto, a estrutura secundária de termômetros de RNA curtos pode ser sensível a mutações, pois uma única mudança de base pode tornar o grampo inativo in vivo.[25]
Mecanismo
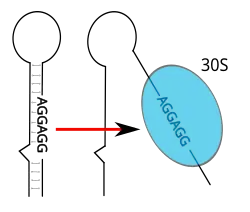
Os termômetros de RNA estão localizados na 5' UTR de RNA mensageiro, a montante de um gene codificador de proteína.[1] Aqui, eles podem ocultar o sítio de ligação ao ribossomo (RBS) e impedir a tradução do mRNA em proteína.[17] Com o aumento da temperatura, a estrutura em grampo pode "derreter", expondo o RBS ou a sequência Shine-Dalgarno, permitindo a ligação da subunidade ribossômica pequena (30S), que então monta a maquinaria de tradução.[1] O códon de início, geralmente encontrado 8 nucleotídeos a jusante da sequência Shine-Dalgarno,[17] sinaliza o início de um gene codificador de proteína, que é então traduzido em um produto peptídeo pelo ribossomo. Além desse mecanismo cis-atuante [en], um único exemplo de termômetro de RNA trans-atuante [en] foi encontrado no RpoS mRNA [en], onde se acredita estar envolvido na resposta à inanição.[1]
Um exemplo específico de motivo de termômetro de RNA é o termômetro FourU encontrado em Salmonella enterica.[5] Quando exposto a temperaturas acima de 45 °C, o grampo que forma pares de bases opostos à sequência Shine-Dalgarno se desfaz, permitindo que o mRNA entre no ribossomo para a tradução ocorrer.[25] A concentração de íons Mg2+ também demonstrou afetar a estabilidade do FourU.[26] O termômetro de RNA mais bem estudado é encontrado no gene rpoH em Escherichia coli.[27] Esse termossensor regula positivamente proteínas de choque térmico em altas temperaturas por meio de σ32, um fator sigma especializado em choque térmico.[13]
Embora tipicamente associados à expressão de proteínas induzida por calor, os termômetros de RNA também podem regular proteínas de choque frio.[22] Por exemplo, a expressão de duas proteínas de 7 kDa é regulada por um termômetro de RNA na bactéria termofílica Thermus thermophilus[28] e um mecanismo semelhante foi identificado em Enterobacteriales [en].[23]
Termômetros de RNA sensíveis a temperaturas de 37 °C podem ser usados por patógenos para ativar genes específicos de infecção.[17] Por exemplo, a regulação positiva de prfA, que codifica um regulador transcricional chave de genes de virulência em Listeria monocytogenes, foi demonstrada pela fusão do 5' DNA de prfA [en] ao gene da proteína fluorescente verde; a fusão gênica foi então transcrita a partir do promotor T7 em E. coli, e a fluorescência foi observada a 37 °C, mas não a 30 °C.[29]
Implicações para a hipótese do mundo de RNA
A hipótese do mundo de RNA afirma que o RNA foi, outrora, tanto o portador de informação hereditária quanto enzimaticamente ativo, com diferentes sequências atuando como biocatalisadores, reguladores e sensores.[30] A hipótese propõe então que a vida moderna baseada em DNA, RNA e proteína evoluiu, e a seleção substituiu a maioria dos papéis do RNA por outras biomoléculas.[4]
Termômetros de RNA e riboswitches são considerados evolutivamente antigos devido à sua ampla distribuição em organismos distantemente relacionados.[31] Foi proposto que, no mundo de RNA, os termossensores de RNA teriam sido responsáveis pela regulação dependente de temperatura de outras moléculas de RNA.[4][32] Termômetros de RNA em organismos modernos podem ser fósseis moleculares, sugerindo uma importância anteriormente mais ampla em um mundo de RNA.[4]
Outros exemplos
- Elemento cis-regulador Hsp90 [en] regula hsp90 [en] em Drosophila, aumentando a taxa de tradução da proteína de choque térmico em altas temperaturas.[6]
- O operon ibpAB de E. coli é previsto para conter dois termômetros de RNA cooperativos: um elemento ROSE [en] e o termômetro IbpB [en].[33]
- ROSE1 e ROSEAT2 [en] são encontrados em hyphomicrobiales [en] Bradyrhizobium japonicum [en] e Agrobacterium tumefaciens, respectivamente. Eles existem na 5’ UTR do mRNA HspA, e reprimem a tradução de proteínas de choque térmico em temperaturas fisiológicas.[7][34]
- Termômetros de RNA cianobacterianos [en]
- Termômetro de RNA intergênico lcrF [en]
- Termômetros de RNA Neisseria [en]
- Termômetro de RNA Lig [en]
Referências
- ↑ a b c d e f g Narberhaus F, Waldminghaus T, Chowdhury S (Janeiro de 2006). «RNA thermometers». FEMS Microbiology Reviews. 30 (1): 3–16. PMID 16438677. doi:10.1111/j.1574-6976.2005.004.x
- ↑ a b c Raza A, Siddique KH, Hu Z (Fevereiro de 2024). «Chloroplast gene control: unlocking RNA thermometer mechanisms in photosynthetic systems». Trends in Plant Science. doi:10.1016/j.tplants.2024.01.005
- ↑ a b c Thomas SE, Balcerowicz M, Chung BY (17 de Agosto de 2022). «RNA structure mediated thermoregulation: What can we learn from plants?». Frontiers in Plant Science. 13. 938570 páginas. PMC 9450479
 . PMID 36092413. doi:10.3389/fpls.2022.938570
. PMID 36092413. doi:10.3389/fpls.2022.938570
- ↑ a b c d Atkins JF, Gesteland RF, Cech T (2006). The RNA world: the nature of modern RNA suggests a prebiotic RNA world. Plainview, N.Y: Cold Spring Harbor Laboratory Press. ISBN 978-0-87969-739-6
- ↑ a b Waldminghaus T, Heidrich N, Brantl S, Narberhaus F (Julho de 2007). «FourU: a novel type of RNA thermometer in Salmonella». Molecular Microbiology. 65 (2): 413–424. PMID 17630972. doi:10.1111/j.1365-2958.2007.05794.x

- ↑ a b Ahmed R, Duncan RF (Novembro de 2004). «Translational regulation of Hsp90 mRNA. AUG-proximal 5'-untranslated region elements essential for preferential heat shock translation». The Journal of Biological Chemistry. 279 (48): 49919–49930. PMID 15347681. doi:10.1074/jbc.M404681200

- ↑ a b Nocker A, Hausherr T, Balsiger S, Krstulovic NP, Hennecke H, Narberhaus F (Dezembro de 2001). «A mRNA-based thermosensor controls expression of rhizobial heat shock genes». Nucleic Acids Research. 29 (23): 4800–4807. PMC 96696
 . PMID 11726689. doi:10.1093/nar/29.23.4800
. PMID 11726689. doi:10.1093/nar/29.23.4800
- ↑ Matsunaga J, Schlax PJ, Haake DA (Novembro de 2013). «Role for cis-acting RNA sequences in the temperature-dependent expression of the multiadhesive lig proteins in Leptospira interrogans». Journal of Bacteriology. 195 (22): 5092–5101. PMC 3811586
 . PMID 24013626. doi:10.1128/jb.00663-13
. PMID 24013626. doi:10.1128/jb.00663-13
- ↑ a b Kortmann J, Sczodrok S, Rinnenthal J, Schwalbe H, Narberhaus F (Abril de 2011). «Translation on demand by a simple RNA-based thermosensor». Nucleic Acids Research. 39 (7): 2855–2868. PMC 3074152
 . PMID 21131278. doi:10.1093/nar/gkq1252
. PMID 21131278. doi:10.1093/nar/gkq1252
- ↑ a b Altuvia S, Kornitzer D, Teff D, Oppenheim AB (Novembro de 1989). «Alternative mRNA structures of the cIII gene of bacteriophage lambda determine the rate of its translation initiation». Journal of Molecular Biology. 210 (2): 265–280. PMID 2532257. doi:10.1016/0022-2836(89)90329-X
- ↑ a b Altuvia S, Oppenheim AB (Julho de 1986). «Translational regulatory signals within the coding region of the bacteriophage lambda cIII gene». Journal of Bacteriology. 167 (1): 415–419. PMC 212897
 . PMID 2941413. doi:10.1128/jb.167.1.415-419.1986
. PMID 2941413. doi:10.1128/jb.167.1.415-419.1986
- ↑ Altuvia S, Kornitzer D, Kobi S, Oppenheim AB (Abril de 1991). «Functional and structural elements of the mRNA of the cIII gene of bacteriophage lambda». Journal of Molecular Biology. 218 (4): 723–733. PMID 1827163. doi:10.1016/0022-2836(91)90261-4
- ↑ a b Storz G (Março de 1999). «An RNA thermometer». Genes & Development. 13 (6): 633–636. PMID 10090718. doi:10.1101/gad.13.6.633

- ↑ Morita MT, Tanaka Y, Kodama TS, Kyogoku Y, Yanagi H, Yura T (Março de 1999). «Translational induction of heat shock transcription factor sigma32: evidence for a built-in RNA thermosensor». Genes & Development. 13 (6): 655–665. PMC 316556
 . PMID 10090722. doi:10.1101/gad.13.6.655
. PMID 10090722. doi:10.1101/gad.13.6.655
- ↑ a b Waldminghaus T, Gaubig LC, Narberhaus F (Novembro de 2007). «Genome-wide bioinformatic prediction and experimental evaluation of potential RNA thermometers». Molecular Genetics and Genomics. 278 (5): 555–564. PMID 17647020. doi:10.1007/s00438-007-0272-7
- ↑ a b Sharma P, Mondal K, Kumar S, Tamang S, Najar IN, Das S, Thakur N (Outubro de 2022). «RNA thermometers in bacteria: Role in thermoregulation». Biochimica et Biophysica Acta (BBA) - Gene Regulatory Mechanisms. 1865 (7). 194871 páginas. PMID 36041664. doi:10.1016/j.bbagrm.2022.194871
- ↑ a b c d e Narberhaus F (2010). «Translational control of bacterial heat shock and virulence genes by temperature-sensing mRNAs». RNA Biology. 7 (1): 84–89. PMID 20009504. doi:10.4161/rna.7.1.10501

- ↑ Johansson J (2009). «RNA thermosensors in bacterial pathogens». Bacterial Sensing and Signaling. Col: Contributions to Microbiology. 16. Basel: S. Karger AG. pp. 150–160. ISBN 978-3-8055-9132-4. PMID 19494584. doi:10.1159/000219378
- ↑ a b Shamovsky I, Ivannikov M, Kandel ES, Gershon D, Nudler E (Março de 2006). «RNA-mediated response to heat shock in mammalian cells». Nature. 440 (7083): 556–560. Bibcode:2006Natur.440..556S. PMID 16554823. doi:10.1038/nature04518
- ↑ a b Chowdhury S, Maris C, Allain FH, Narberhaus F (Junho de 2006). «Molecular basis for temperature sensing by an RNA thermometer». The EMBO Journal. 25 (11): 2487–2497. PMC 1478195
 . PMID 16710302. doi:10.1038/sj.emboj.7601128
. PMID 16710302. doi:10.1038/sj.emboj.7601128
- ↑ Waldminghaus T, Fippinger A, Alfsmann J, Narberhaus F (Dezembro de 2005). «RNA thermometers are common in alpha- and gamma-proteobacteria». Biological Chemistry. 386 (12): 1279–1286. PMID 16336122. doi:10.1515/BC.2005.145
- ↑ a b Breaker RR (Janeiro de 2010). «RNA switches out in the cold». Molecular Cell. 37 (1): 1–2. PMC 5315359
 . PMID 20129048. doi:10.1016/j.molcel.2009.12.032
. PMID 20129048. doi:10.1016/j.molcel.2009.12.032
- ↑ a b Giuliodori AM, Di Pietro F, Marzi S, Masquida B, Wagner R, Romby P, Gualerzi CO, Pon CL (Janeiro de 2010). «The cspA mRNA is a thermosensor that modulates translation of the cold-shock protein CspA». Molecular Cell. 37 (1): 21–33. PMID 20129052. doi:10.1016/j.molcel.2009.11.033

- ↑ Neupert J, Karcher D, Bock R (Novembro de 2008). «Design of simple synthetic RNA thermometers for temperature-controlled gene expression in Escherichia coli». Nucleic Acids Research. 36 (19): e124. PMC 2577334
 . PMID 18753148. doi:10.1093/nar/gkn545
. PMID 18753148. doi:10.1093/nar/gkn545
- ↑ a b Nikolova EN, Al-Hashimi HM (Setembro de 2010). «Thermodynamics of RNA melting, one base pair at a time». RNA. 16 (9): 1687–1691. PMC 2924531
 . PMID 20660079. doi:10.1261/rna.2235010
. PMID 20660079. doi:10.1261/rna.2235010
- ↑ Rinnenthal J, Klinkert B, Narberhaus F, Schwalbe H (Outubro de 2011). «Modulation of the stability of the Salmonella fourU-type RNA thermometer». Nucleic Acids Research. 39 (18): 8258–8270. PMC 3185406
 . PMID 21727085. doi:10.1093/nar/gkr314
. PMID 21727085. doi:10.1093/nar/gkr314
- ↑ Shah P, Gilchrist MA (Julho de 2010). Spirin AS, ed. «Is thermosensing property of RNA thermometers unique?». PLOS ONE. 5 (7): e11308. Bibcode:2010PLoSO...511308S. PMC 2896394
 . PMID 20625392. doi:10.1371/journal.pone.0011308
. PMID 20625392. doi:10.1371/journal.pone.0011308
- ↑ Mega R, Manzoku M, Shinkai A, Nakagawa N, Kuramitsu S, Masui R (Agosto de 2010). «Very rapid induction of a cold shock protein by temperature downshift in Thermus thermophilus». Biochemical and Biophysical Research Communications. 399 (3): 336–340. PMID 20655297. doi:10.1016/j.bbrc.2010.07.065
- ↑ Johansson J, Mandin P, Renzoni A, Chiaruttini C, Springer M, Cossart P (Setembro de 2002). «An RNA thermosensor controls expression of virulence genes in Listeria monocytogenes». Cell. 110 (5): 551–561. PMID 12230973. doi:10.1016/S0092-8674(02)00905-4

- ↑ Gilbert W (Fevereiro de 1986). «The RNA World». Nature. 319 (6055): 618. Bibcode:1986Natur.319..618G. doi:10.1038/319618a0

- ↑ Serganov A, Patel DJ (Outubro de 2007). «Ribozymes, riboswitches and beyond: regulation of gene expression without proteins». Nature Reviews. Genetics. 8 (10): 776–790. PMC 4689321
 . PMID 17846637. doi:10.1038/nrg2172
. PMID 17846637. doi:10.1038/nrg2172
- ↑ Bocobza SE, Aharoni A (Outubro de 2008). «Switching the light on plant riboswitches». Trends in Plant Science. 13 (10): 526–533. PMID 18778966. doi:10.1016/j.tplants.2008.07.004
- ↑ Gaubig LC, Waldminghaus T, Narberhaus F (Janeiro de 2011). «Multiple layers of control govern expression of the Escherichia coli ibpAB heat-shock operon». Microbiology. 157 (Pt 1): 66–76. PMID 20864473. doi:10.1099/mic.0.043802-0

- ↑ Balsiger S, Ragaz C, Baron C, Narberhaus F (Outubro de 2004). «Replicon-specific regulation of small heat shock genes in Agrobacterium tumefaciens». Journal of Bacteriology. 186 (20): 6824–6829. PMC 522190
 . PMID 15466035. doi:10.1128/JB.186.20.6824-6829.2004
. PMID 15466035. doi:10.1128/JB.186.20.6824-6829.2004