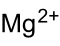Sulfito de magnésio
Magnesium sulfite
| |||||||||
|---|---|---|---|---|---|---|---|---|---|
| |||||||||
| Nomes | |||||||||
| Nome IUPAC | Magnesium sulfite | ||||||||
| Outros nomes | Magnesium sulphite | ||||||||
| |||||||||
| |||||||||
| |||||||||
| Página de dados suplementares | |||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||
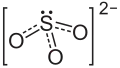
Sulfito de magnésio é o composto químico de fórmula MgSO3. É o sal de magnésio do ácido sulforoso.
Sua forma hidratada mais comum possui 6 moléculas de água, tornando-o um hexahidrato de fórmula MgSO3·6 H2O. Quando aquecido acima de 40°C (104° F), é desidratado em sulfito de magnésio tri-hidratado MgSO3·3 H2O.[1]
Sua forma anidra é higroscópica, ou seja, absorve rapidamente a umidade do ar.
Referências
- ↑ Nývlt, J. (2001). «Solubilities of Magnesium Sulfite.». Journal of Thermal Analysis and Calorimetry (em inglês). 66: 509-512. doi:10.1023/A:1013117001627