Rhinolophus ferrumequinum
Morcego-de-ferradura-grande
| |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
_Hrdovicka.jpg) | |||||||||||||||
| Estado de conservação | |||||||||||||||
 Pouco preocupante [1] | |||||||||||||||
| Classificação científica | |||||||||||||||
| |||||||||||||||
| Distribuição geográfica | |||||||||||||||
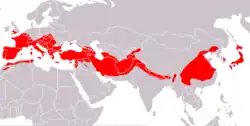 Distribuição do morcego-de-ferradura-grande.
| |||||||||||||||
O morcego-de-ferradura-grande (Rhinolophus ferrumequinum) é um morcego insetívoro do gênero Rhinolophus. Sua distribuição abrange a Europa, o Norte da África, a Ásia Central e a Ásia Oriental.[1] É o maior dos morcegos-de-ferradura na Europa, sendo facilmente distinguido de outras espécies. A espécie é sedentária, normalmente viajando até 30 km entre os poleiros de inverno e verão, com o maior movimento registrado sendo de 180 km. As frequências usadas por esta espécie de morcego para ecolocalização estão entre 69–83 kHz, com maior energia em 81 kHz e uma duração média de 37,4 ms.[2][3]
Descrição
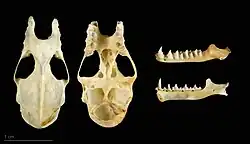
O morcego-de-ferradura-grande é o maior morcego-de-ferradura da Europa.[4] Possui uma folha nasal distinta, com a parte superior pontiaguda e a parte inferior em forma de ferradura.[5] Sua folha nasal em ferradura ajuda a focar o ultrassom que utiliza para "enxergar". O morcego-de-ferradura-grande também possui estruturas dentárias e ósseas distintas de outros rinolofídeos. Seu primeiro pré-molar na mandíbula superior se projeta para fora da fileira de dentes.[6] Em outros morcegos-de-ferradura, esse pré-molar é muito pequeno ou inexistente.[6] Comparado aos seus parentes, o morcego-de-ferradura-grande tem ossos metacarpais terceiro e quarto relativamente curtos em suas asas.[7] Ele também não possui tragus.
O morcego-de-ferradura-grande mede, em média, entre 57-71 mm de comprimento, com uma cauda de 35-43 mm e uma envergadura de 350-400 mm;[6] R. ferrumequinum também exibe leve dimorfismo sexual, com as fêmeas sendo um pouco maiores que os machos.[8] O pelo da espécie é macio e fofo, com a base dos pelos sendo cinza claro, o lado dorsal cinza-acastanhado e o lado ventral cinza-branco, com os filhotes tendo uma tonalidade mais cinza-acinzentada. As membranas das asas e as orelhas são cinza-acastanhadas claras. O morcego-de-ferradura-grande pesa até 30 g e pode viver até 30 anos.[9]
Distribuição
O morcego-de-ferradura-grande abrange desde o norte da África e sul da Europa até o sudoeste da Ásia, Cáucaso, Irã, Afeganistão, Paquistão e Himalaia, até o sudeste da China, Coreia e Japão.[10] A ocorrência mais ao norte é no País de Gales. Alcança as partes sul da Holanda, Alemanha, Polônia e Ucrânia.[11] Geralmente, os morcegos vivem abaixo de 800 m de altitude, mas também habitam, dependendo da disponibilidade de poleiros e umidade, até 3.000 m de altitude no Cáucaso.[1]
Ecologia e comportamento
Habitat e poleiros
Pastagens, florestas temperadas decíduas, matagais mediterrâneos e submediterrâneos e florestas são habitats comuns de forrageamento para esta espécie.[1] Nas partes norte de sua distribuição, o morcego-de-ferradura utiliza locais subterrâneos quentes, tanto naturais quanto artificiais, como poleiros de verão, assim como sótãos. Onde a espécie ocupa construções, a proximidade de boas áreas de forrageamento e locais subterrâneos para torpor em várias épocas do ano e para hibernação no inverno, bem como as próprias características do edifício, são importantes.[12]
Os morcegos-de-ferradura hibernam em locais subterrâneos frios durante o inverno. Eles requerem certos limites de temperatura e umidade, que podem variar com idade, sexo e condição.[1] Os morcegos-de-ferradura são ativos durante todo o ano nas partes sul de sua distribuição. Eles comumente viajam distâncias de 20–30 km entre poleiros de inverno e verão, com a maior distância registrada sendo 180 km.[13] Os morcegos-de-ferradura também vivem em florestas montanhosas entre as montanhas e vales do Himalaia no sul da Ásia e se abrigam em cavernas, templos antigos e construções antigas e em ruínas em grupos compactos.[1]
Dieta e caça
A espécie se alimenta preferencialmente de lepidópteros (mariposas), que compõem cerca de 41% da dieta[14] - em particular as espécies noctuídeas.[15] Por exemplo, a espécie caça a mariposa-da-cera-menor identificando seu chamado de acasalamento de alta frequência.[16] Coleópteros (besouros) constituem cerca de 33% da dieta,[14] dos quais besouros rola-bosta e Melolontha são frequentemente capturados. Acrossus rufipes é um desses besouros rola-bosta que forma uma parte especialmente importante de sua dieta. (Os montes de esterco bovino fazem parte de seu ciclo de vida, servindo como fonte de alimento e habitat para as larvas. Até 100 larvas podem ser encontradas em um único monte de esterco; o besouro adulto é mais abundante em agosto, quando os jovens morcegos começam seus primeiros voos de alimentação.)[17] O restante da dieta consiste em espécies de himenópteros e dípteros, além de aranhas de caverna.[14][8]
A área de alimentação a partir do poleiro de maternidade é tipicamente de um raio de 4 km, pois nem as fêmeas lactantes nem os filhotes podem viajar longe. No final de agosto e setembro, os morcegos se alimentam de mosquitos da superfamília Tipuloidea, para engordar antes da hibernação. As fêmeas reprodutoras dependem de besouros de abril a junho, e de mariposas de junho a agosto.[14][16]
O morcego-de-ferradura-grande deixa seu poleiro ao entardecer. Seu voo é composto por deslocamentos lentos e flutuantes com planeios curtos, normalmente entre 0,3 e 6 metros acima do solo. Pouca caça é realizada durante o tempo chuvoso e ventoso. Ele caça em terrenos com pouca cobertura arbórea, como encostas e falésias, e em jardins, onde localiza insetos a partir de um local de descanso e depois os intercepta. A espécie tem a capacidade de pegar comida do chão enquanto ainda está em voo e também bebe durante voos de baixa altitude ou enquanto paira. O alcance de alimentação das colônias na Inglaterra está entre 8 e 16 quilômetros.
Um estudo sobre espécimes históricos e recentes do morcego-de-ferradura-grande da Itália descobriu que o comprimento do antebraço — uma medida padrão de tamanho corporal em morcegos — aumentou significativamente entre 1869 e 2005.[18] A pesquisa, baseada em 78 indivíduos espacialmente independentes, descartou efeitos de latitude ou insularidade e confirmou que as fêmeas são geralmente maiores que os machos. Essa tendência de longo prazo pode refletir uma resposta a mudanças ambientais ao longo do último século e meio.[18]
Acasalamento e reprodução
As fêmeas tornam-se sexualmente maduras aos três anos, enquanto os machos atingem a maturidade sexual aos dois anos.[19] Algumas fêmeas podem não se reproduzir até o quinto ano.[20] A maioria dos acasalamentos ocorre no outono, embora alguns aconteçam na primavera.[21] O comportamento reprodutivo desta espécie foi estudado em detalhes. Durante o período de acasalamento, as fêmeas visitam machos que estão em poleiros em pequenas cavernas. O sistema de acasalamento é melhor descrito como poliginia, com várias fêmeas visitando machos. No entanto, evidências genéticas mostraram que algumas fêmeas do morcego-de-ferradura-grande visitam e acasalam com o mesmo parceiro macho por anos consecutivos, indicando monogamia ou fidelidade ao parceiro.[22] Curiosamente, fêmeas relacionadas também foram encontradas compartilhando parceiros sexuais, o que pode servir para aumentar a relação e a coesão social na colônia.[22] Os machos variam em seu sucesso reprodutivo, mas não tendem a mostrar desvio reprodutivo dentro de um ano.[22] No entanto, ao longo de vários anos, o desvio torna-se forte devido ao sucesso repetido de certos machos.[23]
Após o acasalamento, o fluido seminal coagula na vulva da fêmea para formar um tampão, que provavelmente funciona para prevenir acasalamentos subsequentes por outros machos,[24] ou para aumentar as chances de que o esperma seja retido para uma fertilização bem-sucedida.[21] Há evidências de que as fêmeas podem ejetar esses tampões, sugerindo que elas podem exercer algum controle sobre as fertilizações que ocorrem.[4] As fêmeas criam seus filhotes em poleiros de maternidade comunais e mostram forte fidelidade aos locais onde nasceram (a chamada filopatria natal). Cada temporada, uma fêmea produz um filhote. A maioria dos filhotes nasce em junho ou julho.[4] Quando têm sete dias de idade, os filhotes podem abrir os olhos e, na terceira ou quarta semana, podem voar. Os filhotes geralmente deixam o poleiro após cinco semanas.[25]
Estado e conservação
Em geral, o morcego-de-ferradura-grande é listado como espécie pouco preocupante pela IUCN porque: "Esta espécie tem uma ampla distribuição. Embora tenham ocorrido declínios marcados e bem documentados em algumas áreas, a espécie permanece amplamente distribuída, abundante e aparentemente estável em outras áreas".[1] No entanto, a população geral do morcego-de-ferradura-grande está diminuindo.[1] Eles são amplamente incomuns em grande parte de sua distribuição. Apesar disso, parecem ser abundantes e amplamente distribuídos em pelo menos partes do sudoeste da Ásia e do Cáucaso. Também em alguns países do noroeste da Europa, parece haver alguma estabilização e/ou recuperação.[12] Menos se sabe sobre as tendências dos morcegos em outras partes da Europa. A espécie já está extinta em Malta.[1] A fragmentação/isolamento de habitats, a mudança no regime de manejo de florestas decíduas e áreas agrícolas, a perda de insetos causada por pesticidas, as mudanças climáticas e a perturbação e perda de habitats subterrâneos e sótãos são as principais ameaças ao morcego-de-ferradura-grande. O desmatamento, principalmente causado por operações de extração de madeira e a conversão de terras para usos agrícolas e outros, ameaça a espécie no sul da Ásia.[26]
Estado na Grã-Bretanha

A espécie é rara na Grã-Bretanha, confinada a apenas um pequeno número de locais.[9] Sua distribuição pode ser encontrada no site da National Biodiversity. Seus locais de reprodução incluem Brockley Hall Stables perto de Bristol, Iford Manor perto de Bath, e Littledean Hall na floresta de Dean. Seus locais de hibernação no inverno incluem cavernas de Banwell [en] e Compton Martin Ochre Mine nas colinas de Mendip, Chilmark Quarries em Wiltshire, e Combe Down and Bathampton Down Mines perto de Bath. Em Dorset, a espécie se abriga em Bryanston, Creech Grange e em Belle Vue Quarry. A espécie também ocorre em Berry Head em Devon e tem um local de poleiro monitorado em Woodchester Mansion em Stroud. Também ocorre no País de Gales.[25]
A espécie desapareceu de mais da metade de sua antiga distribuição no Reino Unido, com cerca de 1% da população sobrevivendo. Como todos os morcegos-de-ferradura, é sensível a perturbações e é ameaçado pelo uso de inseticidas e pela eliminação de besouros pelas mudanças nas práticas agrícolas.[12]
Há dezessete espécies de morcegos registradas na Grã-Bretanha conforme resultados de levantamentos recentes.[4][10] O morcego-de-ferradura-grande é um dos mais raros. Atualmente, existem 35 poleiros de maternidade e permanentes reconhecidos e 369 locais de hibernação. As estimativas atuais variam entre 4.000 e 6.600 indivíduos. Os morcegos-de-ferradura-grandes diminuíram por várias razões,[12] desde o uso de agroquímicos (ivermectina em particular) até a perda de habitat e a redundância dos métodos agrícolas. A ivermectina mata as larvas de insetos e, assim, reduz a abundância de alimentos para os morcegos-de-ferradura, fazendo com que viajem mais longe e enfrentem maiores perigos.
A perda de habitat é principalmente devido à falta de sebes estabelecidas e ecótonos de pastagem-floresta decídua. Os métodos agrícolas modernos reduziram o pastoreio de gado, o que impactou os morcegos-de-ferradura, que anteriormente se beneficiavam do esterco que atraía insetos e sustentava populações entomógenas, proporcionando uma população estável de presas.
Referências
- ↑ a b c d e f g h i Piraccini R. (2016). «Rhinolophus ferrumequinum». Lista Vermelha de Espécies Ameaçadas. 2016: e.T19517A21973253. doi:10.2305/IUCN.UK.2016-2.RLTS.T19517A21973253.en
 . Consultado em 17 de fevereiro de 2022
. Consultado em 17 de fevereiro de 2022
- ↑ Parsons, S.; Jones, G. (2000). «Acoustic identification of twelve species of echolocating bat by discriminant function analysis and artificial neural networks». The Journal of Experimental Biology. 203: 2641–2656. PMID 10934005
- ↑ Obrist, M.K.; Boesch, R.; Flückiger, P.F. (2004). «Variability in echolocation call design of 26 Swiss bat species: Consequences, limits and options for automated field identification with a synergic pattern recognition approach». Mammalia. 68 (4): 307–322. doi:10.1515/mamm.2004.030
- ↑ a b c d Schober, W.; Grimmberger, E. (1997). The Bats of Europe and North America: Knowing Them, Identifying Them, Protecting Them. New Jersey: TFH Publications. ISBN 978-0-7938-2069-6
- ↑ Nowak, R. (1994). Walker's Bats of the World. Baltimore, Maryland: The Johns Hopkins University Press. ISBN 978-0-8018-4986-2
- ↑ a b c «Greater horseshoe bat». Animal Diversity Web. Consultado em 16 de fevereiro de 2023
- ↑ Koopman, K. (1994). Chiroptera: Systematics. New York: Walter de Gruyter. ISBN 978-3-11-013977-8
- ↑ a b Antoni Alcover, J., ed. (1988). «Mamífers Actuals». els Mamífers de les Balears. Palma de Mallorca: Editorial Moll. pp. 88–90. ISBN 84-273-0265-7
- ↑ a b Schober, W.; Grimmberger, E. (1989). A Guide to Bats of Britain and Europe. UK: Hamlyn Publishing Group. ISBN 978-0-600-56424-9
- ↑ a b Csorba, G.; Ujhelyi, P.; Thomas, N. (2003). Horseshoe Bats of the World. Shropshire, England: Alana Books. ISBN 978-0-9539046-2-4
- ↑ «Rhinolophus ferrumequinum». Science for Nature Foundation. Consultado em 16 de fevereiro de 2023
- ↑ a b c d Hutson, A. M.; Mickleburgh, S. P.; Racey, P. A. (2001). Microchiropteran Bats - Global Status Survey and Conservation Action Plan. Gland, Switzerland and Cambridge, U.K.: IUCN/SSC Chiroptera Specialist Group
- ↑ De Paz, O.; Fernández, R.; Benzal, J. (1986). «El anillamiento de quirópteros en el centro de la Península Ibérica durante el periodo 1977-1986». Boletín de la Estación Central de Ecología. 30: 113–138
- ↑ a b c d Jones, G. (1990). «Prey selection by the greater horseshoe bat (Rhinolophus ferrumequinum): Optimal foraging by echolocation?». Journal of Animal Ecology. 59: 587–602. doi:10.2307/4882
- ↑ «Greater Horseshoe bat Species information leaflet». Bat Conservation Trust. Consultado em 16 de fevereiro de 2023
- ↑ a b Cordes, N.; Engqvist, L.; Schmoll, T.; Reinhold, K. (2014). «Sexual signaling under predation: attractive moths take the greater risks». Behavioral Ecology. 25 (2): 409–414. doi:10.1093/beheco/art128
- ↑ «The secret life of the greater horseshoe bat». Wild Devon The Magazine of the Devon Wildlife Trust. Winter: 14. 2009
- ↑ a b Salinas-Ramos, Valeria B.; Agnelli, Paolo; Bosso, Luciano; Ancillotto, Leonardo; Russo, Danilo (2021). «Body size of Italian greater horseshoe bats (Rhinolophus ferrumequinum) increased over one century and a half: a response to climate change?». Mammalian Biology. 101 (6): 1127–1131. ISSN 1618-1476. doi:10.1007/s42991-021-00112-7
- ↑ Ransome, R.D. (1995). «Earlier Breeding Shortens Life in Female Greater Horseshoe Bats». Philosophical Transactions of the Royal Society B. 350: 153–161. doi:10.1098/rstb.1995.0149
- ↑ Racey, P. (1982). «Ecology of Bat Reproduction». In: Kruz, T. Ecology of Bats. New York: Plenum Press. pp. 57–93. ISBN 978-0-306-40874-8
- ↑ a b Rossiter, S.; Jones, J.; Ransome, R.; Barratt, E. (2000). «Genetic variation and population structure in the endangered greater horseshoe bat Rhinolophus ferrumequinum». Molecular Ecology. 9: 1131–1135. doi:10.1046/j.1365-294x.2000.00982.x
- ↑ a b c Rossiter, S.; Ransome, R.D.; Faulkes, C.G.; Le Comber, S.L.; Jones, G. (2005). «Mate-fidelity and intra-lineage polygyny in greater horseshoe bats». Nature. 437: 408–411. doi:10.1038/nature03965
- ↑ Rossiter, S.; Ransome, R.D.; Faulkes, C.G.; Dawson, D.A.; Jones, G. (2006). «Long-term reproductive skew in male greater horseshoe bats». Molecular Ecology. 15: 3035–3043. doi:10.1111/j.1365-294x.2006.02987.x
- ↑ Fenton, M. (1994). Just Bats. Toronto: University of Toronto Press. ISBN 978-0-8020-7668-7
- ↑ a b Tomsett, Alice (2005). A Field Guide to the Wildlife of the British Isles. Bath: Parragon. p. 61. ISBN 978-1-4054-4393-7
- ↑ Molur, S.; Marimuthu, G.; Srinivasulu, C.; Mistry, S.; Hutson, A. M.; Bates, P. J. J.; Walker, S.; Padmapriya, K.; Binupriya, A. R. (2002). Status of South Asian Chiroptera: Conservation Assessment and Management Plan (C.A.M.P.) Workshop Report. Coimbatore, India: Zoo Outreach Organization/CBSG-South Asia
Leitura adicional
- Schober, Wilfried; Eckard Grimmberger (1989). Dr. Robert E. Stebbings, ed. A Guide to Bats of Britain and Europe 1st ed. UK: Hamlyn Publishing Group. ISBN 978-0-600-56424-9
Ligações externas
- «Morcego-ferradura-grande». Consultado em 16 de fevereiro de 2023
- «Guia de Manejo Florestal para Morcegos». Forestry Commission. Consultado em 16 de fevereiro de 2023. Cópia arquivada em 19 de março de 2013