Química de coordenação
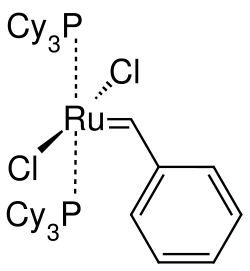
Química dos compostos de coordenação ou coordenação é o ramo da química que estuda os iões complexos, isto é, moléculas em que um catão metálico é coordenado ou coordenado (isto é, ligado por uma ligação química específica) a átomos, iões ou moléculas com um número de ligações superior ao seu número de oxidação. Em particular, esta disciplina trata do estudo da ligação coordenada, dos métodos sintéticos específicos aplicáveis e da caracterização estrutural utilizando técnicas instrumentais como o infravermelho, Mössbauer, fotoelectrónica ou espectrofotometria UV/VIS.
Em contraste com as ligações covalentes convencionais, nos complexos os ligantes contribuem normalmente com todos os electrões para a ligação, em vez de cada reagente contribuir com um electrão para uma ligação de pares de electrões (ligação coordenativa); no entanto, existem também complexos de natureza mais covalente.[1] A formação de complexos pode, assim, ser entendida como uma reação ácido-base no sentido da definição de Lewis, na qual os ligantes (bases) atuam como doadores de pares de eletrões e a partícula central (ácido) como aceptora através de lacunas na sua configuração eletrónica.
Existem vários tipos de complexos, desde o simples metal em solução aquosa coordenado por moléculas de água até complexos metal-enzima ou metal-proteína; têm múltiplas funções e aplicações e hoje abrangem grande parte da investigação em química inorgânica.
Uma grande importância na investigação e na química dos complexos em geral é que estes podem ser catalisadores de fase homogénea para reações químicas (ver figura do catalisador de Grubbs à direita).
Os complexos, que envolvem os orbitais do metal na ligação, são frequentemente coloridos, por exemplo, Fe coordenado com hemoglobina, que dá ao sangue a sua cor vermelha. No organismo humano, o Fe(II) está presente na hemoglobina e na mioglobina, coordenado aos átomos de azoto do anel porfirínico (o "grupo heme" da proteína) e desempenha a função de ligar o oxigénio, que será depois transportado pelo sangue para os tecidos. Muitas enzimas necessitam também de formar complexos com os metais para desempenhar a sua função.
Como os complexos de metais de transição são por vezes muito coloridos, são também utilizados como corantes ou pigmentos (azul da Prússia ou azul de Berlim). Esta característica pode ser explorada em avaliações ou análises volumétricas.
Durante muito tempo, os químicos não tinham qualquer ideia da estrutura dos compostos de coordenação chamados "compostos de ordem superior". Além disso, muitos comportamentos dos complexos não podiam ser explicados pelas teorias da época, como por exemplo a estabilidade do cloreto de cobalto(III) em solução aquosa com a adição de amoníaco. Pela interpretação correta das relações estruturais e de ligação em complexos, o suíço Alfred Werner foi o primeiro e, durante décadas, o único inorgânico a receber o Prémio Nobel da Química em 1913.
Simetria
Como as partículas centrais e os ligantes de um complexo estável, como os iões, possuem n estruturas geometricamente ordenadas dentro da estrutura cristalina, são atribuídos a determinados grupos de pontos de simetria. A rotulagem é geralmente baseada no sistema de Schoenflies.
.svg.png)
O estudo sistemático da estrutura de compostos complexos começou no final do século XIX e é caracterizado principalmente pelos nomes Sophus Mads Jørgensen e Alfred Werner . Embora Jørgensen tenha se destacado com a síntese de vários novos complexos, ele era um defensor da "teoria da cadeia" introduzida por Christian W. Blomstrand . De acordo com essa teoria, os ligantes são dispostos um após o outro, formando assim cadeias, o que parece fazer pouco sentido hoje, mas pelo menos levava em consideração a valência do metal
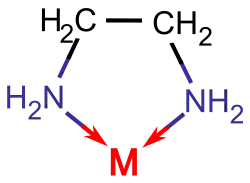
Forma espacial dos complexos (geometria molecular)
Número de coordenação e poliedro de coordenação
4.svg.png)
complexo tetraédrico
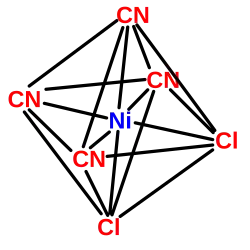
complexo octaédrico
O número de coordenação (KZ) indica quantos átomos doadores do ligante rodeiam uma partícula central. Dependendo do número de coordenação, os ligantes estão dispostos em determinados arranjos em torno do centro, que frequentemente, mas nem sempre, concordam com as previsões do modelo VSEPR. Se pensarmos nas linhas que ligam os ligantes, obtemos os poliedros de coordenação, que são geralmente utilizados para descrever a estrutura dos complexos. São comuns os números de coordenação de 2 a 9; números para além deste só podem ser obtidos no caso de partículas centrais particularmente grandes e ligantes quelantes. No entanto, os mais comuns são os números de coordenação 4 e 6. De acordo com o modelo VSEPR, podem ser assumidos os seguintes poliedros:
Ligantes aniónicos
Ligantes aniónicos são formados a partir do nome do ânion adicionando o sufixo -o : -id torna-se -ido, -it torna-se -ito e -at torna-se -ato . Alguns nomes tradicionais (como cloro, ciano ou oxo) também eram permitidos até a revisão de 2005 da nomenclatura IUPAC.[2] Essas exceções foram eliminadas e não são mais permitidas.
- H − (hidrido)
- F − (flúor) ; Cl − (clorido) ; Br − (bromido) ; Eu − (iodido)
- O 2− (óxido) ; O 2 2− (peróxido) ; OH− (hidróxido)
- Oxalato (ox)
- Acetilacetonato (acac)
- S 2− (tio) ; SO42− (sulfato); S2O32− (tiosulfato);
- S 2 O 3 2− (tiosulfato)
- SCN − (tiocianato ou isotiocianato quando coordenado via N)
- CN − (cianido, isocianido quando coordenado via N ou ciano-C e ciano-N)
- NO 2 − (nitrito-N ou nitrito- κN (anteriormente nitro) quando coordenado via N ou nitrito-O ou nitrito- κO (anteriormente nitrito) quando coordenado via O); NÃO 3 − (nitrato)
- Etilenodiaminotetraacetato EDTA 4− (Etilenodiaminotetraacetato)
- Ácido nitrilotriacético (NTA 3− ) (Nitrilotriacetato)
- Porfina / Porfirinas (importantes em bioquímica )
Ligantes neutros
- NH 3 (amina)
- Etilenodiamina (en)
- H 2 O (aqua, obsoleto aquo)
- CO (carbonila)
- NO (nitrosil)
Ligantes catiónicos
- KZ 2: um complexo linear, por exemplo B. [AuCl 2 ] − ou complexo angular, por exemplo B. [Au(tBuXanthPhos)][AuBr 2 ]
- KZ 3: uma estrutura trigonal-planar ou trigonal-aplanar (a partícula central não está exatamente no meio do triângulo, mas ligeiramente acima dele)
- KZ 4: um tetraedro ou uma estrutura quadrada-plana
- KZ 5: uma estrutura piramidal quadrada ou trigonal-bipiramidal; ambas são interconvertíveis pela pseudorrotação de Berry e estão em equilíbrio na temperatura apropriada
- KZ 6: principalmente um octaedro, às vezes um antiprisma trigonal ou (menos frequentemente) um prisma trigonal
- KZ 7 (muito raro): uma bipirâmide pentagonal, um octaedro simplesmente tampado ou um prisma trigonal simplesmente tampado
- KZ 8: um antiprisma quadrado, um dodecaedro trigonal, um prisma trigonal duplamente coberto ou, mais raramente, um hexaedro ( cubo )
- KZ 9: um prisma trigonal de tripla capa, por exemplo B. [ReH 9 ] 2− ou antiprisma quadrado coberto, por exemplo B.[ Ln(thf)[ N(CH 2 CH 2 OH) 3]] 3+
- KZ 12: Icosaedro ou um cuboctaedro resulta em, por exemplo B. [Ce(NO 3 ) 6 ] 2− ou [Zr(η 3 –BH 4 ) 4 ]
Formação de complexos
A reação clássica de formação de complexos é uma reação ácido-base, de acordo com a teoria de Gilbert Newton Lewis . A partícula central é o ácido de Lewis (aceptor de pares de elétrões); o ligante é a base de Lewis, ou seja, uma molécula ou íon que pode fornecer pelo menos um par de elétrões livres (doador de pares de elétrões) para formar uma ligação.
Um exemplo típico de formação de complexo é a adição de água ao sulfato de cobre(II) . O sal incolor reage com a água para formar um complexo azul:
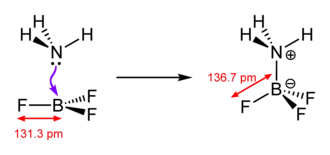
Aplicação da lei da ação das massas
Constantes de equilíbrio podem ser estabelecidas para descrever quantitativamente a estabilidade de complexos, uma vez que as reações ácido-base de Lewis para a formação de complexos são reações de equilíbrio para as quais a lei da ação das massas pode ser estabelecida. A reação geral pode ser dividida em etapas individuais (as chamadas reações elementares), ou seja, ou seja, para a ligação de um ligante. O produto das constantes de equilíbrio das reações elementares individuais para a formação do complexo produz então a constante de equilíbrio para a reação global.
A constante resultante é chamada de constante de formação complexa . Essa constante também indica o quão estável o complexo é, ou se ele tende a se dissociar. Portanto, a constante de formação complexa também é chamada de constante de estabilidade complexa ou constante de associação complexa K A . Seu valor recíproco é chamado de constante de dissociação complexa K D, ou seja, K D = K A −1 . Quanto maior a constante de formação complexa K A, mais estável o complexo; quanto menor, mais fácil é dissociá-lo.
Constantes de formação de complexos
De acordo com Martell & Smith, 1982; Hyvönen & Aksela, 2010; Vasilev et al. 1996; Vasilev et al. 1998
| Agentes complexantes | abreviação | Constante de formação de complexos contra Ca 2+ |
|---|---|---|
| Ácido dietilenotriaminopentaacético | DTPA | 10.8 |
| Ácido etilenodiaminotetracético | EDTA | 10.7 |
| ácido β-alaninadiacético | ADA | 5–7 |
| Ácido metilglicinodiacético | MGDA | 7 |
| Ácido nitrilotriacético | NTA | 6.4 |
| Ácido nitrilotri(metilfosfónico) | NTMP | 5,75 |
| Iminodissuccinato tetrassódico | IDS | 5.2 |
| Tetrassódio de L-Glutamato Diacetato ou GLDA-Na4 | GLDA | 5.2 |
| Ácido etilenodiaminodissuccínico | EDDS | 4.6 |
Ver também
- Química organometálica
- Íons fracamente coordenados
- Química de coordenação de superfície
- Lista de abreviações de ligantes
Bibliografia
- Lutz H. Gade: Química de Coordenação . Wiley-VCH, Weinheim 2012, ISBN 978-3-527-29503-6 .
- Christoph Janiak: Química complexa/de coordenação, em: Erwin Riedel (ed.): Química inorgânica moderna . 3ª ed., de Gruyter, Berlim 2007, pp. 381–579, ISBN 978-3-11-019060-1 .
- Birgit Weber: Química de coordenação: fundamentos e tendências atuais . 2ª ed., Springer Spektrum, 2021, ISBN 978-3-662-63818-7 .
- Lothar Beyer, Jorge Angulo Cornejo: Química de Coordenação: Fundamentos – Sínteses – Aplicações (Livros didáticos de Química) . Vieweg+Teubner Verlag, 2012, ISBN 978-3-8348-1800-3 .
- Friedhelm Kober: Fundamentos de Química Complexa . 1979, Salle + Sauerländer, ISBN 3-7935-5482-1 .
- Joan Ribas Gispert: Química de Coordenação . 1ª ed., Wiley-VCH, Weinheim 2008, ISBN 978-3-527-31802-5 .
- A. F. Holleman
- Henry Taube : Transferência de elétrons entre complexos metálicos – uma revisão (palestra Nobel), em: Angewandte Chemie 1984, 96, pp. 315–326, doi:10.1002/ange.19840960504 .
Ligações externas
- Unidades de aprendizagem para alunos em complexos no servidor educacional de química do Prof. Blume
- Lista muito extensa e classificável interativamente de constantes de formação complexas
- Banco de Dados Estrutural de Cambridge
Referências
- ↑ A. F. Holleman, E. Wiberg, N. Wiberg (2007). "Lehrbuch der Anorganischen Chemie". (Handbook of Inorganic Chemistry) 102, S. 1316. [S.l.]: Walter de Gruyter, Berlin. ISBN 978-3-11-017770-1
- ↑ Wolfgang Liebscher, Ekkehard Fluck. ?Die systematische Nomenklatur der anorganischen Chemie. [S.l.: s.n.] ISBN 3-540-63097-X