Pachysentis
Pachysentis
| |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Classificação científica | |||||||||||||
| |||||||||||||
| Espécie-tipo | |||||||||||||
| Pachysentis canicola Meyer, 1931 | |||||||||||||
| Sinónimos | |||||||||||||
| |||||||||||||
Pachysentis[2] é um gênero de acantocéfalos (vermes parasitas espinhosos) que parasitam primatas e carnívoros. Eles estão distribuídos pela África, Oriente Médio e Américas. As espécies de Pachysentis se fixam à mucosa interna do trato gastrointestinal de seus hospedeiros usando sua probóscide coberta de ganchos. Seu ciclo de vida inclui um estágio de ovo encontrado nas fezes do hospedeiro, um estágio larval (cistacanto) em um hospedeiro intermediário, como a naja-egípcia, e um estágio adulto, onde os cistacantos amadurecem nos intestinos do hospedeiro. Este gênero é morfologicamente muito semelhante ao Oncicola [en], diferenciando-se principalmente pelo maior número de ganchos na probóscide. Há onze espécies atribuídas a este gênero, embora P. septemserialis tenha status taxonômico incerto. As fêmeas variam de 12 mm de comprimento por 1,6 mm de largura em P. lauroi a 50 mm de comprimento por 4 mm de largura em P. dollfusi. Quase todo o comprimento corresponde ao tronco, com uma probóscide curta. Há um pronunciado dimorfismo sexual, com as fêmeas sendo cerca de duas vezes maiores que os machos.
Taxonomia
Análise filogenética foi conduzida em uma das onze espécies do gênero, P. canicola.[3] Sequências do marcador molecular 18S rDNA foram comparadas com as de espécies relacionadas, concluindo que amostras de P. canicola formam um grupo bem suportado com outras espécies da família Oligacanthorhynchidae.[3] Análises filogenéticas também foram realizadas no gênero Oncicola, morfologicamente quase idêntico ao Pachysentis, exceto pelo número de ganchos na probóscide, e também o classificaram na família Oligacanthorhynchidae.[4] A espécie-tipo de Pachysentis é P. canicola.[5][1] Em 1972, Schmidt reclassificou seis espécies do gênero Prosthenorchis e uma do gênero Oncicola no gênero Pachysentis.[6]
| Archiacanthocephala | ||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||
| Reconstrução filogenética para espécies selecionadas da classe Archiacanthocephala com base em uma comparação do gene 28S rRNA de Gomes et al. (2019) e uma comparação do gene 18S rDNA de Amin e colegas (2020).[1][7] Amin e colegas (2022) utilizaram o gene 18S rDNA para adicionar filogeneticamente P. canicola à família Oligacanthorhynchidae.[3] |
Descrição
| Número de ganchos na probóscide[1] | Farpa nos ganchos | |
|---|---|---|
| P. angolensis | 42 | Sem farpas |
| P. canicola | 72 | Sem farpas |
| P. dollfusi | 48 | Com farpas |
| P. ehrenbergi | 102 | Com farpas[nota 1] |
| P. gethi | 42 | Sem farpas |
| P. lauroi | 48 | Com farpas |
| P. lenti | 48 | Sem farpas |
| P. procumbens | 90 | Sem farpas |
| P. procyonis | 42 | Sem farpas |
| P. rugosus | 42 | Sem farpas |
Pachysentis é morfologicamente idêntico ao Oncicola, exceto pelo número de ganchos na probóscide. Espécies de Oncicola possuem 36 ou menos ganchos, enquanto as de Pachysentis têm mais. As probóscides das espécies de Pachysentis não são completamente esféricas e contêm de 42 a 102 ganchos dispostos em 12 fileiras longitudinais de 3 a 12 ganchos cada. Dependendo da espécie, as fileiras podem ser regulares ou irregulares, alternadas ou retas. Os ganchos possuem pontas com ou sem farpas, e os maiores têm cabeças complexas (manúbrios) e raízes, enquanto os espinhos restantes não têm raízes. O tronco é cerca de duas vezes mais longo que largo, com a metade anterior geralmente mais larga que a posterior. Os testículos estão em tandem, com pelo menos um localizado antes da metade do verme. Há oito glândulas de cimento dispostas de forma compacta, cada uma com um núcleo gigante único, usadas para fechar temporariamente a extremidade posterior da fêmea após a cópula.[8][9] Os ovos possuem uma membrana externa esculpida. As espécies podem ser distinguidas pelo número e disposição dos ganchos na probóscide, presença de farpas, arranjo das glândulas de cimento, hospedeiro e comprimento dos lemniscos (feixes de fibras nervosas sensoriais).[1]
| Medidas das fêmeas (mm)[1] | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| Medidas[nota 2] | P. angolensis | P. canicola | P. dollfusi | P. ehrenbergi | P. gethi | P. lauroi | P. lenti | P. procumbens[nota 3] | P. procyonis | P. rugosus | |
| Comprimento da probóscide | 0,55–0,63 | 0,57–0,80 | ? | 0,8 | 0,583 | 0,68 | 0,63 | 0,55 | 0,697 | 0,564 | |
| Largura da probóscide | 0,70–0,82 | 0,57–0,85 | ? | 0,9 | 0,794 | 0,76 | 0,664 | 0,55 | 0,716 | 0,694 | |
| Comprimento do receptáculo da probóscide | 1,5 | 2 | ? | 1,3 | 1,07 | 1,16 | 1,32 | 1,2 | 1,37 | 1,24 | |
| Largura do receptáculo da probóscide | ? | ? | ? | ? | 0,498 | 0,47 | ? | ? | 0,531 | 0,481 | |
| Comprimento do tronco | 34–48 | 20–26 | 50 | 26–29 | 15–25 | 12,07 | 20–25 | 6 | 25–35 | 32 | |
| Largura do tronco | 4,8–5,5 | 5–11 | 4 | 6 | 1,5–3 | 1,62 | 2–2,5 | 1,25 | 2–3 | 3 | |
| Comprimento do lemnisco | 5,8–6 | 7 | 4,3–6,6 | 7 | 3,48 | 4,45 | 3,15 | ? | 3,64 | 4,64 | |
| Largura do lemnisco | ? | ? | ? | 0,8 | ? | ? | ? | ? | ? | ? | |
| Campânula uterina[nota 4] | ? | 3,15–8,15 | ? | ? | 5,56 | 1,19 | 1,41 | ? | 4,64 | 5,86 | |
| Tamanho dos ovos | 0,09 × 0,043 | 0,07 × 0,045 | 0,08 × 0,05 | 0,07 × 0,05 | 0,084 × 0,054 | 0,073 × 0,045 | ? | ? | 0,071 × 0,042 | ? | |
| Medidas dos machos (mm)[1] | |||||||||||
| Comprimento da probóscide | 0,55–0,63 | 0,57–0,80 | ? | 0,8 | 0,583 | 0,68 | 0,63 | 0,55 | 0,697 | 0,564 | |
| Largura da probóscide | 0,70–0,82 | 0,57–0,85 | ? | 0,9 | 0,794 | 0,76 | 0,664 | 0,55 | 0,716 | 0,694 | |
| Comprimento do receptáculo da probóscide | 1,5 | 2 | ? | 1,3 | 1,07 | 1,16 | 1,32 | 1,2 | 1,37 | 1,24 | |
| Largura do receptáculo da probóscide | ? | ? | ? | ? | 0,498 | 0,47 | ? | ? | 0,531 | 0,481 | |
| Comprimento do tronco | 17–23 | 15–28 | 50 | 25 | 10–15 × 1,0–2,5 | 9,63 | 15–20 | 6 | 20–30 | 25 | |
| Largura do tronco | 3,5–4 | 4–8 | 4 | 4 | 1,0–2,5 | 1,91 | 1,0–2,5 | 1,25 | 2–3 | 3,5 | |
| Comprimento do lemnisco | 5,8–6 | 7 | 4,3–6,6 | 7 | 3,48 | 4,45 | 3,15 | ? | 3,64 | 4,64 | |
| Largura do lemnisco | ? | ? | ? | 0,8 | ? | ? | ? | ? | ? | ? | |
| Tamanho do testículo anterior | 2–3 × 0,9 | 2 | ? | 3 | 1,40 × 0,581 | 1,15 × 0,48 | 1,76 × 0,51 | ? | 3,01 × 1,24 | 1,57 × 0,697 | |
| Tamanho do testículo posterior | 2–4,3 × 1,0 | 2 | ? | 3 | 1,40 × 0,581 | 1,27 × 0,55 | 1,82 × 0,547 | ? | 3,15 × 1,07 | 1,69 × 0,664 | |
| Dimensão do grupo de glândulas de cimento | 3 | 3 | ? | 7 | 1,54 | 0,86 × 0,56 | 2,98 | ? | 3,56 | 2,02 | |
| Comprimento do ducto ejaculatório | 2,3 | ? | ? | ? | 4,64 | 1,42 | ? | ? | 3,53 | 1,68 | |
Espécies
O gênero Pachysentis Meyer, 1931 contém onze espécies, embora P. septemserialis tenha status taxonômico incerto.[1][10][nota 5]
P. angolensis foi encontrado infestando Lupulella adusta. A probóscide possui 42 ganchos sem farpas, dispostos em 12 fileiras alternadas regularmente de três e quatro ganchos (seis fileiras de cada).[11] As oito glândulas de cimento estão organizadas em pares.[1] O nome da espécie deriva de Angola, o país onde foi descoberta.[11]
- Pachysentis canicola Meyer, 1931[2]
P. canicola foi encontrado infestando a raposa-vermelha (Vulpes vulpes) na província de Buxer, Irã,[12] o chacal-dourado (Canis aureus) também no Irã,[13] lobos-guará (Chrysocyon brachyurus) em cativeiro em um zoológico no Texas, e a doninha-fedorenta (Mephitis mephitis) encontrada nas proximidades.[3] Também foi encontrado infestando a cascavel-diamante-ocidental (Crotalus atrox).[14][15] É a espécie-tipo do gênero Pachysentis.[2] O nome da espécie canicola deriva da palavra em latim para canino, referente ao tipo de criatura (família Canidae) que esta espécie infesta.[2]
P. dollfusi foi encontrado infestando os intestinos do lêmure Eulemur fulvus em um zoológico brasileiro, mas originário da ilha de Madagascar.[16] Assim, não se sabe se o verme é originário do Brasil ou de Madagascar.[1] A probóscide possui 48 ganchos com farpas, dispostos em seis fileiras de quatro ganchos cada, seguidas por outras seis fileiras de quatro ganchos cada. As glândulas de cimento estão em pares uniformes.[1] É sinônimo de Prosthenorchis spirula Travassos 1917.[17] É nomeado em homenagem ao parasitologista Robert-Philippe Dollfus [en].[16]
- Pachysentis ehrenbergi Meyer, 1931[2]
P. ehrenbergi foi encontrado infestando a raposa-vermelha (Vulpes vulpes) no Egito e em um hospedeiro intermediário, a naja-egípcia (Naja haje). A probóscide é armada com 102 ganchos com farpas, dispostos em seis fileiras de nove ganchos cada, seguidas por seis fileiras de oito ganchos cada.[1] Foi relatado que P. ehrenbergi infesta a cavidade corporal de 5,4% de uma amostra de Trachylepis quinquetaeniata [en] na província de Quena, Egito, mas as medidas e descrição morfológica não correspondem nem à descrição original de Meyer em 1931[2] nem à reexaminação de espécimes originais por Gomes e colegas em 2019.[1] Indivíduos juvenis de P. ehrenbergi foram relatados infestando o ouriço Hemiechinus auritus no oásis de Faran, Sinai do Sul, Egito. O comprimento do tronco juvenil é relatado como 3,22–4,16 mm por 0,87–1,04 mm, o comprimento da probóscide como 0,42–0,60 mm por 0,45–0,68 mm de largura, a bainha da probóscide como 0,79–1,0 mm por 0,37–0,52 mm (enquanto as medidas fornecidas por Meyer na descrição original de 1931 são maiores, com 1,3 mm de comprimento e a probóscide medindo 0,8 mm de comprimento por 0,9 mm de largura). Os ganchos anteriores da probóscide em juvenis são relatados como grandes, de 0,078–0,086 mm de comprimento, e os ganchos posteriores menores, de 0,052–0,062 mm.[18]
P. gethi foi descrito originalmente em 1950 por Machado-Filho infestando irara (Eira barbara) no Pará e Rio de Janeiro, Brasil, mas permaneceu como o único registro até ser redescoberto em 2016 infestando o furão-pequeno (Galictis cuja), também no Rio de Janeiro, com medidas diferentes.[19] A probóscide possui 42 ganchos sem farpas, dispostos em seis fileiras de quatro ganchos seguidas por seis fileiras de três ganchos. As oito glândulas de cimento estão em pares.[1] A espécie é nomeada em homenagem ao Dr. Geth Jansen.[16]
- Pachysentis lauroi Gomes, Amin, Olifiers, Bianchi, Souza, Barbosa & Maldonado, 2019[1]
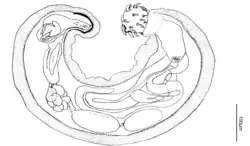
P. lauroi foi encontrado infestando o quati-de-cauda-anelada (Nasua nasua) no Mato Grosso do Sul, Brasil. A probóscide possui 48 ganchos com farpas, dispostos em seis fileiras de quatro ganchos seguidas por seis fileiras de quatro ganchos. As oito glândulas de cimento estão agrupadas. Foi encontrado no intestino delgado.[1] A espécie é nomeada em homenagem a Lauro Pereira Travassos, parasitologista que estudou acantocéfalos brasileiros.[1]
P. lenti foi encontrado infestando o sagui-de-cara-branca (Callithrix geoffroyi) no Espírito Santo, Brasil. A probóscide possui 48 ganchos sem farpas, dispostos em seis fileiras de quatro ganchos seguidas por seis fileiras de quatro ganchos.[1] É nomeado em homenagem a Herman Lent, parasitologista brasileiro.[16]
- Pachysentis procumbens Meyer, 1931[2]
P. procumbens foi encontrado infestando a raposa-vermelha (Vulpes vulpes) em Argo, Egito. A probóscide possui 90 ganchos sem farpas, dispostos em seis fileiras de sete ganchos seguidas por seis fileiras de oito ganchos.[1] O nome da espécie vem do latim procumbens, que significa "deitado prostrado".[20]
P. procyonis foi encontrado infestando os intestinos de um mão-pelada (Procyon cancrivorus) no Rio de Janeiro, Brasil.[21] A probóscide possui 42 ganchos sem farpas, dispostos em seis fileiras de quatro ganchos seguidas por seis fileiras de três ganchos. Características distintivas incluem oito glândulas de cimento agrupadas e lemniscos muito curtos que não alcançam o testículo anterior.[1] A espécie é nomeada em homenagem ao gênero do hospedeiro (Procyon) que infesta.[16] É o único parasita conhecido do mão-pelada no Brasil.[22]
P. rugosus foi encontrado infestando o intestino grosso do macaco-prego-do-papo-amarelo (Sapajus cay) e do macaco-prego-das-guianas (Sapajus apella) no Rio de Janeiro, Brasil.[23] A probóscide é armada com 42 ganchos sem farpas, dispostos em seis fileiras de quatro ganchos cada, seguidas por seis fileiras de três ganchos cada. Esta espécie pode ser identificada por suas glândulas de cimento agrupadas e lemniscos longos que alcançam o testículo anterior.[1] O nome da espécie rugosus vem do latim para "enrugado".
P. septemserialis é considerado por Gomes et al. em 2019 como tendo status taxonômico incerto devido a diferenças entre as características morfológicas dos parátipos e a descrição original, a similaridade nos hospedeiros (primatas da família Callitrichidae, incluindo o sagui-preto),[24] e a ausência de amostras ou medidas de machos adultos. Morfologicamente, novas observações por Gomes et al. em 2019 sugerem que é sinônimo de P. lenti.[1] Especificamente, a descrição original de um parátipo mencionou a ausência de um colar na base da probóscide, enquanto um colar foi observado no parátipo por Gomes et al. em 2019 (sugerindo afiliação com o gênero Prosthenorchis [en]). Uma segunda discrepância de outro parátipo é o número de ganchos; 12 fileiras longitudinais de quatro ganchos, totalizando 48 ganchos, foram observadas por Gomes et al. em 2019, mas contradizem as sete fileiras de sete ganchos, totalizando 49 ganchos, na descrição original de Machado-Filho em 1950. O nome septemserialis refere-se às sete fileiras em série.[16]
Distribuição
A distribuição das espécies de Pachysentis é determinada pela de seus hospedeiros. Espécies de Pachysentis foram encontradas na América do Sul (Brasil), África (Egito e Angola) e Ásia (Egito e Irã).[1]
Hospedeiros
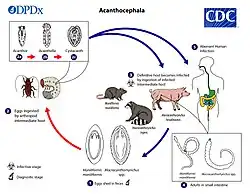
O ciclo de vida de um acantocéfalo consiste em três estágios, começando quando um acantor infeccioso (desenvolvimento de um ovo) é liberado dos intestinos do hospedeiro definitivo e, em seguida, ingerido por um artrópode, o hospedeiro intermediário. Os hospedeiros intermediários da maioria das espécies de Pachysentis não são conhecidos. Quando o acantor sofre ecdise, inicia-se o segundo estágio, chamado acantela. Este estágio envolve a penetração da parede do mesêntero ou do intestino do hospedeiro intermediário e o crescimento. O estágio final é o cistacanto infeccioso, que é o estado larval ou juvenil de um acantocéfalo, diferindo do adulto apenas em tamanho e estágio de desenvolvimento sexual. Os cistacantos dentro dos hospedeiros intermediários são consumidos pelo hospedeiro definitivo, geralmente se fixando às paredes dos intestinos, e como adultos, reproduzem-se sexualmente nos intestinos. O acantor é eliminado nas fezes do hospedeiro definitivo e o ciclo se repete.[27]
As espécies de Pachysentis parasitam exclusivamente primatas e carnívoros como hospedeiros primários.[1] Hospedeiros paratênicos (hospedeiros onde os parasitas infestam, mas não passam por desenvolvimento larval ou reprodução sexual) foram encontrados para P. ehrenbergi (naja-egípcia, Naja haje)[18] e P. canicola (cascavel-diamante-ocidental, Crotalus atrox).[15] Não há casos relatados de espécies de Pachysentis infestando humanos na literatura médica em língua inglesa.[26]
- Hospedeiros das espécies de Pachysentis
-
-_rare_sighting_of_this_nocturnal_animal_..._(13799300905).jpg) Lupulella adusta é um dos hospedeiros de P. angolensis
Lupulella adusta é um dos hospedeiros de P. angolensis -
.jpg) A raposa-vermelha é um dos hospedeiros de P. canicola e P. procumbens
A raposa-vermelha é um dos hospedeiros de P. canicola e P. procumbens -
_male.jpg) O lêmure Eulemur fulvus é um dos hospedeiros de P. dollfusi
O lêmure Eulemur fulvus é um dos hospedeiros de P. dollfusi -
 A irara é um dos hospedeiros de P. gethi
A irara é um dos hospedeiros de P. gethi -
 O quati-de-cauda-anelada é um dos hospedeiros de P. lauroi
O quati-de-cauda-anelada é um dos hospedeiros de P. lauroi -
 O sagui-de-cara-branca é um dos hospedeiros de P. lenti
O sagui-de-cara-branca é um dos hospedeiros de P. lenti -
.jpg) O mão-pelada é um dos hospedeiros de P. procyonis
O mão-pelada é um dos hospedeiros de P. procyonis -
 O macaco-prego-do-papo-amarelo é um dos hospedeiros de P. rugosus
O macaco-prego-do-papo-amarelo é um dos hospedeiros de P. rugosus -
 A cascavel-diamante-ocidental é um hospedeiro paratênico de P. canicola
A cascavel-diamante-ocidental é um hospedeiro paratênico de P. canicola -
.jpg) A naja-egípcia é um hospedeiro paratênico de P. ehrenbergi
A naja-egípcia é um hospedeiro paratênico de P. ehrenbergi
Notas
- ↑ As farpas não foram mencionadas na descrição original da espécie por Meyer (1931),[2] mas foram encontradas na reexaminação das amostras originais em 2019 por Gomes.[1]
- ↑ Um único valor para o comprimento e largura da probóscide, tamanho do receptáculo da probóscide e comprimento dos lemniscos é relatado para ambos os sexos em todas as espécies.
- ↑ Medidas são de um P. procumbens juvenil e um único valor é dado para todas as medidas para ambos os sexos.
- ↑ Uma abertura em forma de funil contínua com o útero.
- ↑ Uma autoridade binomial entre parênteses indica que a espécie foi originalmente descrita em um gênero diferente do atual.
- ↑ P. angolensis foi originalmente nomeado Oncicola angolensis por Golvan em 1957, mas foi renomeado por Schmidt em 1972.[6][5]
- ↑ P. dollfusi foi originalmente nomeado Prosthenorchis dollfusi por Machado-Filho em 1950, mas foi renomeado por Schmidt em 1972.[6][5]
- ↑ P. gethi foi originalmente nomeado Prosthenorchis gethi por Machado-Filho em 1950, mas foi renomeado por Schmidt em 1972.[6][5]
- ↑ P. lenti foi originalmente nomeado Prosthenorchis lenti por Machado-Filho em 1950, mas foi renomeado por Schmidt em 1972.[6][5]
- ↑ P. procyonis foi originalmente nomeado Prosthenorchis procyonis por Machado-Filho em 1950, mas foi renomeado por Schmidt em 1972.[6][5]
- ↑ P. rugosus foi originalmente nomeado Prosthenorchis rugosus por Machado-Filho em 1950, mas foi renomeado por Schmidt em 1972.[6][5]
- ↑ P. septemserialis foi originalmente nomeado Prosthenorchis septemserialis por Machado-Filho em 1950, mas foi renomeado por Schmidt em 1972.[6][5]
- ↑ Não há registros de infecções humanas aberrantes por espécies de Pachysentis.[26]
Referências
- ↑ a b c d e f g h i j k l m n o p q r s t u v w x y z Gomes, Ana Paula N.; Amin, Omar M.; Olifiers, Natalie; Bianchi, Rita de Cassia; Souza, Joyce G. R.; Barbosa, Helene S.; Maldonado, Arnaldo (2019). «A New Species of Pachysentis Meyer, 1931 (Acanthocephala: Oligacanthorhynchidae) in the Brown-Nosed Coati Nasua nasua (Carnivora: Procyonidae) from Brazil, with Notes on the Genus and a Key to Species». Acta Parasitologica. 64 (3): 587–595. PMC 6814649
 . PMID 31286360. doi:10.2478/s11686-019-00080-6
. PMID 31286360. doi:10.2478/s11686-019-00080-6
- ↑ a b c d e f g h i Meyer, A (1931). «Neue Acanthocephalen aus dem Berliner Museum. Burgrundung eines neue Acanthocephalen systems auf Grund einer Untersuchung der Berliner Sammlung» [New Acanthocephala from the Berlin Museum. Foundation of a new Acanthocephala system based on an investigation of the Berlin collection.]. Zoologische Jahrbücher, Abteilung für Systematik, Ökologie und Geographie der Tiere (em alemão). 62: 53–108
- ↑ a b c d Amin, Omar M.; Chaudhary, Anshu; Heckmann, Richard A.; Swenson, Julie; Singh, Hridaya S. (1 de março de 2022). «Redescription and Molecular Characterization of Pachysentis canicola Meyer, 1931 (Acanthocephala: Oligacanthorhynchidae) from the Maned Wolf, Chrysocyon brachyurus (Illiger, 1815) in Texas». Acta Parasitologica (em inglês). 67 (1): 275–287. PMID 34345996. doi:10.1007/s11686-021-00458-5. Consultado em 28 de dezembro de 2022. Cópia arquivada em 22 de julho de 2023
- ↑ Nascimento Gomes, Ana Paula; Cesário, Clarice Silva; Olifiers, Natalie; de Cassia Bianchi, Rita; Maldonado, Arnaldo; Vilela, Roberto do Val (dezembro de 2019). «New morphological and genetic data of Gigantorhynchus echinodiscus (Diesing, 1851) (Acanthocephala: Archiacanthocephala) in the giant anteater Myrmecophaga tridactyla Linnaeus, 1758 (Pilosa: Myrmecophagidae)». International Journal for Parasitology: Parasites and Wildlife. 10: 281–288. Bibcode:2019IJPPW..10..281N. PMC 6906829
 . PMID 31867208. doi:10.1016/j.ijppaw.2019.09.008
. PMID 31867208. doi:10.1016/j.ijppaw.2019.09.008
- ↑ a b c d e f g h Amin, Omar M. (19 de setembro de 2013). «Classification of the Acanthocephala». Folia Parasitologica. 60 (4): 273–305. PMID 24261131. doi:10.14411/fp.2013.031

- ↑ a b c d e f g h Schmidt, G. D. (1972). «Revision of the class Archiacanthocephala Meyer, 1931 (phylum Acanthocephala), with emphasis on Oligacanthorhynchidae Southwell et Macfie, 1925». The Journal of Parasitology. 58 (2): 290–297. JSTOR 3278091. PMID 5022866. doi:10.2307/3278091
- ↑ Amin, O.M.; Sharifdini, M.; Heckmann, R.A.; Zarean, M. (2020). «New perspectives on Nephridiacanthus major (Acanthocephala: Oligacanthorhynchidae) collected from hedgehogs in Iran». Journal of Helminthology. 94: e133. PMID 32114988. doi:10.1017/S0022149X20000073
- ↑ Bush, Albert O.; Fernández, Jacqueline C.; Esch, Gerald W.; Seed, J. Richard (2001). Parasitism: the diversity and ecology of animal parasites. Cambridge, UK New York, NY: Cambridge University Press. p. 203. ISBN 0-521-66278-8. OCLC 44131774
- ↑ Kükenthal, W (2014). Gastrotricha and Gnathifera. Göttingen, Germany: Walter de Gruyter. p. 322. ISBN 978-3110274271. Consultado em 3 de agosto de 2021. Cópia arquivada em 22 de julho de 2023
- ↑ «Oligacanthorhynchidae Petrochenko, 1956». Integrated Taxonomic Information System (ITIS). 20 de maio de 2020. Consultado em 20 de maio de 2020. Cópia arquivada em 30 de outubro de 2013
- ↑ a b c Golvan, Y. J. (1957). «Acanthocephales de l'Angola. I. Oncicola angolensis n. sp.(Archiacanthocephala-Pachysentidae), parasite du Chacal, Canis adustus Sundevall» [Acanthocephala from Angola. I. Oncicola angolensis n. sp.(Archiacanthocephala-Pachysentidae), parasite of the Jackal, Canis adustus Sundevall]. Publicacion Servicos Culturais de la Companhia de Diamantes de Angola. Meseu Dundo Lunda. (em francês). 34: 39–50
- ↑ Tavakol, Sareh; Amin, Omar M.; Luus-Powell, Wilmien J.; Halajian, Ali (22 de outubro de 2015). «The acanthocephalan fauna of Iran, a check list». Zootaxa. 4033 (2): 237–258. PMID 26624401. doi:10.11646/zootaxa.4033.2.3
- ↑ Gherman, Călin Mircea; Mihalca, Andrei Daniel (2017). «A synoptic overview of golden jackal parasites reveals high diversity of species». Parasites & Vectors. 10 (1): 419. PMC 5603039
 . PMID 28915831. doi:10.1186/s13071-017-2329-8
. PMID 28915831. doi:10.1186/s13071-017-2329-8
- ↑ Bolette, David P. (agosto de 1997). «First Record of Pachysentis canicola (Acanthocephala: Oligacanthorhynchida) and the Occurrence of Mesocestoides sp. Tetrathyridia (Cestoidea: Cyclophyllidea) in the Western Diamondback Rattlesnake, Crotalus atrox (Serpentes: Viperidae)». The Journal of Parasitology. 83 (4): 751–752. JSTOR 3284256. PMID 9267421. doi:10.2307/3284256
- ↑ a b Carbajal-Márquez, Rubén Alonso; González-Solís, David; Cedeño-Vázquez, J. Rogelio (2018). «Endoparasites of Crotalus tzabcan (Serpentes: Viperidae), with a checklist in rattlesnakes». Journal of Parasitic Diseases. 42 (2): 303–314. PMC 5962485
 . PMID 29844637. doi:10.1007/s12639-018-1001-3
. PMID 29844637. doi:10.1007/s12639-018-1001-3
- ↑ a b c d e f g h i j k l Machado-Filho, D.A. (1950). «Revisão do gênero Prosthenorchis Travassos, 1915 (Acanthocephala)» [Revision to the genus Prosthenorchis Travassos, 1915 (Acanthocephala)]. Memórias do Instituto Oswaldo Cruz. 48: 495–545. PMID 24539413. doi:10.1590/S0074-02761950000100020
 . Cópia arquivada em 18 de junho de 2022
. Cópia arquivada em 18 de junho de 2022
- ↑ Golvan, Y. J. (1962). «Le phylum des Acanthocephala.(Quatrieme note). La classe des Archiacanthocephala (A. Meyer 1931)» [The Acanthocephala phylum. (Fourth note). The class Archiacanthocephala (A. Meyer 1931)] (PDF). Annales de Parasitologie Humaine et Comparée (em francês). 37 (1–2): 1–72. Cópia arquivada (PDF) em 29 de janeiro de 2023
- ↑ a b Nelson, D. R.; Ward, H. L. (1966). «Acanthocephala from hedgehogs in Egypt» (PDF). Journal of the Tennessee Academy of Science. 41 (3): 101–105. Consultado em 21 de março de 2023. Cópia arquivada (PDF) em 28 de janeiro de 2023
- ↑ Muniz-Pereira, Luís C.; Corrêa, Pilar; Bueno, Cecília; Vieira, Fabiano M. (2016). «Rediscovery of Pachysentis gethi (Acanthocephala: Oligacanthorhynchidae), a parasite of wild lesser grison Galictis cuja (Carnivora: Mustelidae) from Brazil». Revista Mexicana de Biodiversidad. 87 (4): 1356–1359. doi:10.1016/j.rmb.2016.10.010

- ↑ Onions, C. T. (1972). The Shorter Oxford English Dictionary 3rd (rev.) ed. Oxford: Oxford at the Clarendon Press. 1591 páginas
- ↑ Silva, P. C. D. (2015). Estudo da Helmintofauna de Galictis cuja (Molina, 1872) (Carnivora, Mustelidae) atropelados na rodovia BR-040, no trecho entre Rio de Janeiro, RJ e Juiz de Fora, MG (Tese). Rio de Janeiro: Instituto Oswaldo Cruz. Consultado em 9 de julho de 2023. Cópia arquivada em 9 de julho de 2023
- ↑ Oliveira, Wilson Junior; Santos, Andre Luiz Quagliatto; Souza, Wilson Viotto de; Custódio, Ana Elizabeth Iannini; Lux-Hoppe, Estevam Guilherme; Rosalinski-Moraes, Fernanda (2019). «Oncicola luehei in a wild crab-eating raccoon (Procyon cancrivorus) from the Brazilian cerrado savanna». Revista de Patologia Tropical. 48 (4): 243–248. doi:10.5216/rpt.v48i4.61278
 . hdl:11449/228852
. hdl:11449/228852 . Consultado em 9 de julho de 2023. Cópia arquivada em 9 de julho de 2023
. Consultado em 9 de julho de 2023. Cópia arquivada em 9 de julho de 2023
- ↑ Corrêa, Pilar; Bueno, Cecília; Soares, Rita; Vieira, Fabiano M.; Muniz-Pereira, Luís C. (2016). «Checklist of helminth parasites of wild primates from Brazil». Revista Mexicana de Biodiversidad. 87 (3): 908–918. doi:10.1016/j.rmb.2016.03.008

- ↑ Solórzano-García, B., de León, G. P. P., Table, S. I., & Amoebozoa, P. Electronic Supplementary Material Parasites of Neotropical Primates: A Review.
- ↑ CDC’s Division of Parasitic Diseases and Malaria (11 de abril de 2019). «Acanthocephaliasis». www.cdc.gov. Center for Disease Control. Consultado em 17 de julho de 2023. Cópia arquivada em 8 de junho de 2023
- ↑ a b Mathison, BA; et al. (2021). «Human Acanthocephaliasis: a Thorn in the Side of Parasite Diagnostics». J Clin Microbiol. 59 (11): e02691-20. PMC 8525584
 . PMID 34076470. doi:10.1128/JCM.02691-20
. PMID 34076470. doi:10.1128/JCM.02691-20
- ↑ Schmidt, G.D. (1985). «Development and life cycles». In: Crompton, D.W.T.; Nickol, B.B. Biology of the Acanthocephala (PDF). Cambridge: Cambridge Univ. Press. pp. 273–305. Consultado em 17 de julho de 2023. Cópia arquivada (PDF) em 22 de julho de 2023
![Probóscide de P. lenti[1]](./_assets_/0c70a452f799bfe840676ee341124611/Pachysentis_lenti.jpg)