Microarranjo de proteínas
Microarranjo de proteínas (em inglês: protein microarray) é uma técnica de larga escala usada para rastrear as interações e atividade de proteínas e determinar a sua função.[1] A sua principal vantagem reside no facto de ser possível rastrear em simultâneo uma grande quantidade de proteínas. A técnica consiste em ligar um conjunto (microarranjo) de proteínas a uma superfície de suporte, como uma lâmina de vidro ou membrana de nitrocelulose.[2] São então acrescentadas a esse conjunto moléculas-sonda, geralmente etiquetadas com pigmento fluorescente. Qualquer reação entre a sonda e uma proteína imóvel emite um sinal fluorescente, o qual é lido por varrimento laser.[3] Os microarranjos de proteínas são rápidos, automatizados, económicos e extremamente sensíveis, consumindo pequenas quantidades de amostras e reagentes.[4]
Motivação para o desenvolvimento
Os microarranjos proteicos foram desenvolvidos devido às limitações da utilização de microarranjos de ADN para determinar os níveis de expressão genética em proteómica. As quantidades de mRNA na célula não refletem, muitas vezes, os níveis de expressão das proteínas a que correspondem. Como é geralmente a proteína e não o mRNA que tem o papel funcional na resposta da célula, teve de ser utilizada uma nova estratégia focada nas proteínas. Além disso, as modificações pós-traducionais, que são geralmente críticas para determinar a função proteica, não são visíveis nos microarranjos de ADN.[5] Os microarranjos proteicos substituem as técnicas tradicionais de proteómica, como a eletroforese em gel bidimensional ou a cromatografia, que consomem muito tempo e trabalho e não são as mais adequadas para analisar proteínas de baixa abundância.
Construção de matrizes
As proteínas são colocadas numa superfície sólida, como uma lâmina de microscópio, membranas, esferas ou placas de microtitulação. A função desta superfície é fornecer um suporte no qual as proteínas podem ser imobilizadas. Esta deve ter propriedades de ligação máximas, mantendo a conformação nativa da proteína para que as suas capacidades de ligação à molécula sejam preservadas. As lâminas feitas de vidro ou silicone são amplamente utilizadas porque são compatíveis com os posicionadores de proteínas robóticos comuns e os scanners laser que foram desenvolvidos para a tecnologia de microarranjos de ADN. As folhas de filme de nitrocelulose são o substrato mais amplamente aceite com a maior capacidade de ligação para proteínas em aplicações de microarranjos de proteínas.
A superfície sólida escolhida é então coberta com um revestimento que deve desempenhar simultaneamente as funções de imobilizar a proteína, impedindo a sua desnaturação, orientá-la na direção apropriada para que os locais de ligação sejam acessíveis e proporcionar um ambiente hidrofílico no qual a reação de ligação pode ocorrer. Além disso, também necessita de apresentar uma capacidade de ligação não específica tão baixa quanto possível para minimizar o ruído de fundo no sistema de deteção. Além disso, deve ser compatível com diferentes sistemas de deteção. Os agentes imobilizadores incluem camadas de alumínio ou ouro, polímeros hidrófilos e géis de poliacrilamida, ou tratamentos com aminas, aldeídos ou epóxis. As tecnologias de película fina, como a deposição física de vapor (PVD) e a deposição química de vapor (CVD), são utilizadas para aplicar o revestimento à superfície de suporte.
Um meio aquoso é essencial em todas as etapas da fabricação de microarranjos e para operar de forma a evitar a desnaturação das proteínas. Por conseguinte, os tampões de amostra devem ser cuidadosamente regulados para conter uma elevada percentagem de glicerol (para diminuir o ponto de congelação) e a humidade do ambiente de fabrico. Os micropoços têm a dupla vantagem de proporcionar um meio aquoso e, ao mesmo tempo, evitar a contaminação cruzada entre amostras.
No tipo mais comum de matriz proteica, os robôs colocam grandes quantidades de proteínas ou dos seus ligantes num suporte sólido coberto com um padrão predefinido. Isto é conhecido como impressão de contacto robótica ou deteção robótica. Outro método de fabrico é a impressão "jato de tinta", um método que não faz contacto direto e se deposita apenas quando necessário para dispersar polímeros proteicos na superfície sólida no padrão desejado.[6] A deteção piezoelétrica é um método semelhante para esta impressão a jato de tinta. A cabeça de impressão move-se através da matriz e, em cada ponto, utiliza estimulação elétrica para depositar moléculas de proteína na superfície através de pequenos jatos. É também um processo sem contacto direto com a matriz.[7] Fotolitografia é o quarto método para organizar as proteínas na superfície. A luz é utilizada em associação com fotomáscaras, placas opacas com orifícios ou transparências que permitem que a luz brilhe num padrão definido. De seguida, uma série de tratamentos químicos permite que a proteína seja depositada com o padrão desejado no material sob a fotomáscara.[8]
As moléculas de captura dispostas na superfície sólida podem ser anticorpos, antigénios, aptâmeros (ligantes baseados em ácidos nucleicos), affibody (ou Affibodies, pequenas moléculas preparadas por engenharia para imitar anticorpos monoclonais) ou proteínas inteiras. As fontes destas proteínas incluem sistemas de expressão baseados em células para proteínas recombinantes, purificação de fontes naturais, produção in vitro por sistemas de tradução livres de células e métodos de síntese para peptídeos. Muitos destes métodos podem ser automatizados para produção de alto rendimento, mas é necessário ter cuidado para evitar condições de síntese ou extração que resultem na desnaturação das proteínas, que deixariam de ser capazes de reconhecer a molécula à qual se devem ligar, o que tornaria a matriz inútil.
As proteínas são muito sensíveis a alterações no seu microambiente. Isto representa um desafio na manutenção de matrizes proteicas em condições estáveis durante longos períodos de tempo. Os métodos in situ, inventados e publicados por Mingyue He e Michael Taussig em 2001,[9][10] envolvem a síntese de proteínas no chip, conforme e quando forem necessárias, diretamente a partir do DNA que as codifica, utilizando sistemas de expressão de proteínas livres de células. Como o ADN é uma molécula muito estável, não se deteriora com o tempo e, por isso, é muito adequado para o armazenamento a longo prazo. Esta abordagem é também vantajosa porque evita os processos trabalhosos e muitas vezes dispendiosos de purificação separada de proteínas e clonagem de ADN, uma vez que as proteínas são produzidas e imobilizadas simultaneamente numa única etapa na superfície do chip. Exemplos de técnicas in situ de arranjos de proteínas sem células são: PISA (arranjo de proteínas in situ), NAPPA (arranjo de proteínas programável de ácidos nucleicos) e DAPA (arranjo de ADN para arranjo de proteínas).
Tipos de matrizes
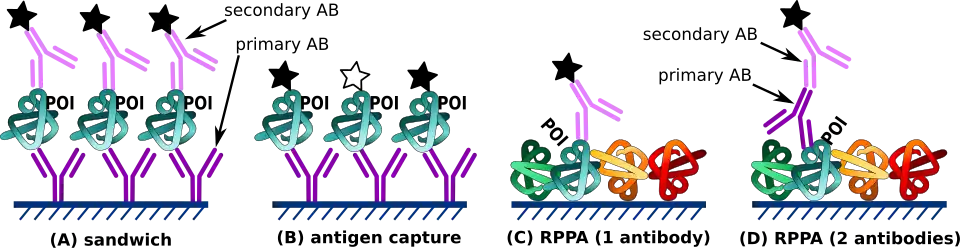
Existem três tipos de microarranjos proteicos utilizados atualmente para estudar as atividades bioquímicas das proteínas.
Os microarranjos analíticos são também conhecidos como arrays de captura. Nesta técnica, uma biblioteca de anticorpos, aptâmeros ou affibodies (Affibodies) são colocados na superfície de suporte. São utilizados para capturar moléculas, uma vez que cada uma se liga especificamente a uma determinada proteína. A matriz é sondada com uma solução proteica complexa, como um lisado celular. A análise das reações de ligação resultantes produzidas utilizando vários sistemas de deteção pode fornecer informações sobre os níveis de expressão de determinadas proteínas na amostra, bem como medições de afinidades e especificidades de ligação. Este tipo de microarranjos é especialmente útil para comparar a expressão proteica em diferentes soluções. Por exemplo, a resposta das células a um determinado fator pode ser identificada através da comparação de lisados de células tratadas com substâncias específicas ou cultivadas em determinadas condições com lisados de células de controlo. Outra aplicação é na identificação e no perfil de tecidos doentes.
O microarranjo de proteínas de fase reversa (RPPA) requer a utilização de amostras complexas, como lisados de tecido. As células são isoladas de vários tecidos de interesse e lisadas. Os lisados são colocados no microarranjo e testados com anticorpos contra a proteína alvo de interesse. Estes anticorpos são normalmente detetados com ensaios de quimioluminescência, fluorescente ou colorimétrico. Os peptídeos de referência são impressos em lâminas para que a proteína nos lisados da amostra possa ser quantificada. As matrizes de fase reversa (RPA) permitem a determinação da presença de proteínas alteradas ou outros agentes que podem ser resultado de doenças. Especificamente, as modificações pós-traducionais, que são normalmente alteradas como resultado de doenças, podem ser detetadas utilizando matrizes de fase reversa.[11]
Microarranjos de proteínas funcionais
Os microarranjos de proteínas funcionais (também designados por arranjos de proteínas alvo) são construídos pela imobilização de grandes quantidades de proteínas purificadas e são utilizados para identificar interações proteína-proteína, proteína-DNA, proteína-RNA, proteína-fosfolípido e proteína-molécula pequena, para realizar ensaios de atividade de enzima e para detetar anticorpos e demonstrar as suas especificidades. Diferem das matrizes analíticas porque as matrizes de proteínas funcionais são compostas por matrizes contendo proteínas funcionais completas ou domínios proteicos. Estes chips de proteína são utilizados para estudar as atividades bioquímicas de todo o proteoma numa única experiência.
O elemento-chave em qualquer ensaio baseado em microarranjos de proteínas funcionais é que as proteínas do arranjo devem manter a sua estrutura nativa, de modo a que possam ocorrer interações funcionais significativas na superfície do arranjo. As vantagens de controlar o modo preciso de ligação da superfície através da utilização de uma etiqueta de afinidade apropriada são que as proteínas imobilizadas terão uma orientação homogénea, resultando numa maior atividade específica e numa maior relação sinal-ruído nos ensaios, com menos interferência de interações não específicas.[12][13]
Detecção
Os métodos de deteção de matrizes de proteínas devem fornecer um sinal alto e um ruído de fundo baixo. O método mais comum e amplamente utilizado para a deteção é a marcação fluorescente, que é altamente sensível, segura e compatível com os scanners laser de microarranjos disponíveis. Podem ser utilizados outros marcadores, como marcadores de afinidade, fotoquímicos ou radioisótopos. Estas marcas estão fixas na própria sonda e podem interferir com a reação entre a sonda e a proteína alvo. No entanto, também estão disponíveis vários métodos de deteção sem etiqueta, como a ressonância plasmónica de superfície (SPR), nanotubos de carbono, sensores de nanofios de carbono (onde a deteção ocorre por alterações na condutância) e suportes de sistemas microeletromecânicos (MEMS). Todos estes métodos de deteção sem etiqueta são relativamente novos e ainda não estão disponíveis para a deteção de proteínas de alto rendimento; no entanto, são muito promissoras para o futuro.
A quantificação de proteínas em lâminas de vidro revestidas com nitrocelulose pode utilizar deteção fluorescente infravermelho. Isto limita a interferência devido à autofluorescência da nitrocelulose nos comprimentos de onda ultravioleta utilizados nas sondas de deteção fluorescentes padrão.[14]
Aplicações
Existem cinco áreas principais nas quais as matrizes proteicas estão a ser aplicadas: diagnóstico, proteómica, análise funcional de proteínas, caracterização de anticorpos e desenvolvimento de tratamentos médicos.
Fazer um diagnóstico implica, por vezes, detetar antigénios e anticorpos em amostras de sangue; o perfil dos soros para descobrir biomarcadores de novas doenças; a monitorização de estados de doença e respostas a terapêuticas na medicina personalizada; a monitorização de ambientes e alimentos. O bioensaio digital é um exemplo de utilização de microarranjos de proteínas para fazer diagnósticos. Nesta tecnologia, uma matriz de micropoços num chip de cristal/polímero é semeada com esferas magnéticas (revestidas com anticorpos marcados fluorescentemente), submetidas a antigénios alvo e depois caracterizadas ao microscópio pela contagem de poços fluorescentes. Uma plataforma de fabrico económica (utilizando polímeros OSTE) para tais matrizes de micropoços foi recentemente apresentada e o sistema de bioensaio modelo foi caracterizado com sucesso.[15]
A proteómica trata do perfil de expressão proteica, ou seja, quais as proteínas que são expressas no lisado de uma determinada célula.
A análise funcional de proteínas é a identificação de interações proteína-proteína (por exemplo, identificação de membros de um complexo proteico), interações proteína-fosfolípido, alvos de pequenas moléculas, substratos enzimáticos (particularmente substratos de cinases) e ligantes de recetores.
A caracterização dos anticorpos é feita através do estudo da reatividade cruzada, especificidade e mapeamento de epítopos.
O desenvolvimento de tratamentos médicos envolve o desenvolvimento de terapias específicas de antigénio para autoimunidade, cancro e alergias, e a identificação de alvos de pequenas moléculas que poderiam ser potencialmente utilizados como novos fármacos.
Desafios
Apesar dos consideráveis investimentos feitos por várias empresas, os chips de proteína ainda não inundaram o mercado. Os fabricantes descobriram que as proteínas são, na verdade, difíceis de manusear. A produção de proteínas fiáveis, consistentes e de alto rendimento, corretamente dobradas e funcionais, está repleta de dificuldades. Um chip de proteína requer muito mais passos para ser criado do que um chip de ADN.
Existem várias estratégias para abordar este problema, que diferem fundamentalmente se as proteínas são imobilizadas através de interações não específicas mal definidas ou por um conjunto específico de interações conhecidas. Esta última estratégia é atraente pela sua simplicidade e é compatível com proteínas purificadas derivadas de fontes nativas e recombinantes.[16][17] mas apresenta vários riscos. A mais notável delas está relacionada com a natureza descontrolada das interações entre cada proteína e a superfície; na melhor das hipóteses, isto poderia resultar numa população heterogénea de proteínas em que os sítios activos são por vezes ocluídos pela superfície e, na pior das hipóteses, poderia destruir a actividade inteiramente devido ao desdobramento parcial ou completo mediado pela superfície da proteína imobilizada.
Os principais desafios desta tecnologia são: 1) encontrar uma superfície e um método de adesão à mesma que permita às proteínas manter as suas estruturas secundária e terciária e, portanto, a sua atividade biológica e as suas interações com outras moléculas, 2) produzir uma matriz com uma longa vida útil ou prazo de validade para que as proteínas no chip não se desnaturem em pouco tempo, 3) identificar e isolar anticorpos ou outras moléculas de captura contra cada proteína do genoma humano, 4) quantificar os níveis de proteína ligada garantindo a sensibilidade e evitando o ruído de fundo, 5) extrair a proteína detetada do chip para análise posterior, 6) reduzir as ligações não específicas com os agentes de captura, 7) a capacidade do chip deve ser suficiente para permitir a visualização de uma representação do proteoma o mais completa possível; As proteínas abundantes obscurecem a deteção de proteínas menos abundantes, como as moléculas de sinalização e os recetores (bioquímica), que são geralmente de maior interesse terapêutico.[18]
Notas
Referências
- ↑ Lisa Melton (6 de maio de 2004). «Protein arrays: Proteomics in multiplex». Nature (429): 101-107. doi:10.1038/429101a
- ↑ «Protein Arrays». Functionalgenomics.org.uk
- ↑ «Rediscovering Biology - Online Textbook: Unit 2 Proteins & Proteomics». Learner.org
- ↑ «A Perspective on Microarrays» (PDF)
- ↑ Talapatra, Anupam; Rouse, Richard; Hardiman, Gary (2002). «Protein microarrays: challenges and promises». Pharmacogenomics. 3 (4): 527–536. ISSN 1462-2416. PMID 12164775. doi:10.1517/14622416.3.4.527
- ↑ Calvert, Paul (2001). «Inkjet Printing for Materials and Devices». Chemistry of Materials. 13 (10): 3299–3305. ISSN 0897-4756. doi:10.1021/cm0101632
- ↑ «DNA Microarrays: Techniques». Arabidopsis.info. Consultado em 19 de janeiro de 2013. Arquivado do original em 28 de agosto de 2008
- ↑ Shin, DS; Kim, DH; Chung, WJ; Lee, YS (30 de setembro de 2005). «Combinatorial solid phase peptide synthesis and bioassays.». Journal of Biochemistry and Molecular Biology. 38 (5): 517–25. PMID 16202229. doi:10.5483/bmbrep.2005.38.5.517
- ↑ US patent 7674752, Mingyue He & Michael John Taussig, "Functional protein arrays", published 2004-08-15, issued 2010-03-10, assigned to Discema Limited
- ↑ He, M; Taussig, MJ (xuño de 2001). «Single step generation of protein arrays from DNA by cell-free expression and in situ immobilisation (PISA method).». Nucleic Acids Research. 29 (15): E73–3. PMC 55838
 . PMID 11470888. doi:10.1093/nar/29.15.e73 Verifique data em:
. PMID 11470888. doi:10.1093/nar/29.15.e73 Verifique data em: |data=(ajuda) - ↑ Hall, DA; Ptacek, J; Snyder, M (2007). «Protein microarray technology». Mech. Ageing Dev. 128 (1): 161–7. PMC 1828913
 . PMID 17126887. doi:10.1016/j.mad.2006.11.021
. PMID 17126887. doi:10.1016/j.mad.2006.11.021
- ↑ Koopmann, JO; Blackburn, J (2003). «High affinity capture surface for matrix-assisted laser desorption/ionisation compatible protein microarrays.». Rapid Communications in Mass Spectrometry. 17 (5): 455–62. PMID 12590394. doi:10.1002/rcm.928
- ↑ Blackburn, JM; Shoko, A; Beeton-Kempen, N (2012). «Miniaturized, microarray-based assays for chemical proteomic studies of protein function». Methods in Molecular Biology. 800: 133–62. ISBN 978-1-61779-348-6. PMID 21964787. doi:10.1007/978-1-61779-349-3_10
- ↑ Williams, Richard J.; Narayanan, Narasimhachari.; Casay, Guillermo A.; Lipowska, Malgorzata.; Peralta, Jose Mauro.; Tsang, Victor C. W.; Strekowski, Lucjan.; Patonay, Gabor. (1994). «Instrument To Detect Near-Infrared Fluorescence in Solid-Phase Immunoassay». Analytical Chemistry. 66 (19): 3102–3107. ISSN 0003-2700. doi:10.1021/ac00091a018
- ↑ Decrop, Deborah (2017). «Single-Step Imprinting of Femtoliter Microwell Arrays Allows Digital Bioassays with Attomolar Limit of Detection». ACS Applied Materials & Interfaces. 9 (12): 10418–10426. PMID 28266828. doi:10.1021/acsami.6b15415
- ↑ MacBeath, G; Schreiber, SL (8 de setembro de 2000). «Printing proteins as microarrays for high-throughput function determination». Science. 289 (5485): 1760–3. PMID 10976071. doi:10.1126/science.289.5485.1760 (inativo 13 de outubro de 2018)
- ↑ Angenendt, P; Glökler, J; Sobek, J; Lehrach, H; Cahill, DJ (15 de agosto de 2003). «Next generation of protein microarray support materials: evaluation for protein and antibody microarray applications.». Journal of Chromatography A. 1009 (1–2): 97–104. PMID 13677649. doi:10.1016/s0021-9673(03)00769-6
- ↑ Fung, Eric T; Thulasiraman, Vanitha; Weinberger, Scot R; Dalmasso, Enrique A (2001). «Protein biochips for differential profiling». Current Opinion in Biotechnology. 12 (1): 65–69. ISSN 0958-1669. doi:10.1016/S0958-1669(00)00167-1
Ver também
Outros artigos
- ELISA
- Microarranjo de anticorpos
- microarranjo de ADN
- Microarranjo de Tecido
- Microarranjo de compostos químicos