Imunoeletroforese
A imunoeletroforese é uma técnica de imunoprecipitação, que combina eletroforese e imunodifusão radial em meio gelificado, em tempos distintos, mas com alto poder de resolução. Esse método tem a capacidade de comparar e evidenciar frações antigênicas que são separadas em geral, em gel de galactose, sob influência de um campo elétrico; Entretanto, apesar de que moléculas podem apresentar cargas elétricas próximas, a técnica junta-as em pontos próximos para a migração eletroforética.[1][2]

A imunoelectroforese é um nome geral aplicado a vários métodos bioquímicos para a separação e a caracterização de proteínas baseados na electroforese e na reação com anticorpos. Todas as variantes de imunoelectroforese requerem imunoglobulinas (anticorpos), que reagem com as proteínas para que sejam separadas ou caracterizadas. Os métodos foram desenvolvidos e usados extensivamente durante a segunda metade do século XX. Por ordem quase cronológica, apareceram os seguintes métodos: análise imunoelectroforética (imunoelectroforese unidimensional ad modum Grabar), imunoelectroforese cruzada (imunoelectroforese quantitativa bidimensional ad modum Clarke e Freeman ou ad modum Laurell), imunoelectroforese foguete (imunoelectroforese quantitativa unidimensional ad modum Laurell), imunoelectroforese foguete fundido ad modum Svendsen e Harboe, imunoelectroforese de afinidade ad modum Bøg-Hansen.
A agarose em lâminas de gel a 1% de aproximadamente 1 mm de espessura, tamponadas a alto pH (cerca de 8,6) é o material tradicionalmente preferido para a electroforese com reação com anticorpos. A agarose foi escolhida como matriz do gel porque tem poros grandes que permitem a livre passagem e separação das proteínas, mas proporciona ao mesmo tempo uma âncora para os imunoprecipitados de proteínas e anticorpos específicos. É realizada a um pH alto porque os anticorpos são praticamente imóveis a pH alto. Recomenda-se geralmente um equipamento de electroforese com uma placa de arrefecimento horizontal. Os imunoprecipitados podem ser observados no gel de agarose húmido, mas são corados com corantes para as proteínas, como o Azul Brilhante Coomassie, no gel seco. Em contraste com a SDS-electroforese em gel, a electroforese em agarose permite manter as condições nativas, conservando a estrutura nativa e as atividades das proteínas em investigação, portanto, a imunoelectroforese permite a caracterização de atividades enzimáticas, de ligação a ligandos, etc., para além da separação electroforética.
Tipos
A análise imunoelectroforética ad modum Grabar é o método clássico de imunoelectroforese. As proteínas são separadas por electroforese, depois os anticorpos são aplicados num sulco próximo às proteínas separadas e formam-se imunoprecipitados após um período de difusão das proteínas separadas e anticorpos. A introdução da análise imunoelectroforética deu um grande impulso à química de proteínas, e alguns dos primeiros resultados foram a resolução de proteínas em fluídos biológicos e extratos biológicos. Entre as importantes observações feitas estiveram a caracterização do grande número de proteínas diferentes do soro, a existência de várias classes de imunoglobulinas e a sua heterogeneidade electroforética.

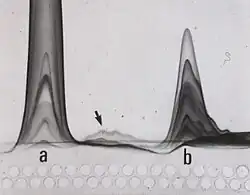
A imunoelectroforese cruzada também se chama imunoelectroforese quantitativa bidimensional ad modum Clarke e Freeman ou ad modum Laurell. Neste método as proteínas são primeiramente separadas durante a electroforese de primeira dimensão, depois em vez da difusão em direção aos anticorpos, as proteínas são submetidas a electroforese num gel que contém anticorpos na segunda dimensão. A imunoprecipitação terá lugar durante a electroforese de segunda dimensão e os imunoprecipitados têm uma característica forma de sino, na qual cada precipitado representa um antigénio; a posição dos precipitados é dependente da quantidade das proteínas, bem como da quantidade de anticorpos específicos no gel, pelo que se pode realizar a quantificação relativa. A sensibilidade e o poder de resolução da imunoelectroforese cruzada é como o da análise imunoelectroforética clássica e há múltiplas variações da técnica úteis para vários propósitos. A imunoelectroforese cruzada foi utilizada para estudos de proteínas em fluídos biológicos, particularmente no soro humano, e extratos biológicos.
A imunoelectroforese foguete é uma imunoelectroforese quantitativa unidimensional. O método foi utilizado para a quantificação de proteínas do soro humano antes do aparecimento dos métodos automatizados.
A imunoelectroforese foguete fundida é uma modificação de uma imunoelectroforese quantitativa unidimensional usada para uma medida detalhada de proteínas em frações procedentes dos experimentos de separação de proteínas.
A imunoelectroforese de afinidade está baseada em mudanças no padrão electroforético de proteínas por meio de interações específicas ou formação de complexos com outras macromoléculas ou ligandos. A imunoelectroforese de afinidade foi utilizada para a estimativa das constantes de ligação, como por exemplo com as lectinas ou a caracterização de proteínas com características específicas, como conter glicanos ou ligação a ligandos. Algumas variantes da imunoelectroforese de afinidade são semelhantes à cromatografia de afinidade no uso de ligandos imobilizados. A estrutura aberta do imunoprecipitado no gel de agarose permite a ligação adicional de anticorpos marcados radioativamente para revelar proteínas específicas. Esta variação foi utilizada para a identificação de alergias por reação com IgE.
Uso atual
Dois fatores determinam que os métodos imunoelectroforéticos não se utilizem amplamente. O primeiro é que dão muito trabalho e requerem certa perícia manual. O segundo é que necessitam de quantidades bastante grandes de anticorpos policlonais. Hoje, a electroforese em gel seguida de electroblotting é o método preferido para a caracterização de proteínas devido à sua facilidade de operação, a sua alta sensibilidade e o seu baixo requerimento de anticorpos específicos. Além disso, as proteínas são separadas por electroforese em gel baseando-se no seu peso molecular aparente, o que não é realizado por imunoelectroforese, mas, no entanto, os métodos imunoelectroforéticos são ainda úteis quando são necessárias condições não redutoras.
Referências
- ↑ Departamento de Microbiologia e Parasitologia (2004). Imunoeletroforese. Universidade Federal de Santa Maria.
- ↑ A. Teva, J.C.C. Fernandez, V. L. Silva. Imunologia.
- ↑ Ling IT.; Cooksley S.; Bates PA.; Hempelmann E.; Wilson RJM. (1986). «Antibodies to the glutamate dehydrogenase of Plasmodium falciparum». Parasitology. 92 (2): 313–324. PMID 3086819. doi:10.1017/S0031182000064088