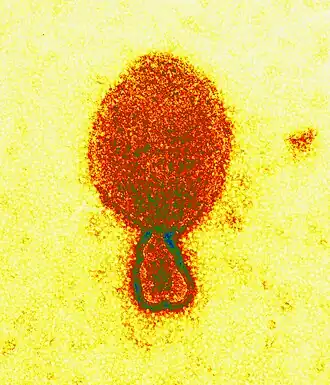
Henipavirus
Henipavírus
| |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Classificação científica | |||||||||||||||
| |||||||||||||||
Henipavírus é um gênero de vírus de RNA de fita negativa da família Paramyxoviridae, ordem Mononegavirales, contendo cinco espécies estabelecidas [1][2] e inúmeras outras ainda em estudo.[3] Os henipavírus são naturalmente encontrados em diversas espécies de pequenos mamíferos, notadamente morcegos frugívoros da família Pteropidae (raposas voadoras), micro-morcegos de várias espécies[4] e musaranhos.[5][6] Os henipavírus são caracterizados por genomas longos e uma ampla gama de hospedeiros. Seu recente surgimento como patógenos zoonóticos capazes de causar doenças e morte em animais domésticos e humanos é motivo de preocupação.[7][8]
O vírus Nipah e o vírus Hendra são ambos considerados agentes selecionados de categoria C (sobreposição USDA-HHS).[9]
Anatomia
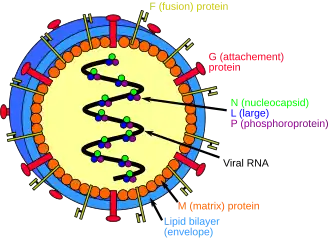
Estrutura
Os henipavírions são pleomórficos (têm formas variáveis), variando em tamanho de 40 a 600. nm de diâmetro.[10] Possuem uma membrana lipídica sobrejacente a uma camada de proteína da matriz viral. No núcleo encontra-se uma única cadeia helicoidal de RNA genômico fortemente ligada à proteína N (nucleocapsídeo) e associada às proteínas L (grande) e P (fosfoproteína), que fornecem atividade de RNA polimerase durante a replicação.
Incorporadas na membrana lipídica, encontram-se espículas de trímeros da proteína F (fusão) e tetrâmeros da proteína G (ligação). A função da proteína G é ajudar a fixação do vírus à superfície de uma célula hospedeira através da efrina B1, B2 ou B3, uma família de proteínas de mamíferos de sequência conservada.[11][12][13] A estrutura da glicoproteína de ligação foi determinada por cristalografia de raios X.[14] A proteína F funde a membrana viral com a membrana da célula hospedeira, liberando o conteúdo do vírion na célula. Ela também faz com que as células infectadas se fundam com as células vizinhas para formar sincícios grandes e multinucleados.
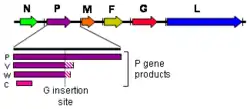
Genoma
Como todos os genomas mononegavirais, os genomas do vírus Hendra e do vírus Nipah são constituídos por uma molécula de RNA de fita simples não segmentado e de sentido negativo. Ambos os genomas têm 18,2 kb de comprimento e contêm seis genes correspondentes a seis proteínas estruturais.[15]
Assim como outros membros da família Paramyxoviridae, o número de nucleotídeos no genoma do henipavírus é um múltiplo de seis.[16][17] O desvio da regra dos seis, por meio de mutação ou síntese incompleta do genoma, leva à replicação viral ineficiente, provavelmente devido a restrições estruturais impostas pela ligação entre o RNA e a proteína N.
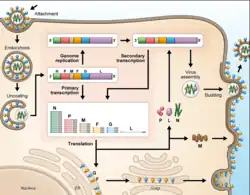
Ciclo de vida
O receptor celular efrina-B2, localizado em células epiteliais ao redor de pequenas artérias, neurônios e células musculares lisas, é o alvo da proteína viral G.[18] Uma vez que a proteína G se liga à efrina-B2, a proteína viral F facilita a fusão com a membrana da célula alvo e libera o RNA viral no citoplasma da célula hospedeira.[19] Após a entrada, ocorre a transcrição do mRNA viral usando o RNA viral como molde. Esse processo é iniciado e interrompido pelo complexo da polimerase. As proteínas virais se acumulam na célula à medida que a transcrição ocorre, até que o complexo da polimerase interrompa a transcrição e inicie a replicação do genoma. A transcrição do RNA viral produz fitas de RNA de sentido positivo, que serão usadas como moldes para produzir mais moléculas de RNA viral. A replicação do genoma é interrompida antes que as partículas virais possam se agrupar para formar um vírion. Assim que a membrana celular estiver pronta, novos vírions saem da célula hospedeira por brotamento.[20]
Surgimento
O surgimento dos henipavírus acompanha o surgimento de outros vírus zoonóticos nas últimas décadas. O SARS-CoV-2, o lyssavirus, o vírus Menangle, o vírus de Marburg, e possivelmente vírus Ebola também foram encontrados em morcegos e apresentam potencial de infecção a outras espécies. O surgimento de cada um desses vírus foi associado a um aumento do contato entre morcegos e humanos, às vezes envolvendo um hospedeiro doméstico intermediário.[21]
Evidências constatam que a perda de habitat para raposas-voadoras, tanto no sul da Ásia quanto na Austrália (principalmente na costa leste), bem como a invasão de habitações humanas e da agricultura nos habitats restantes, está criando uma maior sobreposição das distribuições de humanos e raposas voadoras.[22]
Vacina
Os henipavírus apresentam altas taxas de mortalidade em hospedeiros mamíferos, tanto humanos quanto animais. Devido a isso, há necessidade de imunização contra o VHE e o VNI. A Organização Mundial da Saúde classificou os agentes henipavirais como Patógenos Prioritários do Plano de P&D, indicando que representam um risco significativo devido ao seu potencial epidêmico.[23] O amplo tropismo de espécies do VNI e do VHE resultou em mortalidade em animais de criação, além de humanos, e, como consequência, vacinas veterinárias estão em vários estágios de desenvolvimento ou licenciamento. A EquiVac HeV, uma vacina veterinária para cavalos, foi licenciada na Austrália em 2012.[24][25] Diversas vacinas experimentais desenvolvidas para humanos estão em fase pré-clínica de desenvolvimento, mas nenhuma foi licenciada ainda. Uma vacina solúvel de glicoproteína de ligação ao VHE, desenvolvida para proteger contra o VNI, concluiu um ensaio clínico de fase I em novembro de 2022, mas os resultados ainda não foram publicados.[26]
Referências
- ↑ Rima, B; Balkema-Buschmann, A; Dundon, WG; Duprex, WP; Easton, A; Fouchier, R; Kurath, G; Lamb, R; Lee, B (Dezembro de 2019). «ICTV Virus Taxonomy Profile: Paramyxoviridae.». The Journal of General Virology. 100 (12): 1593–1594. PMC 7273325
 . PMID 31609197. doi:10.1099/jgv.0.001328
. PMID 31609197. doi:10.1099/jgv.0.001328
- ↑ «Family: Paramyxoviridae | ICTV». ictv.global
- ↑ Wu, Zhiqiang; et al. (2014). «Novel Henipa-like Virus, Mojiang Paramyxovirus, in Rats, China, 2012». Emerging Infectious Diseases. 20 (6): 1064–1066. PMC 4036791
 . PMID 24865545. doi:10.3201/eid2006.131022
. PMID 24865545. doi:10.3201/eid2006.131022
- ↑ Li, Y; Wang, J; Hickey, AC; Zhang, Y; Li, Y; Wu, Y; Zhang, Huajun; et al. (Dezembro de 2008). «Antibodies to Nipah or Nipah-like viruses in bats, China [letter]». Emerging Infectious Diseases. 14 (12): 1974–1976. PMC 2634619
 . PMID 19046545. doi:10.3201/eid1412.080359
. PMID 19046545. doi:10.3201/eid1412.080359
- ↑ Cheng, Amy (10 de agosto de 2022). «New Langya virus that may have spilled over from animals infects dozens». The Washington Post
- ↑ Zhang, Xiao-Ai; et al. (2022). «A Zoonotic Henipavirus in Febrile Patients in China». The New England Journal of Medicine. 387 (5): 470–472. PMID 35921459. doi:10.1056/NEJMc2202705

- ↑ Sawatsky (2008). «Hendra and Nipah Virus». Animal Viruses: Molecular Biology. [S.l.]: Caister Academic Press. ISBN 978-1-904455-22-6
- ↑ «Nipah yet to be confirmed, 86 under observation: Shailaja». OnManorama (em inglês). Consultado em 4 de junho de 2019
- ↑ Rima, B; Balkema-Buschmann, A; Dundon, WG; Duprex, WP; Easton, A; Fouchier, R; Kurath, G; Lamb, R; Lee, B (Dezembro de 2019). «ICTV Virus Taxonomy Profile: Paramyxoviridae.». The Journal of General Virology. 100 (12): 1593–1594. PMC 7273325
 . PMID 31609197. doi:10.1099/jgv.0.001328
. PMID 31609197. doi:10.1099/jgv.0.001328
- ↑ Hyatt AD, Zaki SR, Goldsmith CS, Wise TG, Hengstberger SG (2001). «Ultrastructure of Hendra virus and Nipah virus within cultured cells and host animals». Microbes and Infection. 3 (4): 297–306. PMID 11334747. doi:10.1016/S1286-4579(01)01383-1
- ↑ Bonaparte, M; Dimitrov, A; Bossart, K (2005). «Ephrin-B2 ligand is a functional receptor for Hendra virus and Nipah virus». Proceedings of the National Academy of Sciences. 102 (30): 10652–10657. Bibcode:2005PNAS..10210652B. PMC 1169237
 . PMID 15998730. doi:10.1073/pnas.0504887102
. PMID 15998730. doi:10.1073/pnas.0504887102
- ↑ Negrete OA, Levroney EL, Aguilar HC (2005). «EphrinB2 is the entry receptor for Nipah virus, an emergent deadly paramyxovirus». Nature. 436 (7049): 401–405. Bibcode:2005Natur.436..401N. PMID 16007075. doi:10.1038/nature03838

- ↑ Rima, B; Balkema-Buschmann, A; Dundon, WG; Duprex, WP; Easton, A; Fouchier, R; Kurath, G; Lamb, R; Lee, B (Dezembro de 2019). «ICTV Virus Taxonomy Profile: Paramyxoviridae.». The Journal of General Virology. 100 (12): 1593–1594. PMC 7273325
 . PMID 31609197. doi:10.1099/jgv.0.001328
. PMID 31609197. doi:10.1099/jgv.0.001328
- ↑ «Family: Paramyxoviridae | ICTV». ictv.global
- ↑ Wang L, Harcourt BH, Yu M (2001). «Molecular biology of Hendra and Nipah viruses». Microbes and Infection. 3 (4): 279–287. PMID 11334745. doi:10.1016/S1286-4579(01)01381-8
- ↑ Rima, B; Balkema-Buschmann, A; Dundon, WG; Duprex, WP; Easton, A; Fouchier, R; Kurath, G; Lamb, R; Lee, B (Dezembro de 2019). «ICTV Virus Taxonomy Profile: Paramyxoviridae.». The Journal of General Virology. 100 (12): 1593–1594. PMC 7273325
 . PMID 31609197. doi:10.1099/jgv.0.001328
. PMID 31609197. doi:10.1099/jgv.0.001328
- ↑ «Family: Paramyxoviridae | ICTV». ictv.global
- ↑ Rima, B; Balkema-Buschmann, A; Dundon, WG; Duprex, WP; Easton, A; Fouchier, R; Kurath, G; Lamb, R; Lee, B (Dezembro de 2019). «ICTV Virus Taxonomy Profile: Paramyxoviridae.». The Journal of General Virology. 100 (12): 1593–1594. PMC 7273325
 . PMID 31609197. doi:10.1099/jgv.0.001328
. PMID 31609197. doi:10.1099/jgv.0.001328
- ↑ «Family: Paramyxoviridae | ICTV». ictv.global
- ↑ Li, Y; Wang, J; Hickey, AC; Zhang, Y; Li, Y; Wu, Y; Zhang, Huajun; et al. (Dezembro de 2008). «Antibodies to Nipah or Nipah-like viruses in bats, China [letter]». Emerging Infectious Diseases. 14 (12): 1974–1976. PMC 2634619
 . PMID 19046545. doi:10.3201/eid1412.080359
. PMID 19046545. doi:10.3201/eid1412.080359
- ↑ Rima, B; Balkema-Buschmann, A; Dundon, WG; Duprex, WP; Easton, A; Fouchier, R; Kurath, G; Lamb, R; Lee, B (Dezembro de 2019). «ICTV Virus Taxonomy Profile: Paramyxoviridae.». The Journal of General Virology. 100 (12): 1593–1594. PMC 7273325
 . PMID 31609197. doi:10.1099/jgv.0.001328
. PMID 31609197. doi:10.1099/jgv.0.001328
- ↑ Rima, B; Balkema-Buschmann, A; Dundon, WG; Duprex, WP; Easton, A; Fouchier, R; Kurath, G; Lamb, R; Lee, B (Dezembro de 2019). «ICTV Virus Taxonomy Profile: Paramyxoviridae.». The Journal of General Virology. 100 (12): 1593–1594. PMC 7273325
 . PMID 31609197. doi:10.1099/jgv.0.001328
. PMID 31609197. doi:10.1099/jgv.0.001328
- ↑ Rima, B; Balkema-Buschmann, A; Dundon, WG; Duprex, WP; Easton, A; Fouchier, R; Kurath, G; Lamb, R; Lee, B (Dezembro de 2019). «ICTV Virus Taxonomy Profile: Paramyxoviridae.». The Journal of General Virology. 100 (12): 1593–1594. PMC 7273325
 . PMID 31609197. doi:10.1099/jgv.0.001328
. PMID 31609197. doi:10.1099/jgv.0.001328
- ↑ «Family: Paramyxoviridae | ICTV». ictv.global
- ↑ Li, Y; Wang, J; Hickey, AC; Zhang, Y; Li, Y; Wu, Y; Zhang, Huajun; et al. (Dezembro de 2008). «Antibodies to Nipah or Nipah-like viruses in bats, China [letter]». Emerging Infectious Diseases. 14 (12): 1974–1976. PMC 2634619
 . PMID 19046545. doi:10.3201/eid1412.080359
. PMID 19046545. doi:10.3201/eid1412.080359
- ↑ Cheng, Amy (10 de agosto de 2022). «New Langya virus that may have spilled over from animals infects dozens». The Washington Post
Ligações externas
- Relatório do ICTV: Paramyxoviridae
- Cartão de doença
- Zona Viral: Henipavírus
- Henipavírus – Grupo de Pesquisa em Ecologia do Henipavírus (HERG)
- Banco de Dados e Recurso de Análise de Patógenos Virais (ViPR): Paramyxoviridae