Gavião variável
Nisaetus cirrhatus
| |||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Estado de conservação | |||||||||||||||||
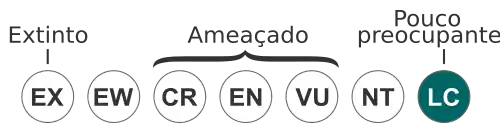 Pouco preocupante | |||||||||||||||||
| Classificação científica | |||||||||||||||||
| |||||||||||||||||
| Subespécies | |||||||||||||||||
| |||||||||||||||||
| Sinónimos | |||||||||||||||||
| |||||||||||||||||
O gavião-variável (Nisaetus cirrhatus) ou gavião-de-crista é uma espécie de grande ave de rapina da família Accipitridae. Nomes comuns em inglês mais informais ou antiquados incluem "gavião-de-pântano" ("marsh hawk-eagle") ou "gavião-de-crista-indiano" ("Indian crested hawk-eagle").[1] É membro da subfamília Aquilinae, com penas características, ausentes em raptores tropicais fora dessa subfamília, cobrindo o tarso.[2]
Anteriormente a espécie era classificada no gênero Spizaetus, mas estudos indicaram que o grupo era parafilético, resultando na transferência dos membros do Velho Mundo para Nisaetus [en], separados das espécies do Novo Mundo. É um típico "gavião-águia" por ser um predador ágil habitante de florestas, que varia facilmente sua seleção de presas entre aves, mamíferos ou répteis, além de outros vertebrados.[3]
Entre os membros de seu gênero, o gavião-variável se destaca como a espécie mais amplamente distribuída, adaptável e abundante.[1] Os indivíduos apresentam grande variação na plumagem, de clara a escura, dependendo da muda e da idade, o que originou o nome "variável".[4][5]
Taxonomia
O gavião-variável foi formalmente descrito em 1788 pelo naturalista alemão Johann Friedrich Gmelin em sua edição revisada e expandida do Systema Naturae de Carl Linnaeus. Ele o classificou com as águias, gaviões e parentes no gênero Falco e cunhou o nome binomial Falco cirrhatus.[6] A descrição de Gmelin foi baseada no "falcão indiano com crista" ou Falco Indicus cirratus, descrito pela primeira vez em 1676 pelos naturalistas ingleses Francis Willughby e John Ray a partir de uma ave viva mantida no áviário real em St James's Park, Londres.[7][8][9] O gavião-variável foi anteriormente classificado no gênero Spizaetus, mas foi transferido para o gênero ressuscitado Nisaetus após a publicação de dois estudos filogenéticos moleculares em 2005 e 2007.[10][11][12]
O gênero Nisaetus foi introduzido em 1836 pelo naturalista inglês Brian Houghton Hodgson.[13] O nome do gênero Nisaetus combina o latim medieval "nisus" para gavião com o grego antigo "aetos" que significa águia. O epíteto específico cirrhatus vem do latim cirratus, que significa "cabeça encaracolada".[14]
A taxonomia do gavião-variável, de ampla distribuição, é complexa e confusa, com poucas autoridades concordando sobre se a espécie constitui um complexo de espécies.[15] Em 2005 foi feito um estudo em que analisaram dados de sequências de mtDNA do citocromo b e da região de controle do mtDNA de um número considerável de espécimes do gavião-variável e alguns parentes. Apesar da grande amostra, mesmo a dicotomia mais conspícua - entre os grupos com e sem crista - não foi tão bem resolvida quanto esperado.[15] Pelo menos um estudo genético amplamente aceito resultou em uma revisão recente, reconhecendo uma nova espécie, já que o Nisaetus floris era tradicionalmente tratado como uma subespécie do gavião-variável, mas agora é frequentemente considerado uma espécie distinta.[16] O gavião-real e o gavião-das-flores são considerados espécies irmãs.[17]
Os três taxa de ilhas pequenas (N. c. andamanensis, N. c. vanheurni e N. floris) parecem ser linhagens monofiléticas. Sua colocação é ainda mais incerta, com N. floris sendo aparentemente uma linhagem muito antiga. Os outros dois parecem derivar de N. c. limnaeetus. Este último taxon tem uma filogenia confusa. Diferentes linhagens existem que aparentemente não são estáveis no espaço e no tempo, sendo melhor descritas como politomia, da qual os taxa insulares similares derivam.[15][17] Obviamente, N. c. limnaeetus não representa uma linhagem monofilética. Nem o conceito de espécie biológica, nem o filogenético, nem a sistemática filogenética podem ser aplicados de forma satisfatória. O grupo com crista parece estar próximo de se tornar uma espécie distinta. Os taxa insulares derivados de N. c. limnaeetus parecem ter sofrido o efeito fundador, o que restringiu sua diversidade genética. Na população continental, a diversidade genética é considerável, e o padrão evolutivo dos dois genes estudados não concordou, nem a origem dos espécimes mostrou estruturas claras. N. c. limnaeetus é, portanto, melhor considerado uma metapopulação.[15]
Gamauf e colaboradores sugeriram que os taxa insulares, que estão em maior risco de extinção, sejam considerados como unidade evolutivamente significativa para fins de biologia da conservação, independentemente de seu status sistemático. Este caso também demonstra que uma interpretação rígida demais da cladística e o desejo por taxa monofiléticos, assim como a aplicação universal de um conceito de espécie única para todas as aves, podem comprometer a compreensão correta das relações evolutivas. Não seria inconcebível encontrar linhagens continentais agrupadas com os taxa insulares ocidentais, se pouca deriva genética tivesse ocorrido na população inicial. No entanto, a divergência das linhagens desta espécie parece ter ocorrido recentemente demais para conceder-lhes status de espécie, em comparação com o nível de divergência genética em que clados são geralmente considerados espécies distintas.
N. c. limnaeetus parece ser um conjunto basal de linhagens no grupo sem crista que, apesar de não ser monofilético, deve ser considerado um taxon válido enquanto o fluxo gênico for possível em sua distribuição. Além disso, como DNA antigo de espécimes de museu foi amplamente utilizado, a possibilidade de linhagens fantasmas deve ser considerada. Se for assumido que todas ou a maioria das linhagens antigas ainda existem hoje, uma considerável recombinação genética deve ter ocorrido, pois as filogenias dos dois genes não concordam muito, indicando um nível saudável de fluxo gênico. Se isso ainda é verdade hoje, permanece a ser determinado.[15]
Existem dois grupos distintos do gavião-variável: um com cristas e outro sem ou com cristas pouco visíveis. Um estudo de 2020 concluiu que o isolamento reprodutivo entre os dois grupos é fraco e recomendou tratá-los como coespecíficos.[18] Morfos escuros existem em algumas populações.[19]
Subespécies

Grupo do gavião-variável com crista
- N. c. cirrhatus (Gmelin, JF, 1788): A subespécie nominal é encontrada no península indiana, desde a planície Indo-Ganges ao sul, por todo o restante do país. É monomórfica em coloração, sem morfo escuro. A subespécie nominal é relativamente clara na parte superior em comparação com outras raças, com uma tonalidade ligeiramente mais ruiva na cabeça. Tende a ser menos estriada abaixo até a parte inferior do peito em comparação com outras raças, com bordas escuras nas asas e uma cauda fortemente barrada. Na plumagem juvenil, a raça nominal tem uma cabeça fortemente amarelada e partes inferiores salpicadas e manchadas. A crista tende a ser mais longa nesta raça, com medidas comuns de 10 a 14 cm de comprimento, sendo, portanto, comumente chamada de gavião-de-crista.[1][15] É uma das duas maiores subespécies. O comprimento da corda máxima varia de 405 a 442 mm em machos e de 448 a 462 mm em fêmeas. Em ambos os sexos, a cauda geralmente mede 280 a 300 mm e o tarso de 102 a 110 mm.[1]
- N. c. ceylanensis (Gmelin, JF, 1788): Esta raça é endêmica do Sri Lanka, mas algumas autoridades também incluem Travancor na ponta sul da Índia como parte de sua distribuição.[1][20] Esta raça tem uma crista proporcionalmente mais longa em média do que a raça nominal, com um comprimento de crista semelhante, cerca de 10 cm. É monomórfica como a raça nominal, sendo em média mais clara e menos estriada, mas uma aparência semelhante foi observada em aves do extremo sul da Índia. As diferenças representadas nesta raça em relação à raça nominal são em grande parte clinais. É consideravelmente menor que a raça nominal. O comprimento da corda máxima varia de 351 a 370 mm em machos e de 353 a 387 mm em fêmeas.[1][20] Além disso, em ambos os sexos, o comprimento da cauda é de 229 a 266 mm e o comprimento do tarso de 89 a 97 mm.[3][21]
Grupo do gavião-variável sem crista

- N. c. limnaeetus (Horsfield, 1821): Esta raça é encontrada nas encostas dos Himalaias desde Nepal, nordeste da Índia, passando por Myanmar até grande parte do sudeste da Ásia, incluindo a península da Malásia ao longo da linha de Wallace até as Filipinas e as Ilhas da Sonda. Esta raça pode parecer semelhante em tamanho e estrutura à raça nominal, mas, ao contrário dela, é bastante polimórfica e é a subespécie mais amplamente distribuída. O polimorfismo desta raça é a origem do nome gavião-variável.[3] O morfo claro desta raça ainda é mais escuro que a raça nominal encontrada mais ao sul na Índia. No entanto, morfos claros das Filipinas tendem a ter uma cabeça e pescoço mais claros. Caracteristicamente, esta raça é fortemente estriada abaixo, enquanto os juvenis parecem bastante diferentes, com cabeça e partes inferiores majoritariamente brancas. Indivíduos de morfo escuro tendem a ser marrom-chocolate por completo, embora a base da cauda possa parecer mais clara em voo.[1][21] Algumas aves desta raça têm uma crista vestigial de apenas 1 a 3 cm de comprimento, mas muitas parecem completamente sem crista. Esta raça é geralmente semelhante em tamanho à raça nominal, mas é mais variável em tamanho em sua grande distribuição, com as aves das ilhas mais ao sul sendo em média as menores, enquanto aquelas encontradas nas encostas dos Himalaias são possivelmente os maiores gaviões-variáveis conhecidos da espécie. O comprimento da corda máxima varia de 380 a 430 mm em machos e de 405 a 462 mm em fêmeas. Em amostras limitadas, o comprimento da cauda foi relatado como 240 a 278 mm e o comprimento do tarso de 100 a 103 mm.[22] Uma amostra de 6 fêmeas teve uma média de 37,9 mm no comprimento da garra traseira (hallux), o principal aparato de matança da maioria dos accipitrídeos, enquanto 7 machos tiveram uma média de 32,3 mm.[23]
- N. c. andamanensis (Tytler, 1865): Esta raça é encontrada nas Ilhas Andamão. A subespécie é mais escura que a subespécie nominal e mais semelhante a N. c. limnaeetus em tonalidade, mas não parece ter um morfo escuro completo como conhecido naquela raça. Juvenis tendem a ter uma cabeça e partes inferiores bastante brancas. Uma crista pode estar presente variavelmente, mas geralmente tem até 5 cm. Esta raça é pequena, um pouco menor que N. c. ceylanensis. O comprimento da corda máxima varia de 330 a 375 mm em machos e de 358 a 377 mm em fêmeas.[1][21]
- N. c. vanheurni (Junge, 1936): Esta raça é nativa da ilha Simeulue. É semelhante em aparência a N. c. limnaeetus, mas não parece possuir um morfo escuro. A subespécie também é muito menos marcada com preto em seu peito de aparência mais branca e nunca apresenta uma crista. É a menor subespécie aceita do gavião-variável, consideravelmente menor que N. c. limnaeetus. O comprimento da corda máxima foi medido como 312 mm em um único macho e 329 a 337 mm em uma pequena amostra de fêmeas.[1]
Descrição
O gavião-variável é uma águia grande, mas esguia. Está entre os tamanhos médios das espécies atualmente aceitas no gênero Nisaetus. Como na maioria das aves de rapina, as fêmeas são maiores que os machos, com uma diferença média de tamanho geral de 7%, mas pode variar individualmente entre 18-22%, com as raças insulares aparentemente sendo menos dimórficas em média. O tamanho é bastante variável, e o comprimento total foi relatado no passado como variando de 51 a 82 cm e a envergadura de 100 a 160 cm, no entanto, esses números parecem incluir os gaviões-águia muito mais robustos de Flores, que atualmente são considerados uma espécie separada pelas autoridades modernas.[1][24] No entanto, comprimentos totais de até 77 cm foram listados para N. c. limnaeetus no Nepal.[25]
Ademais, também foram estimados os seguintes comprimentos totais médios para as subespécies: N. c. cirrhatus em 72 cm, N. c. limnaeetus em 70 cm e N. c. andamanensis em 61 cm.[21] Legge mediu o comprimento dos gaviões-variáveis do Sri Lanka (N. c. ceylanensis) sem incluir o bico como de 55 a 60 cm.[20] O comprimento médio de aves das Filipinas (N. c. limnaeetus) foi medido como de 58,4 cm em machos e 64.9 cm em fêmeas.[26] Os pesos nesta espécie foram relatados de 1,2 a 1,9 kg, mas a fonte disso não é clara e provavelmente subestima a variação de tamanho conhecida na espécie.[3][24][27] As únicas massas corporais precisas conhecidas para a espécie são derivadas da população das Filipinas, onde os machos têm uma média de 1,36 kg e as fêmeas uma média de 1,6 kg, mas podem pesar mais de 1,81 kg.[26][28]

Os gaviões-variáveis adultos são tipicamente marrom-escuros na parte superior e estriados de forma marcante abaixo, com um bico forte, uma crista de tamanho variável, muitas vezes flácida, ou ausente, asas relativamente curtas, uma cauda longa e finamente barrada e pernas longas emplumadas. Esta espécie tende a se empoleirar ereta e pode se empoleirar em vários locais, desde pontos um pouco isolados até áreas bastante abertas.[1][3] Quando empoleirada, suas asas alcançam apenas cerca de um terço a meio da cauda.
Adultos de morfo claro são principalmente marrom-escuros na parte superior com bordas mais claras muito sutis, geralmente apenas conspícuas nas coberteiras das asas. Têm uma cabeça e pescoço estriados de preto e um pouco tingidos de ruivo, com uma crista preta (se presente). A cauda tende a ser marrom mais clara que o dorso, com uma ponta esbranquiçada fina, uma faixa subterminal preta larga (tanto a ponta esbranquiçada quanto a faixa subterminal também são visíveis da parte inferior da cauda) e 3 a 4 barras marrons mais estreitas e muitas vezes bastante obscurecidas. Na parte inferior do morfo claro da espécie, a cor base é branca a amarelada, sobreposta com estrias pretas a marrom-escuras marcantes; as estrias tendem a ser mais sutis no abdômen, mas mais evidentes nas pernas.
Além do típico morfo claro, algumas subespécies, especialmente N. c. limnaeetus, tendem a ter um morfo intermediário e um morfo escuro. O morfo intermediário é um pouco semelhante aos adultos de morfo claro, mas é fortemente cinza-marrom abaixo, com pouco ou nenhum da cor base mais clara visível e estrias mais obscurecidas, com a área do abdômen até o crissum geralmente sem padrão. Enquanto isso, o adulto de morfo escuro pode variar de marrom-chocolate a quase preto puro com bordas variáveis mais claras, aliviado apenas pela metade interna acinzentada da cauda, bem como algumas barras acinzentadas na cauda.[1][3]

A maioria dos gaviões-variáveis juvenis é marrom-escura na parte superior, mas com bordas brancas muito mais conspícuas no manto e nas asas do que os adultos; em alguns casos, as coberteiras medianas são amplamente brancas e as coberteiras maiores e até menores são amplamente escamadas de branco. O juvenil tem uma cauda marrom clara com cerca de sete barras escuras finas e uma ponta esbranquiçada. A cabeça do jovem varia de amarelada com crista de ponta branca (como é o caso na península indiana e no Sri Lanka) a totalmente esbranquiçada, mas quase sempre os jovens são manchados e estriados com preto ou marrom-escuro na coroa traseira e na nuca. Assim como a cabeça, as partes inferiores são variáveis, com juvenis em grande parte da Índia e no Sri Lanka mostrando estrias marrons finas no peito ou pequenas manchas no peito, com barras fulvas obscurecidas na coxa, pernas e crissum. Juvenis em outros lugares são frequentemente quase completamente brancos abaixo.
Quando os jovens atingem o segundo ao terceiro ano, tendem a mostrar menos branco na parte superior e mais marrom ou preto abaixo. Sua cauda começa a mudar para se assemelhar à dos adultos no terceiro ano, mas no segundo ano em N. c. limnaeetus (ou pelo menos nas Filipinas). Indivíduos da espécie podem tentar se reproduzir aos 3 anos de idade, mas a plumagem adulta completa não é obtida até o quarto ano.[3][28] Adultos têm olhos amarelos a amarelo-alaranjados, enquanto os dos juvenis são cinza-marrom a verde claro. Adultos têm uma cera cinza a amarelo-esverdeada clara, e os juvenis têm cera cinza opaca, enquanto todas as idades têm pés amarelos.[1]
Em voo, o gavião-variável é um grande rapinante com uma cabeça proeminente, asas arredondadas e largas relativamente curtas, cauda longa quadrada ou arredondada, mas tem asas um pouco mais esguias e bordas traseiras mais retas do que espécies simpátricas de gaviões-águia. A espécie tende a voar com um voo rápido e ágil, mostrando batidas rasas poderosas intercaladas com deslizes em asas planas ou curvadas, com os carpais bem à frente (acima do nível do bico) e as primárias inclinadas para trás. Ao planar, as asas são suavemente abaixadas ou às vezes mantidas niveladas, com os carpais novamente bem à frente. Em adultos de morfo claro em voo, a mão pode variar de marrom-amarelado escuro (como na península indiana) a um amarelo ou esbranquiçado muito mais claro. Nas penas de voo, a área das pontas das asas até as penas primárias e secundárias frequentemente tem barras pretas, formando linhas irregulares dos carpais às axilares traseiras com outras marcas escuras variáveis em outros lugares.
Os gaviões-variáveis de morfo intermediário adultos têm penas de voo semelhantes, mas têm partes inferiores cinza-marrom com um padrão inferior menos distinto e contrastante. Enquanto isso, tanto em juvenis quanto em adultos de morfo escuro, a cor preta-marrom do corpo se estende à mão, mas a base da cauda, as primárias e, em menor grau, as secundárias são de um cinza muito mais claro e contrastante com estrias semelhantes às de outros gaviões-variáveis. Juvenis típicos mostram grandes áreas de estrias ou manchas esbranquiçadas vistas de cima em voo. Juvenis de grande parte da Índia e do Sri Lanka mostram barras fulvas escuras mais extensas, mas obscurecidas, acima e abaixo, enquanto outras raças são muito mais brancas. Assim como os adultos, o juvenil tem pontas escuras nas primárias e nas coberteiras maiores, produzindo barras diagonais finas e irregulares, mas as barras tendem a ser mais finas.[29]
Voz
O gavião-variável é frequentemente silencioso, mas na época de reprodução pode chamar prontamente, tanto de seu poleiro quanto em voo. Como muitos rapinantes diurnos, seus chamados são uma forma de grito agudo. O chamado estridente e sonoro da espécie é descrito variadamente em padrões de yeep-yip-yip-yip, subindo kwip-kwip-kwip-kwee-ah e penetrante klee-leeuw (para aves das Ilhas Sunda). Ascendentes kri-kri-kri-kree-ah e kreeee-krit com muita ênfase na primeira sílaba alongada são semelhantes. De aves ocidentais da Índia e Sri Lanka, o chamado é ligeiramente diferente, ki-ki-ki-ki-ki-ki-ki-keee, começando curto, crescendo em crescendo e terminando em um grito longo e prolongado. No norte da Índia e na Malásia, os chamados desta espécie foram comparados aos do maçarico-real (Numenius arquata) e da águia-serpentária-de-crista (Spilornis cheela).[1][3][30]
Espécies confundíveis

O gavião-variável é quase sempre a espécie de Nisaetus mais comum e/ou mais amplamente distribuída em qualquer parte de sua distribuição. Sua distribuição se sobrepõe completamente à do (recentemente reconhecido) gavião-de-Legge (N. kelaarti [en]), à maior parte da distribuição do gavião-de-Java (N. bartelsi [en]), do N. alboniger [en] e do N. nanus [en], além de parcialmente com as distribuições do gavião-da-montanha (N. nipalensis [en]), da águia-filipina-stentrional (N. philippinus) (em Mindoro e possivelmente Palauã) e do N. pinskeri [en] (em Mindanau).
Apenas duas espécies do gênero Nisaetus estão fora da distribuição normal do gavião-variável (incluindo sua antiga subespécie, N. floris). Em áreas com a maioria das outras espécies de Nisaetus (como ilhas ou continente do sudeste da Ásia), o gavião-variável é mais provável de ser quase sem crista. Outras espécies tendem a ter asas proporcionalmente mais largas com secundárias mais protuberantes, caudas relativamente mais curtas e, como adultos, corpo inferior mais barrado e padrões de cauda únicos. Os padrões de cores dos adultos podem variar de um pouco diferentes a marcadamente distintos. Os juvenis tendem a ser mais difíceis de distinguir, mas geralmente a maioria das outras espécies de Nisaetus mostra menos branco que os gaviões-variáveis, e esses tendem a mostrar um V ligeiramente mais forte em voo.
O gavião-da-montanha, o gavião-de-flores e o gavião-de-Legge, em ordem decrescente de tamanho, são todos maiores e mais robustos que o gavião-variável, enquanto outras espécies de Nisaetus são menores em diferentes graus.[31][32] Como muitos falcões abelheiros [en] são considerados mimetizadores de rapinantes mais poderosos para se protegerem da predação, o falcão-abelheiro-de-crista (Pernis ptilorhynchus) é considerado semelhante na aparência geral aos gaviões-águia Nisaetus, mas tem uma cabeça distintamente menor e asas mais longas e estreitas do que os gaviões-variáveis. Os falcões-abelheiros-de-crista adultos são barrados, mas o juvenil é estriado, semelhante ao gavião-variável, no entanto, se bem observado, o falcão-abelheiro geralmente parece muito mais solidamente alaranjado-amarelado como cor base, em vez de esbranquiçado abaixo. As ações de voo do P. ptilorhynchus também são distintas, com uma batida mais robótica durante os voos.[33]
Juvenis da águia-serpentária-de-crista são improváveis de serem confundidos com o gavião-variável, exceto à distância e em voo, parecendo mais robustos e menos esguios, com uma cabeça maior, asas ligeiramente mais longas e uma cauda substancialmente mais curta com menos barras (essas diferenças nas proporções são geralmente aplicáveis a várias espécies de águias-serpentárias insulares que podem ser encontradas com gaviões-variáveis também). Juvenis da águia-de-barriga-ruiva (Lophotriorchis kienerii [en]) são um pouco menores e mais compactos, com uma aparência de asas relativamente mais longas e cauda mais curta. O juvenil de barriga-ruiva, quando comparado ao juvenil do gavião-variável, é geralmente mais puramente branco abaixo, o que contrasta mais fortemente com suas estrias pretas esparsas.
N. cirrhatus de morfo escuro podem ser confundidos com a águia-preta (Ictinaetus malaiensis [en]), de tamanho semelhante, mas ainda mais esguio. No entanto, este último tem asas muito mais longas com bases distintamente estreitadas, uma cauda uniformemente escura e bases de penas claras apenas nas primárias. Também o morfo escuro pode ser distinguido de águias-de-botas (Hieraeetus pennatus) de morfo escuro por estes serem um pouco menores, com cauda muito mais curta e asas relativamente mais longas e retangulares. Águias-de-botas de morfo escuro também são cinza-marrom ou canela abaixo na cauda e têm cunhas claras na parte inferior das penas primárias.[1][3][29][31]
Distribuição e habitat
A ampla distribuição do gavião-variável inclui grande parte do subcontinente indiano e do sudeste da Ásia. Sua distribuição abrange nações e áreas como Sri Lanka, encostas do Himalaia (Garhwal até Assão), sul do Nepal e Butão, leste através de Myanmar, oeste do Laos, sul do Vietnã, Camboja, Tailândia e península da Malásia. Na Índia, podem ser encontrados quase continuamente desde a ponta peninsular até Rajastão, Utar Pradexe, Biar e Orissa.
Sua distribuição insular inclui as ilhas Andamão, Sumatra (incluindo Simeulue e Mentawai na costa oeste e Riau, Banca e Bilitom na costa leste), Java, Bornéu e as Filipinas ocidentais e do sul (incluindo Palauã, Calamiãs, Lubang, Mindoro, Mindanau e aparentemente recentemente Bojol). Como a maioria dos rapinantes tropicais, o gavião-variável é amplamente residente, mas indivíduos errantes da península indiana vagaram para o nordeste da Birmânia e sudeste da Tailândia, e alguns registros nas pequenas ilhas da Sunda (Bali, Palau e Lomboque) podem ser de vagantes de Java. A espécie pode viver em savanas arborizada, cultivos com árvores, cursos d'água arborizados, plantações de chá, vilarejos florestados e até em bordas suburbanas. Além desses habitats frequentemente degradados, eles também habitam partes bastante abertas ou menos densas de vastas florestas perenes (incluindo florestas tropicais) ou decíduas (suas áreas decíduas ocorrem principalmente na Índia e nas Ilhas Sunda), mas também podem ser registrados em áreas de crescimento secundário. Em relação à elevação, podem ser encontrados desde o nível do mar até 2 200 m, mas vivem principalmente abaixo de 1500 m.[34][35] Não é incomum nas encostas do Sri Lanka, mas novamente geralmente não excede 1 500 m de elevação lá.[36]
Comportamento e ecologia
_feeding_on_egret.jpg)
_with_Indian_garden_lizard.jpg)
Os gaviões-variáveis ficam à vontade em uma variedade de habitats arborizados e semi-abertos. Sua forma física e estilo de voo são típicos de rapinantes habitantes de florestas em geral e são frequentemente comparados às características de gaviões verdadeiros (gênero Accipiters), em particular espécies maiores. Como a maioria dos outros rapinantes de floresta, os gaviões-variáveis (e espécies de Nisaetus em geral) têm uma cauda longa, asas curtas e largas e pernas relativamente longas, mas poderosas, todas as quais conferem maior manobrabilidade e tempos de ataque mais rápidos em áreas de caça florestais densas do que outros planos corporais de rapinantes. O nome comum gavião-águia é aparentemente uma referência às suas adaptações semelhantes às dos gaviões verdadeiros.[3][37]
Mesmo em comparação com as presas variáveis de grandes açores, a seleção de presas dos gaviões-variáveis parece ser um tanto indiscriminada e oportunista.[38] Infelizmente, em comparação com rapinantes tropicais do neotrópico e especialmente da África, as histórias de vida dos rapinantes da Ásia tropical são geralmente pouco conhecidas, mesmo no caso de rapinantes facilmente observáveis, como os gaviões-variáveis.[39][40] Portanto, o que se sabe sobre a biologia alimentar dos gaviões-variáveis é amplamente reunido com base em relatos confiáveis de testemunhas oculares e anedóticos, evidências fotográficas e amplos levantamentos de censo de aves, em vez de estudos diretos e extensivos. O gavião-variável pode mostrar uma leve preferência por aves como presa, mas também captura livremente vários mamíferos, répteis e alguns outros vertebrados sempre que os encontra.[1][3]
Embora pouca análise quantitativa tenha sido feita sobre seus hábitos alimentares, muitas presas capturadas são relativamente pequenas. Por outro lado, a descrição de Brown & Amadon desta espécie como "não sendo uma ave muito voraz" não é totalmente justificada, pois presas extremamente grandes em relação ao tamanho do gavião-águia também podem ser facilmente capturadas.[3][28][41] Como muitos rapinantes de florestas tropicais, eles são principalmente predadores de emboscada que usam folhagem para caçar furtivamente a partir de galhos escondidos ou galhos abertos com fundo frondoso, lançando-se rapidamente para capturar a maioria de suas presas no chão. Frequentemente caçam de poleiro, com voos curtos de baixa altitude de poleiro em poleiro, intercalados com pausas breves, durante as quais escaneiam por presas potenciais. A caça de poleiro proporciona maior sucesso ao caçar aves que capturam nas árvores.[1][3] Pelo menos alguns casos foram observados de gaviões-variáveis observando e, em seguida, atacando presas diretamente de seu próprio ninho.
_India.jpg)
Uma das únicas análises gerais das preferências alimentares quantitativas do gavião-variável (embora a análise detalhada de presas, incluindo espécies de presas, não tenha sido especificada) foi um estudo desta espécie em contraste com cinco outras espécies de rapinantes em Maarastra, na Índia. Isso mostrou que eles tinham uma preferência por aves como presa, com quase igual número de aves classificadas como pequenas ou grandes, constituindo quase metade de sua dieta em 14 territórios ativos. Além disso, sua seleção de presas foi considerada um tanto semelhante por classe à da águia-de-bonelli (Aquila fasciata), uma águia de habitats muito mais abertos e rochosos, mas o gavião-variável teve a maior diversidade de classes de presas entre os seis rapinantes estudados e foi o único a caçar em áreas fortemente arborizadas.[42] As presas primárias por classe diferiram em Java Ocidental, onde 62% das presas selecionadas eram répteis, 24% aves e 12% mamíferos.[43] Em outros lugares na Índia, a seleção de presas no ninho mostrou quais espécies de presas foram selecionadas pelos gaviões-variáveis, mas carecia de dados quantitativos ou estudos sobre biomassa de presas.
Um estudo em Gujaráti mostrou várias espécies de presas relativamente pequenas sendo capturadas, como o camaleão-indiano (Chamaeleo zeylanicus), o lagarto Calotes versicolor, outros lagartos, o mainá-indiano (Acridotheres tristis), o bulbul de cloaca vermelha (Pycnonotus cafer), outras aves (incluindo periquitos e galináceos de caça não identificados), o roedor Golunda ellioti e um esquilo do gênero Funambulus. As presas identificadas variavam em tamanho de apenas 35 g para um lagarto a 117 g para um mainá, com os lagartos pequenos e camaleões sendo os mais frequentemente entregues.[44][45] No Parque Nacional de Mudumalai [en], apenas três tipos de presas foram especificados por gênero, consistindo no papa-figos-de-capuz (Oriolus xanthornus), na cobra Dendrelaphis tristis [en] e um roedor Ratufa não identificado. Nem todos os ninhos têm presas relativamente pequenas, pois um ninho no norte da Índia mostrou uma composição de presas de galo-vermelho (Gallus gallus), grandes pica-paus como pica-paus-incandescentes e periquitos maiores. Junto com vários tipos de galinhas, praticamente qualquer ave de caça parece ser uma presa quase ideal para os gaviões-variáveis, e várias espécies, incluindo pavão, codornas Perdicula, Galloperdix e francolins [en], são conhecidas por serem caçadas, incluindo tanto jovens quanto adultos. Muitas outras aves com hábitos parcialmente terrestres parecem ser capturadas amplamente, incluindo várias pombas e rolas, saracuras e outras aves aquáticas.[43][46][47][48][49][50]
O limite superior de tamanho para as presas do gavião-variável parece ser bastante fluido, e a espécie é bastante equiparável a várias outras águias de botas em realizar ataques ousados a presas de seu próprio tamanho ou maiores. Muitos dos mamíferos relatados como presas dos gaviões-variáveis são bastante grandes. Presas mamíferas capturadas como adultos incluíram o coelho-asiático (Caprolagus hispidus) com um peso médio estimado de 2.35 kg, a lebre-indiana (Lepus nigricollis) com uma massa média de 2,7 kg, a raposa-voadora (Pteropus giganteus) de 1,3 kg e praticamente qualquer espécie de esquilo-gigante, que pode variar em peso entre 1,1 a 3 kg.[51][52]
Contas e fotos ainda mais impressionantes mostram que o gavião-variável pode caçar e matar mamíferos adultos com defesas formidáveis, como felídeos e primatas, embora não se possa descartar que geralmente atacarão espécimes doentes ou feridos em vez de saudáveis. Além disso, a maioria dos relatos de ataques a macacos do Velho Mundo mostra que os juvenis são, de longe, os membros mais vulneráveis de seus bandos aos ataques de gaviões-águia. Casos de predação verificada, provável ou potencial foram relatados para macaco-de-cauda-de-porco-do-norte (Macaca leonina), macaco-cinomolgo (Macaca fascicularis), macaco Macaca sinica e macaco-cauda-de-leão (Macaca silenus), incluindo espécimes que podem pesar até cerca de 6 kg.[53][54][55] Um caso de predação por um gavião-variável em um juvenil de macaco Presbytis femoralis [en] estimado em 1.9 kg foi fotografado, enquanto casos possíveis foram relatados de predação em juvenis de outros macacos Colobinae e também de primatas maiores, como gibões e macacos-narigudos (Nasalis larvatus).[56][57][58][59][60]
Embora sua relação predador-presa seja ainda nebulosa, sabe-se que os pequenos primatas noturnos peculiares e tóxicos, conhecidos como lóris-lentos, também são presas do gavião-variável.[61][62] Há vários relatos de predação por N. cirrhatus em gatos domésticos (Felis catus), embora em sua maioria filhotes, além de um caso de um grande gato-da-selva adulto (Felis chaus), com peso médio estimado em 7,3 kg, que foi atacado e morto por um desses gaviões.[41][63] Aparentemente, o gavião-variável também está entre os predadores de filhotes de gazelas indianas (Gazella bennetti).[64] Adultos de grandes lagartos-monitores de algumas espécies também podem ser incluídos em seu espectro de presas.[65] As mortes de aves incluem o pavão indiano adulto (Pavo cristatus), com um peso estimado de até 4 kg, e a espécie é considerada uma ameaça também para o pavão-verde (Pavo muticus).[66][67] Foram registradas tentativas de predação de íbis-gigantes (Pseudibis gigantea [en]) adultos e jovens de 4,2 kg, mas todos os ataques conhecidos não tiveram sucesso.[68] Também foram relatados casos de consumo de carcaças de vários veados e macacos, e em um caso um gavião-variável foi filmado perseguindo uma marta-de-garganta-amarela (Martes flavigula [en]) adulta de uma carcaça.[69][70] Também foram observados gaviões-variáveis predando o calau-de-face-branca (Anthracoceros albirostris).[71]
Alimentação
A seleção de habitat e a distribuição geral do gavião-variável é, em grande parte, concomitante com outras aves de rapina de grande porte, como a águia-serpentária-de-crista e o bútio-vespeiro-oriental [en]. Aparentemente, as três espécies são bastante tolerantes e não agressivas entre si, o que talvez seja surpreendente, considerando os hábitos agressivos dos gaviões-águias. Não é de se surpreender que essas espécies tenham nichos ecológicos bastante discrepantes, especialmente em termos de seus hábitos alimentares.[3] Embora os predadores de ninhos provavelmente sejam abundantes, é provável que os gaviões-variáveis pais afastem com agressividade a maioria das ameaças em potencial. Não se conhecem relatos verificados de predação na natureza e a espécie provavelmente cumpre o papel de predador de topo de cadeia. Presume-se que eles consigam persistir ao lado de primos maiores, como o gavião-montês (N. nipalensis [en]), e com o gavião-de-Legge (N. kelaarti), concentrando-se mais em répteis e aves do que nas presas mamíferas provavelmente preferidas pelas espécies maiores (e talvez também se concentrando principalmente em uma classe menor de presas), embora sejam um pouco mais adaptáveis ao habitat do que as outras duas espécies.[72]
O gavião-variável também vivem ao lado da águia-filipina (Pithecophaga jefferyi), que é muito maior, e é provável que também se alimentem de presas menores e evitem encontros diretos com essa águi gigante, que é muito menos numerosa.[26] Por sua vez, os gaviões-variáveis são provavelmente evitados em encontros com aves de rapina florestais menores, como outras espécies menores de Nisaetus, que geralmente se concentram um pouco menos em aves do que os gaviões-variáveis, e os gaviões do gênero Accipiter, que subsistem em grande parte de classes de presas menores.[73] Aparentemente, o gavião-variável é considerado um predador provável (de filhotes) das pequenas águias-indianas-manchadas (Clanga hastata [en]).[74] No entanto, ao contrário, um caso de predação foi relatado em cativeiro, quando um bufo-malaio (Bubo sumatranus), que é encontrado na natureza com gaviões-de-crista no sudeste da Ásia, matou um indivíduo de gavião em um aviário.[75]
Reprodução
N. cirrhatus é, como muitas aves de rapina, uma ave solitária, mas, durante a reprodução, permanece em pares dedicados que geralmente se acasalam por toda a vida. Cada par se envolve em uma exibição territorial nos limites de sua área de residência. Essa exibição aérea geralmente é feita por um macho, mas, às vezes, a fêmea ou ambos os membros do par fazem exibições, geralmente começando com as asas e a cauda arqueadas para cima em posturas exageradas. Durante a exibição, eles disparam verticalmente e mergulham com o nariz para baixo ou se abaixam. Se o gavião-variável rival continuar a atacar o indivíduo que está defendendo, eles voarão um contra o outro na "velocidade da luz", dando uma volta completa no ar. Eles costumam chamar bem alto durante a exibição.[1][3][21]
A temporada de reprodução dos gaviões-variáveis vai de novembro a maio no sul da Índia, com pico entre janeiro e março, enquanto que no clima mais temperado das encostas do Himalaia ela se limita a janeiro-abril. A temporada de reprodução na Índia é comparável à do Sri Lanka, mas é um pouco mais prolongada no último país, continuando às vezes até junho. No entanto, as datas de pico de postura caem mais cedo, por volta de janeiro-fevereiro, no Sri Lanka.[1][28] Nas ilhas equatoriais da Sunda, os ovos foram registrados em 8 meses diferentes, a qualquer momento, de dezembro a outubro, com o pico de atividade caindo geralmente entre fevereiro e agosto. Aparentemente, o maior volume de ovos postos aqui cai em dois períodos distintos, fevereiro-março e julho-agosto. Assim, a estação de reprodução é mais elástica nas áreas de florestas tropicais, mas na parte norte da área de distribuição a estação de reprodução se concentra na estação seca mais fria.
Essa espécie constrói um ninho de vara grande. As dimensões típicas de seu ninho são de 95 a 105 cm de diâmetro, enquanto a profundidade do ninho pode variar de 35 a 120 cm, esta última após repetidos usos e acréscimos.[1][28] Alguns ninhos são muito grandes em relação ao tamanho dessas águias. Um ninho atingiu um diâmetro interno de 1,3 m e uma circunferência de 3,45 m.[3] Os ninhos ativos são forrados com folhas verdes. Ambos os membros do casal participam da construção de novos ninhos e dos reparos. Os ninhos costumam ser construídos de forma sólida e resilientes, mais do que os de outras águias de médio porte, contra ventos fortes e monções. A altura do ninho costuma ser de 6 a 50 m na copa ou na bifurcação alta de uma árvore grande, mas geralmente não fica a menos de 12 m do chão.[1][28] A altura do ninho no subcontinente indiano era normalmente de 12 a 25 m, com uma média de 17 m no Santuário de Vida Selvagem de Shoolpaneshwar [en] e 19 m na Planície Indo-Gangética, e poderia estar em uma grande diversidade de árvores. Os locais de nidificação geralmente ficam perto de um riacho ou talvez perto de um barranco com ampla vista, mas às vezes variam de florestas profundas a árvores isoladas nas bordas de aldeias.[1] Nos espaços verdes periurbanos de Singapura, os gaviões-variáveis fazem seus ninhos principalmente em árvores Albizia, que estão entre as árvores de crescimento mais rápido e mais altas nessas florestas secundárias.[76] Os pais tendem a permitir a aproximação de humanos quando vivem nas proximidades de vilarejos.[28]
N. cirrhatus faz a postura de apenas um ovo. O ovo tende a ser grosseiro e sem brilho, em sua maior parte branco, mas com poucas e fracas manchas ou manchas avermelhadas claras. Os tamanhos dos ovos foram medidos na subespécie nominal (amostra de 40 indivíduos) como variando de 65,3 a 73 mm de altura, com uma média de 68 mm, por um diâmetro de 49,9 a 53,3 mm, com uma média de 52 mm. Na raça N. c. ceylanensis, uma amostra de 24 ovos tinha em média 61,3 mm × 49,8 mm. No N. c. limnaeetus do norte da Índia, 18 ovos tinham em média 69,8 mm × 51,6 mm. Na mesma subespécie, os ovos de Java e Bornéu variaram de 61 a 68,8 mm de altura e de 50 a 54 mm de diâmetro. Já na raça N. c. andamanensis, a média teria sido de 62,2 mm × 50,1 mm, mas o tamanho da amostra é desconhecido.[28]
Normalmente a fêmea incuba o ovo sozinha, por um período estimado de 40 dias.[1][28] Depois que o filhote eclode, a fêmea o cria intensamente por cerca de 25 dias.[3] Um filhote indiano pesava 300 g aos 14 dias e cresceu para 450 g aos 20 dias, tendo desenvolvido um vocabulário de notas sonoras para expressar fome e alarme. O filhote pode estar se preparando, ficando mais em pé e batendo as asas por volta de 4 a 5 semanas de idade, e também pode ser incentivado a comer pela mãe; no entanto, o consumo de um único alimento pode levar até 6 horas nesse momento. Aos 35 dias, o filhote pode ser alimentado progressivamente menos e o crescimento das penas e do tamanho do corpo acelera. Dentro de algumas semanas, as presas são entregues (geralmente por ambos os pais nesse estágio) em galhos próximos, em vez de diretamente no ninho, com os pais chamando ao se aproximarem, aparentemente encorajando o jovem gavião a se aventurar fora do ninho.[3][28]Aos 52 dias de idade, o filhote está totalmente crescido, mas não se reproduz até cerca de 60-68 dias.[1] A dependência total do ninho foi registrada como 81 dias na Índia. No entanto, o ciclo total de reprodução foi registrado como durando cerca de 112 dias em Java Ocidental.[43]
Status de conservação
N. cirrhatus apresenta uma área de distribuição de mais de 13 milhões de quilômetros quadrados. Uma média de apenas um par para cada 1 200 km de sua distribuição colocaria a população em cinco dígitos, mas sua densidade provavelmente é bem maior.[1] Essa espécie é excepcionalmente adaptável, não apenas pelos padrões de seu gênero, mas também pelos padrões de sua subfamília. Embora o desmatamento tenha esgotado as populações de suas espécies semelhantes de Nisaetus, resultando na classificação de quatro delas como espécies ameaçadas de extinção, o gavião-variável tem se mostrado notavelmente resiliente diante do corte e da degradação do habitat. Essa tendência, que mantém a população estável ou até mesmo aumenta enquanto outras espécies de gavião diminuem, foi relatada no subcontinente indiano, na Malásia, em Java e nas Filipinas, bem como em outros lugares do sudeste asiático.[26][77][78][79][80]
Em Java, descobriu-se que o gavião-variável persistia em todos os sete tipos de habitat disponíveis nas ilhas, enquanto o gavião-de-Java (N. bartelsi) estava confinado a apenas quatro tipos de habitat: as áreas florestais primárias mais profundas.[34] No entanto, sua adaptabilidade pode ser exagerada e essa espécie requer árvores altas (embora a floresta de crescimento secundário seja aceitável), composição de habitat apropriada e amplas populações de presas para ter sucesso. É provável que possam persistir na maioria das variedades de silvicultura e em áreas com urbanização de alto grau, mas o desmatamento total é a única grande ameaça a essa espécie.[1][3] Uma preocupação mais secundária, mas que pode esgotar as populações na Índia, é o fato de que não é raro que a espécie cace galinhas (especialmente durante a reprodução, quando é difícil resistir a uma presa tão fácil), o que, por sua vez, resultou na perseguição local de gaviões-variáveis.[3]
Veja também
Referências
- ↑ a b c d e f g h i j k l m n o p q r s t u v w x y z Ferguson-Lees, James; Christie, David A. (2001). Raptors of the World (em inglês). [S.l.]: Houghton Mifflin Harcourt. Consultado em 3 de julho de 2025
- ↑ Sheehy, Robert Rowland (1995). «A phylogenetic analysis of the Accipitridae (class Aves).» (em inglês). Consultado em 3 de julho de 2025
- ↑ a b c d e f g h i j k l m n o p q r s t Naoroji, R., & Schmitt, N. J. (2007). Birds of prey of the Indian subcontinent. Om Books International.
- ↑ «Changeable Hawk-Eagle - eBird». ebird.org
- ↑ «Crested Hawk-eagles or Changeable Hawk-eagles | Beauty of Birds». www.beautyofbirds.com. 13 de julho de 2023
- ↑ Gmelin, Johann Friedrich (1788). Systema naturae per regna tria naturae : secundum classes, ordines, genera, species, cum characteribus, differentiis, synonymis, locis (em latim). 1, Part 1 13th ed. Lipsiae [Leipzig]: Georg. Emanuel. Beer. p. 274
- ↑ Willughby, Francis (1676). Ornithologiae libri tres (em latim). London: John Martyn. p. 48
- ↑ Willughby, Francis (1678). Ray, John, ed. The Ornithology of Francis Willughby of Middleton in the County of Warwick. London: John Martyn. p. 82, No. 12
- ↑ Ray, John (1713). Synopsis methodica avium & piscium (em latim). Avium. London: William Innys. p. 14, No. 12
- ↑ Helbig, Andreas J.; Kocum, Annett; Seibold, Ingrid; Braun, Michael J. (abril de 2005). «A multi-gene phylogeny of aquiline eagles (Aves: Accipitriformes) reveals extensive paraphyly at the genus level». Molecular Phylogenetics and Evolution (em inglês) (1): 147–164. doi:10.1016/j.ympev.2004.10.003. Consultado em 3 de julho de 2025
- ↑ Haring, E.; Kvaløy, K.; Gjershaug, J.-O.; Røv, N.; Gamauf, A. (novembro de 2007). «Convergent evolution and paraphyly of the hawk-eagles of the genus Spizaetus (Aves, Accipitridae) – phylogenetic analyses based on mitochondrial markers». Journal of Zoological Systematics and Evolutionary Research (em inglês) (4): 353–365. ISSN 0947-5745. doi:10.1111/j.1439-0469.2007.00410.x. Consultado em 3 de julho de 2025
- ↑ Gill, Frank; Donsker, David; Rasmussen, eds. (2022). «Hoatzin, New World vultures, Secretarybird, raptors». IOC World Bird List Version 12.2. International Ornithologists' Union. Consultado em 5 de dezembro de 2022
- ↑ Hodgson, Brian Houghton (1836). «Summary description of some new species of Falconidae». Journal of the Asiatic Society of Bengal. 5 (52): 227–231 [228–230]
- ↑ Jobling, James A. (30 de junho de 2010). Helm Dictionary of Scientific Bird Names (em inglês). [S.l.]: Bloomsbury Publishing. Consultado em 3 de julho de 2025
- ↑ a b c d e f Gamauf, Anita; Gjershaug, Jan-Ove; RøV, Nils; KvaløY, Kirsti; Haring, Elisabeth (abril de 2005). «Species or subspecies? The dilemma of taxonomic ranking of some South-East Asian hawk-eagles (genus Spizaetus )». Bird Conservation International (em inglês) (1): 99–117. ISSN 0959-2709. doi:10.1017/S0959270905000080. Consultado em 3 de julho de 2025
- ↑ Gjershaug, J. O., Kvaløy, K., Røv, N., Prawiradilaga, D. M., Suparman, U., and Rahman, Z. (2004). The taxonomic status of Flores Hawk-Eagle Spizaetus floris. Arquivado em junho 10, 2011, no Wayback Machine
- ↑ a b Lerner, Heather; Christidis, Les; Gamauf, Anita; Griffiths, Carole; Haring, Elisabeth; Huddleston, Christopher J.; Kabra, Sonia; Kocum, Annett; Krosby, Meade (9 de janeiro de 2017). «Phylogeny and new taxonomy of the Booted Eagles (Accipitriformes: Aquilinae)». Zootaxa (4). ISSN 1175-5334. doi:10.11646/zootaxa.4216.4.1. Consultado em 3 de julho de 2025
- ↑ Gjershaug, J. O.; Diserud, O. H.; Kleven, O.; Rasmussen, P. C.; Espmark, Y. (9 de junho de 2020). «Integrative taxonomy of the Changeable Hawk-Eagle Nisaetus cirrhatus complex (Accipitriformes: Accipitridae) in India». Zootaxa (2). ISSN 1175-5334. doi:10.11646/zootaxa.4789.2.10. Consultado em 3 de julho de 2025
- ↑ Amadon, Dean (julho de 1953). «REMARKS ON THE ASIATIC HAWK‐EAGLES OF THE GENUS SPIZAËTUS». Ibis (em inglês) (3): 492–500. ISSN 0019-1019. doi:10.1111/j.1474-919X.1953.tb00709.x. Consultado em 3 de julho de 2025
- ↑ a b c Legge, William Vincent; Legge, William Vincent; Keulemans, J. G.; Hanhart; Weller, Edward (1878). A history of the birds of Ceylon. London: Published by the author. Consultado em 3 de julho de 2025
- ↑ a b c d e Ali, Sálim; Ripley, Sidney Dillon; Society, Bombay Natural History (1983). Handbook of the birds of India and Pakistan : together with those of Bangladesh, Nepal, Bhutan, and Sri Lanka Compact ed ed. [S.l.]: Oxford University Press. Consultado em 3 de julho de 2025
- ↑ Baker, E.S. (1928). The Fauna of British India, including Ceylon and Burma. Birds. Vol. V. 2nd. Edition. London.
- ↑ Parry, S. J. (2001). The booted eagles (Aves: Accipitridae): perspectives in evolutionary biology. University of London, University College London (United Kingdom).
- ↑ a b Hoyo, Josep del; Elliott, Andrew; Sargatal, Jordi; Cabot, José, eds. (1992). Handbook of the birds of the world. Barcelona: Lynx Edicions
- ↑ Grimmett, Richard; Inskipp, Carol; Inskipp, Tim; Baral, Hem Sagar (22 de setembro de 2016). Field Guide to the Birds of Nepal: Second Edition (em inglês). [S.l.]: Bloomsbury Publishing. Consultado em 3 de julho de 2025
- ↑ a b c d Winkler, Hans (1998). «Philippine Birds of Prey: Interrelations among Habitat, Morphology, and Behavior». The Auk. 115 (3): 713–726. JSTOR 4089419. doi:10.2307/4089419

- ↑ «Crested Hawk Eagle - Nisaetus cirrhatus». The Eagle Directory. Consultado em 29 de novembro de 2013. Arquivado do original em 18 de dezembro de 2014
- ↑ a b c d e f g h i j Brown, Leslie; Amadon, Dean (1989). Eagles, hawks and falcons of the world. Secaucus, NJ: Wellfleet Press
- ↑ a b Brazil, M. (2009). Birds of East Asia: China, Taiwan, Korea, Japan, and Russia. A&C Black.
- ↑ Grimmett, R.; Inskipp, C.; Inskipp, T. (2013). Birds of the Indian Subcontinent: India, Pakistan, Sri Lanka, Nepal, Bhutan, Bangladesh and the Maldives. [S.l.]: Bloomsbury Publishing
- ↑ a b Robson, C., & Allen, R. (2005). Birds of Southeast Asia: Thailand, Peninsular Malaysia, Singapore, Vietnam, Cambodia, Laos, Myanmar. Princeton University Press.
- ↑ Nijman, V., & Soezer, R. (1998). Field identification of the Javan Hawk Eagle Spizaetus bartelsi. Forktail, 13-16.
- ↑ Decandido, R., Siponen, M., Smit, H., Pierce, A., & Allen, D. (2015). Flight identification and migration pattern of the Oriental Honey Buzzard Pernis ptilorhynchus orientalis in southern Thailand, 2007–2014.
- ↑ a b Nijman, Vincent (2004). «Habitat segregation in two congeneric hawk-eagles (Spizaetus bartelsi and S. cirrhatus) in Java, Indonesia». Journal of Tropical Ecology (em inglês). 20 (1): 105–111. ISSN 0266-4674. doi:10.1017/S026646740300107X
- ↑ Kennedy, Patricia L. (1998). «Raptors in Human Landscapes: Adaptations to Built and Cultivated Environments David M. Bird Daniel E. Varland Juan J. Negro». The Condor. 100 (3): 584–585. ISSN 1938-5129. JSTOR 1369732. doi:10.2307/1369732

- ↑ Harrison, J. (2011). A field guide to the birds of Sri Lanka. Oxford University Press.
- ↑ Petty, S. J. (1998). Ecology and conservation of raptors in forests. [S.l.]: HMSO Publications Centre
- ↑ K., Robert (2006). The Goshawk. London: T & A D Poyser. p. 274. ISBN 978-0-7136-6565-9
- ↑ Whitacre, D. F.; Jenny, J. P. (2013). Neotropical birds of prey: biology and ecology of a forest raptor community. [S.l.]: Cornell University Press
- ↑ Steyn, P. (1983). Birds of prey of southern Africa: Their identification and life histories. Croom Helm, Beckenham (UK).
- ↑ a b Fam, S. D.; Nijman, V. (2011). «Spizaetus hawk-eagles as predators of arboreal colobines». Primates. 52 (2): 105–110. PMID 21340695. doi:10.1007/s10329-011-0240-z
- ↑ Pande, S.; Yosef, R.; Morelli, F.; Pawar, R.; Mone, R. (2018). «Diet and habitat affinities in six raptor species in India». Avian Research. 9 (1). doi:10.1186/s40657-018-0129-2

- ↑ a b c Gunawan, N.; Noske, R. A. (2017). «Nest cycle and nestling development of a pair of Changeable Hawk-Eagles Nisaetus cirrhatus in Gunung Halimun-Salak National Park, West Java». Kukila. 20: 39–47
- ↑ Radder, R. S.; Shanbhag, B. A.; Saidapur, S. K. (2002). «Pattern of yolk internalization by hatchlings is related to breeding timing in the garden lizard, Calotes versicolor». Current Science. 82 (12): 1484–1486. JSTOR 24106186
- ↑ CRC Handbook of Avian Body Masses, 2nd Edition by John B. Dunning Jr. (Editor). CRC Press (2008), ISBN 978-1-4200-6444-5.
- ↑ Wells, D.R. (1999). The Birds of the Thai-Malay Peninsula. Vol. 1, Non-Passerines. Academic Press, London.
- ↑ Tehsin, R.H. (1982). Collective defensive strategy in Blue Rock Pigeon (Columba livia). Journal of the Bombay Natural History Society 79: 414.
- ↑ Wee, Y. C. & Wang, L. K. (2009). Observation On The In-Captivity Development Of A Rescued Chick Of The Striated Heron, Butorides striatus (Linnaeus). Nature in Singapore 2009, 193–202.
- ↑ Murukesh, M. Divin; Balakrishnan, P. (2015). «On the breeding of the Slaty-legged Crake (Aves: Rallidae: Rallina eurizonoides) in Nilambur, Kerala, southern India». Journal of Threatened Taxa. 7 (6): 7298–7301. doi:10.11609/JoTT.o4185.7298-301

- ↑ Pathak, B. J.; Vijayan, S.; Pati, B. P. (2004). «Observations on chick mortality in Darter Anhinga melanogaster in Gir Forest». Journal of the Bombay Natural History Society. 101 (2): 310
- ↑ Datta, A. (1998). «Anti-predatory response of the Indian giant squirrel Ratufa indica to predation attempts by the Crested Hawk Eagle Spizaetus cirrhatus limnaetus». Journal of the Bombay Natural History Society. 95: 332––335
- ↑ Thomas, K.; Das, A. A.; Nameer, P. O. (2017). «A Report on the predation of Grizzled Giant Squirrel (Ratufa macroura) by Changeable Hawk-Eagle (Nisaetus cirrhatus), from Western Ghats, South India». Zoo's Print. 32 (4)
- ↑ Erinjery, J. J.; Kumara, H. N.; Mohan, K.; Singh, M. (2017). «Interactions of lion-tailed macaque (Macaca silenus) with non-primates in the Western Ghats, India». Current Science. 112 (10): 2129–2134. JSTOR 26163955. doi:10.18520/cs/v112/i10/2129-2134
- ↑ José-Domínguez, J. M.; Asensio, N.; García, C. J. G.; Huynen, M.-C.; Savini, T. (2015). «Exploring the Multiple Functions of Sleeping Sites in Northern Pigtailed Macaques (Macaca leonina)». International Journal of Primatology. 36 (5): 948–966. doi:10.1007/s10764-015-9865-x
- ↑ Dittus, W. P. J. (31 de dezembro de 1975). «Population Dynamics of the Toque Monkey, Macaca sinica». Socioecology and Psychology of Primates. [S.l.]: DE GRUYTER MOUTON. pp. 125–152. ISBN 978-90-279-7709-0. doi:10.1515/9783110803839.125
- ↑ Schaik, C. P. van; Hörstermann, M. (1994). «Predation risk and the number of adult males in a primate group: a comparative test». Behavioral Ecology and Sociobiology. 35 (4): 261–272. Bibcode:1994BEcoS..35..261S. doi:10.1007/BF00170707
- ↑ Mcgraw, W. S.; Berger, L. R. (2013). «Raptors and primate evolution». Evolutionary Anthropology: Issues, News, and Reviews (em inglês). 22 (6): 280–293. PMID 24347501. doi:10.1002/evan.21378
- ↑ Harding, L. E. (2015). «Nasalis larvatus (Primates: Colobini)». Mammalian Species. 47 (926): 84–99. doi:10.1093/mspecies/sev009

- ↑ Clarke, E.; Reichard, Ulrich H.; Zuberbühler, Klaus (2012). «The anti-predator behaviour of wild white-handed gibbons (Hylobates lar)». Behavioral Ecology and Sociobiology. 66 (1): 85–96. Bibcode:2012BEcoS..66...85C. doi:10.1007/s00265-011-1256-5
- ↑ Dooley, H. M.; Judge, D. S. (2015). «Kloss gibbon (Hylobates klossii) behavior facilitates the avoidance of human predation in the Peleonan forest, Siberut Island, Indonesia». American Journal of Primatology. 77 (3): 296–308. PMID 25296898. doi:10.1002/ajp.22345
- ↑ Fullera, G., Nijmana, V., Wirdatetic, K. A. I., & Nijman, V. Slow Lorises: 1 avian predators?
- ↑ Svensson, M. S.; Nekaris, K.A.I.; Bearder, S. K.; Bettridge, C. M.; Butynski, T. M.; Cheyne, S. M.; Das, N.; de Jong, Y. A.; Luhrs, A. M.; Luncz, L. V.; Maddock, S. T.; Perkin, A.; Pimley, E.; Poindexter, S. A.; Reinhardt, K. D. (2018). «Sleep patterns, daytime predation, and the evolution of diurnal sleep site selection in lorisiforms». American Journal of Physical Anthropology. 166 (3): 563–577. PMID 29989160. doi:10.1002/ajpa.23450
 . hdl:2436/621568
. hdl:2436/621568
- ↑ Kasambe, R. (2004). «Crested Hawk Eagle (Spizaetus cirrhatus) foraging on Jungle Cat (Felis chaus)». Newsletter for Birdwatchers. 44 (1): 14–15
- ↑ Dookia, S.; Rawat, M.; Jakher, G. R.; Dookia, B. R. (2009). Sivaperuman, C.; Baqri, Q. H.; Ramaswamy, G.; Naseema, M., eds. Status of the Indian Gazelle (Gazella bennettii Sykes, 1831) in the Thar Desert of Rajasthan, India. Berlin, Heidelberg: Springer Berlin Heidelberg. pp. 193–207. ISBN 978-3-540-87408-9. doi:10.1007/978-3-540-87409-6_15
- ↑ Karaunarthna, S.; Surasinghe, T.; Dissayake, D.; Boutejue, M.; Gabadage, D.; Madawala, M. (2017). «Dietary habits and the predators of the Bengal Monitor Varanus bengalensis in Sri Lanka». Biawak. 11 (1): 28–39
- ↑ Dhanwatey, A. S. (1986). «A Crested Hawk-Eagle Spizaetus cirrhatus (Gmelin) killing a Peafowl Pavo cristatus Linnaeus». Journal of the Bombay Natural History Society. 83 (4): 202
- ↑ Hernowo, J. B.; Mardiastuti, A.; Alikodra, H. S.; Kusmana, C. (2011). «Behavior Ecology of the Javan Green Peafowl (Pavo muticus muticus Linnaeus 1758) in Baluran and Alas Purwo National Park, East Java». HAYATI Journal of Biosciences. 18 (4): 164–176. doi:10.4308/hjb.18.4.164

- ↑ Keo, O.; Collar, N. J.; Sutherland, W. J. (2009). «Nest protectors provide a cost-effective means of increasing breeding success in Giant Ibis Thaumatibis gigantea». Bird Conservation International. 19 (1): 77–82. doi:10.1017/S0959270908008319

- ↑ Bhandari, A.; Goyal, N. (2018). «Changeable Hawk Eagle Nisaetus cirrhatus scavenging». Indian Birds. 14 (5): 159–160
- ↑ Pierce, A. J.; Sukumal, N.; Khamcha, D. (2014). «A Yellow-throated Marten Martes flavigula feeding on a Red Muntjac Muntiacus muntjak carcass». Small Carnivore Conservation. 51 (1): 76–78
- ↑ Singh, T.; Lodhi, N.; Gupta, M. (2023). «Observations of Changeable Hawk Eagles (Nisaetus cirrhatus) predating on Oriental Pied Hornbills (Anthracoceros albirostris)». Indian Birds. 19 (3): 84–85
- ↑ Gjershaug, J. O.; Diserud, O. H.; Rasmussen, P. C.; Warakagoda, D. (2008). «An overlooked threatened species of eagle: Legge's Hawk Eagle Nisaetus kelaarti (Aves: Accipitriformes)». Zootaxa. 1792 (1). 54 páginas. doi:10.11646/zootaxa.1792.1.4

- ↑ Prawiradilaga, D. M. (2006). «Ecology and conservation of endangered Javan Hawk-eagle Spizaetus bartelsi». Ornithological Science. 5 (2): 177–186. doi:10.2326/osj.5.177
- ↑ Sant, N., Shelke, V., & Shelke, S. (2006). On the breeding biology of the Indian Spotted Eagle Aquila hastata. Indian Birds.
- ↑ König, C.; Weick, F. (2008). Owls of the World 2nd ed. London: Christopher Helm. ISBN 9781408108840
- ↑ Tan, K.H. (2005). The status and distribution of Changeable Hawk-eagle (Nisaetus cirrhatus) in Singapore. Singapore Bird Group.
- ↑ Sodhi, Navjot S.; Lee, Tien Ming; Koh, Lian Pin; Dunn, Robert R. (2005). «A century of avifaunal turnover in a small tropical rainforest fragment». Animal Conservation (em inglês). 8 (2): 217–222. Bibcode:2005AnCon...8..217S. ISSN 1367-9430. doi:10.1017/S1367943005001927

- ↑ Turner, I. M. (1996). «Species Loss in Fragments of Tropical Rain Forest: A Review of the Evidence». Journal of Applied Ecology. 33 (2): 200–209. Bibcode:1996JApEc..33..200T. ISSN 0021-8901. JSTOR 2404743. doi:10.2307/2404743
- ↑ Sodhi, Navjot S.; Soh, Malcolm C. K.; Prawiradilaga, Dewi M.; Brook, Barry W. (2005). «Persistence of lowland rainforest birds in a recently logged area in central Java». Bird Conservation International (em inglês). 15 (2): 173–191. ISSN 0959-2709. doi:10.1017/S0959270905000146
 . hdl:2440/36827
. hdl:2440/36827
- ↑ Brooks, Thomas M.; Pimm, Stuart L.; Kapos, Valerie; Ravilious, Corinna (1999). «Threat from deforestation to montane and lowland birds and mammals in insular South-east Asia». Journal of Animal Ecology (em inglês). 68 (6): 1061–1078. Bibcode:1999JAnEc..68.1061B. ISSN 0021-8790. doi:10.1046/j.1365-2656.1999.00353.x

