Fluxo migratório rostral
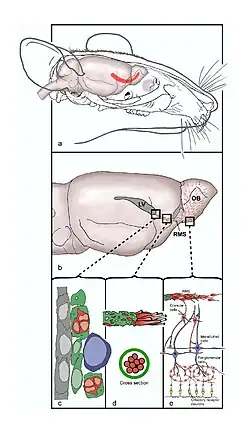
O fluxo migratório rostral (FMR), no inglês conhecido como "rostral migratory stream", é uma rota migratória especializada encontrada no cérebro de alguns animais ao longo da qual precursores neuronais originados na zona subventricular (ZSV) do cérebro migram para alcançar o bulbo olfatório principal (BO). A importância do FMR reside em sua capacidade de refinar e até mesmo alterar a sensibilidade de um animal a odores, o que explica sua relevância e maior tamanho no cérebro de roedores em comparação com o cérebro humano, uma vez que nosso sentido olfativo não é tão desenvolvido.[2]
Essa via foi estudada em roedores, coelhos, e em macacos, como o macaco-esquilo e o macaco-rhesus.[3] Quando os neurônios atingem o BO, eles se diferenciam em interneurônios GABAérgicos à medida que são integrados na camada de células granulares ou na camada periglomerular. Embora se acreditasse originalmente que os neurônios não poderiam se regenerar no cérebro adulto, a neurogênese foi demonstrada em cérebros de mamíferos, incluindo os de primatas. No entanto, a neurogênese é limitada ao hipocampo e à ZSV, e o FMR é um dos mecanismos que os neurônios usam para se realocar a partir dessas áreas.[4]
História breve
O FMR foi nomeado e descoberto por J. Altman em 1969[5] usando autorradiografia com 3H-timidina no cérebro de ratos. Ele rastreou a migração de células marcadas a partir da ZSV, situada ao longo das paredes laterais dos ventrículos laterais, rostralmente até o bulbo olfatório principal. Ele também estudou quantitativamente o efeito da idade no tamanho do FMR. Ainda há algum debate em curso sobre a extensão do FMR e a neurogênese de novos neurônios na ZSV adulta em humanos.[6]
Biologia celular
Células vasculares
As células vasculares desempenham um papel proeminente na regulação da proliferação de precursores neurais adultos. Na zona subgranular [en] (ZSG) adulta, aglomerados densos de células em divisão foram encontrados anatomicamente próximos ao sistema vascular, especialmente capilares. Contatos entre precursores neurais da ZSV adulta e vasos sanguíneos são excepcionalmente permeáveis e frequentemente desprovidos de interferências de astrócitos e pericitos, sugerindo que pistas derivadas do sangue têm acesso direto aos precursores neurais adultos e sua prole. O sistema vascular também fornece o substrato para a migração de novos neurônios após lesões no corpo estriado adulto.
No fluxo migratório rostral, as células vasculares são organizadas paralelamente à rota das células em migração e fornecem um suporte estrutural. Células gliais também estão associadas aos vasos sanguíneos; a comunicação entre essas células pode ser importante para a migração no FMR, por exemplo, no BDNF (fator neurotrófico derivado do cérebro), um fator de crescimento que se acredita modular a migração no FMR.[7]
Astrócitos
Astrócitos formam junções comunicantes[8] e estão intimamente associados ao sistema vascular e sua lâmina basal na ZSV adulta e, subsequentemente, no FMR. Eles podem atuar como uma interface para modular influências de fatores endoteliais e derivados da circulação, bem como a disponibilidade de citocinas e fatores de crescimento nesse sistema. Além disso, astrócitos derivados do hipocampo neurogênico e da ZSV, mas não da medula espinhal não neurogênica, promovem a proliferação e o comprometimento do destino neuronal de células-tronco neurais adultas multipotentes em cultura, sugerindo um papel no FMR.
Astrócitos expressam diversos fatores secretados e ligados à membrana, tanto in vitro quanto in vivo, que são conhecidos por regular a proliferação e a especificação de destino de precursores neurais adultos, bem como a migração, maturação e formação de sinapses neuronais. Na ZSV adulta, astrócitos expressam receptores Robo e regulam a rápida migração de neuroblastos expressando a proteína SLIT1 através do FMR. Além disso, foi proposto que os próprios neuroblastos desempenham um papel na modulação dos astrócitos por meio de interações Slit-Robo. Na ausência de Slit, os processos astrocíticos não se alinham corretamente, nem formam os "tubos", correndo, em vez disso, através dos neurônios em migração.[9]
Astrócitos da ZSV adulta também parecem liberar glutamato para regular a sobrevivência de neuroblastos. Exclusivo da ZSV adulta, células ependimárias que revestem a parede ventricular estão em estreita associação com precursores neurais e sua prole, agindo como um escudo para proteger o "nicho neurogênico", uma zona em que células-tronco são retidas após o desenvolvimento embrionário para a produção de novas células do sistema nervoso.[6][10]
Outras células gliais
Células ependimárias regulam ativamente a especificação do destino neuronal de precursores neurais adultos por meio da liberação de Noggin. O batimento dos cílios das células ependimárias parece estabelecer gradientes de concentração de moléculas de orientação, como citocinas TNF-α (fator de necrose tumoral) e IGF-1 (fator de crescimento semelhante à insulina),[11] para direcionar a migração de neuroblastos, como no FMR. Micróglias também regulam ativamente a neurogênese adulta. Em condições basais, corpos apoptóticos de neurônios recém-gerados são rapidamente fagocitados do nicho por micróglias não ativadas na ZSG adulta. Em condições inflamatórias, a micróglia reativada pode ter efeitos benéficos e prejudiciais em diferentes aspectos da neurogênese adulta, dependendo do equilíbrio entre moléculas secretadas com ação pró e anti-inflamatória. Em um estudo, a ativação da micróglia e o recrutamento de células T foram sugeridos como necessários para a neurogênese na ZSG induzida por ambiente enriquecido, sugerindo um possível papel no FMR.
Mecânica da migração
As células no fluxo migratório rostral são consideradas como se movendo por "migração em cadeia". Esses neuroblastos são conectados por especializações de membrana, incluindo junções comunicantes e junções aderentes, movendo-se ao longo umas das outras em direção ao bulbo olfatório através de tubos gliais. A via e os mecanismos por trás desse movimento incluem um sistema neurogênico ventrículo-olfatório (SNVO), uma estrutura glial e um sistema de sinalização celular quimiotáxica.
Sistema neurogênico ventrículo-olfatório (SNVO)
O sistema olfatório é composto, em parte, pelo FMR, que se estende desde a zona subventricular na parede do ventrículo lateral, através do prosencéfalo basal, até o bulbo olfatório (BO). O SNVO é o nome dado a essa via, que consiste na zona subventricular, no FMR, no trato olfatório e no bulbo olfatório.[12] Os neurônios em desenvolvimento deixam a zona subventricular e entram no FMR, viajando caudalmente e ventralmente ao longo da superfície inferior do núcleo caudado; isso é chamado de membro descendente. Ao alcançar o lado ventral do núcleo caudado, os neurônios seguem o membro rostral e viajam ventral e rostralmente, entrando no córtex olfatório anterior (COA). O COA dá origem ao trato olfatório, que termina no bulbo olfatório.
Estrutura glial
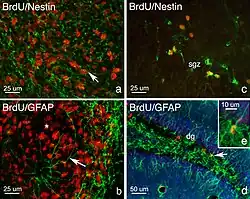
Os neurônios em desenvolvimento viajam em direção ao bulbo olfatório ao longo do FMR por meio de tubos gliais, que marcam a divisão entre o tecido nervoso diferenciado e o tecido com características embrionárias.[14] De forma única, as células viajam tangencialmente à superfície do cérebro, paralelas às superfícies piais, em vez de radialmente, como a maioria dos neurônios em desenvolvimento. Neurônios que migram tangencialmente são geralmente considerados como migrando independentemente da glia radial,[15] mas no FMR os pesquisadores acreditam que esse não é o caso. Tubos gliais de ratos adultos foram observados por microscopia de luz e eletrônica e descritos como uma malha de corpos e processos astrocíticos.[14] Eles foram determinados como astrócitos com base na expressão típica de GFAP (proteína ácida fibrilar glial) e, mais especificamente, como astrócitos protoplasmáticos com base em sua morfologia.
Além disso, verificou-se que essas células gliais eram positivas para a expressão de vimentina, uma proteína comumente encontrada em células gliais embrionárias ou imaturas. Os neurônios em desenvolvimento são identificados pela expressão da molécula de superfície celular, uma forma embrionária polissiálica (PSA) da molécula de adesão de células neurais (NCAM) denominada PSA-NCAM, bem como da β-tubulina, uma proteína frequentemente encontrada em neuroblastos pós-mitóticos, provando que as células do FMR estão comprometidas com o desenvolvimento de neurônios e o farão ao entrar no bulbo olfativo. Com a remoção das NCAM, os neuroblastos se dispersam, comprovando a importância do NCAM na formação da cadeia. Os neurônios formam aglomerados e cadeias ao longo do lúmen desses tubos gliais.
Quando os neurônios em desenvolvimento atingem o núcleo do bulbo olfativo, eles se desprendem do FMR, que é iniciado pela reelina e tenascina[16] e se movem radialmente em direção aos glomérulos, essa migração depende da tenascina-R, e se diferenciam em subtipos de interneurônios. Esses neurônios foram estudados in vivo por meio de eletrofisiologia e imagens confocais.[6]
Sinalização celular
A natureza das pistas moleculares envolvidas no direcionamento correto dos precursores em migração permanece uma questão. A secreção de um fator quimioatrativo pelo BO parece uma possibilidade. Quimioatrativos e repelentes agem sobre os neurônios em migração induzindo mudanças no cone de crescimento [en] para direcioná-los. No entanto, tecidos derivados dessa estrutura não tiveram influência diretiva na migração. Por outro lado, um fator secretado derivado do septo mostrou um efeito repulsivo nas células da ZSV. Mais recentemente, foi demonstrado que a molécula secretada SLIT apresenta tal efeito repulsivo em precursores derivados da ZSV.
Além disso, integrinas demonstraram ter uma influência regulatória na migração em cadeia de células precursoras e na regulação de suas divisões. O PSA-NCAM aparece como outro candidato. Camundongos sem NCAM mostram um BO dramaticamente reduzido em tamanho e um acúmulo de precursores em migração ao longo do FMR. É possível que a falta de NCAM resulte em agitação das interações neurônio-glia, e modificações nessas interações podem, por sua vez, ser responsáveis pela inibição da migração no FMR. Foi demonstrado que existe uma comunicação cruzada entre neurônios e células gliais, e dados a favor de um papel ativo do PSA-NCAM nesse processo foram apresentados. A falta de PSA-NCAM na superfície dos precursores em migração pode alterar as propriedades proliferativas dessa população de células gliais, um cenário que parece remeter à astrogliose que ocorre em doenças neurodegenerativas mesmo antes de quaisquer sinais de dano neuronal.[17]
Pesquisa atual
Existência em humanos
A presença de um fluxo migratório rostral análogo em humanos tem sido difícil de identificar, possivelmente porque o bulbo olfatório é significativamente menos desenvolvido em humanos do que em roedores e, portanto, mais difícil de estudar, e muito do trabalho científico anterior foi questionado em relação ao FMR em humanos. No cérebro fetal em desenvolvimento e em bebês pós-natais jovens, cadeias de neurônios imaturos típicos do FMR foram observadas. No entanto, havia pouca evidência da existência de uma cadeia migratória ao longo da ZSV ou do pedúnculo olfatório até o bulbo no cérebro humano adulto, embora houvesse uma população distinta de células-tronco neuronais adultas na ZSV.[18] Esses pesquisadores estudaram indivíduos de 0 a 84 anos analisando seções cerebrais removidas durante cirurgias ou autópsias. Eles descobriram que células que expressam DCX (doublecortina) e PSA-NCAM estão presentes nas seções cerebrais retiradas de bebês, mas desapareceram por volta dos 18 meses.[18] Estudos adicionais indicaram a presença de uma pequena população de neurônios imaturos em migração, que se originam exclusivamente da ZSV. Esses neuroblastos aparecem isoladamente ou em pares, sem formar cadeias, em contraste com as cadeias alongadas de neuroblastos observadas no FMR de roedores.[19] No entanto, outros estudos indicaram a presença de uma pequena população de neurônios imaturos em migração, que se originam exclusivamente da ZSV. Esses neuroblastos aparecem individualmente ou em pares sem formar cadeias, em contraste com as cadeias alongadas de neuroblastos observadas no FMR de roedores.[20] Isso sugere que o FMR é drasticamente reduzido após a infância[21] e, especialmente, na idade adulta, mas não está ausente. No entanto, uma correlação direta entre a quiescência de células-tronco e a idade ainda não foi definida devido a um alto nível de variabilidade entre indivíduos.[22] Assim, uma estrutura análoga ao FMR no cérebro humano adulto permanece altamente controversa.
Declínio relacionado à idade
A extensão do declínio do FMR relacionado à idade em humanos tem sido objeto de debate significativo. O declínio da neurogênese e da migração a partir do hipocampo em humanos já foi bem documentado.[23] Além disso, declínios relacionados à idade nas atividades das células-tronco da ZSV, que migram para o BO via FMR, estão presentes na meia-idade em roedores. Em camundongos idosos, estudos mostraram que a população de células da ZSV em divisão ativa e a taxa de substituição de interneurônios no BO são ambas drasticamente reduzidas, indicando um declínio relacionado à idade na proliferação neuronal e na migração através do FMR. Esse declínio foi demonstrado como sendo devido à quiescência das células-tronco neuronais na ZSV, mesmo na meia-idade, e não à destruição, muito semelhante ao que ocorre no hipocampo.[24]
Fármacos
Outro tópico em pesquisa atual sobre o FMR diz respeito à fármacos. Cientistas ainda estão tentando enfrentar a difícil tarefa de administrar medicamentos no cérebro e fazê-los ultrapassar a seletiva barreira hematoencefálica. Em um estudo recente, pesquisadores testaram o papel do FMR na "administração intranasal de medicamentos no sistema nervoso central (SNC)".[25] Nesse estudo, os experimentadores interromperam o FMR em camundongos, o que obstruiu "a captação de radioligantes administrados intranasalmente no SNC". Marcadores fluorescentes também foram usados para rastrear o medicamento por todo o cérebro. Foi constatado que o medicamento se espalhou por todas as regiões do cérebro, incluindo o bulbo olfatório. O estudo concluiu que o FMR era extremamente prevalente e necessário no sistema nervoso central para entregar medicamentos intranasalmente. O estudo também observou que essa pesquisa sobre o FMR não é suficiente, mas precisa ser expandida. Algumas das limitações e capacidades do FMR ainda são desconhecidas, assim como alguns dos riscos associados. Se os medicamentos forem administrados no SNC através do FMR, todos os detalhes do FMR devem ser conhecidos para garantir a entrega segura dos medicamentos ao cérebro.
Integrina α6β1
Um estudo foi conduzido testando uma integrina específica, alfa-seis-beta-um, e o papel que ela desempenha no FMR. O estudo pesquisou o princípio de que moléculas quimioatrativas podem desempenhar um papel importante na migração de neuroblastos no FMR. O estudo dessa integrina específica foi conduzido em camundongos. Ao usar anticorpos para se ligar às subunidades da integrina α6β1, encontradas nos neuroblastos, os pesquisadores observaram que a migração foi interrompida. Além disso, eles investigaram o mecanismo pelo qual a integrina α6β1 funciona e determinaram que era por meio do quimioatrativo laminina. Isso foi concluído injetando laminina perpendicularmente ao FMR e observando que isso "desviava neuroblastos de seu curso normal de migração".[26] Os pesquisadores concluíram com a ideia que essa pesquisa poderia ser útil para fins terapêuticos, pois neuroblastos poderiam potencialmente ser atraídos para locais de lesão ou doença.
Referências
- ↑ Lennington, Jessica B; Yang, Zhengang; Conover, Joanne C (13 de novembro de 2003). «Neural stem cells and the regulation of adult neurogenesis». Reproductive Biology and Endocrinology (em inglês) (1). ISSN 1477-7827. PMC 293430
 . PMID 14614786. doi:10.1186/1477-7827-1-99. Consultado em 20 de agosto de 2025
. PMID 14614786. doi:10.1186/1477-7827-1-99. Consultado em 20 de agosto de 2025
- ↑ Curtis, Maurice A.; Faull, Richard L. M.; Eriksson, Peter S. (setembro de 2007). «The effect of neurodegenerative diseases on the subventricular zone». Nature Reviews Neuroscience (em inglês) (9): 712–723. ISSN 1471-003X. doi:10.1038/nrn2216. Consultado em 20 de agosto de 2025
- ↑ Kam, Monica; Curtis, Maurice A.; McGlashan, Susan R.; Connor, Bronwen; Nannmark, Ulf; Faull, Richard L.M. (maio de 2009). «The cellular composition and morphological organization of the rostral migratory stream in the adult human brain». Journal of Chemical Neuroanatomy (em inglês) (3): 196–205. doi:10.1016/j.jchemneu.2008.12.009. Consultado em 20 de agosto de 2025
- ↑ Verkhratsky, Alexei; Butt, Arthur (2007). Glial Neurobiology. West Sussex: Wiley. pp. 96. ISBN 978-0-470-51740-6
- ↑ Altman, Joseph (dezembro de 1969). «Autoradiographic and histological studies of postnatal neurogenesis. IV. Cell proliferation and migration in the anterior forebrain, with special reference to persisting neurogenesis in the olfactory bulb». Journal of Comparative Neurology (em inglês) (4): 433–457. ISSN 0021-9967. doi:10.1002/cne.901370404. Consultado em 20 de agosto de 2025
- ↑ a b c Ming, Guo-li; Song, Hongjun (maio de 2011). «Adult Neurogenesis in the Mammalian Brain: Significant Answers and Significant Questions». Neuron (em inglês) (4): 687–702. PMC 3106107
 . PMID 21609825. doi:10.1016/j.neuron.2011.05.001. Consultado em 20 de agosto de 2025
. PMID 21609825. doi:10.1016/j.neuron.2011.05.001. Consultado em 20 de agosto de 2025
- ↑ Sun, Woong; Kim, Hyun; Moon, Younghye (2010). «Control of neuronal migration through rostral migration stream in mice». Anatomy & Cell Biology (em inglês) (4). 269 páginas. ISSN 2093-3665. PMC 3026178
 . PMID 21267400. doi:10.5115/acb.2010.43.4.269. Consultado em 20 de agosto de 2025
. PMID 21267400. doi:10.5115/acb.2010.43.4.269. Consultado em 20 de agosto de 2025
- ↑ Bennett, Michael V.L.; Contreras, Jorge E.; Bukauskas, Feliksas F.; Sáez, Juan C. (novembro de 2003). «New roles for astrocytes: Gap junction hemichannels have something to communicate». Trends in Neurosciences (em inglês) (11): 610–617. PMC 3694339
 . PMID 14585601. doi:10.1016/j.tins.2003.09.008. Consultado em 20 de agosto de 2025
. PMID 14585601. doi:10.1016/j.tins.2003.09.008. Consultado em 20 de agosto de 2025
- ↑ Eom, Tae-Yeon; Li, Jingjun; Anton, E.S. (julho de 2010). «Going Tubular in the Rostral Migratory Stream: Neurons Remodel Astrocyte Tubes to Promote Directional Migration in the Adult Brain». Neuron (em inglês) (2): 173–175. PMC 3866012
 . PMID 20670825. doi:10.1016/j.neuron.2010.07.013. Consultado em 20 de agosto de 2025
. PMID 20670825. doi:10.1016/j.neuron.2010.07.013. Consultado em 20 de agosto de 2025
- ↑ Conover, Joanne C.; Notti, Ryan Q. (janeiro de 2008). «The neural stem cell niche». Cell and Tissue Research (em inglês) (1): 211–224. ISSN 0302-766X. doi:10.1007/s00441-007-0503-6. Consultado em 20 de agosto de 2025
- ↑ Ekdahl, C.T.; Kokaia, Z.; Lindvall, O. (fevereiro de 2009). «Brain inflammation and adult neurogenesis: The dual role of microglia». Neuroscience (em inglês) (3): 1021–1029. doi:10.1016/j.neuroscience.2008.06.052. Consultado em 20 de agosto de 2025
- ↑ Curtis, Maurice; Kam, Monica; Nannmark, Ulf; Anderson, Michelle; Axell, Mathilda; Wikkelso, Carsten; Holtas, Stig; Roon-Mom, Willeke; Bjork-Eriksson, Thomas; Nordborg, Claes; Firsen, Jonas; Dragunow, Michael; Faull, Richard; Eriksson, Peter (2007). «Human Neuroblasts Migrate to Olfactory Bulb via a Lateral Ventricular Extension». Science. 315 (5816): 1243–1249. Bibcode:2007Sci...315.1243C. PMID 17303719. doi:10.1126/science.1136281

- ↑ Faiz, Maryam; Acarin, Laia; Castellano, Bernardo; Gonzalez, Berta (2005). «Proliferation dynamics of germinative zone cells in the intact and excitotoxically lesioned postnatal rat brain». BMC Neuroscience. 6: 26. PMC 1087489
 . PMID 15826306. doi:10.1186/1471-2202-6-26
. PMID 15826306. doi:10.1186/1471-2202-6-26
- ↑ a b Peretto, Pablo; Merighi, Adalberto; Fasolo, Aldo; Bonfanti, Luca (1997). «Glial Tubes in the Rostral Migratory Stream of the Adult Rat». Brain Research Bulletin. 42 (1): 9–21. PMID 8978930. doi:10.1016/S0361-9230(96)00116-5
- ↑ Ghasheghaei, H. Troy; Lai, Cary; Anton, E.S (2007). «Neuronal migration in the adult brain: are we there yet?». Nature Reviews Neuroscience. 8 (2): 141–151. PMID 17237805. doi:10.1038/nrn2074
- ↑ Abrous, Djoher Nora; Koehl, Muriel; Le Moal, Michel (abril de 2005). «Adult Neurogenesis: From Precursors to Network and Physiology». Physiological Reviews (em inglês) (2): 523–569. ISSN 0031-9333. doi:10.1152/physrev.00055.2003. Consultado em 20 de agosto de 2025
- ↑ Chazal, Genevieve; Durbec, Pascale; Jankovski, Aleksandar; Rougon, Genevieve (2000). «Consequences of Neural Cell Adhesion Molecule Deficiency on Cell Migration in the Rostral Migratory Stream of the Mouse». The Journal of Neuroscience. 20 (4): 1446–1457. PMC 6772373
 . PMID 10662835. doi:10.1523/JNEUROSCI.20-04-01446.2000
. PMID 10662835. doi:10.1523/JNEUROSCI.20-04-01446.2000
- ↑ a b Sanai, Nader; Nguyen, Thuhien; Ihrie, Rebecca; Tsai, Hui-Hsin (2011). «Corridors of Migrating Neurons in the Human Brain and their Decline During Infancy». Nature. 478 (7369): 382–386. Bibcode:2011Natur.478..382S. PMC 3197903
 . PMID 21964341. doi:10.1038/nature10487
. PMID 21964341. doi:10.1038/nature10487
- ↑ Wang, Congmin; Liu, Fang; Liu, Ying-Ying; Zhao, Cai-Hong (2011). «Identification and characterization of neuroblasts in the subventricular zone and rostral migratory stream of the adult human brain». Cell Research. 21 (11): 1534–50. PMC 3365638
 . PMID 21577236. doi:10.1038/cr.2011.83
. PMID 21577236. doi:10.1038/cr.2011.83
- ↑ Wang, Congmin; Liu, Fang; Liu, Ying-Ying; Zhao, Cai-Hong; You, Yan; Wang, Lei; Zhang, Jingxiao; Wei, Bin; Ma, Tong (novembro de 2011). «Identification and characterization of neuroblasts in the subventricular zone and rostral migratory stream of the adult human brain». Cell Research (em inglês) (11): 1534–1550. ISSN 1001-0602. PMC 3365638
 . PMID 21577236. doi:10.1038/cr.2011.83. Consultado em 20 de agosto de 2025
. PMID 21577236. doi:10.1038/cr.2011.83. Consultado em 20 de agosto de 2025
- ↑ Arellano, Jon; Rakic, Pasko (2011). «Neuroscience: Gone with the Wean». Nature. 478 (7369): 333–334. Bibcode:2011Natur.478..333A. PMID 22012389. doi:10.1038/478333a

- ↑ Van Den Berge, Simone; Middeldorp, Jinte; Zhang, C.; Curtis, Maurice (2010). «Longterm quiescent cells in the aged human subventricular neurogenic system specifically express GFAP-δ». Aging Cell. 9 (3): 313–326. PMID 20121722. doi:10.1111/j.1474-9726.2010.00556.x
 . hdl:20.500.11755/42ee490d-f1d2-4534-b427-d330cf254327
. hdl:20.500.11755/42ee490d-f1d2-4534-b427-d330cf254327
- ↑ Knoth, Rolf; Singec, Ilyas; Ditter, Margarethe; Pantazis, Georgios (2011). «Murine Features of Neurogenesis in the Human Hippocampus across the Lifespan from 0 to 100 Years». PLOS ONE. 5 (1). 1 páginas. PMC 2813284
 . PMID 20126454. doi:10.1371/journal.pone.0008809
. PMID 20126454. doi:10.1371/journal.pone.0008809
- ↑ Bouab, M.; Paliouras, G.N.; Aumont, A.; Forest-Berard, K.; Fernandes, K.J.L. (2011). «Aging of the subventricular zone neural stem cell niche: evidence for quiescence-associated changes between early and mid-adulthood». Neuroscience. 173: 135–149. PMID 21094223. doi:10.1016/j.neuroscience.2010.11.032
- ↑ Scranton, RA; Fletcher, L; Sprague, S; Jimenez, DF; Digicayliogly, M (2011). «The rostral migratory stream plays a key role in intranasal delivery of drugs into the CNS». PLOS ONE. 6 (4). 4 páginas. Bibcode:2011PLoSO...618711S. PMC 3076435
 . PMID 21533252. doi:10.1371/journal.pone.0018711
. PMID 21533252. doi:10.1371/journal.pone.0018711
- ↑ Emsley, J.G; Hagg, T (2003). «α6β1 Integrin Directs Migration of Neuronal Precursors in Adult Mouse Forebrain». Experimental Neurology. 183 (2): 273–285. PMID 14552869. doi:10.1016/S0014-4886(03)00209-7