Donanemab
Donanemab
| |
Nome IUPAC (sistemática)
| |
| Sem informação. | |
Identificadores
| |
| 1931944-80-7 | |
| 472420541 | |
| DB16647 | |
Informação química
| |
| C=6452 | H=10038 | N=1708 | O=2013 | S=42 | | |
| 145089.74 g·mol−1 | |
Farmacocinética
| |
Considerações terapêuticas
| |
Donanemab, vendido sob o nome Kisunla, é um anticorpo monoclonal usado para o tratamento da doença de Alzheimer.[1][2] Donanemab foi desenvolvido por Eli Lilly and Company.[3][4]
Os efeitos colaterais mais comuns incluem imagens anormais relacionadas a amiloides, como hemorragias e inchaço cerebral, que podem causar derrames, convulsões, quedas e dificuldades de raciocínio. hemorragia cerebral e inchaço ocorreram em 36.8% dos pacientes usando donanemab e 14.9% em pacientes placebo.[5] Dores de cabeça e reações alérgicas à medicação foram outros efeitos colaterais comuns.
Donanemab foi aprovado para uso médico nos Estados Unidos em julho de 2024.[6][7][8] A maioria dos membros do painel consultivo da FDA (Food and Drug Administration) tiveram conflitos de interesse financeiros.[9] O tratamento é destinado para pessoas com leve deficiência cognitiva ou em estágio leve de demência, o que é a mesma população em que o tratamento foi estudado nos testes clínicos.[10] Diversos grupos de interesse público se mostraram contra a aprovação da droga em audições da FDA.[11]
Usos Médicos
Donanemab é indicado para o tratamento da doença de Alzheimer para pessoas com leve deficiência cognitiva ou em estágio leve de demência.[12]
Efeitos Colaterais
A Food and Drug Administration (FDA) dos Estados Unidos em seu rótulo para o donanemab apresenta um aviso sobre anormalidades em imagens relacionadas a amiloides.[13]
Efeitos colaterais podem incluir reações relacionadas a infusões, com sintomas como sintomas gripais, náusea, vômito e mudanças na pressão sanguínea, e reações de hipersensibilidade, incluindo anafilaxia (uma reação alérgica grave e potencialmente fatal) e angioedema (inchaço).[14]
Edema cerebral
Em maiores doses de donanemab, algumas pessoas desenvolvem uma forma de edema cerebral (inchaço no cérebro) chamado de "anormalidades em imagens relacionadas a amiloides com edema ou efusão" (ARIA-E); algumas dessas pessoas foram assintomáticas enquanto outras apresentaram edema.[15]
Histórico
A eficácia do donanemab foi avaliada em um estudo duplo-cego, controlado por placebo e paralelo (estudo 1, NCT04437511/TRAILBLAZER-ALZ 2)[16] em participantes com a doença de Alzheimer.[17] Os participantes tiveram a presença de patologia amiloide confirmada e leve deficiência cognitiva ou em estágio leve de demência. 1736 participantes foram randomizados (1:1) para receber 700mg de donanemab a cada quatro semanas para as três primeiras doses, e então 1400mg a cada quatro semanas (N = 860) ou placebo (N = 876) por um total de até 72 semanas.[18] O tratamento foi trocado para o placebo baseado na redução pré-específica de níveis de amiloides medidos pela tomografia por emissão de pósitrons (PET) nas semanas 24, 52 e 76.[19]
O Donanemab apresentou resultados positivos em seus primeiros ensaios. [20] [15]
Fase I
Primeiro Estudo
Nos Estados Unidos e no Japão, Eli Lilly aplicou o estudo de fase I de maio de 2013 até agosto de 2016.[21] O estudo foi conduzido em pessoas com doença de Alzheimer leve, demonstrada por meio de uma positiva tomografia PET de amiloide realizada em cada indivíduo. 100 participantes receberam injeções intravenosas de donanemab até quatro vezes por mês. A Fase I fez parte de um estudo multicêntrico que utilizou um grupo de controle nos diferentes ensaios. O resultado positivo indicou que os participantes tinham excesso de proteína amiloide no cérebro, representando um sinal precoce da doença de Alzheimer. Mensalmente, doses de 0,1 mg/kg a 10 mg/kg foram injetados em machos e fêmeas não férteis com idade média de 74 anos. [22]
Lilly revelou que haviam efeitos colaterais nas primeiras 37 pessoas que receberam tratamento e 12 voluntários que receberam o placebo. a dose maior de donanemab reduziu o efeito de placas no cérebro.[23] Um achado geral foi de que a dosagem maior levou a uma redução de 40% em placas de proteínas no cérebro.
Efeitos colaterais
Até quatro injeções foram realizadas mensalmente até que efeitos adversos levassem Lilly a alterar o ensaio, aumentando o número de injeções em até 8 por mês e aumentando a dosagem dos pacientes de 0.1 mg/kg para 0.3 mg/kg. A mudança nas dosagens veio em conjunto com a diminuição de participantes de 37 voluntários documentados para 9 participantes com resultados disponíveis ao público.
Não houveram sintomas adversos quando os foram dado uma única dose. Donanemab considerado altamente imunogênico, criando uma resposta imune que aumenta a eficiência do anticorpo original infundido. Na próxima parte do ensaio, em que pacientes receberam múltiplas doses, seis pacientes tiveram uma reação de infusão que incluía calafrios, rubor, tontura, erupção cutânea e febre. nenhum paciente teve ARIA-E, mas houveram casos de ARIA-H deixando pequenas hemorragias no cérebro. os dois casos com ARIA-H foram assintomáticos. A maioria das pessoas desenvolveu anticorpos anti-droga diminuindo a efetividade da droga, com um uma pequena meia-vida de dez dias.
Segundo estudo
A segunda fase I do estudo foi conduzida em dezembro de 2015 nos Estados Unidos e no Japão.[24] Este estudo teve 150 participantes, aumentando o tamanho da amostra em 50 pessoas. O método foi alterado em comparação com o primeiro estudo conduzido. Esse estudo usou três regimes de dosagem: um com uma única dosagem de 10, 20 ou 40mg/kg, outro com 10mg/kg a cada duas semanas durante 24 semanas, e uma terceira com 10 ou 20mg/kg todo mês durante 16 meses. Os participantes foram aleatoriamente selecionados para serem parte para ou o grupo placebo ou para o ensaio real, coma uma relação de 3:1. O intuito desse ensaio foi o mesmo do primeiro, medir principalmente a eficácia na redução de placas amiloides cerebrais.[25]
Efeitos colaterais
O aumento na dosagem levou a uma maior porcentagem de participantes experienciando ARIA-E sintomáticas, aumentando para 1 em 4 participantes. Os autoanticorpos também foram se tornando problemáticos para o donanemab, reconhecendo a droga como um antígeno levando a uma luta do corpo contra a droga. Anticorpos anti-droga, que se enquadram em autoanticorpos foram produzidos em quase todos os pacientes. Enquanto esse ensaio mostrou um resultado positivo para participantes tomando doses mensais por 16 meses, à medida que a tomografia PET amiloide se tornava negativa, o estudo terminou em agosto de 2019.[26]
Trailblazer-alz
O estudo de fase II diferiu metodicamente da fase I, alterando a duração, a quantidade de donanemab e o número de pacientes. Houve um aumento na quantidade de donanemab infundido no sangue todo mês durante 72 semanas. Os pacientes que receberam donanemab e os que receberam placebo tornaram-se iguais, criando uma proporção próxima de 1:1 com 257 pacientes no total. [20] Para as três primeiras doses 700 mg foi infundido e 1400 mg de donanemab para cada dose depois disso. Uma tomografia por emissão de pósitrons (PET) também foi usada para medir a quantidade de placa no cérebro. TRAILBLAZER-ALZ foi o método usado para aprimorar o grupo controlado por placebo, pois foi randomizado. Este avaliou a segurança e eficácia do donanemab. [21]
Este consistiu em um ensaio combinando duas drogas experimentais sob Lilly que atingem partes separadas da cascata amiloide. O objetivo dessa fase II foi ver o quão seguro, tolerável, e efetivo um período de 18 meses de donanemab sozinho e em combinação com o inibidor BACE LY3202626 da Lilly.[27] Esse inibidor BACE foi administrado oralmente comparado com o donanemab que injetado de forma intravenosa. Para se observar de maneira efetiva a comparação entres os pacientes que só usaram donanemab e pacientes que usaram ambos as drogas da Lilly foram efetivamente alcançados pelo estudo de três grupos distintos. Um grupo tinha injeções de donanemab e inibidor BACE aplicado oralmente, outro tinha apenas injeções de donanemab, e o terceiro foi o grupo placebo. O ensaio planejou inscrever 375 pessoas cujas memórias estivessem se deteriorando há pelo menos seis meses e que pontuassem acima de um certo limite no Teste de Pontes da CogState (Bridging Test), mas acabaram com 257 participantes.
Resultados
Houve uma redução no nível de placas o que foi destacado através da melhoria da cognição e da capacidade de realizar atividades diárias. A fase II demonstrou resultados promissores inicialmente, sem analisar seus efeitos e os dados em detalhes. Concluiu-se que não houve diferença substancial nos resultados entre o grupo placebo e os pacientes que receberam donanemab. após a fase II o ensaio foi parado.[28]
Efeitos Colaterais
Houve uma visão geral na Escala Integrada de Avaliação da Doença de Alzheimer (iADRS) quando administrando o donanemab e as pontuações foram similares ao grupo placebo, não mostrando uma diferença significante. Houveram casos de ARIA-E, mas apenas assintomáticos, o que representa uma melhoria em relação aos pacientes sintomáticos observados na fase I.[29] Lilly decidiu continuar os ensaios de donanemab mas interrompeu oos ensaios com o inibidor BACE em outubro de 2018. em 2021, os ensaio TRAILBLAZER-ALZ foi completo, indicando o sucesso atual do donanemab, pois ele retarda o desenvolvimento da doença de Alzheimer; mas como os efeitos colaterais ainda eram problemáticos, mais investigações eram necessárias.
Fase III
Em outubro e novembro de 2020, Lilly estendeu o TRAILBLAZER-ALZ para ter um segundo estudo. Foi realizado em 87 locais pelo Canadá, Holanda e Polônia.[30]
Em maio de 2023, a empresa reportou o estudo de fase III mostrando que a droga poderia desacelerar o desenvolvimento da doença de Alzheimer em 35%.[31] A desaceleração de 35% é uma redução relativa baseada em uma análise de subgrupo, o que é considerado uma hipótese, não uma prova da afirmação. Vários especialistas criticaram o uso de valores relativos, chamando-os de "enganosos".[32] Em julho de 2023, resultados de 1.736 pessoas tratadas com donanemab mostraram uma desaceleração da progressão do Alzheimer em 76 semanas, com 24% das pessoas apresentando edema cerebral.[33]
Sociedade e cultura
Em julho de 2024, o donanemab foi aprovado para uso médico nos Estados Unidos. [34] [35] [36] A Food and Drug Administration (FDA) dos EUA concedeu o pedido de designação de fast track, revisão prioritária e terapia inovadora para donanemab. [34]
Em outubro de 2024, o donanemab foi aprovado para uso médico no Reino Unido pela Agência Reguladora de Medicamentos e Produtos de Saúde . [37]
Em março de 2025, o Comité de Medicamentos para Uso Humano (CHMP) da Agência Europeia de Medicamentos recomendou a recusa de uma autorização de comercialização para o Kisunla, um medicamento destinado ao tratamento da doença de Alzheimer precoce. [38] Em Junho de 2025, o CHMP iniciou um reexame da sua recusa. [39]
Economia
O preço de tabela do donanemab é de US$32,000 para um tratamento com duração de um ano. [40]
Nomes
Donanemab é a denominação comum internacional.[41]
Pesquisa
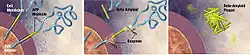
Aprimoramentos na tecnologia de imagem de amiloides relacionou o excesso de peptídeo Aβ fora da célula com o desenvolvimento da doença de Alzheimer.[42] A superprodução de peptídeo Aβ cria uma placa em certas partes do cérebro, interrompendo a neurotransmissão.[43] Donanemab ataca o acúmulo de placa solúvel e insolúvel, retardando a progressão da doença.
Referências
- ↑ «Kisunla- donanemab-azbt injection, solution». DailyMed. 2 de julho de 2024. Consultado em 15 de agosto de 2024. Cópia arquivada em 26 de dezembro de 2024
- ↑ «FDA approves treatment for adults with Alzheimer's disease». U.S. Food and Drug Administration (FDA) (Nota de imprensa). 2 de julho de 2024. Consultado em 2 de julho de 2024. Cópia arquivada em 2 de julho de 2024
 Este artigo incorpora texto desta fonte, que está no domínio público.
Este artigo incorpora texto desta fonte, que está no domínio público.
- ↑ Mintun MA, Lo AC, Duggan Evans C, Wessels AM, Ardayfio PA, Andersen SW, Shcherbinin S, Sparks J, Sims JR, Brys M, Apostolova LG, Salloway SP, Skovronsky DM (maio 2021). «Donanemab in Early Alzheimer's Disease». The New England Journal of Medicine. 384 (18): 1691–1704. PMID 33720637. doi:10.1056/NEJMoa2100708

- ↑ Long JM, Holtzman DM (outubro 2019). «Alzheimer Disease: An Update on Pathobiology and Treatment Strategies». Cell. 179 (2): 312–339. PMC 6778042
 . PMID 31564456. doi:10.1016/j.cell.2019.09.001
. PMID 31564456. doi:10.1016/j.cell.2019.09.001
- ↑ Lenzer J, Brownlee S (setembro 2024). «Donanemab: Conflicts of interest found in FDA committee that approved new Alzheimer's drug». BMJ. 386: q2010. PMID 39322239. doi:10.1136/bmj.q2010
- ↑ «FDA approves treatment for adults with Alzheimer's disease». U.S. Food and Drug Administration (FDA) (Nota de imprensa). 2 de julho de 2024. Consultado em 2 de julho de 2024. Cópia arquivada em 2 de julho de 2024
 Este artigo incorpora texto desta fonte, que está no domínio público.
Este artigo incorpora texto desta fonte, que está no domínio público.
- ↑ «Novel Drug Approvals for 2024». U.S. Food and Drug Administration (FDA). 1 de outubro de 2024. Consultado em 29 de novembro de 2024. Cópia arquivada em 30 de abril de 2024
- ↑ New Drug Therapy Approvals 2024 (PDF). U.S. Food and Drug Administration (FDA) (Relatório). Janeiro 2025. Consultado em 21 de janeiro de 2025. Cópia arquivada em 21 de janeiro de 2025
- ↑ Lenzer J, Brownlee S (setembro 2024). «Donanemab: Conflicts of interest found in FDA committee that approved new Alzheimer's drug». BMJ. 386: q2010. PMID 39322239. doi:10.1136/bmj.q2010
- ↑ «FDA approves treatment for Alzheimer's disease - The Yucatan Times». 12 de julho de 2024. Consultado em 15 de julho de 2024. Cópia arquivada em 15 de julho de 2024
- ↑ «UPDATED PUBLIC PARTICIPATION INFORMATION: June 10, 2024: Meeting of the Peripheral and Central Nervous System Drugs Advisory Committee Meeting Announcement - 06/10/2024». U.S. Food and Drug Administration (FDA). 26 de julho de 2024. Consultado em 17 de março de 2025
- ↑ «FDA approves treatment for adults with Alzheimer's disease». U.S. Food and Drug Administration (FDA) (Nota de imprensa). 2 de julho de 2024. Consultado em 2 de julho de 2024. Cópia arquivada em 2 de julho de 2024
 Este artigo incorpora texto desta fonte, que está no domínio público.
Este artigo incorpora texto desta fonte, que está no domínio público.
- ↑ «Kisunla- donanemab-azbt injection, solution». DailyMed. 2 de julho de 2024. Consultado em 15 de agosto de 2024. Cópia arquivada em 26 de dezembro de 2024
- ↑ «FDA approves treatment for adults with Alzheimer's disease». U.S. Food and Drug Administration (FDA) (Nota de imprensa). 2 de julho de 2024. Consultado em 2 de julho de 2024. Cópia arquivada em 2 de julho de 2024
 Este artigo incorpora texto desta fonte, que está no domínio público.
Este artigo incorpora texto desta fonte, que está no domínio público.
- ↑ a b Sims JR, Zimmer JA, Evans CD, Lu M, Ardayfio P, Sparks J, Wessels AM, Shcherbinin S, Wang H, Monkul Nery ES, Collins EC, Solomon P, Salloway S, Apostolova LG, Hansson O, Ritchie C, Brooks DA, Mintun M, Skovronsky DM (agosto 2023). «Donanemab in Early Symptomatic Alzheimer Disease: The TRAILBLAZER-ALZ 2 Randomized Clinical Trial». JAMA. 330 (6): 512–527. PMC 10352931
 . PMID 37459141. doi:10.1001/jama.2023.13239
. PMID 37459141. doi:10.1001/jama.2023.13239
- ↑ «A Study of Donanemab (LY3002813) in Participants With Early Alzheimer's Disease (TRAILBLAZER-ALZ 2)». ClinicalTrials.gov. Consultado em 2 de julho de 2024. Cópia arquivada em 6 de julho de 2024
- ↑ «FDA approves treatment for adults with Alzheimer's disease». U.S. Food and Drug Administration (FDA) (Nota de imprensa). 2 de julho de 2024. Consultado em 2 de julho de 2024. Cópia arquivada em 2 de julho de 2024
 Este artigo incorpora texto desta fonte, que está no domínio público.
Este artigo incorpora texto desta fonte, que está no domínio público.
- ↑ «FDA approves treatment for adults with Alzheimer's disease». U.S. Food and Drug Administration (FDA) (Nota de imprensa). 2 de julho de 2024. Consultado em 2 de julho de 2024. Cópia arquivada em 2 de julho de 2024
 Este artigo incorpora texto desta fonte, que está no domínio público.
Este artigo incorpora texto desta fonte, que está no domínio público.
- ↑ «FDA approves treatment for adults with Alzheimer's disease». U.S. Food and Drug Administration (FDA) (Nota de imprensa). 2 de julho de 2024. Consultado em 2 de julho de 2024. Cópia arquivada em 2 de julho de 2024
 Este artigo incorpora texto desta fonte, que está no domínio público.
Este artigo incorpora texto desta fonte, que está no domínio público.
- ↑ a b Mintun MA, Lo AC, Duggan Evans C, Wessels AM, Ardayfio PA, Andersen SW, Shcherbinin S, Sparks J, Sims JR, Brys M, Apostolova LG, Salloway SP, Skovronsky DM (maio 2021). «Donanemab in Early Alzheimer's Disease». The New England Journal of Medicine. 384 (18): 1691–1704. PMID 33720637. doi:10.1056/NEJMoa2100708

- ↑ a b «Donanemab Confirms: Clearing Plaques Slows Decline—By a Bit». AlzForum Foundation. 2021. Consultado em 23 de abril de 2021. Cópia arquivada em 23 de abril de 2021
- ↑ Lowe SL, Willis BA, Hawdon A, Natanegara F, Chua L, Foster J, Shcherbinin S, Ardayfio P, Sims JR (2021). «Donanemab (LY3002813) dose-escalation study in Alzheimer's disease». Alzheimer's & Dementia. 7 (1): e12112. PMC 7882532
 . PMID 33614890. doi:10.1002/trc2.12112
. PMID 33614890. doi:10.1002/trc2.12112
- ↑ «Donanemab Confirms: Clearing Plaques Slows Decline—By a Bit». AlzForum Foundation. 2021. Consultado em 23 de abril de 2021. Cópia arquivada em 23 de abril de 2021
- ↑ «Donanemab Confirms: Clearing Plaques Slows Decline—By a Bit». AlzForum Foundation. 2021. Consultado em 23 de abril de 2021. Cópia arquivada em 23 de abril de 2021
- ↑ «Donanemab Confirms: Clearing Plaques Slows Decline—By a Bit». AlzForum Foundation. 2021. Consultado em 23 de abril de 2021. Cópia arquivada em 23 de abril de 2021
- ↑ Mintun MA, Lo AC, Duggan Evans C, Wessels AM, Ardayfio PA, Andersen SW, Shcherbinin S, Sparks J, Sims JR, Brys M, Apostolova LG, Salloway SP, Skovronsky DM (maio 2021). «Donanemab in Early Alzheimer's Disease». The New England Journal of Medicine. 384 (18): 1691–1704. PMID 33720637. doi:10.1056/NEJMoa2100708

- ↑ «Donanemab Confirms: Clearing Plaques Slows Decline—By a Bit». AlzForum Foundation. 2021. Consultado em 23 de abril de 2021. Cópia arquivada em 23 de abril de 2021
- ↑ «Donanemab Confirms: Clearing Plaques Slows Decline—By a Bit». AlzForum Foundation. 2021. Consultado em 23 de abril de 2021. Cópia arquivada em 23 de abril de 2021
- ↑ Mintun MA, Lo AC, Duggan Evans C, Wessels AM, Ardayfio PA, Andersen SW, Shcherbinin S, Sparks J, Sims JR, Brys M, Apostolova LG, Salloway SP, Skovronsky DM (maio 2021). «Donanemab in Early Alzheimer's Disease». The New England Journal of Medicine. 384 (18): 1691–1704. PMID 33720637. doi:10.1056/NEJMoa2100708

- ↑ «Donanemab Confirms: Clearing Plaques Slows Decline—By a Bit». AlzForum Foundation. 2021. Consultado em 23 de abril de 2021. Cópia arquivada em 23 de abril de 2021
- ↑ «Eli Lilly Alzheimer's treatment donanemab slowed disease progression in clinical trial». CNBC. 3 de maio de 2023. Consultado em 3 de maio de 2023. Cópia arquivada em 3 de maio de 2023
- ↑ «The Deadly Secrets Behind "Breakthrough" Alzheimer's Drugs». McGraw Center for Business Journalism. Consultado em 17 de março de 2025. Cópia arquivada em 17 de março de 2025
- ↑ Sims JR, Zimmer JA, Evans CD, Lu M, Ardayfio P, Sparks J, Wessels AM, Shcherbinin S, Wang H, Monkul Nery ES, Collins EC, Solomon P, Salloway S, Apostolova LG, Hansson O, Ritchie C, Brooks DA, Mintun M, Skovronsky DM (agosto 2023). «Donanemab in Early Symptomatic Alzheimer Disease: The TRAILBLAZER-ALZ 2 Randomized Clinical Trial». JAMA. 330 (6): 512–527. PMC 10352931
 . PMID 37459141. doi:10.1001/jama.2023.13239
. PMID 37459141. doi:10.1001/jama.2023.13239
- ↑ a b «FDA approves treatment for adults with Alzheimer's disease». U.S. Food and Drug Administration (FDA) (Nota de imprensa). 2 de julho de 2024. Consultado em 2 de julho de 2024. Cópia arquivada em 2 de julho de 2024
 Este artigo incorpora texto de uma publicação atualmente em domínio público: «erro: parâmetro 'obra' não indicado»
Este artigo incorpora texto de uma publicação atualmente em domínio público: «erro: parâmetro 'obra' não indicado»
- ↑ «Notable Approvals». U.S. Food and Drug Administration (FDA). 2 de julho de 2024. Consultado em 3 de julho de 2024. Cópia arquivada em 13 de junho de 2024
- ↑ «Lilly's Kisunla (donanemab-azbt) Approved by the FDA for the Treatment of Early Symptomatic Alzheimer's Disease» (Nota de imprensa). Eli Lilly. 2 de julho de 2024. Consultado em 2 de julho de 2024. Cópia arquivada em 2 de julho de 2024 – via PR Newswire
- ↑ «New Alzheimer's drug, donanemab – what is it and how does it work?». Alzheimer's Research UK. 23 de outubro de 2024. Consultado em 23 de outubro de 2024. Cópia arquivada em 23 de outubro de 2024
- ↑ «Kisunla EPAR». European Medicines Agency (EMA). 27 de março de 2025. Consultado em 28 de março de 2025
- ↑ «Meeting highlights from the Committee for Medicinal Products for Human Use (CHMP) 16-19 June 2025». European Medicines Agency (EMA). 20 de junho de 2025. Consultado em 30 de junho de 2025
- ↑ «New Drug Approved for Early Alzheimer's». The New York Times. 2 de julho de 2024. Consultado em 3 de julho de 2024. Cópia arquivada em 2 de julho de 2024
- ↑ World Health Organization (2019). «International nonproprietary names for pharmaceutical substances (INN): recommended INN: list 82». WHO Drug Information. 33 (3). hdl:10665/330879

- ↑ Long JM, Holtzman DM (outubro 2019). «Alzheimer Disease: An Update on Pathobiology and Treatment Strategies». Cell. 179 (2): 312–339. PMC 6778042
 . PMID 31564456. doi:10.1016/j.cell.2019.09.001
. PMID 31564456. doi:10.1016/j.cell.2019.09.001
- ↑ Demattos RB, Lu J, Tang Y, Racke MM, Delong CA, Tzaferis JA, Hole JT, Forster BM, McDonnell PC, Liu F, Kinley RD, Jordan WH, Hutton ML (dezembro 2012). «A plaque-specific antibody clears existing β-amyloid plaques in Alzheimer's disease mice». Neuron. 76 (5): 908–20. PMID 23217740. doi:10.1016/j.neuron.2012.10.029
